ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 10.11.2023
Просмотров: 185
Скачиваний: 8
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Соотношение H2 и СО
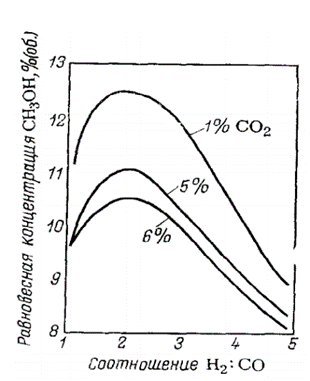
В равновесной газовой системе метиловый спирт достигает максимальной концентрации в результате увеличения отношения H2:CO в исходном сырье и соответствие его стехиометрическому соотношению. С увеличением данного значения возрастает степени превращения оксидов углерода, причем для диоксида более интенсивно.
Снижение данного соотношения снижает ступень превращения оксида и диоксида углерода в метиловый спирт, но увеличивает степень превращения водорода. [5]
Объёмная скорость
В производстве процесс синтеза осуществляется при объемных скоростях 20 000-40 000 ч-1 и выход метанола составляет около 4 % за один проход. При увеличении объемной скорости до 100 000 ч-1 степень превращения исходной смеси за один проход уменьшается, но при циклической схеме с рециркуляцией газов количество полученного метилового спирта возрастает, так как степень превращения снижается медленнее, чем увеличивается объемная скорость. [5]
Охрана окружающей среды в производстве метанола
Газовые выбросы в производстве метанола подразделяют на две категории: постоянные и периодические. К постоянным относятся отходящие газы и пар, выделяющиеся из метанола-сырца на стадии дистилляции, а также продувочные газы из ёмкостей. Основной категорией выбросов в атмосферу являются периодические, которые возникают при остановках из агрегатов, отдельных машин, аппаратов, узлов технологической линии. Из остановленных систем выбрасываются при продувке оставшиеся в них газы и пары. Основным направлением уменьшения периодических выбросов газов в окружающий воздушный бассейн является повышение влажности надёжности всех узлов системы, сведение количества остановок и пусков агрегатов до минимума, удлинение пробегов между ремонтами. Источником загрязнения биосферы в производстве метанола являются сточные воды. В них содержится до 0,3% метанола и других кислородсодержащих соединений углерода. В основном это воды от промывки шламов и емкостей вместе с отходами со стадии очистки метанола. Практически полная очистка сточных вод достигается только при их биологической обработке. Биологическое окисление проводят в аэротенках с активным илом. Предельно допустимая концентрация метанола в сточных водах, поступающих на биохимическую очистку до 200 мг/л. Как правило, до поступления на биологические очистные сооружения сточные воды производства метанола многократно разбавляются сточными водами других производств и хозяйственно бытовыми водами. [1]
-
Описание технологической схемы процесса
Рассмотрим два варианта производства метанола
Процесс при 32 МПа:
Технологический процесс получения метанола из оксида углерода и водорода включает ряд операций, обязательных для любой технологической схемы синтеза. Газ предварительно очищается от карбонила железа, сернистых соединений, подогревается до температуры начала реакции и поступает в реактор синтеза метанола. По выходе из зоны катализа из газов выделяется образовавшийся метанол, что достигается охлаждением смеси, которая затем сжимается до давления синтеза и возвращается в процесс.
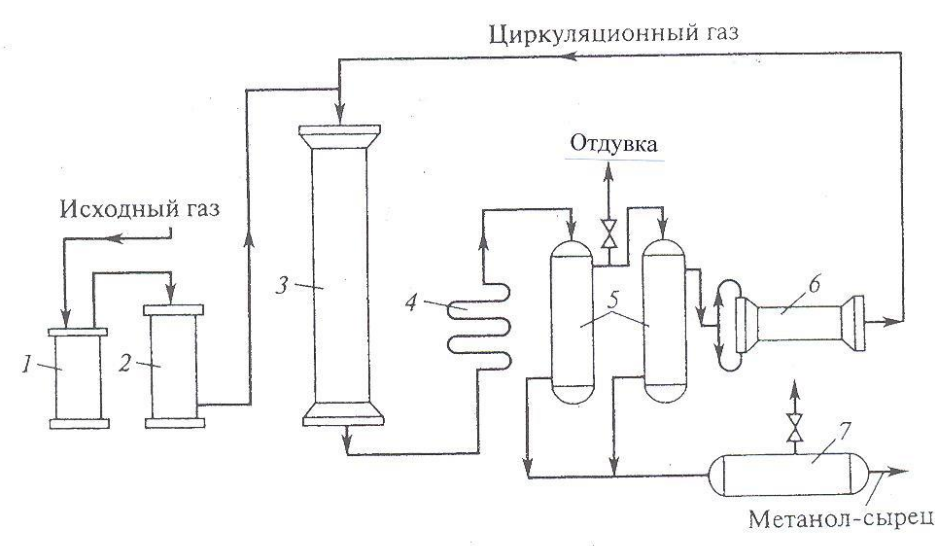
Рис 1. Технологическая схема получения метанола при давлении 32 Мпа.1,2 – фильтры (масляный и угольный), 3 – колонна синтеза, 4 – холодильник-конденсатор, 5 – сепараторы, 6 – компрессор, 7 – сборник метанола-сырца.
Сжатый до 32 МПа синтез-газ проходит очистку в масляном фильтре 1 и в угольном фильтре 2, после чего смешивается с циркуляционным газом и поступает в колонну синтеза 3. Из колонны синтеза выходят метанол-сырец и непрореагировавший синтез газ (Н2 + СО). Смесь направляется в холодильник-конденсатор 4, где охлаждается до 30°С и продукты синтеза конденсируются. Метанол-сырец отделяют в сепараторе 5, направляют в сборник 7 и выводят на ректификацию. Газ проходит второй сепаратор 5 для выделения капель метанола, компримируется до давления синтеза турбоциркуляционным компрессором 6 и возвращается на синтез. Продувочные газы выводят перед компрессором и используют в качестве топлива.
Смешанный газ, пройдя кольцевой зазор между катализаторной коробкой и корпусом колонны 3, поступает в межтрубное пространство теплообменника, расположенного в нижней части колонны. В теплообменнике газ нагревается до 330°С и по центральной трубе, в которой размещен электроподогреватель, поступает в верхнюю часть колонны и проходит последовательно пять слоев катализатора.
Колонны синтеза метанола
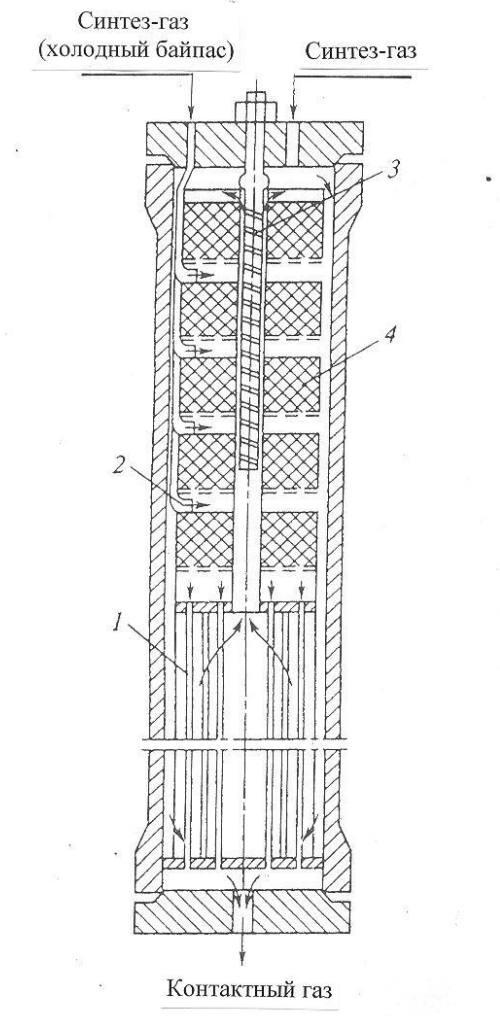 | 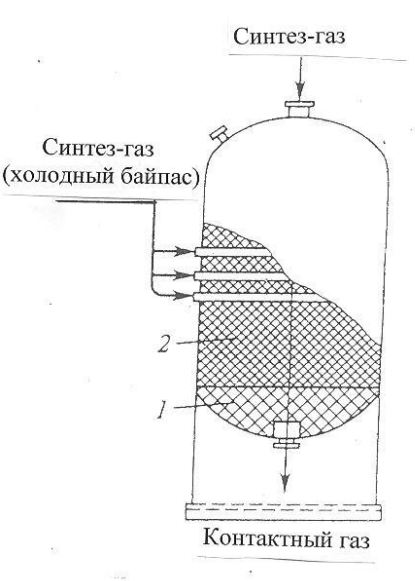 |
| Рис 2. Колонна синтеза метанола при 32 МПа: 1 – теплообменник; 2 – холодный байпас; 3 –электроподогреватель; 4 - катализатор | Рис 3. Колонна синтеза метанола при 5 МПа: 1- фарфоровые шары; 2 – катализатор |
После каждого слоя катализатора, кроме последнего, в колонну вводят определенное количество холодного циркуляционного газа для поддержания необходимой температуры. После пятого слоя катализатора газ направляется в теплообменник, где охлаждается до 130°С и выходит из колонны.
Размещение теплообменника внутри корпуса колонны, подача смешанного газа в колонну синтеза метанола через кольцевой зазор между катализаторной коробкой и корпусом колонны, значительно снижает потери тепла в окружающую среду (принцип наилучшего использования энергии).
Процесс производства метанола при низком давлении включает практически те же стадии, но имеет некоторые особенности.
Процесс при 5 МПа:
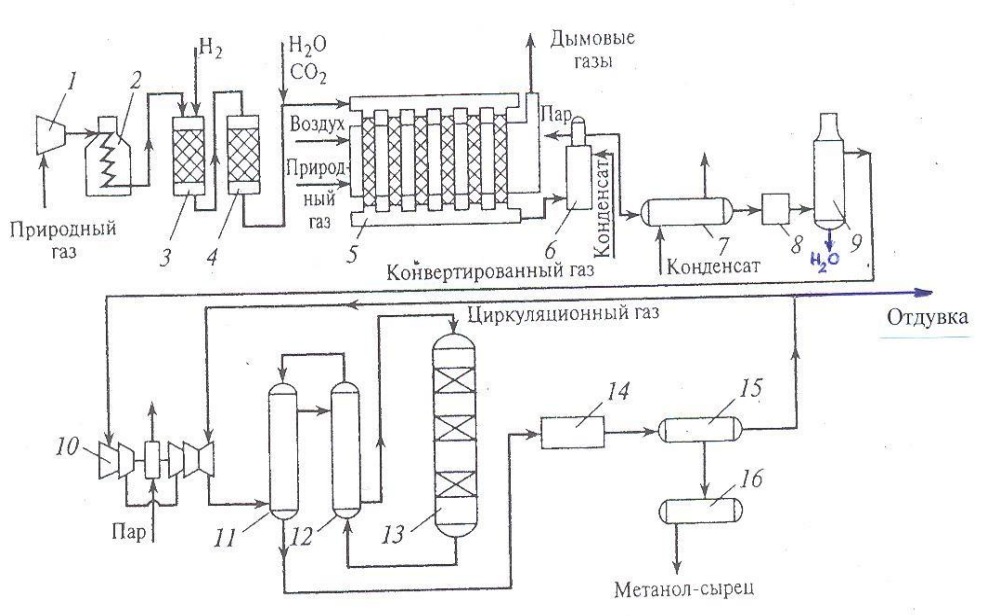
Рис 4. Технологическая схема получения метанола при давлении 5 МПа.1, 10 –турбокомпрессоры, 2 –подогреватель природного газа, 3 –реактор гидрированиясернистых соединений, 4 –адсорбер, 5 –трубчатый конвектор, 6 –котел-утилизатор, 7, 11, 12 –теплообменники, 8, 14 –холодильники-конденсаторы, 9, 15 –сепараторы, 13 –колонна синтеза,16 –сборник.
Природный газ сжимается турбокомпрессором 1 до давления 3 МПа, подогревается в подогревателе 2 за счет сжигания в межтрубном пространстве природного газа и направляется на сероочистку в аппараты 3 и 4, где последовательно осуществляется каталитическое гидрирование органических соединений серы и поглощение образующегося сероводорода адсорбентом на основе оксида цинка. После этого газ смешивается с водяным паром и диоксидом углерода в соотношении СН4 : Н2О : СО2 = 1:3,3:0,24. Смесь направляют в трубчатый конвектор 5, где на никелевом катализаторе происходит паро-углекислотная конверсия при температуре 850-870°С. Теплоту, необходимую для конверсии, получают в результате сжигания природного газа в специальных горелках. Конвертированный газ поступает в котел-утилизатор 6, где охлаждается до 280-290°С. Затем теплоту газа используют в теплообменнике 7 для подогрева питательной воды, направляемой в котел-утилизатор. Пройдя воздушный холодильник 8 и сепаратор 9, газ охлаждается до 35-40°С. Охлажденный конвертированный газ сжимают до 5 МПа в компрессоре 10, смешивают с циркуляционным газом и подают в теплообменники 11, 12
, где он нагревается до 220-230°С. Нагретая газовая смесь поступает в колонну синтеза 13, температурный режим в которой регулируют с помощью холодных байпасов. Далее газовая смесь охлаждается в холодильнике-конденсаторе 14, сконденсировавшийся метанол-сырец отделяется в сепараторе 15 и поступает в сборник 16. Циркуляционный газ возвращается на синтез, продувочные газы отдают на сжигание в трубчатую печь.
Вследствие снижения температуры синтеза при низком давлении процесс осуществляется в условиях, близких к равновесию, что позволяет увеличить производительность агрегата. [5]
Функциональная схема синтеза метанола
Как и любой технологический процесс синтез метанола из оксида углерода и водорода включает ряд стадий. Для начала газ очищают от карбонила железа и сернистых соединений. Затем его нагревают до температуры при которой начнётся реакция, и подают его в реактор.
Образовавшийся метанол выделяется при выходе из зоны катализа. Это происходит из-за охлаждения смеси, которую затем сжимают до давления синтеза.
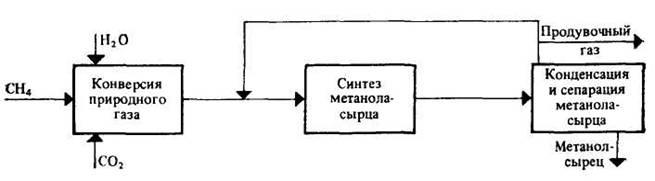
Рис 5. Функциональная схема получения метанола
Химическая схема синтеза метанола
1. Получение синтез-газа паро-углекислой конверсией метана с целью получения определенного соотношения Н2:СО.
2. Возврат непрореагировавшего синтез-газа.
3. Смешение, нагрев и сжатие до соответствующих параметров в зависимости от используемого катализатора.
4. Охлаждение газа после синтеза с целью выделения метанола и при этом нагрев входящих в реактор потоков.
5. Разделение непрореагировавших газов и жидкой фазы.
6. Отделение метанола от побочных продуктов.
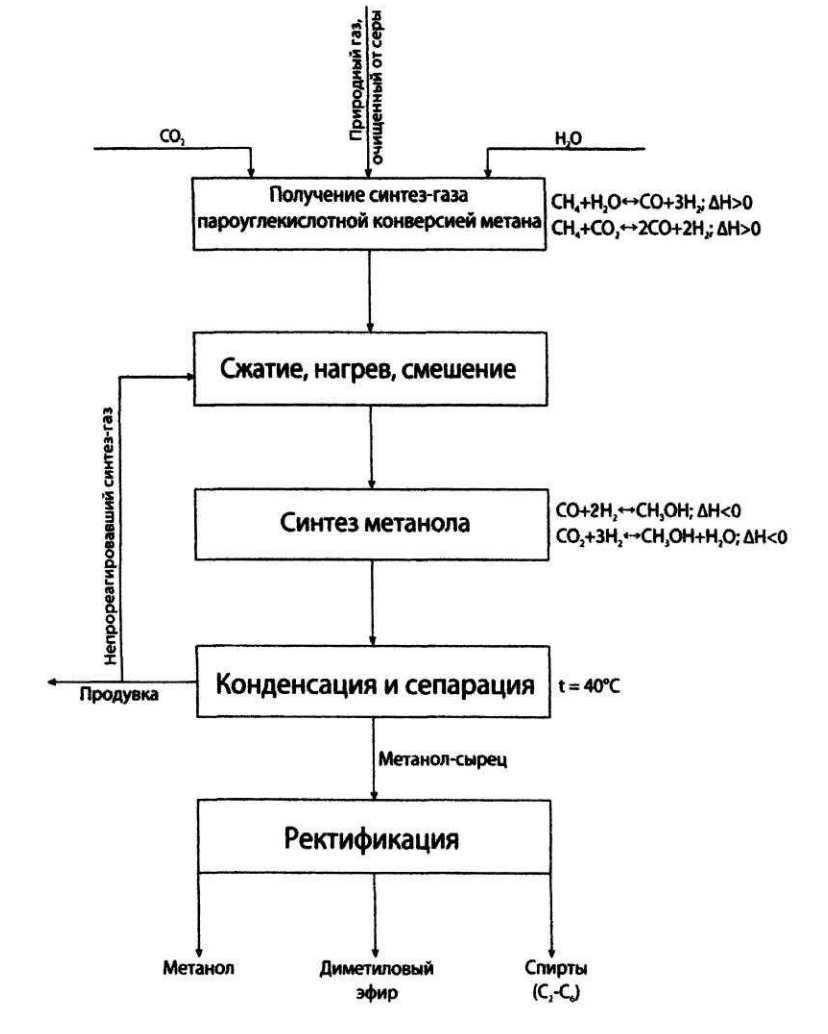
Рис 6. Химическая схема получения метанола
-
Расчёт материального баланса ХТС
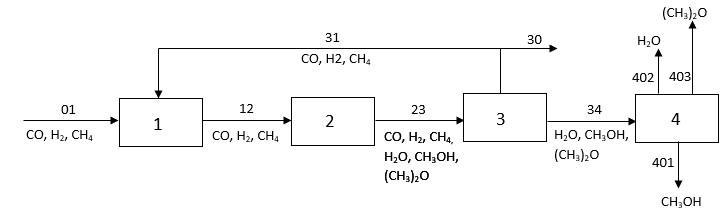
Рис 7. Структурная блок-схема синтеза метанола
Потоки: 01 - свежий газ; 12 - Смесь газов; 23,34 – смесь продуктов; 31 – циркуляционный газ; 30 – отдувочный газ; 401 – метанол-ректификат; 402 – вода; 403 – эфир
Блоки: 1 – смешение; 2 – синтез; 3 – конденсация и сепарация; 4 – ректификация
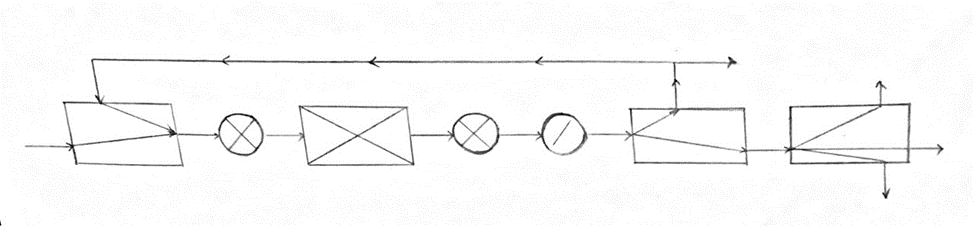
Рис 8. Операторная схема синтеза метанола
Исходные данные для расчёта
| Показатель | Кол-во | Обозначение |
| Содержание инертных примесей в свежем газе, мольн.доли | 0,04 | 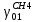 |
| Содержание СО в циркуляционном газе, мольн.доли | 0,12 | 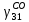 |
| Содержание H2 в циркуляционном газе, мольн.доли | 0,74 | 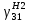 |
| Содержание инертных примесей в циркуляционном газе, мольн.доли | 0,14 | 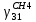 |
| Конверсия СО, доли: | 0,2 | X |
| - селективность образования метанола на СО, доли | 0,95 | 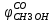 |
| - доля СО, превратившегося в эфир | 0,03 | 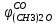 |
| - доля СО, превратившегося в метан | 0,02 | 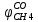 |
| Базис расчёта, кг. СH3ОН: | | |
| - сырца | 1500 |  |
| - ректификата | - | - |
Производство метанола основано на реакции:
СО + 2Н2 СН3ОН +Q
Одновременно протекают побочные реакции:
СО +3Н2 СН4 +Н2О
2СО + 4Н2 (СН3)2О +Н2О
4СО + 8Н2 С4Н9ОН + 3Н2О [6]
Составляем уравнения материального баланса: