ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 66
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Олимпиада есептері
10 сынып-1 Көмірсутек. 5 балл.
Өнеркәсіптік органикалық синтезде кеңінен қолданылатын газ тәрізді көмірсутектің үлгісі толық жанғанда түзілшен судың массасы бастапқы үлгінің массасына тең болады. Көмірсутектің құрылысын анықтаңыздар.
Шешуі:
газ тәтізді көмірсутектің жану теңдеуі:
Cn Hm +
Көмірсутектің үлгісінің массасы 12n + m, түзілген судың массасы
Демек, көмірсутектің қарапайым формуласы: C2H3. Мұнда нақты қосылыс жоқ. Демек, көмірсутектің формуласы -C4 H6. Алкиндер мен алка- диендердің қатарынан есептің шартына ең сәйкес келетіні өнеркәсіпте каучук алу үшін кең қолданатын бутадиен - 1,3 (CH2 = CH - CH = CH2).
10 сынып-2 Қоспалар. 6 балл
Массасы 50 г CaCO3, Ca3 (PO 4)2 және (NH4)2 CO3 қоспасын қақтағанда түзілген 25,2 г қалдыққа алдымен судың артық мөлшерін жіберген. Сонда ерімей қалған қалдықтың массасы 14,0 болған. Қоспадағы аммоний карбонатының массасын анықтаңыздар.
Шешуі: қақтағанда кальций мен аммоний карбонаттары ғана ыдырайды:
t0
CaCO3
100г/моль 56 г/моль
t0
(NH4)2 CO3
Демек, 25,2 г қалдық CaO немесе Ca3 (PO4)2 қоспасы болғаны.
m(CaO) + m(Ca3(PO4)2) = 25,2 г
Кальций окциді мен фосфатының қалдығын сумен өңдегенде тек кальций оксиді ғана суда ериді:
CaO + H2O = Ca (OH)2
Оған CO2 газының артық мөлшерін жібергенде:
Ca (OH)2 + CO2
CaO3 + H2O
CaCO3 + CO2 + H2O
Демек, кальций фосфатының массасы 14 г (2) теңдеу бойынша CaO массасын табамыз
m(CaO) = 25,2 г - 14 = 11,2 г
(1) теңдеуге сүйеніп, CaCO3 массасын табыңыз:
n(CaCO3) = n (CaO) =
m (CaCO3) = 0,2 моль * 100г/ моль = 20г
Демек, m ((NH4)2 CO3) = 50г - (14г + 20г) = 16г
10 сынып - 3 Көмірсутек. 5 балл.
Этан, пропилен және ацетиленнің 448 мл (қ.ж.) көлем алады және бромның тетрахлорметандағы 40 мл 5% - (тығыздығы 1,6 г/мл) түссіздендіре алады.Қоспа толық жанғанда түзілген көміртек (IV) толық жұту үшін қажетті калий гидроксидінің 40% - дық ерітінгдісінің (тығыздығы 1,4 г/ мл) минималь мөлшері -
5 мл . Қоспадағы газдардың көлемдік үлестерін анықтаңыздар (%, көлемдері бойынша).
Шешуі: көмірсутектер қоспасының жалпы зат мөлшері:
v (қоспа)=
v (этан) =х,v (пропилен) = y,v (ацетилен) = z болсын делік.
Онда: х+у+z= 0,02
Ерітіндідегі бромның массасы мен зат мөлшері:
m(Br2)=Vp
v(Br2) =
Бром тек пропилен мен ацетиленмен әрекеттеседі:
C3 H6 + Br2 = C3 H6 Br2
C2 H2 + 2Br2 = C1 H2 Br4
Демек : у +2z = 0,02моль
Қоспа толық түзілген CO2 сіңіруге кеткен сілті мөлшері:
v(KOH)=
Титреуге кеткен КОН мөлшері минимал, демек ракция теңдеуі:
KOH + CO2 = KHCO3 демек, v(CO2) = 0,05моль
Көмірсутектің жану ракциялары:
C2 H6 + 3,5O2 = 2CO2 + 3H2O
C3 H6 + 4,5O2 = 3CO2 + 3H2O
C2 H2 + 2,5O2 = 2CO2 + H2O
Бұдан (коэффиценттерін ескере отырып):
2x + 2y + 2z = 0.05 моль
(1), (2) және (3) теңдеулер жүйесін шешсек:
x= 0.005 моль; у= 0,01 моль; z = 0,005 моль
Онда: х:у:z = 1:2:1 (немесе 25% этан: 50% пропилен: 25% ацетилен).
10 сынып - 4 Белгісіз заттарды олардың қасиеттері бойынша анықтау. 5 балл.
Екі тұз берілген – А және В. Оның бірі, А, оранж түсті, суда жақсы ериді, оның ерітіндісі жалынды жасыл түске бояйды. А тұзы тотықтырғыш, ол қышқыл ортада тотықсыздандырғышпен әрекеттескенде оның түсі жасылдау- күлгінге айналады. Екінші тұз, В – ақ түсті, қыздырғанда газ тәрізді өнімдерге ыдырайды. Тұздың ерітіндісі күміс нитратының ерітіндісімен ірімшік тәрізді ақ тұнба береді. А және В тұдары қыздырғанда бір – бірімен әрекеттеседі. Тұздардың құрамын анықтаңыздар. Егер А және В тұздары қоспасын қыздырғанда 2,24 л (қ.ж) газ бөлінсе, ал реакция өнімін сумен өңдегенде 15,2 г суда ерімейтін металл (ІІІ) оксиді алынған болса, онда қоспаның молярлық құрамы қандай болған?
Шешуі:
A – K2 Cr2O7 (0,1 моль – 29,4г); B – NH4 Cl (0,2 моль – 10,7).
К2 Cr2 O7 + 4H2 SO4 +3H2S = Cr2 (SO4)3 + 3S
К2 Cr2 O7 + 7H2 SO4 + 6 KI = Cr2(SO4)3 + 3I2 + K2 SO4 + 7H2O
Әдетте үш валентті хромның тұздарының ерітінділері жасыл болады.
NH4 Cl
v (газ) =
NH4Cl + AgNO3 = AgCl
2Cl(OH)3 = Cr2O3 + 3H2O
152моль
v (Cr3 O3) =
10 сынып - 5 изотоптар. 9 балл.
12 CH4 пен 14CH қоспасындағы сутектің массалық үлесі 23%. Қоспадағы 12С изотобының массалық үлесін анықтаңыздар.
Шешуі: қоспаның 100г үлгісін қарастырамыз:
Үлгінің құрамындағы сутектің массасы:
m(C) = m(үлгі) *
Үлгінің құрамындағы көміртегінің массасы:
m(C)=100-23 =77 г
Қоспадағы сутек атомдарының мөлшері:
n(H)=
Үлгідегі көміртек атомдарының мөлшерін анықтаймыз. CH4 молекуласының формуласын көміртек атомдарының мөлшері сутек атомдарының мөлшерінен 4 есе аз екендігі көрініп тұр.
n(C) = 0,25n(H) = 0,25 * 23 моль = 5,75 моль
Егер үлгідегі 12 С изотопының массасын у г деп белгілесек, онда үлгідегі 14С изотобының массасы (77- у) г болады.
Үлгідегі әр изотоптың мөлшерін табамыз:
n(12C)=
n(14C)=
Көміртек атомдарының жалпы мөлшері көміртек изотоптарының мөлшерінің қосындысына те:
n(C) = n(12C) + n(14C) = 5,75 моль немесе
Теңдеуді шешсек: у= 21г, т.е m(12C ) =21г
Қоспадағы 12C изотобының массалық үлесі:
11- сынып -1 Химиялық өзгерістер. 5 балл.
Келесі сызбанұсқаға сәйкес химиялық реакцияларды жүзеге асырытын реакция теңдеулерін жазыңдар:
ацетелин
11- сынып -2 Иондық тепе - теңдіктер. 6 балл.
Сутектің көрсеткіші 4,18 болатын көмір қышқылының 0,01М ерітіндісіндегі H2 CO3, HCO3- немесе CO32- бөлшектерінің концентрацияларынан анықтаңыздар. Көмір қышқылы үшін
K1= 4,45 * 10-7; K2 =4,69 * 10-11
Шешуі: ерітіндідегі сутек иондарының концентрациясы:
-lg
Көмір қышқылының бірінші сатыс бойынша диссоциялану константасы:
K1=
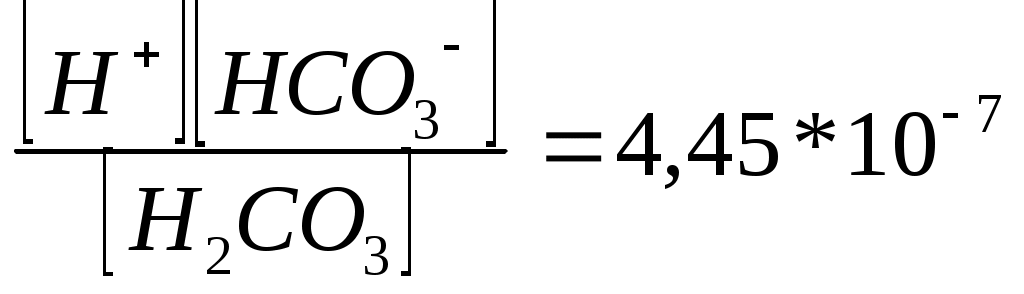
Сол сияқты, көмір қышқылының екінші саты бойынша диссоциациялану константасы:
K2 =
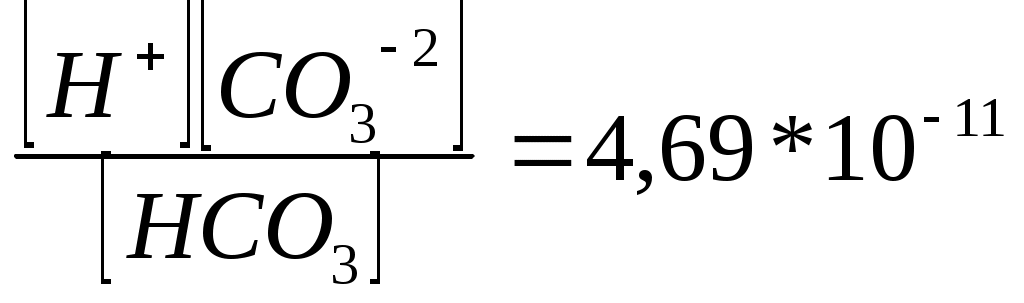
11- сынып – 3. Қоспалар. 7 балл
А затын күкірт қышқылымен әсер еткенде түзілген өткір иісті Б газын жай сұйық В затының судағы түсті ерітіндісі арқылы өткізгенде ерітінді түссізденген. Алынған ерітіндідегі барий тұзын қосқанда қышқылдарда ерімейтін ақ тұнба түзіледі. Алынған ерітінді арқылы сары-жасыл түсті газды өткізгенде В заты түзіледі және бұрыңғы түсі қалпына келеді. А,Б,В және Г заттарын анықтаңыздар және тиісті реакция теңдеулерін жазыңыздар.
Шешуі: өткір иісті түссіз газ күкірт (IV)оксиді болуы мүмкін. Сұйық күйде болатын жай заттар – бром мен сынап. Сынап күкіртті газбен
Реакция теңдеулері:
Na2SO3 + H2SO4 = Na2SO4 + SO2
SO2 +2H2O +Br2 = Na2SO4+ 2HBr
BaCl2 + Na2SO4 = BaSO4
Cl2 + 2HBr = 2HCl +Br2
Демек, А- сульфит, Б- SO2, В- BaSO4, Г- Cl2.
11- сынып -4. белгісіз заттың формуласын анықтау. 8- балл
75 мл газ тәрізді органикалық затты 150 мл оттекпен араластырып, алынған қоспаны қопараған. Түзілген су буынан арылғаннан кейін көлем 150 мл дейін кеміген, ал қалған газды сілті ерітіндісінің артық мөлшері арқылы өткізгеннен кейін оның көлемі 75 мл болған. Осы қалған газды өте жоеғары температураға дейін қыздырылған металл күйіндегі мыс арқылы өткізгенде, ол толық жұтылған. Барлық өлшеулер 1100С температура мен атмосфералық қысымда жүргізілген. Заттың формуласын анықтаңыздар. Сөз болған реакция теңдеулерін жазыңдар.
Шешуі: су буларының көлемі: V(H2) = 225 мл – 150 мл = 75 мл
Көмір қышқыл газының сілтімен жұтылу ракцисы:
CO2 + 2NaOH =Na2CO3 + H2O
Көмір қышқыл газының көлемі: V(СО