ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 68
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
2) = 150 мл – 75 мл = 75 мл
Жоғарғы температурада металл күйіндегі мыс арқылы өткізгенде жұтылған газ – артық мөлшерде алынған оттек:
Cu + O2 = 2Cu O
Оттектің артық мөлшерінің көлемі: V артық (O2) = 75 мл
Оттектің әрекеттескен мөлшері: V рак (O2) = 150 мл – 75 мл = 75 мл
Заттың құрамына оттек кіреді.
Реакция схемасы: Cx Hy Oz + O2 = CO2 + H2 O
Көлемдік қатынастар заңына сүйене отырып, коэффиценттерді анықтаймыз:
V(Cx Hy Oz) : Vпрореаг (O2):V (CO2) : V(H2 O)г = 75:75:75:75 = 1:1:1:1.
Бұдан:x =1, y =2, z = 1, ал заттың формуласы CH2 O
11 сынып -5. Изотоптар. 9 балл
Хлорсутек пен дейтерий хлоридінің қоспасы берілген. Қоспадағы хлордың массалық үлесі 96,73 %.қоспадағы дейтерий хлоридінің массалық үлесін анықтаңыздар.
Шешуі: қоспаның массасы 100 г үлгісін қарастырамыз. Қоспадағы атомдық хлордың массасы:
m(Cl) = m (Cl) = 100 * 0,9673 г =96,73 г
(Cl) = 100 * 0,9673 г =96,73 г
Қоспадағы атомаралық сутек пен дейтерийдің массасын есептейміз:
m(H) + m(D) = m – m((Cl) = 100 – 96,73 = 3,27 г
немесе
m(H) + m(D) = 3,27 г (1)
Атомаралық хлордың массасы хлорсутектің құрамындағы m1(Cl) хлор мен дейтерий хлоридінің құрамындағы хлордың m2(Cl) массаларының қосындысынан тұрады:
m(Cl) = m1(Cl) + m2(Cl) (2)
m1(Cl) массасын табамыз: m1(Cl) = n(Cl) * M(Cl) = n1(Cl) * 35,5 (3)
n1(Cl) – HCl құрамындағы атомаралық хлордың зат мөлшері.
HCl құрамындағы атомаралық сутектің массасын табамыз:
m(H) = n( H) * M(H) = n(H) *1 (4)
n(H) – HCl. Құрамындағы атомаралық сутектің зат мөлшерін табамыз:
Хлорсутектің формуласы бойынша:
Демек, (3) и (4) теңдеулерден:
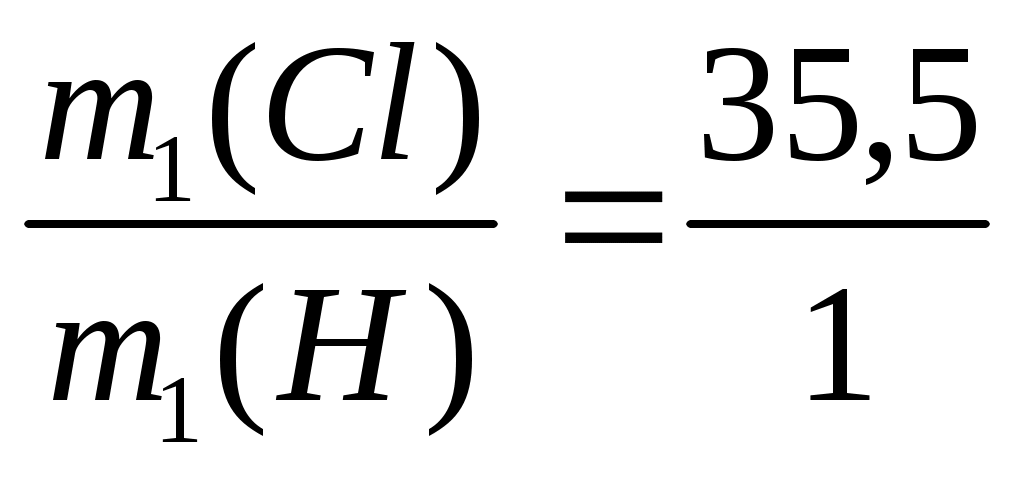 немесе m(Cl)= 35,5 m(H) (5)
немесе m(Cl)= 35,5 m(H) (5)
Сол сияқты, дейтерий хлоридінің формуласы бойынша:
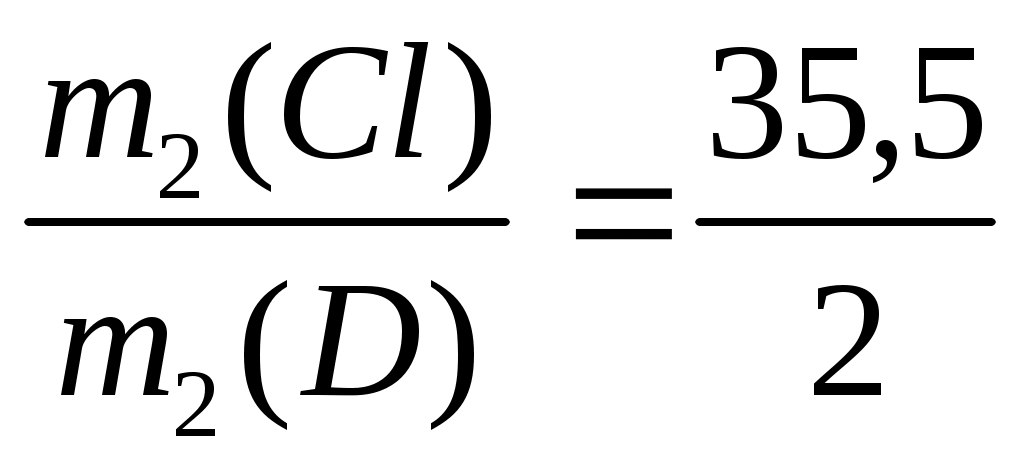 немесе m= 35,5 m(D)/2 (6)
немесе m= 35,5 m(D)/2 (6)
m1(Cl) және m2(Cl) мәндерін (5) және (6) формуллаларға сүйене отырып, m(H) және m(D) арқылы өрнектелген атомаралық хлордың жалпы массасын табамыз:
m(Cl)= 35,5 m(H)+35,5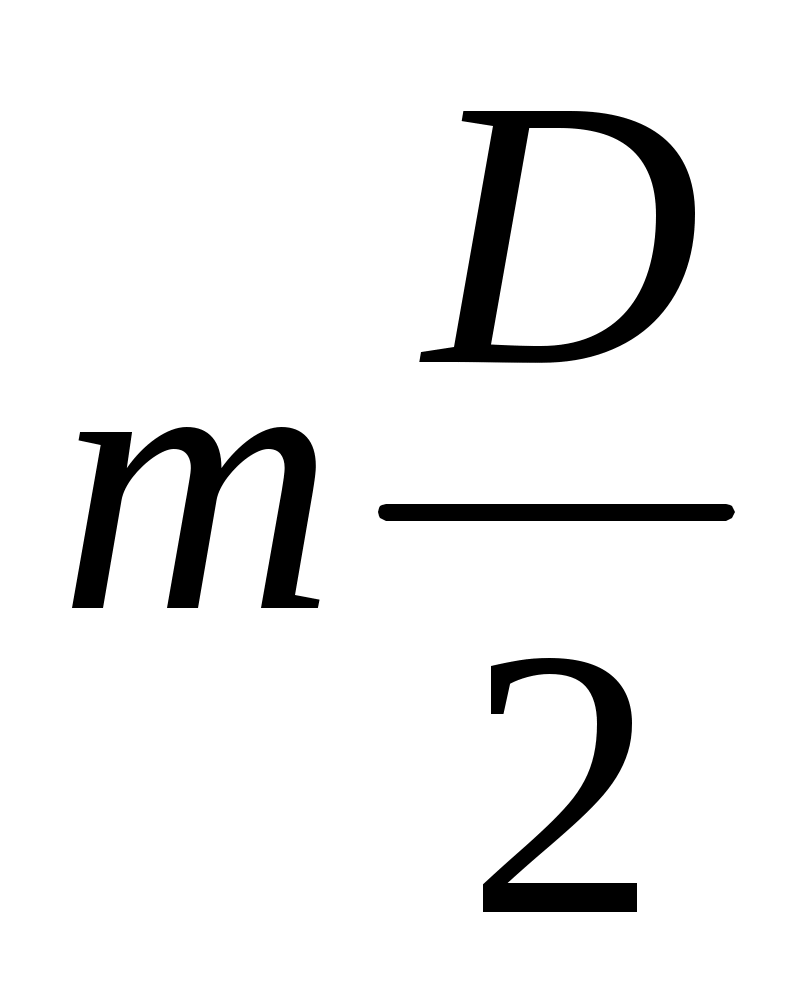
немесе
35,5 m(H)+ 17,75m(D)= 96,73
Екі белгісізі бар (1) және (7) теңдеулер жүйесін аламыз:
m(H)+ m(D) = 3,27 г
35,5 m(H)35,5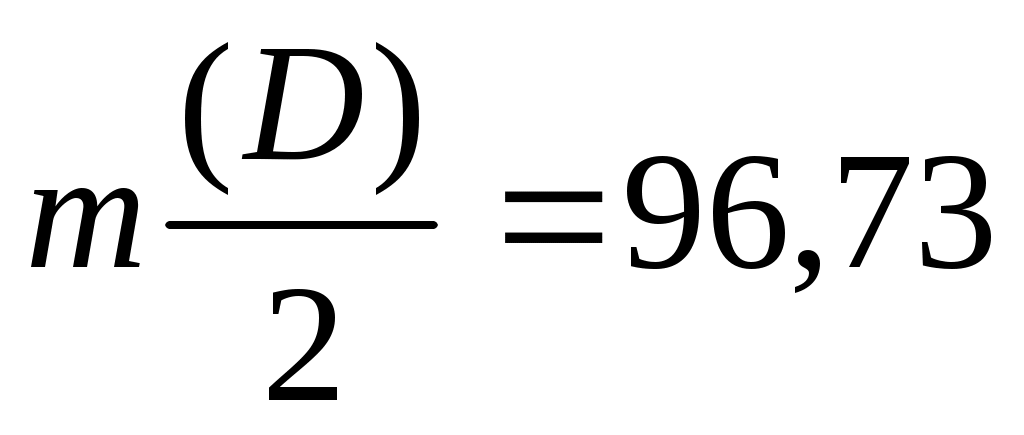
Оны шессек: m(D)= 1,09 г
(6) теңдеуді пайдаланып, дейтерий хлоридінің құрамындағы хлордың массасын табымыз:
m2(Cl) = 17,75 m(D)= 17,75Ч1,09=19,35 г
Дейтерий хлоридінің массасын табамыз:
m(DCl)=m(D)+m(Cl)= 1,09+1935 = 20,44 г.
Қоспадағы дейтерий хлоридінің DCl массалық үлесі:
W(DCl)=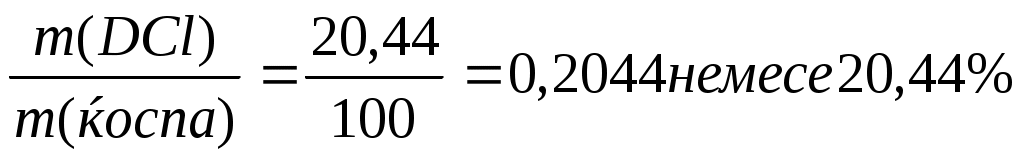
Олимпиада есептері
11 сынып
1-есеп.
Өлшеніп алынған ашудас түзуге бейім белгісіз, сусыз тұз аммиак суында ерітілді. Алынған ерітіндіге көмір қышқыл газын жібергенде немесе оны көп уақыт бойы қайнатқанда ақ тұнба түзіледі. Азот ағынында қыздырылғаннан кейін тұнбаның массасы 9,37г болды. Егер тұнбаның осындай массасы сутегінің ағынында қыздырылса, 8,57г сұр түсті ұнтақ зат түзіледі. Аталған заттардың бәрін анықтағанда, реакция теңдеулерін жазыңдар, өлшеніп алынған белгісіз тұздардың массасын табыңдар.
Шешуі: Белгісіз тұз І және ІІІ топтағы металдардың сульфаты болуы керек, себебі ашудастардың жалпы формуласы
Шешуі: Белгісіз тұз І және ІІІ топтағы металдардың сульфаты болуы керек, себебі ашудастардың жалпы формуласы Me(I)ME(III)(So4)2*12H2O
І топтың металының өкілдері болуы мүмкін емес, себебі олардың гидроксидтері ақ тұнба түзбейді.
Me2(SO4)2+18NH4OH=3(NH4)2SO4+2[Me(NH3)]*(OH)3+12H2O
t0
[Me(NH3)6](OH)3→6NH3+Me(OH)3
[Me(NH3)6](OH)3+3CO2+3H2O=3(NH4)2CO3+Me(OH)3
Бұл ақ түсті металл гидроксидінің қыздырғанда мынадай реакция жүреді
t0
2Ме(ОН)3→Ме2О3+3Н2О
Ал сутек ағынында тотықсыздану процесі жүруі мүмкін:
Ме2О3+3Н2=2Ме+3Н2О
Егер металдың эквиваленттік массасын Х деп белгілесек, онда эквивалент заңы бойынша теңдеу құрамыз.
Х+Э0/Х+m(Me2O3)/m(Me)
X+8/X=9.37/8.57
Бұдан Х=85.7
Ame=85.7*Z
Ame=85.7*3=257.1
Бұл атомдық масса есептің шартына сәйкес келмейді. Демек тотықсыздану процесі металға дейін емес, оксидке дейін жүрген:
Ме2О3+Н2=2МеО+Н2О (1)
Ме2О3+Н2=Ме2О+2Н2О (2)
Егер металдың атомдық массасын Х деп белгілесек, онда (1) реакция теңдеуі бойынша 2х+48/2х+32=9.37/8.57
x=A=69.7
Бұл Ga металы.
Екінші теңдеу бойынша:
2х+48/2х+16=19.37/8.57
x=A=163.4
Бұл атомдық масса есептің шартына сәйкес келмейді. Сонымен бастапқы тұз Ga(SO
4)3. Өлшеніп алынған тұздың массасын былай есептейміз:
М(Ga2(So4)3)/y=M(Ga2O3)/m(Ga2O3)
427.4/y=187.4/9.37
y=21.37г.
№ 2-есеп.
100г этанолдың гександағы ерітіндісі 10,3г натриймен әрекеттеседі. Ерітіндінің осындай мөлшерін 1500С-та алюминий оксидінен өткізгенде ол толық әрекеттесті. Катализдік түтіктен шыққан қоспа қараңғыда 12г бромнан дайындалған, бром суымен реакцияға түседі.
Түтіктен шыққан қоспаның сапалық және сандық құрамын анықтаңыздар.
Шешуі:
Жүретін реакция теңдеулерін жазайық.
2С2Н5ОН+2Na=2C2H5ONa+H2 (1)
C2H5OH→CH2+H2O (2)
2C2H5OH→C2H5-O-C2H5+H2O (3)
CH2=CH2+Br2=CH2Br-CH2Br (4)
1500С температурада (2) және (3) реакция жүреді. (1) және (4) реакция бөлме температурасындада жақсы жүреді. Енді 10,3г натрий массасын зат мөлшеріне (мольге) айналдырайық, VNa=mNa/mNa=10.3г/23г/моль=0,45моль
(1) реакция бойынша 0,45 моль натриймен 0,45 моль этанол әрекеттеседі.
mэт=Vэт*Мэт=0,45*46=20,7г
Онда гексанның (еріткіш) массасы 79,3г (100г-20,7г) тең болады. 12г бромды мольге айналдырсақ, VBr=12г/80=0,15моль тең болады. (4) реакция бойынша 0,15 моль броммен 0,15 моль этилен әрекеттеседі. Демек, (2) реакция бойынша 0,15 моль су түзіледі. Енді (3) теңдеу бойынша реакцияға қатысқан этанолдың мөлшері 0,3 мольге тең болады. Осы реакция бойынша 0,3 моль этанолдан 0,15 моль жай эфир және 0,15 моль су түзіледі. (2) және (3) реакциялар бойынша барлығы 0,3 моль су түзіледі.
Сонымен қоспаның массалық құрамы мынадай болады:
Гексан – 79,3г
Этилен – mэ=0.15 моль
28г/моль=4.2г
Диэтилэфир mэф=0.15*74=11,1г
Су- mсу=0.3моль*18г/моль=5,4
10 сынып
№ 1-есеп.
Қанықпаған 4 көмірсутегінің проценттік құрамдары бірдей: 8,5,7 процент С және 14,3 процент Н. Олардың ауамен салыстырғандағы тығыздықтары 0,98; 1,5; 2,0; 2,43 болса, олар қандай көмірсутектер? Бұл көмірсутектердің алыну реакциялары теңдеулерін жаз. Структуралық (графикалық) формулаларын келтір.
Шешуі:
Ауамен салыстырмалы тығыздықтары негізінде көмірсутектердің жеке-жеке салыстырмалы молекулалық массаларын есептейік:
Dауа= Mr(CxHy)/Mr(ауа)
Mr(ауа)=29;
M1(CxHy)=29*0.98=28.42;
M2(CxHy)=29*1.5=43.5
M3(CxHy)=29*2.58
M4(MxHy)=29*2.43=70.47
Енді көмірсутектердің проценттік құрамы бойынша көміртегі мен сутегінің мөлшерін есептейік:
100г CxHy -85,7г С болса,
28,42г CxHy –х1 г.
Х1=28,42* 85,7/100:=23,25г С;
23,25: 12≈2; екі атом С
100г CxHy -14,3г Н,
28,42г CxHy –х2 г;
х2=28.42*14.3/100=4.1г Н
сутегінің атом саны-4,1:1=47
Бірінші көмірсутегінің формуласы – С2Н4, бұл-этилен;
СН2=CH2-этиленнің графикалық (структуралық) формуласы.
Этиленнің алынуы:
С2Н5ОН*Н2SO4/t0*C2H4↑+H2O немесе С2Н6→С2Н4+Н2;
100г СхНу – 85,7г С;
43,5г СхНу –х3г;
х3=85.7*43.5/100=37.28г С
37,28:12=3 атом С.
100г СхНу –14,3г Н,
43,5г СхНу –х4;
Х4=43,5*14,3/100=6,2г Н.
6,2:1=6 атом Н.
Екінші көмірсутегі С3Н6-пропен, СН2=СН-СН3.
Алынуы:
С3Н8→С3Н6+Н2;
100г СхНу –85,7г С,
58г СхНу –х5 г;
х5=85,7*58/100=49,7г С.
100г СхНу –14,3г Н бар 58г СхНу –х6 г;
х6=58*14,3/100=8,3г Н
8,3:1=8 атом Н№
Үшінші көмірсутегі С4Н8-бутен.
Н2С=СН-СН2-СН3 бутен-1
СН3-СН=СН-СН3 бутен-2
С4Н10→С4Н3+Н2
100г СхНу –85,7г С
100г СхНу –14,3г Н бар
79,47гт СхНу –х8 г
х8=79,47*14,3/100=10,08г Н
10,08:1=10 атом Н№
Төртінші көмірсутегінің формуласы С5Н10-пентен. Кейбір изомерлерінің формуласы мен аттары:
Н2С=СН-СН2-СН3 пентен-1
Н2С=СН-СН2-СН3-СН3 пентен-2
СН3-СН=С-СН3 2-метилбутен-2
|
СН3
Жауабы: С2Н4-этилен, С3Н6-пропилен (пропен), С4Н10-пентен.
Бәрі де қанықпаған көмірсутектерінің өкілдері.
9 – сынып
№ 1-есеп.
41,3г мыс пен мыс(ІІ) оксидінің 88 проценттік күкірт қышқылының біраз мөлшерінде ерітілген. Реакция нәтижесінде, 8,96л газ(қ.ж) бөлінген. Қоспаның алғашқы құрамын және түзілген тұздың мөлшерін есепте.
Шешуі:
Концентрлі күкір қышқылы қоспа құрамындағы екі затпен де әрекеттеседі
Cu+2H2SO4=CuSO2+SO2↓+2H2O
CuO+H2SO4=CuSO4+H2O
Реакция нәтижесінде бөлінген газ күкірт (ІҮ) оксиді SO2. Бөлінген газдың көлемі бойынша әрекеттескен қоспадағы мыстың мөлшерін есептейміз:
Х1 8,96
Cu+2H2SO4=CuSO4+SO2↓2H2O
64г 22,4
х1:8,96=64:22,4;
х1=25,6г Cu.
Қоспа құрамындағы мыс(ІІ) оксидінің мөлшері 41,3-25,6=15,7г болады. Есептің шартына сәйкес түзілген тұздың мөлшерін есептесек:
25,6 х2
Cu2H2SO4=CuSO4+SO2↓+2H2O
25.6:x2=64:160, бұдан
х2=25.6*100/64=64г CuSO4
CuO+H2SO4=CuSO4+H2O
80 160
15.7:x3=80:160, бұдан
х2=15.7*160/80=31.4г CuSO4
Барлық түзілген тұздың мөлшері
64+31,4=95.4г.
Жауабы 25,6г Cu 15,7г CuO, 95,4г Cu SO4
№ 2-есеп.
81,95г калий хлориді, калий нитраты және бертолет тұздарының қоспасы массалары тұрақталғанда дейін қатты қыздырылған кезде газ бөлінген. Ол газды сутегімен әрекеттестіргенде, 14,4г су түзілген. Қатты қыздырылғаннан кейінгі өнім суда ерітіліп, күміс нитратының ерітіндісімен өңделген. Сонда 100,45г тұнба түзілген. Қоспаның проценттік құрамын анықтаңдар.
Шешуі:
Қатты қыздырғанда, калий нитраты мен бертолет тұзы айырылып, оттегі бөлінеді:
2КNO3=2KNO2+O2↑ (1)
2KCIO3=2KCI+3O2↑ (2)
Бөлінген оттегінің сутегімен әрекеттесуі нәтижесінде түзілген судың мөлшерін біле отырып, оған кеткен оттегінің мөлшерін есептейміз:
Х1 14,4
2Н2+О2=2H2O
x1:14.4=32:36, бұдан
х1=14.4*32/36=12.8г О2;
Оттегінің бұл мөлшері екі тұздың (КNO3 мен KCIO3) айыру нәтижесінде түзілгенін ескере осынша мөлшерде газ түзілу үшін қанша тұздар айырылғанын (1) және (2) теңдеулер бойынша есептейміз. Екі теңдеудің сол жақ бөлігін, оң жақ бөлігіне оң жақ бөлігін қосып, төмендегідей теңдеу құрайық:
2KNO3+2KCI3=2KNO3+2KCI+4O2↑ (3)
Бұл теңдеудегі коэффициенттер жұп санды болғандықтан, екіге қысқартып, төмендегідей теңдеу аламыз:
KNO3+KCIO3=KNO2+KCI+2O2↑ (4)
Осы теңдеуді (4) пайдаланып, 12,8г О2 түзілу үшін қоспада KNO3 пен KCIO3 –тің мөлшері қандай екенін есептейміз:
Х2 12,8
KNO3+KCIO3/223,5=KNO2+KCI+2O2↑
64
x2:12.8=223.5:64, бұдан
х2=12.8*223.5/64=44.7KNO3 пен KCIO3
Енді әуелгі қоспадағы калий хлоридінің мөлшерін табайық:
81,95-44,7=37,25г KCI
Қатты қыздырғаннан кейінгі қалдық құрамындағы калий хлоридінің мөлшерін күміс нитратымен әрекеттескеннен кейінгі түзілген тұнбаның мөлшері бойынша табамыз:
Х3 100,45
KCI+AgNO3=AgCI↓+KNO3 (5)
x3:100.45=74.5:143.5 бұдан
х3=100.45*74.5/143.5=52.15г KCI
Бертолет тұзы айырылуы кезінде түзілген калий хлоридінің мөлшері:
Жоғарғы температурада металл күйіндегі мыс арқылы өткізгенде жұтылған газ – артық мөлшерде алынған оттек:
Cu + O2 = 2Cu O
Оттектің артық мөлшерінің көлемі: V артық (O2) = 75 мл
Оттектің әрекеттескен мөлшері: V рак (O2) = 150 мл – 75 мл = 75 мл
Заттың құрамына оттек кіреді.
Реакция схемасы: Cx Hy Oz + O2 = CO2 + H2 O
Көлемдік қатынастар заңына сүйене отырып, коэффиценттерді анықтаймыз:
V(Cx Hy Oz) : Vпрореаг (O2):V (CO2) : V(H2 O)г = 75:75:75:75 = 1:1:1:1.
Бұдан:x =1, y =2, z = 1, ал заттың формуласы CH2 O
11 сынып -5. Изотоптар. 9 балл
Хлорсутек пен дейтерий хлоридінің қоспасы берілген. Қоспадағы хлордың массалық үлесі 96,73 %.қоспадағы дейтерий хлоридінің массалық үлесін анықтаңыздар.
Шешуі: қоспаның массасы 100 г үлгісін қарастырамыз. Қоспадағы атомдық хлордың массасы:
m(Cl) = m
Қоспадағы атомаралық сутек пен дейтерийдің массасын есептейміз:
m(H) + m(D) = m – m((Cl) = 100 – 96,73 = 3,27 г
немесе
m(H) + m(D) = 3,27 г (1)
Атомаралық хлордың массасы хлорсутектің құрамындағы m1(Cl) хлор мен дейтерий хлоридінің құрамындағы хлордың m2(Cl) массаларының қосындысынан тұрады:
m(Cl) = m1(Cl) + m2(Cl) (2)
m1(Cl) массасын табамыз: m1(Cl) = n(Cl) * M(Cl) = n1(Cl) * 35,5 (3)
n1(Cl) – HCl құрамындағы атомаралық хлордың зат мөлшері.
HCl құрамындағы атомаралық сутектің массасын табамыз:
m(H) = n( H) * M(H) = n(H) *1 (4)
n(H) – HCl. Құрамындағы атомаралық сутектің зат мөлшерін табамыз:
Хлорсутектің формуласы бойынша:
Демек, (3) и (4) теңдеулерден:
Сол сияқты, дейтерий хлоридінің формуласы бойынша:
m1(Cl) және m2(Cl) мәндерін (5) және (6) формуллаларға сүйене отырып, m(H) және m(D) арқылы өрнектелген атомаралық хлордың жалпы массасын табамыз:
m(Cl)= 35,5 m(H)+35,5
немесе
35,5 m(H)+ 17,75m(D)= 96,73
Екі белгісізі бар (1) және (7) теңдеулер жүйесін аламыз:
m(H)+ m(D) = 3,27 г
35,5 m(H)35,5
Оны шессек: m(D)= 1,09 г
(6) теңдеуді пайдаланып, дейтерий хлоридінің құрамындағы хлордың массасын табымыз:
m2(Cl) = 17,75 m(D)= 17,75Ч1,09=19,35 г
Дейтерий хлоридінің массасын табамыз:
m(DCl)=m(D)+m(Cl)= 1,09+1935 = 20,44 г.
Қоспадағы дейтерий хлоридінің DCl массалық үлесі:
W(DCl)=
Олимпиада есептері
11 сынып
1-есеп.
Өлшеніп алынған ашудас түзуге бейім белгісіз, сусыз тұз аммиак суында ерітілді. Алынған ерітіндіге көмір қышқыл газын жібергенде немесе оны көп уақыт бойы қайнатқанда ақ тұнба түзіледі. Азот ағынында қыздырылғаннан кейін тұнбаның массасы 9,37г болды. Егер тұнбаның осындай массасы сутегінің ағынында қыздырылса, 8,57г сұр түсті ұнтақ зат түзіледі. Аталған заттардың бәрін анықтағанда, реакция теңдеулерін жазыңдар, өлшеніп алынған белгісіз тұздардың массасын табыңдар.
Шешуі: Белгісіз тұз І және ІІІ топтағы металдардың сульфаты болуы керек, себебі ашудастардың жалпы формуласы
Шешуі: Белгісіз тұз І және ІІІ топтағы металдардың сульфаты болуы керек, себебі ашудастардың жалпы формуласы Me(I)ME(III)(So4)2*12H2O
І топтың металының өкілдері болуы мүмкін емес, себебі олардың гидроксидтері ақ тұнба түзбейді.
Me2(SO4)2+18NH4OH=3(NH4)2SO4+2[Me(NH3)]*(OH)3+12H2O
t0
[Me(NH3)6](OH)3→6NH3+Me(OH)3
[Me(NH3)6](OH)3+3CO2+3H2O=3(NH4)2CO3+Me(OH)3
Бұл ақ түсті металл гидроксидінің қыздырғанда мынадай реакция жүреді
t0
2Ме(ОН)3→Ме2О3+3Н2О
Ал сутек ағынында тотықсыздану процесі жүруі мүмкін:
Ме2О3+3Н2=2Ме+3Н2О
Егер металдың эквиваленттік массасын Х деп белгілесек, онда эквивалент заңы бойынша теңдеу құрамыз.
Х+Э0/Х+m(Me2O3)/m(Me)
X+8/X=9.37/8.57
Бұдан Х=85.7
Ame=85.7*Z
Ame=85.7*3=257.1
Бұл атомдық масса есептің шартына сәйкес келмейді. Демек тотықсыздану процесі металға дейін емес, оксидке дейін жүрген:
Ме2О3+Н2=2МеО+Н2О (1)
Ме2О3+Н2=Ме2О+2Н2О (2)
Егер металдың атомдық массасын Х деп белгілесек, онда (1) реакция теңдеуі бойынша 2х+48/2х+32=9.37/8.57
x=A=69.7
Бұл Ga металы.
Екінші теңдеу бойынша:
2х+48/2х+16=19.37/8.57
x=A=163.4
Бұл атомдық масса есептің шартына сәйкес келмейді. Сонымен бастапқы тұз Ga(SO
4)3. Өлшеніп алынған тұздың массасын былай есептейміз:
М(Ga2(So4)3)/y=M(Ga2O3)/m(Ga2O3)
427.4/y=187.4/9.37
y=21.37г.
№ 2-есеп.
100г этанолдың гександағы ерітіндісі 10,3г натриймен әрекеттеседі. Ерітіндінің осындай мөлшерін 1500С-та алюминий оксидінен өткізгенде ол толық әрекеттесті. Катализдік түтіктен шыққан қоспа қараңғыда 12г бромнан дайындалған, бром суымен реакцияға түседі.
Түтіктен шыққан қоспаның сапалық және сандық құрамын анықтаңыздар.
Шешуі:
Жүретін реакция теңдеулерін жазайық.
2С2Н5ОН+2Na=2C2H5ONa+H2 (1)
C2H5OH→CH2+H2O (2)
2C2H5OH→C2H5-O-C2H5+H2O (3)
CH2=CH2+Br2=CH2Br-CH2Br (4)
1500С температурада (2) және (3) реакция жүреді. (1) және (4) реакция бөлме температурасындада жақсы жүреді. Енді 10,3г натрий массасын зат мөлшеріне (мольге) айналдырайық, VNa=mNa/mNa=10.3г/23г/моль=0,45моль
(1) реакция бойынша 0,45 моль натриймен 0,45 моль этанол әрекеттеседі.
mэт=Vэт*Мэт=0,45*46=20,7г
Онда гексанның (еріткіш) массасы 79,3г (100г-20,7г) тең болады. 12г бромды мольге айналдырсақ, VBr=12г/80=0,15моль тең болады. (4) реакция бойынша 0,15 моль броммен 0,15 моль этилен әрекеттеседі. Демек, (2) реакция бойынша 0,15 моль су түзіледі. Енді (3) теңдеу бойынша реакцияға қатысқан этанолдың мөлшері 0,3 мольге тең болады. Осы реакция бойынша 0,3 моль этанолдан 0,15 моль жай эфир және 0,15 моль су түзіледі. (2) және (3) реакциялар бойынша барлығы 0,3 моль су түзіледі.
Сонымен қоспаның массалық құрамы мынадай болады:
Гексан – 79,3г
Этилен – mэ=0.15 моль
28г/моль=4.2г
Диэтилэфир mэф=0.15*74=11,1г
Су- mсу=0.3моль*18г/моль=5,4
10 сынып
№ 1-есеп.
Қанықпаған 4 көмірсутегінің проценттік құрамдары бірдей: 8,5,7 процент С және 14,3 процент Н. Олардың ауамен салыстырғандағы тығыздықтары 0,98; 1,5; 2,0; 2,43 болса, олар қандай көмірсутектер? Бұл көмірсутектердің алыну реакциялары теңдеулерін жаз. Структуралық (графикалық) формулаларын келтір.
Шешуі:
Ауамен салыстырмалы тығыздықтары негізінде көмірсутектердің жеке-жеке салыстырмалы молекулалық массаларын есептейік:
Dауа= Mr(CxHy)/Mr(ауа)
Mr(ауа)=29;
M1(CxHy)=29*0.98=28.42;
M2(CxHy)=29*1.5=43.5
M3(CxHy)=29*2.58
M4(MxHy)=29*2.43=70.47
Енді көмірсутектердің проценттік құрамы бойынша көміртегі мен сутегінің мөлшерін есептейік:
100г CxHy -85,7г С болса,
28,42г CxHy –х1 г.
Х1=28,42* 85,7/100:=23,25г С;
23,25: 12≈2; екі атом С
100г CxHy -14,3г Н,
28,42г CxHy –х2 г;
х2=28.42*14.3/100=4.1г Н
сутегінің атом саны-4,1:1=47
Бірінші көмірсутегінің формуласы – С2Н4, бұл-этилен;
СН2=CH2-этиленнің графикалық (структуралық) формуласы.
Этиленнің алынуы:
С2Н5ОН*Н2SO4/t0*C2H4↑+H2O немесе С2Н6→С2Н4+Н2;
100г СхНу – 85,7г С;
43,5г СхНу –х3г;
х3=85.7*43.5/100=37.28г С
37,28:12=3 атом С.
100г СхНу –14,3г Н,
43,5г СхНу –х4;
Х4=43,5*14,3/100=6,2г Н.
6,2:1=6 атом Н.
Екінші көмірсутегі С3Н6-пропен, СН2=СН-СН3.
Алынуы:
С3Н8→С3Н6+Н2;
100г СхНу –85,7г С,
58г СхНу –х5 г;
х5=85,7*58/100=49,7г С.
100г СхНу –14,3г Н бар 58г СхНу –х6 г;
х6=58*14,3/100=8,3г Н
8,3:1=8 атом Н№
Үшінші көмірсутегі С4Н8-бутен.
Н2С=СН-СН2-СН3 бутен-1
СН3-СН=СН-СН3 бутен-2
С4Н10→С4Н3+Н2
100г СхНу –85,7г С
100г СхНу –14,3г Н бар
79,47гт СхНу –х8 г
х8=79,47*14,3/100=10,08г Н
10,08:1=10 атом Н№
Төртінші көмірсутегінің формуласы С5Н10-пентен. Кейбір изомерлерінің формуласы мен аттары:
Н2С=СН-СН2-СН3 пентен-1
Н2С=СН-СН2-СН3-СН3 пентен-2
СН3-СН=С-СН3 2-метилбутен-2
|
СН3
Жауабы: С2Н4-этилен, С3Н6-пропилен (пропен), С4Н10-пентен.
Бәрі де қанықпаған көмірсутектерінің өкілдері.
9 – сынып
№ 1-есеп.
41,3г мыс пен мыс(ІІ) оксидінің 88 проценттік күкірт қышқылының біраз мөлшерінде ерітілген. Реакция нәтижесінде, 8,96л газ(қ.ж) бөлінген. Қоспаның алғашқы құрамын және түзілген тұздың мөлшерін есепте.
Шешуі:
Концентрлі күкір қышқылы қоспа құрамындағы екі затпен де әрекеттеседі
Cu+2H2SO4=CuSO2+SO2↓+2H2O
CuO+H2SO4=CuSO4+H2O
Реакция нәтижесінде бөлінген газ күкірт (ІҮ) оксиді SO2. Бөлінген газдың көлемі бойынша әрекеттескен қоспадағы мыстың мөлшерін есептейміз:
Х1 8,96
Cu+2H2SO4=CuSO4+SO2↓2H2O
64г 22,4
х1:8,96=64:22,4;
х1=25,6г Cu.
Қоспа құрамындағы мыс(ІІ) оксидінің мөлшері 41,3-25,6=15,7г болады. Есептің шартына сәйкес түзілген тұздың мөлшерін есептесек:
25,6 х2
Cu2H2SO4=CuSO4+SO2↓+2H2O
-
160
25.6:x2=64:160, бұдан
х2=25.6*100/64=64г CuSO4
-
x3
CuO+H2SO4=CuSO4+H2O
80 160
15.7:x3=80:160, бұдан
х2=15.7*160/80=31.4г CuSO4
Барлық түзілген тұздың мөлшері
64+31,4=95.4г.
Жауабы 25,6г Cu 15,7г CuO, 95,4г Cu SO4
№ 2-есеп.
81,95г калий хлориді, калий нитраты және бертолет тұздарының қоспасы массалары тұрақталғанда дейін қатты қыздырылған кезде газ бөлінген. Ол газды сутегімен әрекеттестіргенде, 14,4г су түзілген. Қатты қыздырылғаннан кейінгі өнім суда ерітіліп, күміс нитратының ерітіндісімен өңделген. Сонда 100,45г тұнба түзілген. Қоспаның проценттік құрамын анықтаңдар.
Шешуі:
Қатты қыздырғанда, калий нитраты мен бертолет тұзы айырылып, оттегі бөлінеді:
2КNO3=2KNO2+O2↑ (1)
2KCIO3=2KCI+3O2↑ (2)
Бөлінген оттегінің сутегімен әрекеттесуі нәтижесінде түзілген судың мөлшерін біле отырып, оған кеткен оттегінің мөлшерін есептейміз:
Х1 14,4
2Н2+О2=2H2O
-
36
x1:14.4=32:36, бұдан
х1=14.4*32/36=12.8г О2;
Оттегінің бұл мөлшері екі тұздың (КNO3 мен KCIO3) айыру нәтижесінде түзілгенін ескере осынша мөлшерде газ түзілу үшін қанша тұздар айырылғанын (1) және (2) теңдеулер бойынша есептейміз. Екі теңдеудің сол жақ бөлігін, оң жақ бөлігіне оң жақ бөлігін қосып, төмендегідей теңдеу құрайық:
2KNO3+2KCI3=2KNO3+2KCI+4O2↑ (3)
Бұл теңдеудегі коэффициенттер жұп санды болғандықтан, екіге қысқартып, төмендегідей теңдеу аламыз:
KNO3+KCIO3=KNO2+KCI+2O2↑ (4)
Осы теңдеуді (4) пайдаланып, 12,8г О2 түзілу үшін қоспада KNO3 пен KCIO3 –тің мөлшері қандай екенін есептейміз:
Х2 12,8
KNO3+KCIO3/223,5=KNO2+KCI+2O2↑
64
x2:12.8=223.5:64, бұдан
х2=12.8*223.5/64=44.7KNO3 пен KCIO3
Енді әуелгі қоспадағы калий хлоридінің мөлшерін табайық:
81,95-44,7=37,25г KCI
Қатты қыздырғаннан кейінгі қалдық құрамындағы калий хлоридінің мөлшерін күміс нитратымен әрекеттескеннен кейінгі түзілген тұнбаның мөлшері бойынша табамыз:
Х3 100,45
KCI+AgNO3=AgCI↓+KNO3 (5)
-
143.5
x3:100.45=74.5:143.5 бұдан
х3=100.45*74.5/143.5=52.15г KCI
Бертолет тұзы айырылуы кезінде түзілген калий хлоридінің мөлшері: