ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 121
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Общие константы устойчивости комплексных ионов 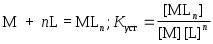
| Комплексный ион | Куст | lg Куст |
| | Аммиачные | |
| Ag(NH3)2+ | 1,74 107 | 7,24 |
| Cd(NH3)42+ | 3,63 106 | 6,56 |
| Co(NH3)62+ | 2,45 104 | 4,39 |
| Co(NH3)63+ | 1,99 1035 | 35,2 |
| Cu(NH3)2+ | 7,25 1010 | 10,86 |
| Cu(NH3)42+ | 1,07 1012 | 12,03 |
| Hg(NH3)42+ | 1,99 1019 | 19,3 |
| Ni(NH3)62+ | 1,02 108 | 8,01 |
| Zn(NH3)42+ | 5,01 108 | 8,7 |
| | Бромидные | |
| AgBr2– | 2,19 107 | 7,34 |
| AuBr2– | 2,88 1012 | 12,46 |
| BiBr4– | 6,92 107 | 7,84 |
| HgBr42– | 1,00 1021 | 21,00 |
| Комплексный ион | Куст | lg Куст |
| | Гидроксидные | |
| Ag(OH)2– | 1,00 104 | 4,0 |
| Al(OH)4– | 1,0 1033 | 33,0 |
| Au(OH)4– | 1,00 1033 | 33,0 |
| Be(OH)42– | 1,0 1015 | 15,0 |
| Cd(OH)42– | 2,63 108 | 8,42 |
| Cr(OH)4– | 7,94 1029 | 29,9 |
| Cu(OH)42– | 3,63 1014 | 14,56 |
| Fe(OH)42– | 3,63 108 | 8,56 |
| Fe(OH)4– | 2,6 1034 | 34,4 |
| Sb(OH)4– | 2,0 1038 | 38,3 |
| Zn(OH)42– | 5,02 1017 | 17,70 |
| | Иодидные | |
| AgI2– | 5,5 1011 | 11,74 |
| BiI4– | 8,91 1014 | 14,95 |
| CdI42– | 2,24 105 | 5,35 |
| HgI42– | 6,76 1029 | 29,83 |
| PbI42– | 8,32 103 | 3,92 |
| ZnI42– | 3,1 10-1 | -0,51 |
| Нитритные | ||
| Ag(NO2)2– | 6,76 102 | 2,83 |
| Оксалатные | ||
| Cr(C2O4H)3 | 2,6 1015 | 15,4 |
| Fe(C2O4H)3 | 1,70 1020 | 20,23 |
| Роданидные | ||
| Ag(SCN)2– | 1,7 108 | 8,23 |
| Cd(SCN)42– | 7,9 102 | 2,91 |
| Co(SCN)42– | 5,12 10-1 | -0,309 |
| Cr(SCN)63– | 6,3 103 | 3,8 |
| Cu(SCN)42– | 3,3 106 | 6,52 |
| Pb(SCN)42– | 0,71 | 0,85 |
| Zn(SCN)42– | 1,1 103 | 3,02 |
| Fe(CNS)63– | 1,70 103 | 3,23 |
| Комплексный ион | Куст | lg Куст |
| Fe(CNS)4– | 3,39 104 | 4,53 |
| Fe(CNS)2+ | 2,20 104 | 4,33 |
| Hg(CNS)42– | 1,7 1021 | 21,23 |
| Тиосульфатные | ||
| Ag(S2O3)23-– | 2,88 1013 | 13,46 |
| Cu(S2O3)23– | 1,86 1012 | 12,27 |
| Фторидные | ||
| AlF63– | 4,68 1020 | 20,67 |
| BeF42– | 2,45 1013 | 13,39 |
| FeF63– | 1,26 1016 | 16,10 |
| Хлоридные | ||
| AgCl2– | 1,1 105 | 5,04 |
| AuCl2– | 2,63 109 | 9,42 |
| AuCl4– | 2,0 1021 | 21,30 |
| BiCl63– | 2,63 106 | 6,42 |
| CuCl2– | 2,24 105 | 5,35 |
| HgCl42– | 1,66 1015 | 15,22 |
| SnCl42– | 30,2 | 1,48 |
| SnCl62– | 6,61 106 | 6,82 |
| Цианидные | ||
| Ag(CN)2– | 7,08 1019 | 19,85 |
| Au(CN)2– | 2,0 1038 | 38,3 |
| Au(CN)4– | 1056 | 56 |
| Cd(CN)42– | 1,29 1017 | 17,11 |
| Co(CN)64– | 1,23 1019 | 19,09 |
| Co(CN)63– | 1 1064 | 64 |
| Cu(CN)2– | 1,00 1024 | 24 |
| Fe(CN)64– | 7,94 1036 | 36,9 |
| Fe(CN)63– | 7,94 1043 | 43,9 |
| Hg(CN)42– | 9,33 1038 | 38,97 |
| Ni(CN)42– | 1,0 1031 | 31,0 |
| Цитратные | ||
| Fe[(СН2)2 С(ОН)(СОО)3] | 2,6 1011 | 11,4 |
Стандартные электродные потенциалы некоторых систем
в водных растворах
| Уравнение процесса | Е0, В |
| Азот | |
| 3N2+2e =2N3 | -3,4 |
| N2+4H2O+2e =2NH2OH+2OH | -3,04 |
| N2+4H2O+4e =N2H4+4OH | -1,16 |
| N2+8H++6e=2NH4 | 0,26 |
| NO2 +H2O+e =NO+2OH | -0,46 |
| 2NO2 +4H2O+6e =N2+8OH | 0,41 |
| NO3 +2H2O+3e =NO+4OH | -0,14 |
| NO3 +H2O+2e =NO2+2OH | -0,01 |
| NO3 +2H+ + e =NO2+H2O | 0,80 |
| NO3 +10H+ +8e =NH4+ +3H2O | 0,87 |
| NO3 +3H+ +2e =HNO2+H2O | 0,94 |
| NO3 +4H+ +3e =NO+2H2O | 0,957 |
| 2HNO2+6H+ +6e =N2+4H2O | 1,44 |
| HNO2+H+ + e =NO+H2O | 0,99 |
| Алюминий | |
| AlO2 +2H2O+3e =Al+4OH | -2,35 |
| Al(OH)3+3e=Al+3OH– | -2,29 |
| AlF63 +3e =Al+6F | -2,07 |
| Al3+ +3e =Al | -1,663 |
| Барий | |
| Ba2+ +2e =Ba | -2,905 |
| Бериллий | |
| Be2+ +2e =Be | -1,97 |
| Бор | |
| BF4 +3e =B+4F | -1,04 |
| BO33 +6H+ +3e =B+3H2O | -0,165 |
| Бром | |
| BrO +H2O+2e =Br +2OH | 0,76 |
| Br2+2e =2Br | 1,065 |
| BrO3 +6H+ +6e =Br +3H2O | 1,44 |
| Уравнение процесса | Е0, В |
| 2BrO3 +12H+ +10e =Br2 +6H2O | 1,52 |
| BrO4 +2H+ +2e = BrO3 +H2O | 1,88 |
| Ванадий | |
| V2++ 2e =V | -1,186 |
| V3+ +3e =V | -0,87 |
| V3+ +e =V2+ | -0,255 |
| VO2++ 2H+ +e =V3++H2O | 0,337 |
| VO2+ +e =VO+ | -0,044 |
| VO2+ +2H+ +e =VO2++H2O | 1,00 |
| VO2+ +4H+ +2e =V3++2H2O | 0,668 |
| VO2+ +4H+ +3e =V2++2H2O | 0,36 |
| VO2+ +4H+ +5e =V+2H2O | -0,25 |
| Висмут | |
| Bi(OH)3 +3e =Bi+3OH | -0,46 |
| BiO3– +6H+ +2e =Bi3++3H2O | 1,81 |
| Водород | |
| H2 +2e =2H | -2,251 |
| 2H2O+2e =H2+2OH | -0,828 |
| 2H+ +2e =H2 | 0,000 |
| Вольфрам | |
| WO42 +4H2O+6e =W+6OH | -1,05 |
| WO42 +8H+ +6e =W+4H2O | 0,049 |
| Галлий | |
| Ga3+ +3e =Ga | -0,53 |
| Гафний | |
| Hf 4+ +4e =Hf | -1,70 |
| Германий | |
| H2GeO3 +4H+ +2e =Ge2+ +3H2O | -0,363 |
| H2GeO3 +4H+ +4e =Ge +3H2O | -0,13 |
| Ge2+ +2e =Ge | 0,000 |
| Железо | |
| Fe(OH)3 + e =Fe(OH)2 +OH | -0,53 |
| Fe(OH)2 +2e =Fe+2OH | -0,877 |
| Fe3O4+8H++2e=3Fe2++4H2O | 1,21 |
| Уравнение процесса | Е0, В |
| Fe3O4+8H++8e=3Fe+4H2O | -0,085 |
| Fe2+ +2e =Fe | -0,440 |
| Fe3+ +3e =Fe | -0,037 |
| Fe(CN)63 + e = Fe(CN)64 | 0,356 |
| Fe3+ + e =Fe2+ | 0,771 |
| FeO42 +8H+ +3e =Fe3+ +4H2O | 1,700 |
| Золото | |
| Au(CN) + e =Au+2CN | -0,61 |
| Au3+ +2e =Au+ | 1,401 |
| Au3+ +3e =Au | 1,498 |
| Au+ +e =Au | 1,692 |
| Иод | |
| 2IO3 +6H2O+10e =I2 +12OH | 0,21 |
| IO3 +3H2O+6e =I +6OH | 0,25 |
| 2IO +2H2O+2e =I2 +4OH | 0,45 |
| IO +H2O+2e =I +2OH | 0,49 |
| I2 +2e =2I | 0,536 |
| 2IO3 +12H+ +10e =I2 +6H2O | 1,19 |
| IO3 +6H+ +6e =I– +3H2O | 1,08 |
| 2HIO +2H+ +2e =I2 +2H2O | 1,45 |
| H5IO6 +H+ +2e =IO3 +3H2O | 1,6 |
| IO4 +2H+ +2e =IO3 +H2O | 1,64 |
| Кадмий | |
| Cd(CN)42 +2e =Cd +4CN | -1,09 |
| Cd(NH3)42+ +2e =Cd +4NH3 | -0,61 |
| Cd2+ +2e = Cd | -0,403 |
| Калий | |
| K+ +e =K | -2,924 |
| Кальций | |
| Ca2+ +2e =Ca | -2,866 |
| Кислород | |
| O2 +2H2O+4e =4OH | 0,401 |
| O2 +2H+ +2e =H2O2 | 0,682 |
| O2 +4H+ +4e =2H2O | 1,228 |
| Уравнение процесса | Е0, В |
| H2O2 +2H+ +2e =2H2O | 1,776 |
| O3 +H2O +2e =O2 +2OH– | 1,24 |
| O3 +2H+ +2e =O2 +H2O | 2,07 |
| Кобальт | |
| Co(CN)63 + e =Co(CN)64 | -0,83 |
| Co2+ +2e =Co | -0,277 |
| Co(NH3)63+ + e = Co(NH3)62+ | 0,1 |
| Co(OH)3 + e =Co(OH)2 +OH | 0,17 |
| Co3+ +3e =Co | 0,33 |
| Co3+ + e =Co2+ | 1,808 |
| Кремний | |
| Si+4H++4e=SiH4 | 0,10 |
| SiO2+4H++4e=Si+2H2O | -0,86 |
| SiO32 +3H2O +4e =Si+6OH | -1,7 |
| SiF62 +4e =Si+6F | -1,2 |
| SiO32 +6H+ +4e =Si+3H2O | -0,455 |
| Литий | |
| Li+ + e =Li | -3,045 |
| Магний | |
| Mg2+ +2e =Mg | -2,363 |
| Марганец | |
| Mn2+ +2e =Mn | -1,179 |
| MnO4 + e =MnO42 | 0,564 |
| MnO4 +2H2O+3e =MnO2 +4OH | 0,60 |
| MnO2 +4H+ +2e =Mn2+ +2H2O | 1,228 |
| MnO4 +8H+ +5e =Mn2+ +4H2O | 1,507 |
| Mn3+ + e =Mn2+ | 1,509 |
| MnO4 +4H+ +3e =MnO2 +2H2O | 1,692 |
| MnO42 +4H+ +2e =MnO2 +2H2O | 2,257 |
| Медь | |
| Cu(CN)2 + e =Cu+2CN | -0,43 |
| Cu(NH3)42+ +2e =Cu+4NH3 CuI+ e =Cu+I | -0,07 -0,185 |
| Уравнение процесса | Е0, В |
| Cu2+ +2e =Cu | 0,337 |
| Cu+ + e =Cu | 0,52 |
| Cu2+ +Cl + e =CuCl | 0,53 |
| Cu2+ +Br + e =CuBr | 0,64 |
| Cu2+ +I + e =CuI | 0,84 |
| Cu2+ +2CN + e =Cu(CN)2 | 1,12 |
| Молибден | |
| Mo3+ +3e =Mo | -0,200 |
| MoO42 +8H+ +6e =Mo+4H2O | 0,154 |
| Мышьяк | |
| As+3H++3e =AsH3 | -0,60 |
| H3AsO4 +2H+ +2e =HAsO2 +2H2O | 0,56 |
| AsO43 +2H2O+2e =AsO2 +4OH | -0,71 |
| Натрий | |
| Na+ +e =Na | -2,714 |
| Никель | |
| Ni2+ +2e =Ni | -0,250 |
| Ni(OH)3 + e =Ni(OH)2 +OH | 0,49 |
| Ниобий | |
| Nb3+ +3e =Nb | -1,1 |
| Nb2O5 +10H+ +10e =2Nb+5H2O | -0,65 |
| Олово | |
| Sn(OH)62 +2e =HSnO2 +3OH +H2O | -0,90 |
| SnCl42 +2e =Sn+4Cl | -0,19 |
| SnF62 +4e =Sn+6F | -0,25 |
| Sn2+ +2e =Sn | -0,136 |
| SnO2 +4H+ +4e =Sn +2H2O | -0,106 |
| Sn4+ +4e =Sn | 0,01 |
| Sn4+ +2e =Sn2+ | 0,151 |
| Осмий | |
| OsO4 +8H+ +8e =Os+4H2O | 0,85 |
| Os2+ +2e =Os | 0,85 |
| Палладий | |
| Pd2+ +2e =Pd | 0,987 |
| Уравнение процесса | Е0, В |
| PdCl62 +2e =PdCl42 +2Cl | 1,288 |
| Платина | |
| Pt2+ +2e =Pt | 1,188 |
| Рений | |
| ReO4 +4H2O+7e =Re+8OH | -0,584 |
| Re3+ +3e =Re | -0,18 |
| ReO4 +8H+ +7e =Re+4H2O | 0,37 |
| Родий | |
| Rh3+ +3e =Rh | 0,8 |
| Ртуть | |
| Hg(CN)42 +2e =Hg+4CN | -0,37 |
| Hg22+ +2e =2Hg | 0,788 |
| Hg2Cl2 +2e =2Hg+2Cl– | 0,27 |
| Hg2+ +2e =Hg | 0,850 |
| 2Hg2+ +2e =Hg22+ | 0,920 |
| Рубидий | |
| Rb+ + e =Rb | -2,925 |
| Рутений | |
| Ru+ +2e =Ru | 0,45 |
| RuO2 +4H+ +4e =Ru+2H2O | 0,79 |
| Свинец | |
| Pb2+ +2e =Pb | -0,126 |
| PbO32 +H2O+2e =PbO22 +2OH | 0,2 |
| PbO2 +4H+ +2e =Pb2+ +2H2O | 1,449 |
| Pb4+ +4e =Pb2+ | 1,694 |
| Селен | |
| Se+2e =Se2 | -0,92 |
| Se+2H+ +2e =H2Se | -0,40 |
| H2SeO3 +4H+ +4e =Se+3H2O | -0,741 |
| SeO42 +4H+ +2e =H2SeO3 +H2O | 1,15 |
| SeO42 +H2O +2e =SeO32– +2OH– | 0,05 |
| Сера | |
| SO42 +H2O+2e =SO32 +2OH | -0,93 |
| SO42 +4H2O+6e =S +8OH | -0,75 |
| Уравнение процесса | Е0, В |
| S+2e =S2 | -0,48 |
| SO42 +10H+ +8e =H2S +4H2O | 0,31 |
| SO42 +4H2O +8e =S2– +8OH– | -0,68 |
| S+2H+ +2e =H2S | 0,17 |
| SO42 +2H+ +2e =SO32 +H2O | 0,22 |
| 2SO42 +10H+ +8e =S2O32 +5H2O | 0,29 |
| 2SO42 +5H2O +8e =S2O32 +10OH– | -0,76 |
| SO42 +8H+ +6e =S +4H2O | 0,357 |
| S2O82 +2e =2SO42 | 2,010 |
| S4O62 +2e =2S2O32 | 0,09 |
| Серебро | |
| Ag(CN)2 +e =Ag+2CN | -0,29 |
| Ag(NH3)2+ +e =Ag+2NH3 | 0,373 |
| Ag+ +e =Ag | 0,799 |
| AgCl +e =Ag+Cl– | 0,222 |
| Ag2O+H2O+2e =2Ag+2OH– | 0,342 |
| Стронций | |
| Sr2+ +2e =Sr | -2,888 |
| Сурьма | |
| Sb+3e =Sb | 0,20 |
| SbO+ +2H+ +3e =Sb+H2O | 0,212 |
| SbO2 +4H+ +3e =Sb+2H2O | 0,446 |
| Sb2O5 +6H+ +4e =2SbO+ +3H2O | 0,58 |
| Таллий | |
| Tl+ +e =Tl | -0,336 |
| Tl3+ +2e =Tl+ | 1,252 |
| Тантал | |
| Ta2O5 +10H+ +10e =2Ta+5H2O | -0,750 |
| Теллур | |
| Te +2e =Te2 | -1,14 |
| Te +2H+ +2e =H2Te | -0,51 |
| TeO42 +2H+ +2e =TeO32 +H2O | 0,892 |
| H2TeO6 +2H+ +2e =TeO2 +4H2O | 1,02 |
| Уравнение процесса | Е0, В |
| Технеций | |
| Tc2+ +2e =Tc | 0,4 |
| TcO4 +8H+ +5e =Tc2+ +4H2O | 0,5 |
| Титан | |
| Ti2+ +2e =Ti | -1,630 |
| Ti3+ +3e =Ti | -1,23 |
| TiO2+4H++4e =Ti+2H2O | -0,86 |
| TiO2+ +2H+ +4e =Ti+H2O | -0,88 |
| Ti3+ +e =Ti2+ | -0,368 |
| TiO2+ +2H+ +5H2O+e =Ti(H2O)63+ | 0,1 |
| Углерод | |
| CO2 +2H+ +2e =CO+H2O | -0,12 |
| CO2 +2H+ +2e =HCOOH | -0,20 |
| CO32 +6H+ +4e =C+3H2O | 0,475 |
| Фосфор | |
| PO43 +2H2O+2e =HPO32 +3OH | -1,12 |
| P+3H2O+3e =PH3 +3OH | -0,89 |
| H3PO4 +4H+ +4e =H3PO2 +2H2O | -0,39 |
| H3PO4 +5H+ +5e =P +4H2O | -0,383 |
| H3PO2 +H+ +e =P +2H2O | -0,51 |
| H3PO3+3H+ +3e =P +3H2O | -0,50 |
| Фтор | |
| OF2 +2H+ +4e =2F +H2O | 2,1 |
| F2 +2e =2F | 2,87 |
| Хлор | |
| 2ClO +2H2O+2e =Cl2 +4OH | 0,40 |
| ClO4 +4H2O+8e =Cl +8OH | 0,56 |
| ClO3 +3H2O+6e =Cl +6OH | 0,63 |
| ClO +H2O+2e =Cl +2OH | 0,88 |
| ClO4 +2H+ +2e =ClO3 +H2O | 1,189 |
| Cl2 +2e =2Cl | 1,359 |
| ClO4 +8H+ +8e =Cl +4H2O | 1,38 |
| 2ClO4 +16H+ +14e =Cl2 +8H2O | 1,39 |
| ClO3 +6H+ +6e =Cl +3H2O | 1,451 |
| Уравнение процесса | Е0, В |
| Хром | |
| Cr2+ +2e =Cr | -0,913 |
| Cr3+ +3e =Cr | -0,744 |
| Cr3+ +e =Cr2+ | -0,404 |
| Cr(OH)3 +3e =Cr+3OH– | -1,3 |
| CrO42 +4H2O+3e =Cr(OH)3 +5OH | -0,13 |
| CrO42 +4H+ +3e =CrO2 +2H2O | 0,945 |
| CrO2 +4H+ +e =Cr2+ +2H2O | 1,188 |
| Cr2O72 +14H+ +6e =2Cr3+ +7H2O | 1,333 |
| CrO42 +8H+ +3e =Cr3+ +4H2O | 1,477 |
| | |
| Цезий | |
| Cs+ + e =Cs | -2,923 |
| | |
| Цинк | |
| Zn(CN)42 +2e =Zn+4CN | -1,26 |
| Zn2+ +2e =Zn | -0,763 |
| ZnO22 +2H2O+2e =Zn+4OH | -1,216 |
| | |
| Цирконий | |
| ZrO2+ +2H+ +4e =Zr+H2O | -1,570 |
| Zr4+ +4e =Zr | -1,539 |
| ZrO2 +4H+ +4e =Zr+2H2O | -1,43 |
| | |
| Лантаниды | |
| La3+ +3e =La | -2,522 |
| Ce3+ +3e =Ce | -2,48 |
| Ce4+ + e =Ce3+ | 1,61 |
| Pr3+ +3e =Pr | -2,462 |
| Pm3+ +3e =Pm | -2,423 |
| Sm2+ +2e =Sm | -3,121 |
| | |
Произведения растворимости
малорастворимых веществ
-
Вещество
ПР
рПР = –lgПР
Ag3AsO4
1,0 · 10-22
22,0
AgBr
5,3 · 10-13
12,28
AgCN
1,4 · 10-16
15,84
Ag2CO3
8,2 · 10-12
11,09
Ag2C2O4
1,1 · 10-11
10,96
AgCl
1,78 · 10-10
9,75
Ag2CrO4
1,1 · 10-12
11,97
Ag2Cr2O7
1,0 · 10-10
10,0
AgI
8,3 · 10-17
16,08
AgIO3
3,0 · 10-8
7,50
Ag2O (AgOH)
1,6 · 10-8
7,80
Ag3PO4
1,3 · 10-20
19,89
Ag2S
2,0 · 10-50
49,70
Ag2SO4
2,0 · 10-5
4,70
AgSNC
1,1 · 10-12
11,97
Al(OH)3
1,0 · 10-32
32,0
AlРO4
5,8 · 10-19
18,24
AuBr3
4,0 · 10-36
35,40
AuCl3
3,2 · 10-25
24,50
BaC2O4 2H2O
1,1 · 10-7
6,96
BaCO3
4,0 · 10-10
9,40
BaCrO4
1,2 · 10-10
9,93
BaF2
1,7 · 10-6
5,77
Ba(IO3)2 · H2O
1,5 · 10-9
8,82
BaMnO4
2,5 · 10-10
9,60
Ba(OH)2
5,0 · 10–3
2,30
Ba3(PO4)2
6,0 · 10-39
38,22
BaSO4
1,1 · 10-10
9,97
Be(OH)2
6,3 · 10-22
21,2
BiI3
8,1 · 10-19
18,09
Bi(OH)3
3,0 · 10-36
35,50
Вещество
ПР
рПР = –lgПР
BiPO4
1,3 · 10-23
22,90
Bi2S3
1,0 · 10-97
97,0
CaCO3
4,8 · 10-9
8,32
CaC2O4
2,3 · 10-9
8,64
CaCrO4
7,1 · 10-4
3,15
CaF2
4,0 · 10-11
10,40
Ca(OH)2
5,5 · 10-6
5,26
CaHPO4
2,7 · 10–7
6,57
Ca3(PO4)2
2,0 · 10-29
28,70
CaSO4
2,5 · 10-5
4,60
Cd(OH)2
1,0 · 10-14
14,0
CdS
1,6 · 10-28
27,8
Co(OH)2 роз.
1,0 · 10-16
16,0
Co(OH)3
1,0 · 10-43
43,0
CoS
4,0 · 10-21
20,40
Cr(OH)2
1,0 · 10–17
17,0
Cr(OH)3
6,7 · 10-31
30,18
CuBr
5,25 · 10-9
8,28
CuCO3
2,5 · 10-10
9,60
CuCN
3,2 · 10-20
19,49
CuCl
1,2 · 10-6
5,92
CuI
1,1 · 10-12
11,96
CuOH
1,0 · 10–14
14,0
Cu(OH)2
2,2 · 10-20
19,66
(CuOH)2CO3
1,7 · 10-34
33,76
CuS
6,3 · 10-36
35,20
Cu2S
2,5 · 10-48
47,60
FeCO3
3,5 · 10–11
10,46
Fe(OH)2
8,0 · 10-16
15,10
Fe(OH)3
6,3 · 10-38
37,20
FePO4
1,3 · 10-22
21,89
FeS
5,0 · 10-18
17,30
Hg2Cl2
1,3 · 10-18
17,83
HgI2
1,0 · 10-26
26,0
Вещество
ПР
рПР = –lgПР
HgS
1,6 · 10-52
51,8
K3[AlF6]
1,6 · 10-9
8,80
KClO4
1,1 · 10-2
1,97
K3[Co(NO2)3]
4,3 · 10-10
9,37
La(OH)3
2,0 · 10-19
18,70
Li2CO3
4,0 · 10-3
2,40
LiOH
4,0 · 10–2
1,40
Li3PO4
3,2 · 10-9
8,50
Mg(OH)2
6,0 · 10-10
9,22
MgNH4PO4
2,5 · 10-13
12,60
Mg3(PO4)2
1,0 · 10-13
13,0
MnCO3
1,8 · 10-11
10,74
Mn(OH)2
1,9 · 10-13
12,73
MnS телесного цвета
2,5 · 10-10
9,60
(NH4)2IrCl6
3,0 · 10-5
4,50
Na3[AlF6]
4,1 · 10-10
9,39
Ni(CN)2
3,0 · 10-23
22,50
Ni(OH)2
6,3 · 10-18
17,2
NiS
1,0 · 10-24
24,00
PbCO3
7,5 · 10-14
13,13
PbCl2
1,6 · 10-5
4,79
PbCrO4
1,8 · 10-14
13,75
PbI2
1,1 · 10-9
8,98
PbО2
3,0 · 10-66
65,5
Pb(OH)2
8,7 · 10–14
13,06
Pb3(PO4)2
8,0 · 10-43
42,10
PbS
2,5 · 10-27
26,60
PbSO4
1,6 · 10-8
7,80
PtBr4
3,0 · 10-41
40,50
PtCl4
8,0 · 10-29
28,1
Sb(OH)3
4,0 · 10–42
41,40
Sb2S3
1,6 · 10-93
92,8
Sn(OH)2
6,0 · 10-27
26,20
Sn(OH)4
1,0 · 10-57
57,00
Вещество
ПР
рПР = –lgПР
SnS
1,0 · 10-26
26,00
SrCO3
1,1 · 10-10
9,96
SrSO4
3,2 · 10-7
6,49
Sr(OH)2
1,4 · 10–3
2,85
TlBr
3,9 · 10-6
5,41
TlCl
1,7 · 10-4
3,76
Tl I
5,8 · 10-8
7,24
Tl(OH)3
1,0 · 10-45
45,00
Tl2S
5,0 · 10-21
20,30
Tl2SO4
4,0 · 10-3
2,40
Zn(CN)2
2,6 · 10-13
12,59
ZnCO3
1,5 · 10-11
10,82
Zn(OH)2
1,2 · 10-17
16,92
ZnS
1,6 · 10-24
23,80