Файл: Химия пні бойынша тосана арналан жиынты баалау спецификациясы 8 сынып.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 454
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Жауабы:
[1]
-
Химиялық элементтердің периодтық жүйесінен жаратылыстың барлық заңдылықтарын көруге болады. Сонымен қатар периодтық жүйедегі сандар өзара байланысы бар және олардан көптеген ақпарат алуға болады. (Бос орындарды қажетті сөздер/ сөйлемдермен толықтырыңыз)
-
Бір периодта орналасқан элемент атомдарының
бірдей болады, бұл период
физикалық мәнін түсіндіреді.
-
Бір топта орналасқан элемент атомдарының
бірдей болады, бұл топ
физикалық мәнін түсіндіреді.
[2]
-
Бос орындарды қажетті сөздерментолықтырыңыз:
-
периодта орналасқан Na →Cl дейін атом ядро зарядтары артқан сайын
қасиеті артып,қасиеті кемиді.
-
Cуретте бірінші топ элементтерінің атом радиустарының артуы көрсетілген. Li→Rb элементтердің қандай қасиеті артады?
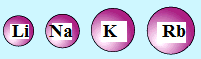
[1]
[1]
-
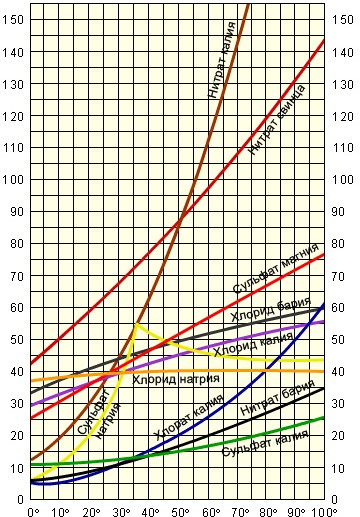 Суретте 100 г судағы әр түрлі тұздардың температураға қатысты ерігіштігі көрсетілген. Температураның артуына байланысты калий нитратының (нитрат калия) ерігіштігіне қорытынды жасаңыз.
Суретте 100 г судағы әр түрлі тұздардың температураға қатысты ерігіштігі көрсетілген. Температураның артуына байланысты калий нитратының (нитрат калия) ерігіштігіне қорытынды жасаңыз.
[1]
-
Жаздың ыстық күндері бөлме температурасында тұрған газдалған сусындарды ішу әркімге ұнай бермейді. Сондықтан газдалған сусынды салқындатқышқа қойып, салқындағаннан кейін ішеміз. Себебін түсіндіріңіз.
[1]
-
Су -тіршілік көзі ретінде жер қыртысында ең көп тараған химиялық қосылыс. Су молекуласындағы ковалентті байланыстардың түзілу механизмін «айқыштар мен нүктелер» диаграммасы арқылы түсіндіріңіз.
[1]
-
 Магний хлориді табиғатта бишофит минералы ретінде кезедеседі. Суретте бұрғылау нәтижесінде алынған минерал көрсетілген. Магний хлориді тағамдық қоспа - Е511 ретінде тіркелген химиялық қосылыс.
Магний хлориді табиғатта бишофит минералы ретінде кезедеседі. Суретте бұрғылау нәтижесінде алынған минерал көрсетілген. Магний хлориді тағамдық қоспа - Е511 ретінде тіркелген химиялық қосылыс.
-
Магний хлоридіндегі химиялық байланыстың түзілуін «айқыштар мен нүктелер» диаграммасы арқылы көрсетіңіз.
[1]
-
Магний хлоридінің суда ерігіштігі қасиетін болжап жазыңыз.
[1]
-
Ерітіндідегі еріген заттың массалық үлесін сипаттайтын формуланы жазыңыз.
[1]
-
Массасы 200г 15%-дық ерітіндіге тағы да 30 г тұз қосты. Алынған ерітіндідегі еріген заттың массалық үлесін есептеңіз.
[3]
-
Молярлық концентрация дегеніміз 1 л ерітіндідегі еріген заттың мөлшерін көрсетеді. Математикалық өрнегі төмендегідей:
 См = ʋ
См = ʋ????(ер−ді)
. Осы формуладан еріген заттың массасын өрнектеп шығарыңыз.
[1]
-
Мұғалім оқушыға 500 мл ерітіндіде 8 г натрий гидроксиді ерітілгендігін айтты. Оқушының мұғалімнен алған ерітіндінің концентрациясы қандай? Жауабыңызды есептеп дәлелдеңіз.
[2]
-
Кестеде екінші топтың негізгі топша элементтерінің физикалық және химиялық қасиеттері көрсетілген. Барий элементі үшін қалдырылған бос ұяшықтарды өз болжауларыңыз арқылы толтырыңыз.
| Элементтер | Түсі, металдық жылтыры | Ауадағы оттегімен тотығуы | Сумен реакциясы |
| Берилий | Ақ түсті, күмісше жылтыраған металл | Әдетте сыртын оксидтік қабықша қаптайды | Сумен әрекеттеспейді |
| Магний | Ақ түсті, күмісше жылтыраған металл | Қыздырған кезде әрекеттеседі | Тек ыстық сумен баяу әрекеттесіп, магний гидроксиді мен сутегі газын түзеді |
| Кальций | Ақ түсті, күмісше жылтыраған металл | Бөлме температурасында бірден тотығады | Бөлме температурасында сумен әрекеттесіп, кальций гидроксиді мен сутегі газын түзеді |
| Стронций | Ақ түсті, алтын жалатылған тәрізді металл | Бөлме температурасында бірден тотығады | Бөлме температурасында сумен шабытты әрекеттесіп, стронций гидроксиді мен сутегі газын түзеді |
| Барий | | | |
[3]


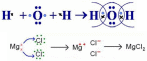 Балл қою кестесі
Балл қою кестесі | № | Жауап | Балл | Қосымша ақпарат | ||
| 1 | С | 1 | Басқа жауаптар қабылданбайды | ||
| 2 | А | 1 | |||
| 3 | В | 1 | |||
| 4 | D | 1 | |||
| 5 | D | 1 | |||
| 6 | С, D | 1 | |||
| 7 | (a)Энергетикалық деңгей саны, период нөмірінің | 1 | |||
| (b) Сыртқы электрондық қабаттағы электрон саны, топ нөмірінің | 1 | ||||
| 8 | Бейметалдық , металдық | 1 | | ||
| 9 | Металдық | 1 | Тотықсыздандырғыш қабылданады | ||
| 10 | Калий нитратының ерігіштігі артады | 1 | Көпшілік тұздардың ерігіштігі артады қабылданады | ||
| 11 | Газдардың ерігішітігі температура төмендегенде артады | 1 | Басқа жауап қабылданбайды | ||
| 12 | | 1 | | ||
| 13 | (a) | 1 | | ||
| (b) жақсы ериді | 1 | | |||
| 14 | w(ер.з) = ????(ер.з) •100% ????(ер−ді) | 1 | | ||
| 15 | Формуланы түрлендіріп m1(ер.з) = 30г m2 (ер.з) = 60г есептейді | 1 | Пропорциямен шығарылған есеп қабылданбайды | ||
| m2 (ер-ді) = 230г есептейді | 1 | ||||
| w2 (ер.з) = 26.09% | 1 | ||||
| 16 | m(ер.з) = Cm•M•V(ер-ді) | 1 | | ||
| 17 | V(ер-ді) = 500 мл=0.5л | 1 | | ||
| ???????? = 8 = 0.4 ???? 40 • 0.5 | 1 | ||||
| 18 | Ақ түсті, күмісше жылтыраған металл | 1 | | ||
| Бөлме температурасында бірден тотығады | 1 | | |||
| Бөлме температурасында сумен шабытты әрекеттесіп, стронций гидроксиді мен сутегі газын түзеді | 1 | | |||
| Барлығы | 25 | | |||
-
ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
4-тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты - 40 минут
Балл саны - 25
Тапсырмалар түрлері:
КТБ- Көп таңдауы бар тапсырмалар;
ҚЖ- Қысқа жауапты қажет ететін тапсырмалар;
ТЖ -Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Тоқсан бойынша жиынтық бағалауда әртүрлі тапсырмалар: көп жауапты таңдауы бар сұрақтар, қысқа/толық жауапты қажет ететін сұрақтар қолданылады.
Қысқа жауапты қажет ететін сұрақтарға сөздер немесе қысқа сөйлемдер түрінде жауап береді.
Толық жауапты қажет ететін сұрақтарда білім алушылар орындаушылық және шығармашылық дағдыларын көрсетеді.
Нұсқа: 18 тапсырмадан тұрады: соның ішінде бірнеше жауап нұсқаларынан тұратын сұрақтар, қысқаша жауапты қажет ететін сұрақтар, толық жауапты қажет ететін тапсырмалар берілген.
ЖОБА
4-тоқсан бойынша жиынтық бағалау тапсырмаларының сипаттамасы
| Бөлім | Тексерілетін мақсат | Ойлау дағдыларының деңгейі | Тап сыр ма саны* | № тап сыр ма* | Тапсыр ма түрі | Орында у уақыты, мин* | Балл* | Бөлім бойынш а балл |
| Бейоргани- калық қосылыстар- дың негізгі кластары. Генетикалық байланыс | 8.3.4.7 Оксидтердің жіктелуін және қасиет-терін білу, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру | Қолдану | 1 | 5 | ҚЖ | 2 | 1 | 10 |
| 8.3.4.8 Қышқылдардың жіктелуін, қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру | Қолдану | 2 | 6, 7 | ҚЖ | 3 | 2 | ||
| 8.3.4.9 Негіздердің жіктелуі мен қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру | Қолдану | 2 | 8, 9 | ҚЖ | 3 | 2 | ||
| 8.3.4.12 Бейорганикалық қосылыстардың негізгі кластары арасындағы генетикалық байланысты зерттеу | Жоғары деңгей дағдылары | 2 | 13, 14 | ТЖ | 8 | 5 | ||
| Көміртек және оның қосылыстары | 8.4.3.1 Көміртек неліктен көптеген қосылыстарында төрт байланыс түзетінін түсіндіру; | Қолдану | 1 | 15 | ТЖ | 3 | 2 | 8 |
| 8.4.3.3 Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстыру; | Білу және түсіну | 2 | 1, 10 | КТБ/ ҚЖ | 3 | 2 | ||
| 8.4.3.6 Көміртек жанған кезде көміртек диоксиді мен көміртек монооксидінің түзілу жағдайларын сипаттау және тірі ағзаларға иіс газының физиологиялық әсерін түсіндіру; | Қолдану | 1 | 3 | КТБ | 2 | 1 | ||
| 8.4.3.7 Көмірқышқыл газын ала алу, оны анықтау және қасиеттерін зерттеу; | Қолдану | 2 | 2, 16 | КТБ/ ТЖ | 5 | 3 | ||
| Су | 8.4.2.8 Судың ластануының қауіптілігі мен себебін анықтау, суды тазарту әдістерін түсіндіру; | Қолдану | 2 | 11, 12 | ҚЖ | 3 | 2 | 7 |
| 8.4.2.9 Судың «кермектігін» анықтау және оны жою тәсілдерін түсіндіру; | Қолдану | 3 | 4, 17, 18 | КТБ/ ТЖ | 8 | 5 | ||
| Барлығы | | | | | | | | 25 |