Добавлен: 06.12.2023
Просмотров: 131
Скачиваний: 5
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Источником электрического поля в соединениях с ионным типом связи являются сами ионы. Поэтому, говоря о поляризационных свойствах иона, необходимо различать поляризующее действие данного иона и способность его самого поляризоваться в электрическом поле.
Поляризующее действие иона будет тем большим, чем больше его силовое поле, т. е. чем больше заряд и меньше радиус иона. Поэтому в пределах подгрупп в Периодической системе элементов поляризующее действие ионов понижается сверху вниз, так как в подгруппах при постоянной величине заряда иона сверху вниз увеличивается его радиус.
Поэтому поляризующее действие ионов щелочных металлов например растет от цезия к литию, а в ряду галогенид-ионов - от I к F. В периодах поляризующее действие ионов растет слева направо вместе с увеличением заряда иона и уменьшением его радиуса.
Поляризуемость иона, способность его к деформации растут с уменьшением силового поля, т. е. с уменьшением величины заряда и увеличением радиуса. Поляризуемость анионов обычно выше, чем катионов и в ряду галогенидов растет от F к I.
На поляризационные свойства катионов оказывает влияние характер их внешней электронной оболочки. Поляризационные свойства катионов как в активном, так и в пассивном смысле при одинаковом заряде и близком радиусе растут при переходе от катионов с заполненной оболочкой к катионам с незаконченной внешней оболочкой и далее к катионам с 18-электронной оболочкой.
Например, в ряду катионов Mg2+, Ni2+, Zn2+ поляризационные свойства усиливаются. Эта закономерность согласуется с изменением в приведенном в ряду радиуса иона и строения его электронной оболочки:
| Катион | Мg 2+ | Ni 2+ | Zn 2+ |
| Радиус, нм | 0,078 | 0,079 | 0,083 |
| Электронная оболочка | 2s22р6 | 3s23р63d8 | 3s23р63d10 |
Для анионов поляризационные свойства ухудшаются в такой последовательности:
I-, Br-, Cl-, CN-, OH-, NO3-, F-, ClO4-.
Результатом поляризационного взаимодействия ионов является деформация их электронных оболочек и, как следствие этого, сокращение межионных расстояний и неполное разделение отрицательного и положительного зарядов между ионами.
Например, в кристалле хлорида натрия величина заряда на ионе натрия составляет +0,9, а на ионе хлора - 0,9 вместо ожидаемой единицы. В молекуле KCl, находящейся в парообразном состоянии, величина зарядов на ионах калия и хлора составляет 0,83 единицы заряда, а в молекуле хлороводорода - лишь 0,17 единицы заряда.
Поляризация ионов оказывает заметное влияние на свойства соединений с ионной связью, понижая их температуры плавления и кипения, уменьшая электролитическую диссоциацию в растворах и расплавах и др.
Ионные соединения образуются при взаимодействии элементов, значительно различающихся по химическим свойствам. Чем больше удалены друг от друга элементы в периодической системе, тем в большей степени проявляется в их соединениях ионная связь. Напротив, в молекулах, образованных одинаковыми атомами или атомами элементов, близких по химическим свойствам, возникают другие типы связи. Поэтому теория ионной связи имеет ограниченное применение.
1.6 Влияние поляризации ионов на свойства веществ и свойства Ионной связи и ионных соединений
Представления о поляризации ионов помогают объяснить различия в свойствах многих однотипных веществ. Например, сравнение хлоридов натрия и калия с хлоридом серебра показывает, что при близких ионных радиусах
поляризуемость катиона Ag+, имеющего 18-электронную внешнюю оболочку, выше, что приводит к увеличению прочности связи металл-хлор и меньшей растворимости хлорида серебра в воде.
Взаимная поляризация ионов облегчает разрушение кристаллов, что приводит к понижению температур плавления веществ. По этой причине температура плавления TlF (327 oС) существенно ниже, чем RbF (798 oC). Температура разложения веществ также понижатся с усилением взаимной поляризации ионов. Поэтому иодиды обычно разлагаются при более низких температурах, чем остальные галогениды, а соединения лития - термически менее устойчивы, чем соединения других щелочных элементов.
Деформируемость электронных оболочек сказывается и на оптических свойствах веществ. Чем более поляризована частица, тем ниже энергия электронных переходов. Если поляризация мала, возбуждение электронов требует более высокой энергии, что отвечает ультрафиолетовой части спектра. Такие вещества обычно бесцветны. В случае сильной поляризации ионов возбуждение электронов происходит при поглощении электромагнитного излучения видимой области спектра. Поэтому некоторые вещества, образованные бесцветными ионами, окрашены.
Характеристикой ионных соединений служит хорошая растворимость в полярных растворителях (вода, кислоты и т. д.). Это происходит из-за заряженности частей молекулы. При этом диполи растворителя притягиваются к заряженным концам молекулы, и, в результате Броуновского движения, «растаскивают» молекулу вещества на части и окружают их, не давая соединиться вновь. В итоге получаются ионы окружённые диполями растворителя.
При растворении подобных соединений, как правило, выделяется энергия, так как суммарная энергия образованных связей растворитель-ион больше энергии связи анион-катион. Исключения составляют многие соли азотной кислоты (нитраты), которые при растворении поглощают тепло (растворы охлаждаются). Последний факт объясняется на основе законов, которые рассматриваются в физической химии.
1.7 Кристаллическая решётка
Ионные соединения (например, хлорид натрия NaCl) - твердые и тугоплавкие от того, что между зарядами их ионов ("+" и "–") существуют мощные силы электростатического притяжения.
Отрицательно заряженный ион хлора притягивает не только "свой" ион Na+, но и другие ионы натрия вокруг себя. Это приводит к тому, что около любого из ионов находится не один ион с противоположным знаком, а несколько (рис. 1).
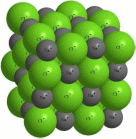
Рис. 1. Строение кристалла поваренной соли NaCl.
Фактически, около каждого иона хлора располагается 6 ионов натрия, а около каждого иона натрия - 6 ионов хлора.
Такая упорядоченная упаковка ионов называется ионным кристаллом. Если в кристалле выделить отдельный атом хлора, то среди окружающих его атомов натрия уже невозможно найти тот, с которым хлор вступал в реакцию. Притянутые друг к другу электростатическими силами, ионы крайне неохотно меняют свое местоположение под влиянием внешнего усилия или повышения температуры. Но если температура очень велика (примерно 1500°C), то NaCl испаряется, образуя двухатомные молекулы. Это говорит о том, что силы ковалентного связывания никогда не выключаются полностью.
Ионные кристаллы отличаются высокими темпертурами плавления, обычно значительной шириной запрещенной зоны, обладают ионной проводимостью при высоких температурах и рядом специфических оптических свойств (например, прозрачностью в ближней области ИК спектра). Они могут быть построены как из одноатомных, так и из многоатомных ионов. Пример ионных кристаллов первого типа - кристаллы галогенидов щелочных и щелочно-земельных металлов; анионы располагаются по закону плотнейшей шаровой упаковки или плотной шаровой кладки, катионы занимают соответствующие пустоты. Наиболее характерные структуры такого типа - NaCl, CsCl, CaF2. Ионные кристаллы второго типа построены из одноатомных катионов тех же металлов и конечных или бесконечных анионных фрагментов. Конечные анионы (кислотные остатки) - NO3-, SO42-, СО32- и др. Кислотные остатки могут соединяться в бесконечные цепи, слои или образовывать трехмерный каркас, в полостях которого располагаются катионы, как, например, в кристаллических структурах силикатов. Для ионных кристаллов можно рассчитать энергию кристаллической структуры U (см. табл.), приближенно равную энтальпии сублимации; результаты хорошо согласуются с экспериментальными данными.
Согласно уравнению Борна-Майера, для кристалла, состоящего из формально однозарядных ионов:
U = -A/R + Ве-R/r - C/R6 - D/R8 + E0
(R - кратчайшее межионное расстояние, А - константа Маделунга, зависящая от геометрии структуры, В и r - параметры, описывающие отталкивание между частицами, C/R6 и D/R8 характеризуют соответствующие диполь-дипольное и диполь-квадрупольное взаимодействие ионов, E0 - энергия нулевых колебаний, е - заряд электрона). С укрупнением катиона возрастает вклад диполь-дипольных взаимодействий.