ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.12.2023
Просмотров: 17
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего образования
Санкт-Петербургский горный университет
Кафедра общей химии

Аналитическая химия
ОТЧЁТ


(наименование учебной дисциплины согласно учебному плану)
По дисциплине:

Действие групповых реагентов. Качественные аналитические реакции катионов

Тема работы:







(шифр группы)
(Ф.И.О)
(подпись)
Выполнил: студент гр.

Оценка:

Дата:







(Ф.И.О)
(подпись)
(должность)
руководитель работы:

Санкт-Петербург
2023
Лабораторная работа №1. Действие групповых реагентов
Цель работы: изучить действие и аналитические реакции групповых реагентов качественного анализа по кислотно-основному методу.
Ход работы:
Опыт 1. Групповые реакции II аналитической группы
-
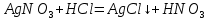 – Белый студенистый осадок
– Белый студенистый осадок
Ag++N
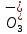 +H++Cl-=AgCl
+H++Cl-=AgCl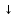 +H++N
+H++N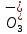
Ag++Cl-=AgCl
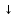
-
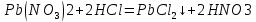 - Выпадение белого осадка
- Выпадение белого осадка
Pb2++2N
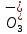 +2H++2Cl-=PbCl2
+2H++2Cl-=PbCl2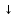 +2H++2N
+2H++2N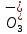
Pb2++2Cl-= PbCl2
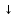
-
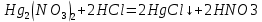 – Образование белого осадка
– Образование белого осадка
2Hg++2N
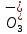 +2H++2Cl-=2HgCl
+2H++2Cl-=2HgCl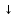 +2H++2N
+2H++2N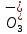
2Hg++2Cl-= 2HgCl
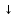
Опыт 2. Групповые реакции III аналитической группы
-
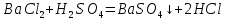 – Выпадение белого осадка
– Выпадение белого осадка
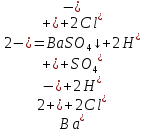
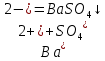
-
 – Выпадение белого осадка
– Выпадение белого осадка
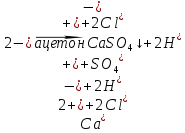
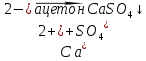
Опыт 3. Групповые реакции IV аналитической группы
-
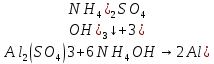 - белый осадок
- белый осадок
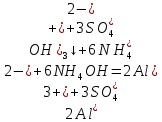
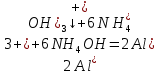
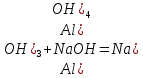 – растворение осадка
– растворение осадка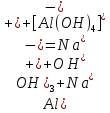
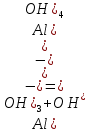
-
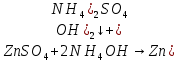 – белый осадок
– белый осадок
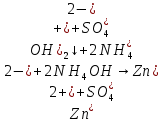
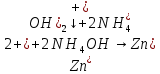
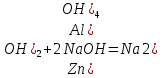 –растворение осадка
–растворение осадка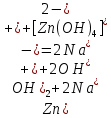
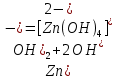
-
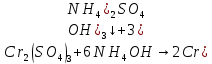 – осветление раствора, выпадение осадка
– осветление раствора, выпадение осадка
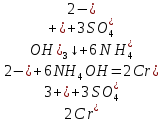
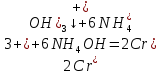
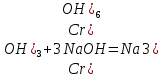 – растворение осадка, раствор светло-зеленый
– растворение осадка, раствор светло-зеленый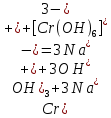
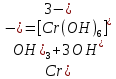
Опыт 4. Групповые реакции V аналитической группы
-
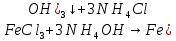 – раствор оранжевый, выпадение осадка
– раствор оранжевый, выпадение осадка
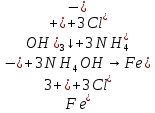
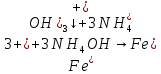
-
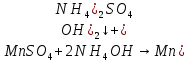 – выпадение осадка (бежевый студнеобразный)
– выпадение осадка (бежевый студнеобразный)
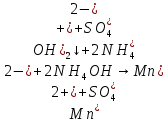
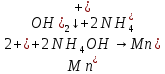
-
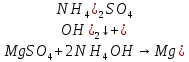 – образование мутного белого осадка
– образование мутного белого осадка
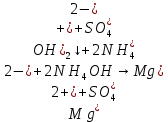
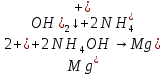
Опыт 5. Разделение элементов IV и V аналитических групп
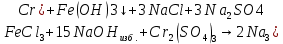 – образование осадка. После отфильтровали, наблюдали раствор окрасился в зеленый цвет.
– образование осадка. После отфильтровали, наблюдали раствор окрасился в зеленый цвет. 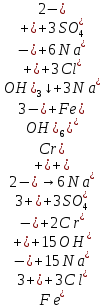
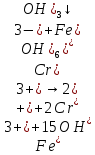
Опыт 6. Групповые реакции VI аналитической группы
-
HgCl2 + NH4OH = HgOHCl↓ + NH4Cl - осадок черного цвета
Hg2++2Сl- + NH4OH-= HgOHCl + NH4++ Сl-
Hg2+ + Сl-+ NH4OH-= HgOHСl+ NH4+
HgOHCl + NH4Cl+ 3NH4OH=
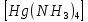 Cl2 +4 H2O – растворение осадка
Cl2 +4 H2O – растворение осадкаHgOHCl+ NH4++ Cl-+3NH4OH-=
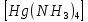 2++ 2Cl-+4H2O
2++ 2Cl-+4H2OHgOHCl+ NH4++3NH4OH-=
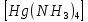 2+ + Сl-+4H2O
2+ + Сl-+4H2O-
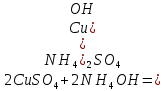 – осадок синий яркий
– осадок синий яркий
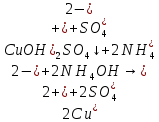
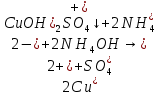
(CuOH)2SO4 +6NH4OH + (NH4)2SO4=
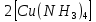 SO4+8H2O – растворение осадка
SO4+8H2O – растворение осадка(CuOH)2SO4+6NH4OH+2NH4++SO42-=2
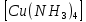 2++ 2SO42-+8H2O
2++ 2SO42-+8H2O(CuOH)2SO4+6NH4OH+2NH4+=2
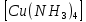 2++8H2O
2++8H2O-
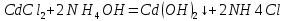 – белый осадок
– белый осадок
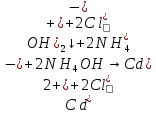
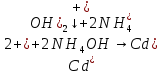
-
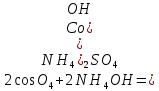 выпадение синего осадка
выпадение синего осадка
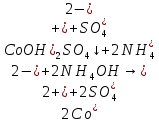
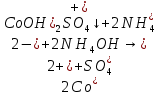
-
2Ni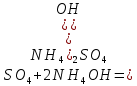 образование осадка, раствор ярко голубого цвета
образование осадка, раствор ярко голубого цвета
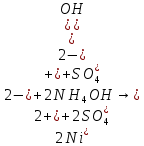
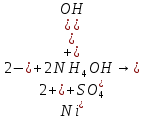
Опыт 7. Разделение элементов V и VI аналитических групп
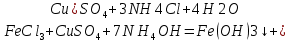 – выпадение осадка. После отфильтровали, наблюдали раствор окрасился синим цветом.
– выпадение осадка. После отфильтровали, наблюдали раствор окрасился синим цветом.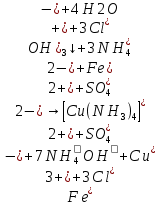
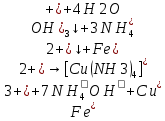
Лабораторная работа №2. Качественные аналитические реакции катионов
Цель работы: изучить качественные аналитические реакции катионов.
Ход работы:
Первая аналитическая группа катионов:
-
Катион Na+.
NaCl + KH2SbO4 = NaH2SbO4↓ + KCl – выпадение белого кристаллического осадка.
Na+ + Cl-+ K++ H2SbO4- = NaH2SbO4↓ + K+ + Cl-
Na++ H2SbO4-= NaH2SbO4
-
Катион K+.
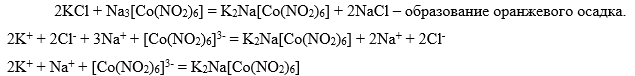
-
Катион NH4+. Образование бурого осадка
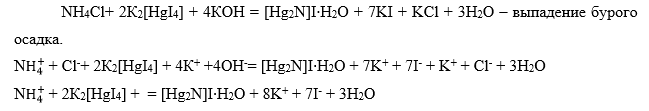
Вторая аналитическая группа катионов:
-
Катион Ag+.
AgNO3 + KCl
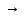 AgCl
AgCl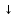 + KNO3 – выпадение белого осадка
+ KNO3 – выпадение белого осадка Ag+ + N
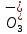 + K+ +
+ K+ + 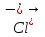 AgCl
AgCl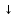 + K+ + N
+ K+ + N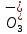
Ag+ +
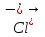 AgCl
AgCl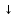
AgCl +
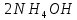
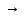
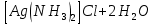 – растворение белого осадка
– растворение белого осадка AgCl +
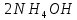
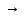
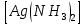 + +
+ + 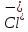 +
+ 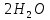
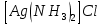 + 2HNO3
+ 2HNO3 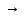 AgCl
AgCl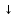 +
+ 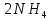 NO3 – выпадение белого осадка
NO3 – выпадение белого осадка 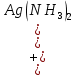 +
+ 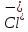 + 2H+ + 2N
+ 2H+ + 2N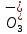
 AgCl
AgCl +
+ 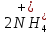 + 2N
+ 2N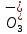
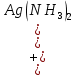 +
+ 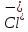 + 2H+
+ 2H+  AgCl
AgCl +
+ 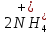
-
Катион Pb2+.
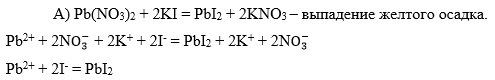
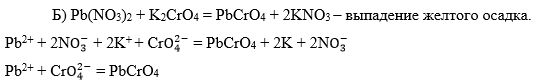
-
Катион Hg22+
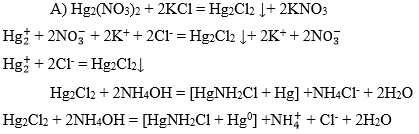
образование темного осадка
Белый осадок остался на фильтре, после добавления NH4OH цвет раствора – черный.
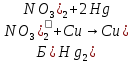 – образование светлого металлического пятна.
– образование светлого металлического пятна.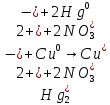
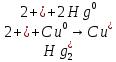
В)
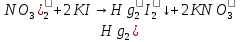 - выпадение мутно-оранжевого осадка.
- выпадение мутно-оранжевого осадка.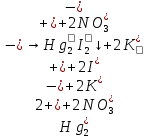
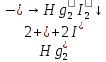
Г)
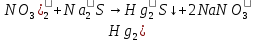 - образование черного осадка
- образование черного осадка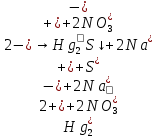
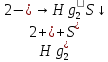
Д)
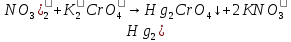 - образование красного осадка
- образование красного осадка 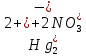 +
+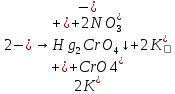
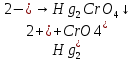
Третья аналитическая группа катионов:
-
Катион Ba2+.
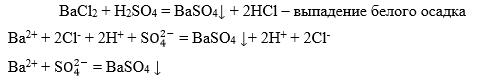
-
Катион Ca2+.
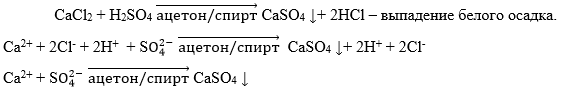
Четвертая аналитическая группа катионов:
-
Катион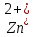 .
.

-
Катион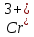 .
.
А)
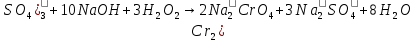 – раствор жёлтого цвета.
– раствор жёлтого цвета.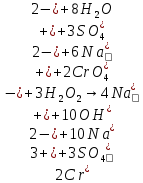
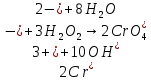
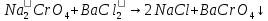 - выпадение осадка желтого цвета.
- выпадение осадка желтого цвета.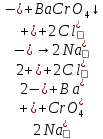
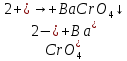
Б)
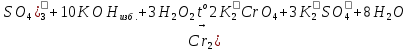 – желтый раствор хромата калия.
– желтый раствор хромата калия.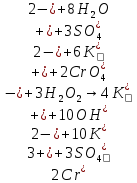
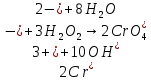
По каплям добавим раствор серной кислоты до перехода окраски в оранжевую и красную.
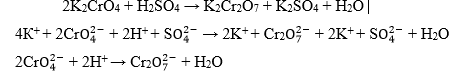
-
Катион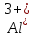 . Образование красного осадка.
. Образование красного осадка.
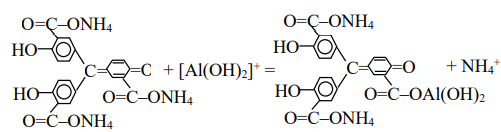
Пятая аналитическая группа катионов:
-
Катион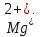
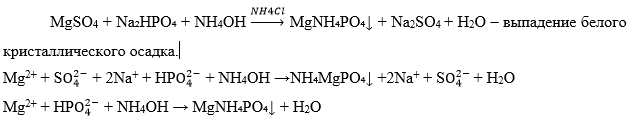
-
Катион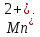 Выпадение осадка розового цвета.
Выпадение осадка розового цвета.
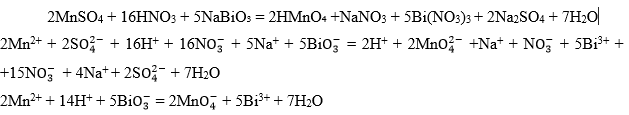
-
Катион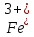 .
.
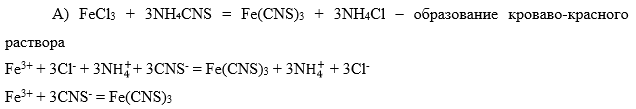
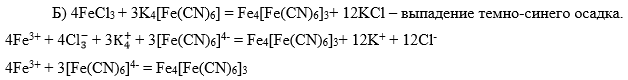
Шестая аналитическая группа катионов:
-
Катион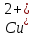 .
.
А.
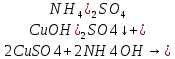 – образование зелёно-голубого осадка.
– образование зелёно-голубого осадка.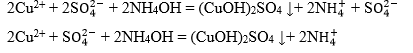
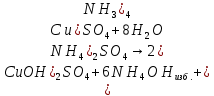 – раствор темно-синий
– раствор темно-синий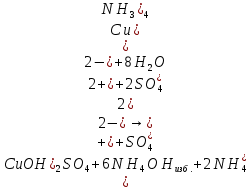
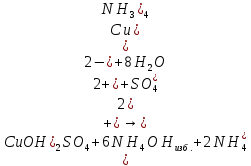
Б.
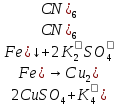 - красно-бурый осадок
- красно-бурый осадок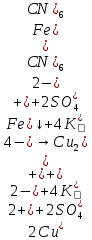
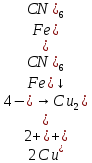
-
Катион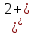 . Образование розового осадка.
. Образование розового осадка.
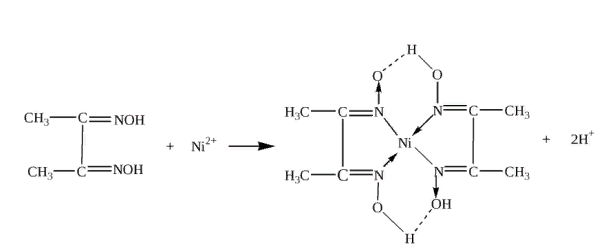
-
Катион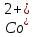 .
.
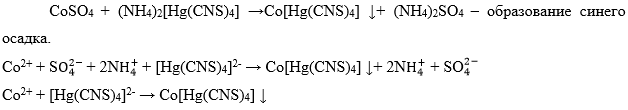
-
Катион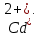
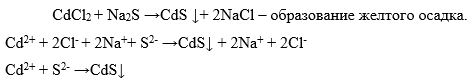
-
Катион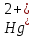 .
.