Файл: 1. Разновидности электрохимической обработки Механизм процесса анодного растворения металла.rtf
Добавлен: 09.12.2023
Просмотров: 75
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
1. Разновидности электрохимической обработки
2. Механизм процесса анодного растворения металла
3. Виды электрохимической обработки
4. Физико-химическая сущность метода
5. Методы размерной электрохимической обработки
5.1 Обработка с неподвижными электродами
5.2 Прошивание полостей и отверстий
5.2.1 Получение отверстий струйным методом
5.3 Точение наружных и внутренних поверхностей
5.4 Протягивание наружных и внутренних поверхностей в заготовках
Содержание
Введение
1. Разновидности электрохимической обработки
2. Механизм процесса анодного растворения металла
3. Виды электрохимической обработки
4. Физико-химическая сущность метода
5. Методы размерной электрохимической обработки
5.1 Обработка с неподвижными электродами
5.2 Прошивание полостей и отверстий
5.2.1 Получение отверстий струйным методом
5.3 Точение наружных и внутренних поверхностей
5.4 Протягивание наружных и внутренних поверхностей в заготовках
5.5 Разрезание заготовок
5.6 Шлифование
6. Законы Фарадея и скорость электрохимического процесса
7. Электрохимический станок
Заключение
Библиографический список
Введение
В современном машиностроении возникают технологические проблемы, связанные с обработкой новых материалов и сплавов (например, жаро- и кислотостойкие, специальные никелевые стали, тугоплавкие сплавы, композиты, неметаллические материалы: алмазы, рубины, германий, кремний, порошковые тугоплавкие материалы и т.п.) форму и состояние поверхностного слоя которых трудно получить известными механическими методами.
К таким проблемам относится обработка весьма прочных или весьма вязких материалов, хрупких и неметаллических материалов (керамика), тонкостенных нежестких деталей, а также пазов и отверстий, имеющих размеры в несколько МКМ; получение поверхностей деталей с малой шероховатостью, и очень малой толщиной дефектного поверхностного слоя.
В этих условиях, когда возможность обработки резанием ограничены плохой обрабатываемостью материала изделия, сложностью формы обрабатываемой поверхности или обработка вообще невозможна, целесообразно применять электрофизические и электрохимические методы обработки. Их достоинства следующие:
) механические нагрузки либо отсутствуют, либо настолько малы, что практически не влияют на суммарную погрешность точности обработки;
) позволяют изменять форму обрабатываемой поверхности заготовки (детали);
) позволяют влиять и даже изменять состояние поверхностного слоя детали;
) не образуется наклеп обработанной поверхности;
) дефектный слой не образуется;
) удаляются прижоги поверхности, полученные при шлифовании;
) повышаются: износостойкость, коррозионная стойкость, прочность и другие эксплуатационные характеристики поверхностей деталей.
Кинематика формообразования поверхностей деталей электрофизическими и электрофизическими методами обработки, как правило, проста, что обеспечивает точное регулирование процессов и их автоматизацию.
Цель работы: доказать преимущества, а в некоторых случаях незаменимость электрохимической размерной обработки. Понять механизм действия методов электрохимической обработки.
1. Разновидности электрохимической обработки
В основе электрохимической обработки (ЭХО) металлов и сплавов лежит принцип анодного растворения обрабатываемой заготовки в растворе электролита. Для осуществления процесса необходимо иметь два электрода, из которых один - заготовка (анод), другой - инструмент (катод), электролит между ними, а также источник питания. Совокупность двух электродов (анода, катода) и электролита между ними называется электролитической ячейкой.
Электрохимическая обработка в стационарном электролите, к ним относятся:
ü очистка поверхностей металлов от окислов, ржавчины, жировых пленок и других загрязнений;
ü заострение и затачивание режущего инструмента;
ü электрополирование;
ü гравирование и маркирование по металлам и др.
Отличительные особенности:
обработка осуществляется при низких плотностях тока (не более 2 А/см);
обеспечиваются сравнительно небольшие скорости растворения (10 - 10 мм/мин);
общий объем удаляемого материала невелик;
в межэлектродном пространстве отсутствуют (или имеется лишь малое количество)
нерастворенных продуктов процесса;
межэлектродное расстояние достаточно велико и может составлять сотни миллиметров.
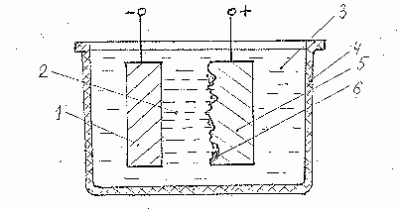
Рис. 1.1 Схема электролитического полирования (обработка в стационарном электролите):
- катод, 2 - силовые линии тока, 3 - электролит, 4 - ванна, 5 - заготовка (анод), 6 - продукты растворения.
2. Механизм процесса анодного растворения металла
Протекание тока в электролитической ячейке осуществляется посредством движения ионов под действием приложенного внешнего электрического поля. Жидкие растворы, проводящие электрический ток за счет ионной проводимости, называются электролитами.
В качестве электролитов используются водные растворы неорганических солей NaCl, NaNO3,Na2SO4 и др. реже кислот и щелочей. Удельная электропроводимость электролитов находится в пределах (0,1-0,4) см, а их температура в интервале (4-60) оС.
При этом применяют так называемые сильные электролиты, в которых все молекулы растворенного вещества диссоциируют на анионы (Аn-) и катионы (Кn+). Например, водный раствор поваренной соли (NaCl) диссоциирует на Na+ (катион) иCl - (анион). Кроме этого сама вода содержит ион водорода Н+ и гидроксила (ОН) - .
При отсутствии u1074 внешнего электрического поля (электроды разомкнуты) ионы движутся в электролите хаотически и электрического тока в нем не наблюдается. При этом на границе раздела твердой и жидкой фазы (металлического электрода и электролита) образуются два электрически заряженных слоя: поверхностный слой металла, заряженный положительно или отрицательно, и слой ионов, имеющий противоположный заряд.
Между этими слоями устанавливается определенный потенциал, который называется равновесным (Φр). Этот потенциал измеряется относительно стандартного водородного электрода, потенциал которого при всех условиях принимается равным нулю.
Подключение электродов ячейки к источнику напряжения сдвигает их потенциалы от равновесных: и вызывает протекание электродных процессов.
На аноде происходит:
) основная реакция - растворение (окисление) металла с образованием гидрата окиси металла, выпадаемого в осадок при обработке в нейтральных и щелочных электролитах.
(2.1) Ме - ne - > Men+; Men+ + n OH - >Me (OH) n
где - валентность металла (Ме) или с образованием растворимой соли при обработке в кислотах
(2.2) Men+ + n R - >Me (R) n
) возможна побочная реакция - образование кислорода, снижающая К.П.Д. процесса анодного растворения:
(2.3) 2 OH - 2 e - > H2O +O; O+O->O2
На катоде происходит выделение водорода, процесс образования которого в зависимости от условий протекает по разному:
а) в кислотах и при малых плотностях тока в нейтральных и слабо щелочных растворах восстановление водорода осуществляется по схеме:
(2.4) H+ + e - > H; H+H->H2
б) в нейтральных растворах при больших плотностях тока и больших напряжениях на электродах образование молекулярного водорода может осуществляться за счет разложения молекул воды:
(2.5) H2O + e - > H+ OH-; H+H->H2
Перечисленные уравнения отражают лишь конечный результат процесса анодного растворения, который представляет собой совокупность сложных взаимосвязанных процессов (диффузионных, миграции ионов, выделение тепла, гидродинамики электролита в зазоре, образование окисных пленок и др.).
Характер электрохимических реакций и технологических показателей ЭХРО зависят от кислотности и щелочности электролита, который оценивают водородным показателем рН. При обработке значительного количества деталей в одном и том же электролите его рН повышается до 9-11, что ухудшает условия растворения металлов.
Для сохранения постоянства шероховатости обработанной поверхности, скорости съема и энергоемкости процесса осуществляют стабилизацию рН электролита за счет буферирования раствора, например, борной кислотой в количестве 3-30 г/л.
О характере протекания электродных процессов можно судить по поляризационным кривым, которые представляют собой зависимость между плотностью тока (i) и потенциалом на электроде (Φ), сравниваемым с потенциалом стандартного водородного электрода.
3. Виды электрохимической обработки
Электрохимическое объемное копирование - Электрохимическая обработка, при которой форма электрода-инструмента отображается в заготовке.
Электрохимическое прошивание - Электрохимическая обработка, при которой электрод-инструмент, углубляясь в заготовку, образует отверстие постоянного сечения.
Струйное электрохимическое прошивание - Электрохимическое прошивание с использованием сформированной струи электролита.
Электрохимическое калибрование - Электрохимическая обработка поверхности с целью повышения ее точности.
Электрохимическое точение - Электрохимическая обработка, при вращении заготовки и поступательном перемещении электрода-инструмента.
Электрохимическая отрезка - Электрохимическая обработка, при которой заготовка разделывается на части.
Электрохимическое удаление заусенцев (ЭХУЗ, Electrochemical debuting) - Электрохимическая обработка, при которой удаляются заусенцы заготовки.
Электрохимическое маркирование
Многоэлектродная электрохимическая обработка