Файл: Курсовая работа использование дидактического материала на уроках химии представлена к защите.docx
Добавлен: 12.12.2023
Просмотров: 81
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
-
Методологические особенности использования разнообразных дидактических материалов на уроках химии в 8 классе-
Разработка дидактических материалов по разделу «Соединение химических элементов»
-
Общие правила техники безопасности при работе в кабинете химии[18]
-
В кабинете химии запрещается принимать в пищу любые продукты питания. -
Вещества нельзя брать руками и пробовать на вкус. -
При выяснении запаха нельзя подносить сосуд близко к лицу, а нужно ладонью сделать движение от отверстия сосуда к носу. -
Без указания учителя нельзя смешивать вещества. -
При выполнении опыта нужно брать небольшие порции вещества. Если в описании работы рекомендуется брать немного вещества, то следует помнить, что твердого вещества требуется примерно четверть чайной ложки, а жидкости – 1-2 мл. -
Особую осторожность необходимо соблюдать при работе с кислотами и щелочами. При случайном попадании кислоты или щелочи на руки или на одежду необходимо немедленно смыть их большим количеством воды. -
При разбавлении кислот водой нужно помнить следующее правило: кислоту медленно тонкой струйкой при перемешивании льют в воду, а не наоборот. -
Необходимо пользоваться только чистой лабораторной посудой. -
Остатки веществ не высыпать и не выливать обратно в сосуд с чистым веществом. -
После работы необходимо навести порядок на рабочем месте.
Тема: Классы неорганических соединений
Класс: 8.
Цели урока.
Обучающая. Повторение, углубление и обобщение сведений об основных классах неорганических соединений: построение названий соединений, классификация.
Развивающая. Развитие «химического» мышления, умения использовать терминологию, ставить и разрешать проблемы, анализировать, сравнивать, обобщать и систематизировать информацию.
Воспитывающая. Формирование интереса к учению, стремления добиваться успеха в учебе за счет добросовестного отношения к своему труду, создание положительной психологической атмосферы, воспитание чувства взаимного уважения между ребятами для максимального раскрытия их способностей на уроке.
Форма урока: Беседа с элементами исследовательской и самостоятельной работы обучающихся, работа у доски, индивидуальная, групповая работа, выполнение лабораторных опытов.
Техническое оборудование урока: компьютер, мультимедийный проектор.
Оборудование и реактивы: на столах учеников: опорные схемы (оксиды, кислоты, основания),
дидактические карточки с заданиями, пробирки с реактивами: индикаторная бумага, пронумерованные пробирки (1, 2, кислота, основание), чистые листы.
Девиз урока: «Повторение – мать учения».
Ход урока
Организационный момент.
Вступительное слово учителя о целях урока.
Итак, ребята, на предыдущих уроках химии мы подробно разбирали состав и свойства неорганических соединений различных классов.
На доске записана тема (Слайд 1.): “Важнейшие классы неорганических соединений”.
На доске: эпиграф
“Человек рождается на свет,
Чтоб творить, дерзать, а не иначе,
Чтоб оставить в жизни добрый след
И решить все трудные задачи”.
Учитель. Целью сегодняшнего урока является повторение и обобщение знаний по этой теме в занимательной форме.
У каждого из вас на столе лежит оценочный лист. Быстро подпишите их. В течение всего урока вы будете выполнять задания, и отмечать результаты своей работы в этих оценочных листах. Если ответили правильно, ставите себе в оценочном листе “+”, если неправильно, то “-”.
Повторение и обобщение знаний.
Ребята, если вы обратили внимание на доску, то, наверное, заметили, что от названия темы вниз идут четыре стрелки. Пустые места под стрелками мы будем заполнять по мере отгадывания загадок.
Загадки:
“Их получают путем горения
Или сложных веществ разложения.
В них два элемента, один – кислород.
Я отнесу к ним и известь, и лед”.
Какие это вещества?
(Ответ: Оксиды.)
“Они имеют кислый вкус.
В них изменяет цвет лакмус.
C фиолетового на красный”.
(Ответ: Кислоты.)
“В каких веществах у фенолфталеина
Бывает не жизнь, а сплошная малина?”.
(Ответ: Щелочи.)
“Хлориды и нитраты,
Сульфаты, карбонаты
Я без труда и боли
Объединю в класс...”.
(Ответ: Соли.)
Повторение оксидов.
Учитель. Ребята, к нам в гости напрашивается одно вещество. Вы должны отгадать, кто это?
Сценка “Кто я?”.
Я у древних химиков самым главным веществом считалась. “Начало всех начал”, – говорил греческий ученый Фалес, живший в VI в. до н.э. и утверждавший, что окружающий мир возник из меня – “первичной материи”. Я в древности считалась матерью жизни и смерти. Мне поклонялись, а по преданиям древней Руси во мне жили русалки и водяные.
Я у древних народов Азии в прошлом служила причиной войн и борьбы.
Я являюсь вечным двигателем, который не ломается, не ржавеет, не горит, не гниет и никем не уничтожается. Кто я? (Ответ: Вода.)
Учитель. (Слайд 5.) К какому классу веществ относится вода?
Какие вещества называются оксидами?
Ответы обучающихся.
Самостоятельная работа “Крестики нолики”.
Выигрышный путь в обоих случаях составляют формулы оксидов. (После завершения работы – устная проверка ответов). Карточки с заданиями можно раздать каждому ученику, используя Слайд 6-9 можно проверить ответы.
Карточка № 1
| HNO3 | CO2 | O2 |
| SO2 | CuO | NaOH |
| SO2 | MgO | ZnSO4 |
Карточка № 2
| KСlO3 | NaOH | Cu(OH)2 |
| ZnO | SO2 | N 2O3 |
| Na 2O | H 2SO4 | CO2 |
Повторение оснований.
Если в формуле заметишь –
Впереди металл стоит
И своей ОН-подвеской
Как большим хвостом вертит,
Ты не думая ответишь:
“Знаю, это – гидроксид”.
Но гидроксид – начало названия,
А класс веществ – основания.
Учитель. Какие вещества называются основаниями?
Вспомните классификацию оснований. (Слайд 10.)
Ответы обучающихся.
Учитель: Давайте посмотрим “Взаимодействие щелочей с индикаторами” (учитель проводит опыт: взаимодействие фенолфталеина, метилоранжа, лакмуса с раствором гидроксида натрия).
Самостоятельная работа.
Из предложенного списка веществ выбрать основания и отдельно расположить щелочи и нерастворимые основания.
Карточка № 3
NaOH, HCl, LiOH, Cu(OH)2, H 2SO4, Fe(OH)3, CaO, CO2, Ca(OH)2, Al(OH)3.
KОН, H2SO4, Ba(OH)2, Fe(OH)2, CuO, SO2, Zn(OH)2, Mg(OH)2, Al 2O3, HNO3.
Ученики вместе с учителем проверяют правильность выполнения работы. (Слайд 11)
Физминутка. Соответствие движению (игра).
Учитель называет вещества, учащиеся выполняют соответствующее действие (действия записаны на доске). Слайд 13.
| Класс соединений | Действие |
| кислота | поднять правую руку |
| основание | поднять левую руку |
| кислотный оксид | правое ухо |
| основный оксид | левое ухо |
| соль | хлопок в ладоши |
а) Гидроксид кальция, оксид азота (V), фосфорная кислота, нитрат магния, гидроксид меди (II), оксид натрия, серная кислота, хлорид серебра.
Повторение свойств кислот и солей.
Учитель. Дайте определение кислотам. Как классифицируются кислоты? (Схема 2; таблица) (Слайд 14-15)
Ответы обучающихся.
Самостоятельная работа
Задание: Установите соответствия: (сначала выполняют все на оценочных листах, затем один выходит и пишет ответ на доске)
| №№ | Названия кислот | №№ | Названия солей |
| 1 | Соляная | А. | Сульфаты |
| 2 | Серная | Б. | Карбонаты |
| 3 | Угольная | В | Хлориды |
| 4 | Азотная | Г. | фосфаты |
| 5 | Фосфорная | Д. | Нитраты |
Ответы: 1В, 2А, 3Б, 4Д, 5Г.
Учитель. Королева “Кислота” решила устроить бал-маскарад и пригласила на него своих друзей. Гостей прибыло много, все они были в масках Ребята, как королеве отыскать среди гостей своих подруг-кислот?
Правильно, нужно воспользоваться индикаторами (слайд 18).
Учитель: Проведем небольшую исследовательскую работу. Перед вами две пронумерованные пробирки. Вам надо определить, в какой пробирке находится кислота.
- О чём вы должны помнить при выполнении опытов? (Вспоминаем правила техники безопасности: Кислоты и щёлочи, попав на кожу могут вызвать ожог. Осторожно!)
Подведение итогов.
Учитель. Теперь мы с вами подведем итоги.
И для закрепления того, что мы с вами прошли, выполним тест “Улыбка”. В задании по вариантам выберите правильный ответ и обведите красной ручкой или фломастером соответствующие точки на рисунке. А теперь эти точки соедините линией. Затем поднимите свои работы, и я увижу ваши улыбки.
Забавная рожица для ответов на вопросы теста. Верхний ряд кружков соответствует ответу “а”, средний – “б”, нижний – “в”. Если ответы верные, то получается улыбка, как показано на рисунке.
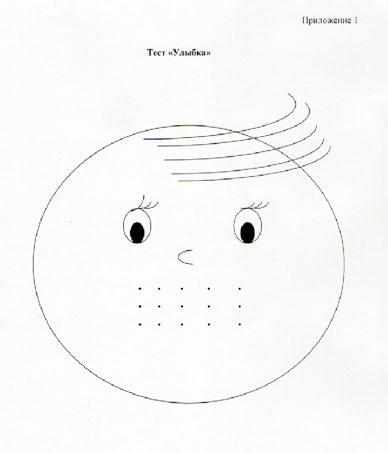
Рисунок 2. Иллюстрация к тесту «Улыбка»
Тест «Улыбка»
Вариант 1.
1) Из предложенного перечня выберите оксид:
а) Na2 О;
б) Na(OH);
в) H3PO4
2) Вещества, состоящие из атомов Н и кислотных остатков называются:
а) основание;
б) кислота;
в) соль.
3) В растворах щелочей фенолфталеин имеет цвет:
а) бесцветный;
б) синий;
в) малиновый.
4) Из предложенного перечня выберите щелочь:
а) гидроксид железа (II);
б) гидроксид натрия;
в) гидроксид цинка (II).
5) Вещества, состоящие из атомов металлов и кислотных остатков называются:
а) соли;
б) кислоты;
в) основания.
Вариант 2.
1) Из предложенного перечня выберите оксид:
а) СО2 ;
б) Са(ОH)2;
в) K2 SО4.
2) Из предложенного перечня выберите щелочь:
а) гидроксид железа(III);
б) гидроксид бария;
в) гидроксид меди (II).
3) В растворах щелочей лакмус имеет цвет:
а) бесцветный;
б) красный;
в) синий.
4) Вещества, состоящие из атомов Н и кислотных остатков называются:
а) основания;
б) кислоты;
в) соли.
5) Вещества, состоящие из атомов металлов и кислотных остатков называются:
а) соли;
б) кислоты;
в) основания.
Домашнее задание.
Подготовиться к контрольной работе, повторить главу 5 .
Заключение и критерии выставления итоговой оценки.
Учитель. С какой трудностью вы столкнулись и как вы решили эту проблему? Что понравилось и не понравилось на уроке? Почему?
(Выслушивается мнение одного-двух учеников. Подводятся итоги.)
1) Если все задания выполнены и большая часть оценок “5” – поставьте “5”;
2) если все задания выполнены, но преобладает оценка “4” – поставьте “4”;
3) если задания сделаны на оценку “3” или “4”, или есть прочерки – поставьте “3”;
4) если вы не справились с двумя и более заданиями – поставьте прочерк.
-
Разработка технологической карты урока по теме «Соединение химических элементов» с использованием дидактического материала
Технологическая карта урока «Классы неорганических соединений»
| Деятельность учителя | Прогнозируемая деятельность обучающегося | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.Организационный момент. | Здравствуйте, ребята. Сегодня на уроке мы будем анализировать, сравнивать, составлять интеллект - карты, решать тесты для того, чтобы повторить изученный материал по темам «Оксиды», «Основания», «Кислоты», «Соли», закрепить умения находить эти вещества, составлять формулы, называть их. | Обучающиеся в течение урока будут оценивать себя по балльно -рейтинговой системе: за каждый правильный ответ или выполненное упражнение на полях листа ставят балл. В конце урока подсчитывают баллы, оценивают свою активность на уроке. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.Обобщение изученного материала. | Задание 1. Учитель предлагает по СЛАЙДАМ 2-3 обучающимся найти общие и отличительные признаки в предложенных формулах химических соединений (Игра: третий-лишний). 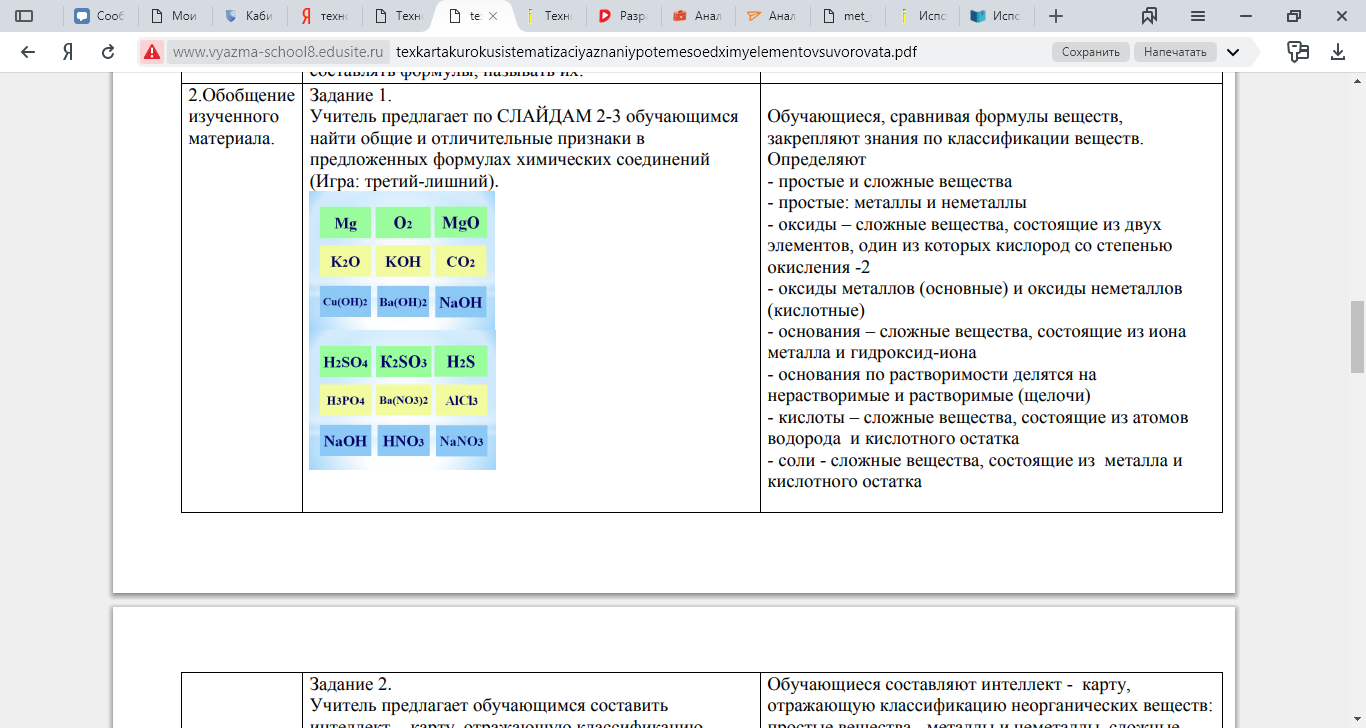  | Обучающиеся, сравнивая формулы веществ, закрепляют знания по классификации веществ. Определяют - простые и сложные вещества - простые: металлы и неметаллы - оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород со степенью окисления -2 - оксиды металлов (основные) и оксиды неметаллов (кислотные) - основания – сложные вещества, состоящие из иона металла и гидроксид-иона - основания по растворимости делятся на нерастворимые и растворимые (щелочи) - кислоты – сложные вещества, состоящие из атомов водорода и кислотного остатка - соли - сложные вещества, состоящие из металла и кислотного остатка | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | Задание 2. Учитель предлагает обучающимся составить интеллект - карту, отражающую классификацию неорганических веществ. (Мини проект) | Обучающиеся составляют интеллект - карту, отражающую классификацию неорганических веществ: простые вещества - металлы и неметаллы, сложные вещества – оксиды (основные и кислотные), основания, кислоты, соли. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Задание 3. Учитель предлагает обучающимся из лежащих на партах конвертов достать карточки с напечатанными формулами веществ, разложить их по группам в соответствии с составленными ими интеллект картами. | Обучающиеся работают в парах, проводят взаимопроверку. Обучающиеся, выполнившие работу быстро и без ошибок, становятся помощниками учителя, подходят к ребятам, испытывающим сложности определения класса соединений по составу формулы. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | Задание 4. Учитель предлагает по СЛАЙДАМ 4-5 обучающимся фронтально решить тестовые упражнения. 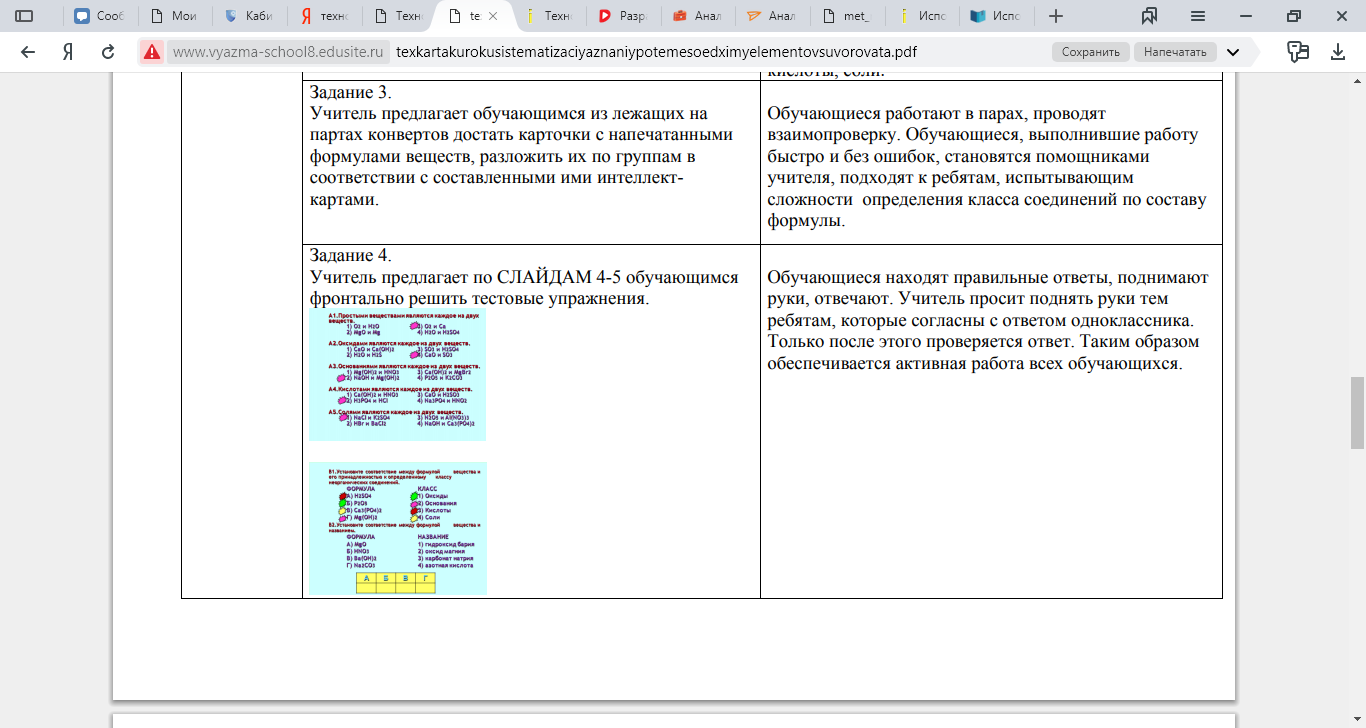  | Обучающиеся находят правильные ответы, поднимают руки, отвечают. Учитель просит поднять руки тем ребятам, которые согласны с ответом одноклассника. Только после этого проверяется ответ. Таким образом обеспечивается активная работа всех обучающихся. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Задание 5. Учитель предлагает обучающимся выполнить упражнение по составлению формул солей, пользуясь таблицей растворимости. Для этого предлагает обучающимся вспомнить правила составления формул по СЛАЙДАМ 6-10 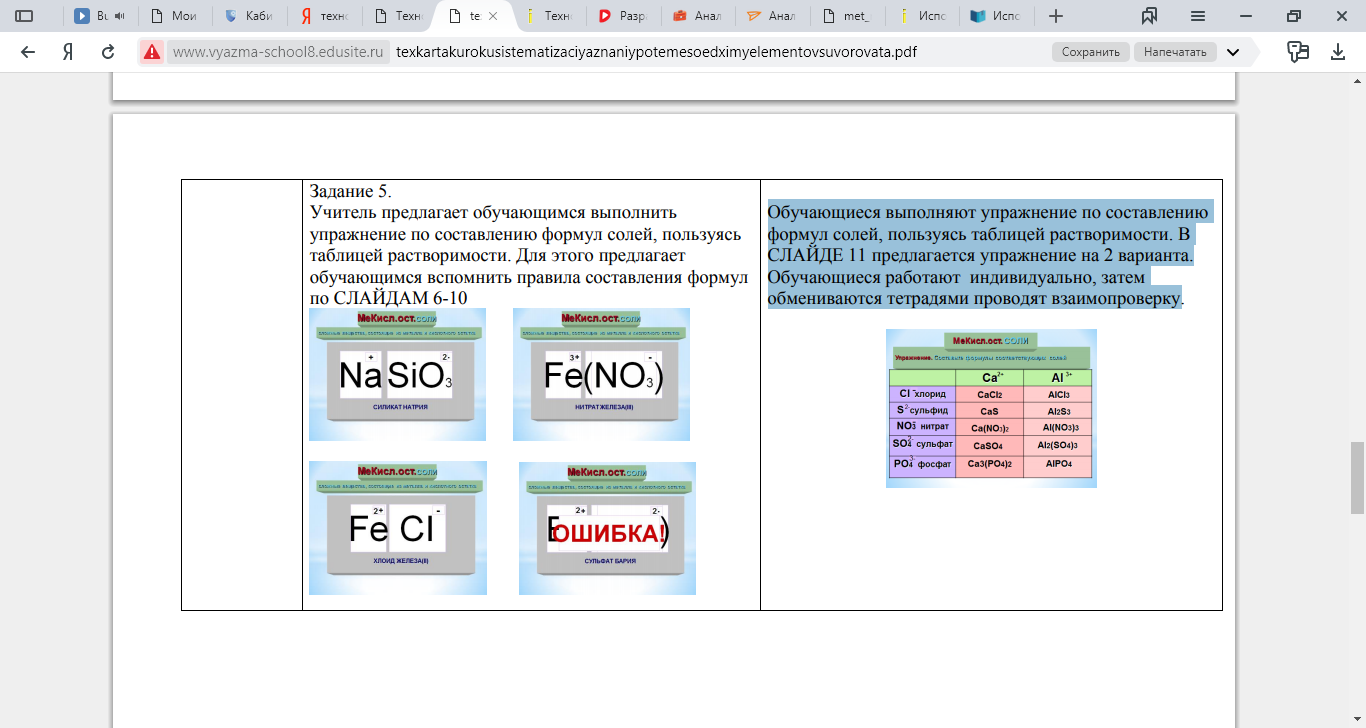 | Обучающиеся выполняют упражнение по составлению формул солей, пользуясь таблицей растворимости. В СЛАЙДЕ 11 предлагается упражнение на 2 варианта. Обучающиеся работают индивидуально, затем обмениваются тетрадями проводят взаимопроверку  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | Задание 6. Учитель предлагает обучающимся на составленных интеллект - картах цветным карандашом одного цвета соединить металл – основный оксид (оксид металла) – основание – соль; карандашом другого цвета соединить неметалл – кислотный оксид (оксид неметалла) – кислота – соль. | Обучающиеся таким образом выявляют генетическую связь химических соединений. Подтверждение находят своему открытию на СЛАЙДЕ 12. 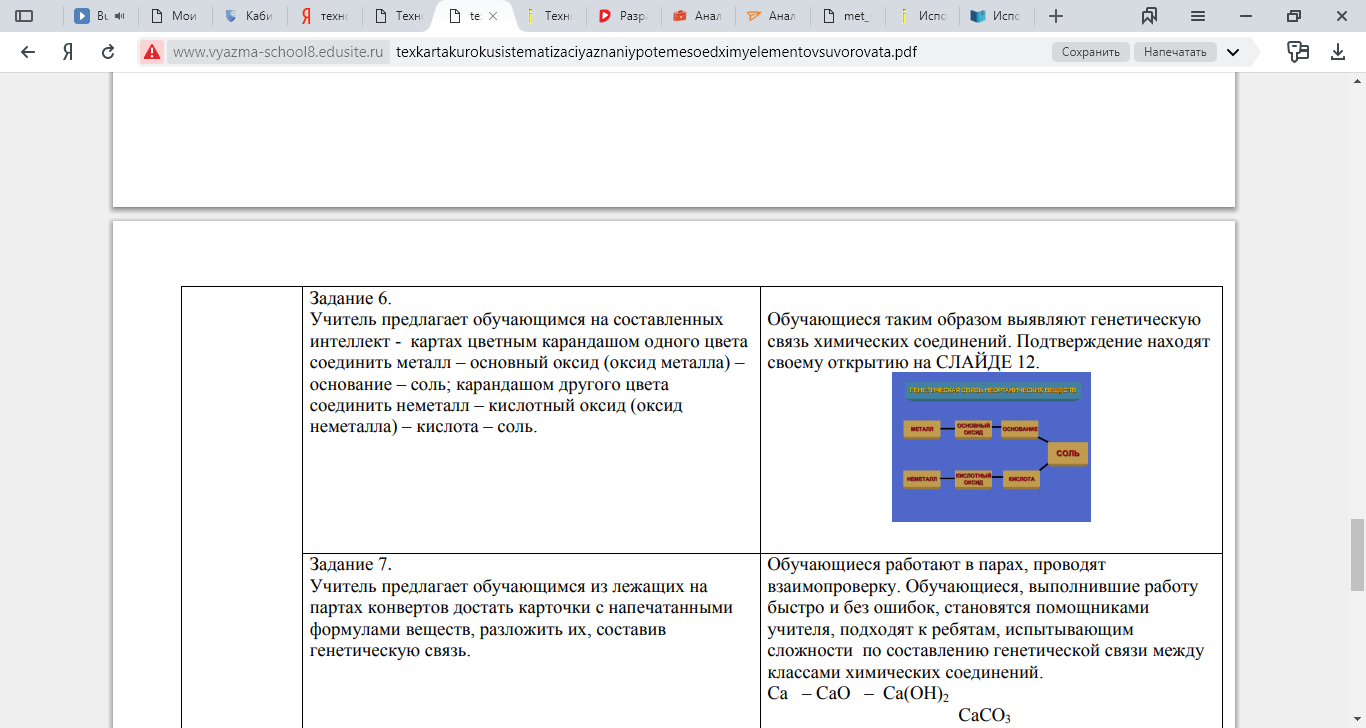 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Задание 7. Учитель предлагает обучающимся из лежащих на партах конвертов достать карточки с напечатанными формулами веществ, разложить их, составив генетическую связь. | Обучающиеся работают в парах, проводят взаимопроверку. Обучающиеся, выполнившие работу быстро и без ошибок, становятся помощниками учителя, подходят к ребятам, испытывающим сложности по составлению генетической связи между классами химических соединений. Са – СаО – Са(ОН)2 СаСО3 С – СО2 – Н2СО3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Домашнее задание. | Учитель предлагает обучающимся письменно составить 2 цепочки СЛАЙДЫ 13-14. 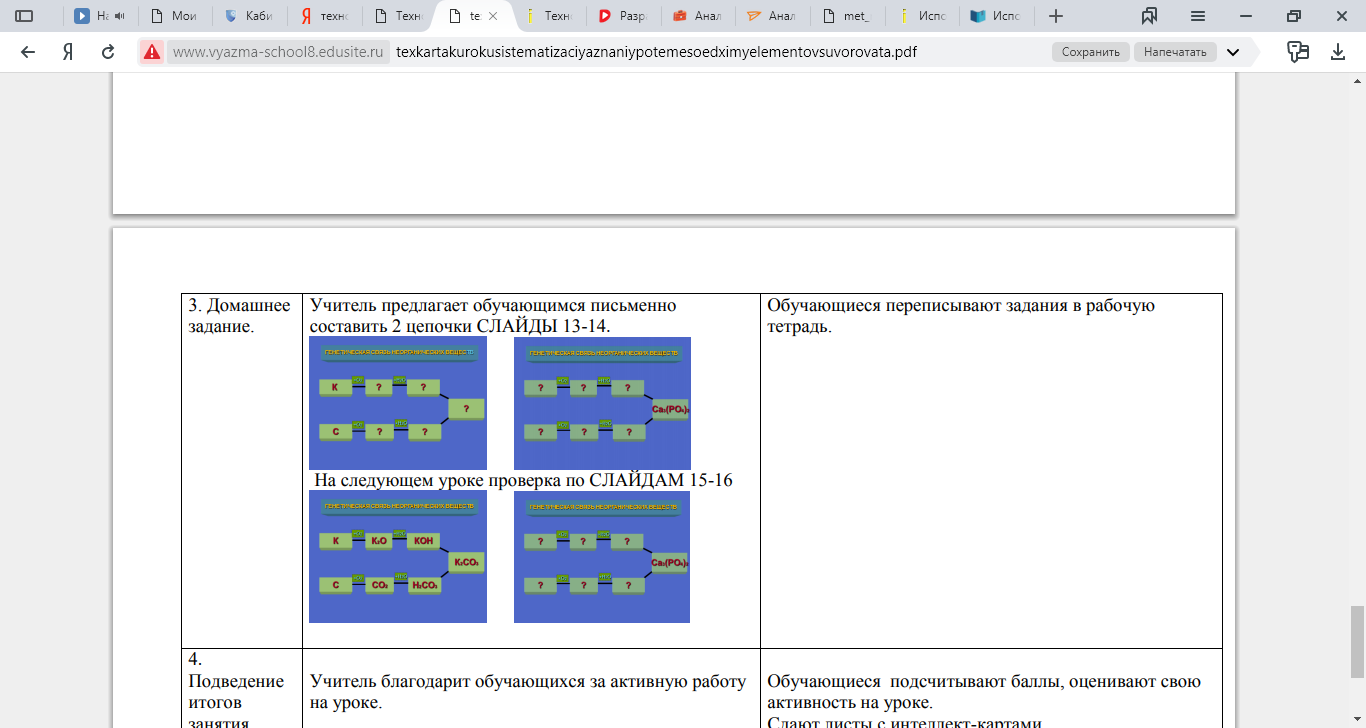 На следующем уроке проверка по СЛАЙДАМ 15-16  | Обучающиеся переписывают задания в рабочую тетрадь. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Подведение итогов занятия. | Учитель благодарит обучающихся за активную работу на уроке. | Обучающиеся подсчитывают баллы, оценивают свою активность на уроке. Сдают листы с интеллект-картами | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Рефлексия | Учитель просит поднять приготовленные за ранее кружки. Красные – я работал творчески Желтые – я старался, но что-то не получалось Белые – я не старался, урок прошел и это хорошо | Обучающиеся подняли только красные и желтые кружки. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||