ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.01.2024
Просмотров: 64
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Вопросы к экзамену по дисциплине «Минералогия», часть I II семестр 2022 г.
-
Предмет и задачи минералогии. Ее связь с другими науками.
Слово «минералогия» впервые прозвучало в 1636. В 18-ом веке оно было узаконено в литературе.
Минералогия – наука изучающая состав и свойства минералов, условия их образования в природе, процессы изменения и причины гибели.
Предмет: минерал, его химический состав, свойства, структура и условия образования
Задачи:
1. разработка научной классификации выявление связей между их составом, строением, свойствами и условиями образованиями.
2. создание научных основ для поисков и оценки месторождений полезных ископаемых, совершенствование технологии его переработки, вовлечение новых видов минерального сырья в промышленное производство.
3. разработка методов искусственного выращивания минералов.
-
Этапы возникновения и становления минералогии.
-
Каменный век (палеолит(20 минералов) и неолит(40)) – от появления каменных орудий до распространения орудий из меди и бронзы. Знакомство человека с металлом обусловливает переход к культуре меди, бронзы, и железа
-
Знакомство со свойствами – древние египтяне, шумеры, индийцы, греки.
-
Аристотель – трактаты о свойствах минералов (классификация минеральных тел на камни и руды)
-
Плиний Старший – 37 томов естественной истории (5 о геологии и минералогии)
4 трактата о камнях (свойства и условия местонахождения минералов) Много вымысла.
-
Эпоха феодализма:
-
Лапидарии – средневековые сборники с описаниями драг. камней. -
Ал-Бируни – «Собрание сводок для познания драгоценностей»: описал 36 минералов, к которым также отнес органические соединения (камни мускусных животных, жемчуг) и искусственные образования (стекло, эмаль, фарфор) и 12 металлов, в том числе 4 сплава. -
Георгий Бауэр(Агрикола)– «О происхождении минералов» (1546 г.), «О природе ископаемых» (1546 г.), «О горном деле» (1550 г.) Агрикола подробно описывает физические свойства минералов: спайность, твердость, относительный вес, цвет, блеск и пр., а также их внешнюю форму.
-
15-16 вв. – увеличение добычи различных полезных ископаемых.
Бернард Цезий (Италия) – применение слова «минералогия» (1636 г.)
Успехи в области кристаллографии (французы одни из лидеров) 17 в.
До 18 века – описательный характер
-
18 век – формирование минералогии как науки
Сформировано два направления:
-
Морфоописательное – описание внешних форм минералов. -
Химикогенетическое –использование вновь появившихся знаний.
Объяснение химического состава и условий образования
Михаил Севергин – критика классификации Вернера (попытка применить хим.принципы к классификации)
1773 г. – Открытие Горного училища в Петербурге (Горный институт)
1817 г. – Основание «Минералогического общества» в Петербурге
-
Начало 19 века – окончательное формирование науки
Два направления:
-
графическое – изучение геометрических форм -
Химическое – изучение состава минерала
-
Вторая половина 19 века – упрочение микроскопического метода
*химический принцип (Фёдоров) – закономерность хим.состава минералов, их структуры и свойств, взаимосвязь между ними.
*Генетический принцип (Вернадский) – зависимость данных закономерностей от условий образования как отдельных минералов, взаимных ассоциаций во времени и пространстве.
-
Развитие экспериментальной минералогии -
Анатолий Бетехтин
-
Начало 20 века – Золотой век геологии и минералогии
1958 г. – образование международной минералогической ассоциации (14 стран), упорядочение минералогических знаний.
3. Основные понятия минералогии (минерал, минеральный вид, минеральный индивид). Количество минеральных видов и индивидов в природе. Причины, определяющие это.
Минерал – химически и физически индивидуализированный неорганический продукт природной физико-химической реакции, находящийся в кристаллическом состоянии или утративший его в результате метамиктного распада.
Минеральный вид – совокупность минералов одинаковой структуры, состав которых отвечает индивидуализированному соединению и может непрерывно меняться в пределах, ограничивающихся изменением структуры или в условно принятых границах.
Минеральный индивид – кристаллическое неделимое любой формы и размера образование.
В настоящее время число минеральных видов лишь несколько превышает 4600. Количество же минеральных индивидов определить невозможно
, так как в них входит каждый отдельный кристалл и любое зерно любой формы и размера.
Ограниченность количества минеральных видов в природе объясняется действием в пределах земной коры законов геохимии и термодинамики.
- Первая, заключается в отсутствии сильно различающихся физических воздействий (температуры и давления), Следовательно, для ряда химических элементов просто не возникают условия их воссоединения, а значит, не возникают потенциально возможные минералы такого состава.
- Второй причиной является крайне неравномерное распределение химических элементов в пределах земной коры, что также препятствует их соединению с образованием соответствующих минеральных видов.
4. Обусловленность появления физических свойств минералов, разновидности минералов, их свойства.
Разновидность – изменение физических свойств в пределах минерального вида в связи с изменением химического состава:
-
По цвету (кварц) -
По агрегатному состоянию (кварц, халцедон) -
По плотности
Физические свойства минералов обусловлены хим. составом и строением кристаллической решётки.
Группы физических свойств
-
Морфологические: облик, габитус, характер двойников, типы минеральных агрегатов -
Оптические (св-ва, которые воспринимаются нашими органами зрения (визуально)): прозрачность, цвет, цвет черты, блеск -
Механические: спайность, отдельность, излом, твёрдость, хрупкость, ковкость, упругость, пластичность -
Прочие: плотность, магнитность, радиоактивность, растворимость, люминесценция, вкус, запах, химические реакции.
5. Кристаллическая структура минералов. Кристалл. Элементы кристаллической решётки и элементы кристалла.
Структура– способ пространственной организации структурных элементов минерала. Включает в себя атомы, ионы, молекулы.
Существует 2 модели строения атома:
-
Классическая модель:
Атом представляет собой сферу, внутри которой расположено положительно заряженное ядро(состоит из протонов и нейтронов), в котором концентрируется положительный заряд, равный заряду электронов, вращающихся вокруг ядра по соответствующим орбитам. Атом представляет собой электронейтральную частицу.
-
Квантово-механическая модель
Кристаллическая решетка минералов
–это бесконечное трехмерное периодически повторяющееся образование.
Элементы кристаллической решетки:
А) Узлы кристаллической решетки – материальные точки, использующиеся для построения кристаллической решётки.
Б) Ряд - прямая, проведенная через 2 и более узла кристаллической решётки.
В) Плоская сетка- плоскость, проведённая минимум через 3 узла кристаллической решётки
Элементы кристалла: Вершины(=узлы), ребра(=ряды), грани(=сетки).
6. Химическая связь в минералах. Ее природа, типы и отражение в физических свойствах минералов.
Химическая связь - сила, которая возникает между структурными элементами кристаллической решётки и удерживает её в стабильном состоянии.
Химическая связь имеет электростатическую природу, т. к. под химической связью понимают электрические силы притяжения, удерживающие частицы друг около друга (частицами могут быть атомы, молекулы или ионы).
Типы химической связи:
-
Ионная связь - Осуществляется взаимным электростатическим притяжением противоположно заряженных частиц. Ее образованию предшествует ионизация нейтральных атомов, т.е. переход электрона с внешнего слоя одного ядра на другой (+анионы, - катионы). Чем больше заряд и меньше ионный радиус, тем ионная связь сильнее. Она является ненаправленной (силы притяжения и отталкивания действуют во все стороны одинаково) и ненасыщенной (два притянутых друг к другу иона не теряют способность взаимодействия с другими).
Большинство минералов с ионной связью довольно светло окрашены, прозрачные или полупрозрачные и имеют большую твёрдость.
-
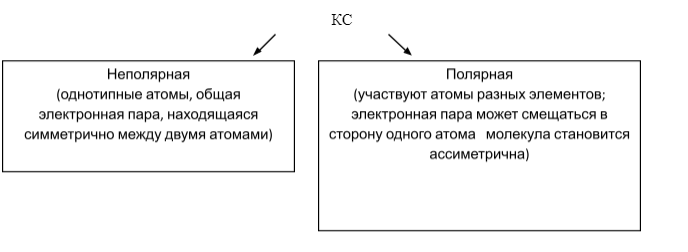
Ковалентная связь - осуществляется посредством образования общей электронной пары между атомами, отдающими по одному электрону на образование этой пары. В образовании участвуют лишь неспаренные электроны с разными спинами. Причиной ее возникновения служит желание перейти в устойчивое состояние с заполненным внешним электронным уровнем.
В КС могут участвовать одинаковые и различные атомы, поэтому:
-
Металлическая связь - характерна для класса самородных элементов. Характеризуется тем, что в узлах кристаллической решетки находится атомы металла, от которых отделяются электроны внешнего электронного уровня и, свободно перемещаясь по узлам кристаллической решетки, осуществляют ХС, обеспечивая стабильность структуры. Благодаря такому типу ХС самородные металлы обладают металлическим блеском, высокой тепло- и электропроводностью, ковкостью и низкой твердостью. -
Ван-дер-Ваальсовская связь- самая слабая химическая связь, возникающая между нейтральными частицами благодаря их строению и возникновению дипольности.
7. Понятие координационного числа. Координационные полиэдры.
Координационное число- число ближайших равноудалённых атомов или ионов в кристаллической решётке минерала. Координационное число отражает плотность упаковки структурных единиц.
Чаще всего принимаю значения 3, 4, 6, 8, 12.
Координационные полиэдры- термин, характеризующий геометрию расположения атомов вокруг центрального атома. Координационный полиэдр – многогранник, в вершине которого расположены атомы.
8. Элементарная ячейка минерала. Параметры элементарной ячейки.
Элементарной ячейкой - называется минимальный по объёму параллелепипед в кристаллической решётке минерала, который, во-первых, полностью соответствует составу минерала, а во-вторых, позволяет построить весь кристалл простым его перемещением в трёх измерениях. Элементарную ячейку можно сравнить с кирпичом в стене, поскольку, повторяя её в пространстве, можно заполнить весь объём решётки.
Параметры элементарной ячейки:
- 1) Углы α, β, γ между направлениями. Принятыми за координатные оси X, Y, Z.
- 2) a, b, c - отрезки отсекаемые по этим осям.
- 3) Z – количество структурных единиц в элементарной ячейке. Z всегда целое число
9. Явление полиморфизма в минералогии. Скорость и температура полиморфного перехода. Свойства полиморфных модификаций.
Полиморфизм – явление существования вещество одного и того же химического состава, но разной кристаллической структуры.
Природные соединения одинакового состава, но разной структуры относятся к разным минералам. Такие минералы получили название полиморфных модификаций (ПМ), а само явление, при котором одно и то же химические соединение может находиться в разных структурных формах, имея разную кристаллическую решетку, названо полиморфизмом.
ПМ отличаются:
- либо сингонией, либо симметрией,
- типами химических свойств,
- характером химической связи,
- координационным числом катионов,
- степенью упорядочения ионов.
ПМ образуются при изменении температуры. Каждая ПМ образуется в своей области температур и давления. В этой области модификация может находиться сколь угодно долго, оставаясь стабильной.
Та температура, при которой происходит полиморфный переход одной модификации в другую, получила название