Файл: Исследование кинетики омыления сложного эфира Цель работы Определить константу скорости реакции омыления сложного эфира щелочью.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 10.01.2024
Просмотров: 71
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Лабораторная работа № 8. Исследование кинетики омыления
сложного эфира
Цель работы
Определить константу скорости реакции омыления сложного эфира щелочью.
Сущность работы
Реакциями омыления называют реакции разложения сложных эфиров под действием щелочей, например, взаимодействие уксусно-этилового эфира и гидроксида натрия протекает по реакции: CH3COOC2H5 + NaOH = CH3COONa + C2H5OН, которая протекает по суммарному второму порядку (по первому порядку для каждого из компонентов). Кинетическое уравнение реакции описывается формулой:
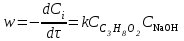 .
. Оборудование и реактивы
Магнитная мешалка с якорем – 1 шт., штатив лабораторный с муфтой и лапой – 1 шт., мерная колба объемом 500 мл – 1 (2) шт.; бюретка объемом 25 мл – 1 шт.; коническая колба объемом 100 или 250 мл – 10 шт.; реактор объемом 1000 мл (банка или круглая колба с пробкой) – 1 шт.; стакан химический объёмом 100 мл – 1 шт., стакан химический объёмом 50 или 75 мл – 2 шт., мерная пипетка объемом 10 мл – 2 шт.; градуированная пипетка объёмом 5 или 10 мл – 1 шт., соляная кислота – 0,05 М раствор; гидроксид натрия – 0,05 М раствор; уксусно-этиловый эфир, фенол-фталеин – 1 % раствор в этаноле.
Выполнение работы
1. Вычислить объем эфира, необходимый для приготовления 500 мл его ратсвора концентрацией 0,05 моль/л по формуле:
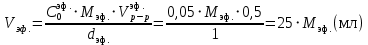
2. В каждую из конических колб объемом 100 или 200 мл мерной пипеткой налить 10 мл раствора соляной кислоты концентрацией 0,05 моль/л.
3. Приготовить 500 мл раствора эфира в воде концентрацией 0,05 М: в мерную колбу объемом 500 мл градуированной пипеткой рассчитанный в п. 1 объем эфира и довести объем раствора в мерной колбе до метки дистиллированной водой.
4. В емкость объемом 1 л (реактор) вылить приготовленный в п. 2 раствор эфира и добавить при помощи мерного цилиндра 500 мл 0,05 М раствора гидроксида натрия.
5. Засечь время начала реакции и перемешать раствор.
6. Через 10 минут после начала реакции отобрать из реактора пробу объемом 10 мл при помощи мерной пипетки, перенести ее в коническую колбу объемом 200 мл № 1, содержащую 10 мл раствора соляной кислоты.
7. Еще через 10 минут отобрать из реактора пробу объемом 10 мл при помощи мерной пипетки, перенести ее в коническую колбу объемом 200 мл № 2.
8. Всего надо собрать от 6 до 10 проб.
9. Все пробы титровать щелочью в присутствии фенолфталеина. Титрант – 0,05 М NaOH.
Содержание протокола лабораторной работы
| Название эфира | |
| Химическая брутто-формула | |
| Молярная масса эфира 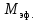 , г/моль , г/моль | |
| Концентрация раствора эфира: 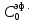 , моль/л , моль/л | |
| Объем раствора эфира 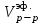 , мл , мл | |
| Объем эфира, взятого на приготовление раствора: Vэф., мл | |
| Объем раствора щелочи, взятого на омыление: VNaOH, мл | |
| Концентрация раствора щелочи, взятого на омыление: СNaOH, моль/л | |
| Объем пробы, отбираемой для анализа: 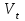 , мл , мл | |
| Концентрация соляной кислоты: 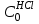 , моль/л , моль/л | |
| Объем соляной кислоты, отбираемой для остановки реакции 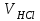 , мл , мл | |
| Концентрация щелочи для титрования: 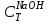 , моль/л , моль/л | |
Результаты титрования проб:
| № | t, мин | 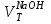 , мл , мл |
| 1 | 10 | |
| 2 | 20 | |
| 3 | 30 | |
| 4 | 40 | |
| 5 | 50 | |
| 6 | 60 | |
| 7 | 70 | |
| 8 | 80 | |
| 9 | 90 | |
| 10 | 100 | |
Обработка результатов эксперимента
1. По результатам титрования для каждой из отобранных проб рассчитать концентрацию гидроксида натрия
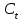 по формуле
по формуле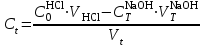
2. Заполнить таблицу
| № | t, мин |  , мл , мл | 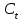 | ‑ 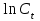 | 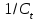 | 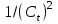 |
| 1 | 10 | | | | | |
| 2 | 20 | | | | | |
| 3 | 30 | | | | | |
| | … | | | | | |
| 10 | 100 | | | | | |
3. По данным таблицы построить
3.1) зависимость
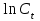 от времени;
от времени;3.2) зависимость
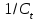 от времени;
от времени;3.3) зависимость
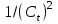 от времени.
от времени.4. Для каждой из зависимостей построить линейную линию тренда и вывести на график уравнение линии тренда и коэффициент апппроксимации.
5. Выбрать зависимость, у которой коэффициент аппроксимации будет ближе всего к единице.
6. Угловой коэффициент уравнения линии тренда – значение константы скорости реакции.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.