Файл: Факультет химикофармацевтических технологий и биомедицинских препаратов Кафедра.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 174
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Температурный режим:
| | Время, мин | Температура (°C) |
| Колонка | 0 - 1,6 | 40 |
| 1,6 - 9,9 | 40 65 | |
| 9,9 - 13,6 | 65 175 | |
| 13,6 - 20,0 | 175 | |
| Блок ввода проб | | 200 |
| Детектор | | 200 |
Хроматографируют испытуемый раствор и раствор сравнения В.
Относительные времена удерживания компонентов: этанол - 1 (около 5,3 мин); метанол - около 0,8; 2-пропанол - 1,2; пропанол - около 1,6.
Пригодность хроматографической системы с использованием раствора сравнения В определяется в соответствии с со следующим уточнением:
- разрешение (R) между пиками метанола и этанола должно быть не менее 5;
- фактор асимметрии пика (AS) каждого компонента должен быть от 0,8 до 1,5.
Содержание 2-пропанола в объемных процентах (X, %) в испытуемом лекарственном средстве вычисляют по формуле:
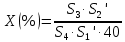
Где S3 - площадь пика 2-пропанола на хроматограмме испытуемого раствора;
S4 - площадь пика 2-пропанола на хроматограмме раствора сравнения В;
S'1 - площадь пика внутреннего стандарта на хроматограмме испытуемого раствора;
S'2 - площадь пика внутреннего стандарта на хроматограмме раствора сравнения В.
Норма содержания 2-пропанол – не более 0,5 %
Бактериальные эндотоксины. Испытание проводят в соответствии с ФЕАЭС, ОФС 2.1.6.8. Бактериальные эндотоксины, по методике ГФ XIV, ФС.2.1.0098.18 «Дротаверина гидрохлорид».
Для проведения испытания готовят исходный раствор субстанции (концентрация 10 мг/мл), а затем разбавляют его не менее чем в 200 раз.
Контроль по показателю качества "Бактериальные эндотоксины" проводят в субстанции, предназначенной для производства лекарственных препаратов для парентерального применения.
Не более 4,3 ЕЭ на 1 мг активного вещества субстанции.
Микробиологическая чистота.
Определение проводится в соответствии с Фармакопеей ЕАЭС, ОФС 2.1.6.6 Микробиологические испытания нестерильных лекарственных средств: общее количество жизнеспособных аэробных микроорганизмов и 2.1.6.7 Микробиологические испытания нестерильных лекарственных средств на наличие отдельных видов микроорганизмов методом прямого посева. Выбор категории микробиологической чистоты осуществляют в соответствии с ФЕАЭС, ОФС 2.3.1.2 Требования к микробиологической чистоте лекарственных препаратов, фармацевтических субстанций и вспомогательных веществ для их производства.
Субстанция в условиях испытания не обладает антимикробным действием.
Категория 1.2Б.
Количественное определение. Определение проводят методом титриметрии (ФЕАЭС, ОФС 2.1.2.19. Потенциометрическое титрование по методике из ФС.2.1.0098.18 «Дротаверина гидрохлорид»).
Около 0,3 г (точная навеска) субстанции растворяют в 20 мл уксусной кислоты ледяной, прибавляют 3 мл раствора ртути (II) ацетата и титруют 0,1 М раствором хлорной кислоты до появления зеленого окрашивания (индикатор - 0,1% раствор кристаллического фиолетового).
Параллельно проводят контрольный опыт.
1 мл 0,1 М раствора хлорной кислоты соответствует 43,40 мг дротаверина гидрохлорида C24H31NO4·HCl.
Упаковка. Проводится в соответствии ГФ XIV ОФС.1.1.0025.18 «Упаковка, маркировка и транспортирование лекарственных средств».
По 5, 7, 10 кг фармацевтической субстанции в мешок из пленки полиэтиленовой (первичная упаковка) по ГОСТ 12302-2013. Мешок помещают в пакет из бумаги мешочной. (вторичная упаковка) по ГОСТ 33772-2016.
По 20, 25 кг фармацевтической субстанции в мешок из пленки полиэтиленовой (первичная упаковка) по ГОСТ 12302-2013. Мешок помещают в картонный барабан (вторичная упаковка) по ГОСТ 17065-94.
Транспортирование. Проводится в соответствии ГФ XIV ОФС.1.1.0025.18 «Упаковка, маркировка и транспортирование лекарственных средств». Транспортирование (перевозка) лекарственных средств осуществляется всеми видами транспорта (автомобильным, железнодорожным, авиационным, морским, речным) в закрытых транспортных средствах, соблюдая правила перевозки грузов, установленные для соответствующего вида транспорта. Лекарственные средства, подлежащие транспортированию, должны быть помещены в контейнер (грузовой) или другую, регламентированную действующими стандартами, транспортную упаковку.
Хранение. В защищенном от света месте при температуре не выше 25 °С.
Срок годности. 5 лет.
Фармакологическая группа. Спазмолитическое средство
Приложение.
Синтез фармацевтической субстанции. (Бахарев В. П. Способ получения дротаверина гидрохлорида: пат. RU2661150С9 – 2015.) [1]
Стадия ТП-1: Получение о-диэтоксибензола (ОДЕБ) формулы
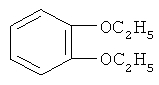
путем взаимодействия пирокатехина с диэтилсульфатом в щелочной среде при температуре 50-60ºС.
Стадия ТП-2: Получение диэтоксинитрила (ДЭН) формулы
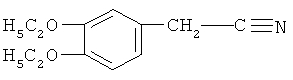
путем взаимодействия ОДЕБ с параформом в присутствии HCl и цианировании полученного диэтоксибензилхлорида (ДЭБХ) при температуре 80-85ºС.
Стадия ТП-3: Получение 3,4-диэтоксифенилуксусной кислоты (ДЭФУ кислоты) формулы
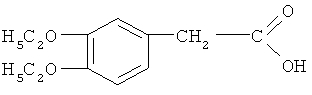
путем взаимодействия диэтоксинитрила со стадии ТП-2 с гидроксидом натрия и выделением диэтоксифенилуксусной кислоты соляной кислотой.
Стадия ТП-4: Получение диэтоксиамина (ДЭАмина) формулы
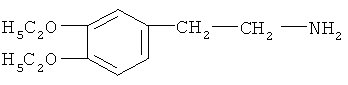
путем каталитического гидрирования диэтоксинитрила со стадии ТП-2, где в качестве катализатора используется никель - Ренея.
Стадия ТП-5: Получение этоксиамида (ЭАмида) формулы
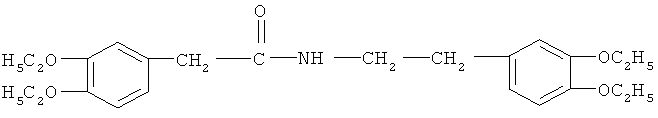
путем конденсации диэтоксифенилуксусной кислоты, полученной на стадии ТП-3 с диэтоксиамином, полученным на стадии ТП-4.
Стадия ТП-6: Получение технического дротаверина гидрохлорида формулы
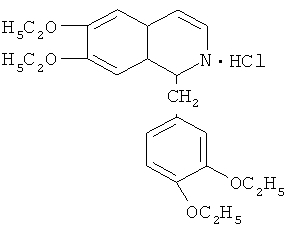
путем циклизации этоксиамида со стадии ТП-5 с помощью POCl3 и дегидрировании полученного вещества в присутствии катализатора никеля - Ренея.
Стадия ТП-7: Получение фармакопейного дротаверина гидрохлорида перекристаллизацией технического дротаверина со стадии ТП-6 в среде 2-пропанола с подкислением хлористым водородом. По окончании кристаллизации реакционная масса перемещается на центрифугу и промывается 2-пропанолом. По окончании промывки паста дротаверина гидрохлорида передается на стадию сушки.
Органические растворители используются только на заключительной стадии синтеза, когда технический дротаверин растворяют в 2-пропаноле и сам оканчательный продукт промывается тем же спиртом.
Таблица 1. Растворители, используемые
| № | Растворитель | Стадия процесса | Класс токсичности |
| 1 | 2-пропанол | последняя | 3 |
В процессе синтеза фармацевтической субстанции используется следующий растворитель: 2-пропанол (растворитель класса 3, согласно таблице 2.3.2.0.-5). Предельная суточная доза фармацевтической субстанции составляет 240 мг (ГРЛС № ЛС-001745), что превышает 10 г и допустимые нормы концентраций растворителей 3 класса токсичности на последней стадии (2-пропанола), превышающее 50 мг/сут (соответствует 5000 ppm или 0,5 % по Способу 2). Содержание растворителя 3 класса, который в данном способе получения использован на последних стадиях, должен быть ограничен и нормирован.
Таблица 2. Нормируемые растворители
| № | Растворитель | Стадия процесса | Класс токсичности | ПДК/ppm |
| 1 | 2-пропанол | последняя | 3 | 5000 |
Список литературы
-
Государственная фармакопея Российской Федерации / МЗ РФ. – XIV изд. – Т.3. – Москва, 2018. – 3820 с. -
Фармакопея Евразийского экономического союза. URL:[http://www.eurasiancommission.org/ru/act/texnreg/deptexreg/LSMI/Pages/pharmacopoeia_utv.aspx](Дата обращения 10.05.2023). -
Пат. 2561489С2 Российская Федерация / Бахарев В.П.; заявитель и патентообладатель. – No 2013122379/04 ; заявл. 14.05.2013; опубл. 27.08.2015, Бюл. No 24. URL:[https://patents.s3.yandex.net/RU2561489C2_20150827.pdf](Дата обращения 10.05.2023). -
Государственный реестр лекарственных средств. [https://grls.minzdrav.gov.ru/Grls_View_v2.aspx?routingGuid=bf67bb45-298d-45a0-a03a-9bbee2b1ecbc](Дата обращения 10.05.2023).