Файл: Отчет по практике вид (тип) практики Преддипломная практика Курс (группа).docx
Добавлен: 11.01.2024
Просмотров: 186
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
1.3. Свойства пероксидазы хрена
1.4. Инактивация пероксидазы хрена
1.5. Методы выделения пероксидазы хрена
1.6. Применение пероксидазы хрена
2.1. Выделение пероксидазы хрена
2.2. Определение концентрации фермента
3.1. Выделение и концентрирование пероксидазы хрена
3.2. Количественное определение белка
Вторая реакция не очень специфична, но весьма чувствительна. Поэтому метод Лоури позволяет вести определения белков в сильно разбавленных растворах.
Таблица 2. Данные для построения градуировочного графика

y = 0,0039x+0,06
R2 = 0,9923
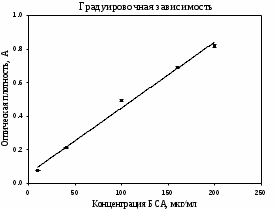
Рисунок 3. Градуировочный график по методу Лоури
Полученная зависимость была обработана в координатах линейного уравнения:
y = a∙x + y0
Таблица 3. Параметры уравнения для градуировочного графика
Таблица 4. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
0,186 = 0,0039x + 0,06; x = 32,31 мкг/мл
0,185 = 0,0039x + 0,06; x = 32,05 мкг/мл
0,184 = 0,0039x + 0,06; x = 31,79 мкг/мл
Разбавление в 200 раз
x = 32,1∙200 = 6420 мкг/мл; x = 6,42 мг/мл
Таблица 5. Данные измерения оптической плотности в растворенном осадке после высаливания 70% и его концентрация
0,455 = 0,0039x + 0,06; x = 101,28мкг/мл
0,456 = 0,0039x + 0,06; x = 101,54 мкг/мл
0,463 = 0,0039x + 0,06; x = 103,3 мкг/мл
Разбавление в 200 раз
x = 102∙200 = 20400 мкг/мл; x = 20,04 мг/мл
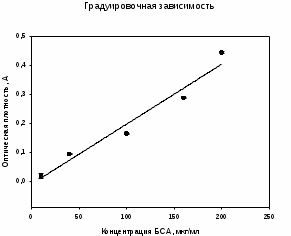
Таблица 6. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
Таблица 6. Параметры уравнения для градуировочного графика
Таблица 7. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
0,138 = 0,002x - 0,01; x = 70,48 мкг/мл
0,140 = 0,002x - 0,01; x = 71,43 мкг/мл
0,137 = 0,002x - 0,01; x = 70,00 мкг/мл
Разбавление в 200 раз
x = 71∙200 = 14200 мкг/мл; x = 14,2 мг/мл
Таблица 8. Данные измерения оптической плотности в растворенном осадке после высаливания 70% и его концентрация
0,470 = 0,0020x - 0,01; x = 228,57 мкг/мл
0,500 = 0,0020x - 0,01; x = 242,86 мкг/мл
0,500 = 0,0020x - 0,01; x = 242,86 мкг/мл
Разбавление в 200 раз
x = 238∙200 = 47600 мкг/мл; x = 47,6 мг/мл
Концентрирование проводили на концентрирующих фильтрах 10 кДа, центрифугировали при 5000 об/мин. Концентрация фермента после концентрирования в фракции после 35% высаливания увеличилась примерно в 2,2 раза, а концентрация в фракции после 70% высаливания увеличилась примерно в 2,4 раза.
Таблица 2. Данные для построения градуировочного графика
| № пр. | Сбелка, мкг/мл | А1 | А2 | А3 | Аср |
| 1 | 10 | 0,074 | 0,076 | 0,077 | 0,076 |
| 2 | 40 | 0,212 | 0,211 | 0,208 | 0,210 |
| 3 | 100 | 0,490 | 0,494 | 0,497 | 0,494 |
| 4 | 160 | 0,684 | 0,686 | 0,695 | 0,688 |
| 5 | 200 | 0,811 | 0,818 | 0,828 | 0,819 |

y = 0,0039x+0,06
R2 = 0,9923

Рисунок 3. Градуировочный график по методу Лоури
Полученная зависимость была обработана в координатах линейного уравнения:
y = a∙x + y0
Таблица 3. Параметры уравнения для градуировочного графика
| Параметр | Значение | Доверительный интервал |
| a, см3/мкг | 0,0039 | 0,0002 |
| y0 | 0,06 | 0,03 |
3.2.1. Количественное определение белка в растворенном осадке после высаливания 35% от насыщения сульфата аммония
Таблица 4. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
| А | Концентрация (X), мкг/мл | 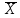 | Доверительный интервал (δX) | Концентрация 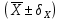 , мкг/мл , мкг/мл |
| 0,186 | 32,31 | 32,05 | 0,7 | 32,1±0,7 |
| 0,185 | 32,05 | |||
| 0,184 | 31,79 |
0,186 = 0,0039x + 0,06; x = 32,31 мкг/мл
0,185 = 0,0039x + 0,06; x = 32,05 мкг/мл
0,184 = 0,0039x + 0,06; x = 31,79 мкг/мл
Разбавление в 200 раз
x = 32,1∙200 = 6420 мкг/мл; x = 6,42 мг/мл
3.2.2. Количественное определение белка в растворенном осадке после высаливания 70% от насыщения сульфата аммония
Таблица 5. Данные измерения оптической плотности в растворенном осадке после высаливания 70% и его концентрация
| А | Концентрация (X), мкг/мл |  | Доверительный интервал (δX) | Концентрация  , мкг/мл , мкг/мл |
| 0,455 | 101,28 | 102,04 | 3 | 102±3 |
| 0,456 | 101,54 | |||
| 0,463 | 103,3 |
0,455 = 0,0039x + 0,06; x = 101,28мкг/мл
0,456 = 0,0039x + 0,06; x = 101,54 мкг/мл
0,463 = 0,0039x + 0,06; x = 103,3 мкг/мл
Разбавление в 200 раз
x = 102∙200 = 20400 мкг/мл; x = 20,04 мг/мл
3.2.3. Количественное определение белка после концентрирования в растворенном осадке после высаливания 35% отнасыщения

Таблица 6. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
Таблица 6. Параметры уравнения для градуировочного графика
| Параметр | Значение | Доверительный интервал |
| a, см3/мкг | 0,0020 | 0,0003 |
| y0 | -0,01 | 0,04 |
Таблица 7. Данные измерения оптической плотности в растворенном осадке после высаливания 35% и его концентрация
| А | Концентрация (X), мкг/мл |  | Доверительный интервал (δX) | Концентрация  , мкг/мл , мкг/мл |
| 0,138 | 70,48 | 70,63 | 2 | 71±2 |
| 0,140 | 71,43 | |||
| 0,137 | 70 |
0,138 = 0,002x - 0,01; x = 70,48 мкг/мл
0,140 = 0,002x - 0,01; x = 71,43 мкг/мл
0,137 = 0,002x - 0,01; x = 70,00 мкг/мл
Разбавление в 200 раз
x = 71∙200 = 14200 мкг/мл; x = 14,2 мг/мл
3.2.4. Количественное определение белка после концентрирования в растворенном осадке после высаливания 70% отнасыщения
Таблица 8. Данные измерения оптической плотности в растворенном осадке после высаливания 70% и его концентрация
| А | Концентрация (X), мкг/мл |  | Доверительный интервал (δX) | Концентрация  , мкг/мл , мкг/мл |
| 0,470 | 228,57 | 238,10 | 21 | 238±21 |
| 0,500 | 242,86 | |||
| 0,500 | 242,86 |
0,470 = 0,0020x - 0,01; x = 228,57 мкг/мл
0,500 = 0,0020x - 0,01; x = 242,86 мкг/мл
0,500 = 0,0020x - 0,01; x = 242,86 мкг/мл
Разбавление в 200 раз
x = 238∙200 = 47600 мкг/мл; x = 47,6 мг/мл
3.3. Концентрирование фермента
Концентрирование проводили на концентрирующих фильтрах 10 кДа, центрифугировали при 5000 об/мин. Концентрация фермента после концентрирования в фракции после 35% высаливания увеличилась примерно в 2,2 раза, а концентрация в фракции после 70% высаливания увеличилась примерно в 2,4 раза.
Выводы
-
Провели ступенчатое разделение белков из гомогенизированных тканей корней Armoracia Rusticana. Получено 2 осажденых белковых фракции с суммарным содержанием 32,1±0,7 мкг/мл в высаливание 35% от насыщения сульфата аммония и 102±3 мкг/мл в высаливание 70% от насыщения сульфата аммония; -
Концентрирование проводили на фильтрах 10 кДа. Провели концентрирование фермента в 2 осажденных белковых фракциях с суммарным содержанием 71±2 мкг/мл в высаливание 35% от насыщения сульфата аммония и 238±21 мкг/мл в высаливание 70% от насыщения сульфата аммония;
Список литературы
-
Banci L. Structural properties of peroxidases //Journal of biotechnology. – 1997. – Т. 53. – №. 2-3. – С. 253-263. -
Захарова Г. С., Упоров И. В., Тишков В. И. Пероксидаза из корней хрена: модулирование свойств химической модификацией белковой глобулы и гемма //Успехи биологической химии. – 2011. – Т. 51. – С. 37-64. -
Wuhrer M. et al. New features of site-specific horseradish peroxidase (HRP) glycosylation uncovered by nano-LC-MS with repeated ion-isolation/fragmentation cycles //Biochimica et Biophysica Acta (BBA)-General Subjects. – 2005. – Т. 1723. – №. 1-3. – С. 229-239. -
Veitch N. C. Horseradish peroxidase: a modern view of a classic enzyme //Phytochemistry. – 2004. – Т. 65. – №. 3. – С. 249-259. -
Pandey V. P. et al. A comprehensive review on function and application of plant peroxidases //Biochem Anal Biochem. – 2017. – Т. 6. – №. 1. – С. 308. -
Mao L. et al. Horseradish peroxidase inactivation: heme destruction and influence of polyethylene glycol //Scientific Reports. – 2013. – Т. 3. – №. 1. – С. 1-7. -
Arnao M. B. et al. Inactivation of peroxidase by hydrogen peroxide and its protection by a reductant agent //Biochimica et Biophysica Acta (BBA)-Protein Structure and Molecular Enzymology. – 1990. – Т. 1038. – №. 1. – С. 85-89. -
Amao, M. В.; Acosta, M.; Del Rio, J. A.; Garcia-Canovas, F. //Inactivation of Peroxidase by Hydrogen Peroxide and Its Protection by a Reductant Agent. Biochim. Biophys. Acta 1990,1038, pp: 85-89. -
Amao, M. В.; Acosta, M.; Del Rio, J. A.; Varon, R.; Garcia-Canovas, F. //A Kinetic Study on the Suicide Inactivation of Peroxidase by Peroxide. Biochim. Biophys. Acta 1990,1041, pp: 43-47. -
Полозников А. А. и др. Способ получения пероксидазы из корней хрена. – 2013. -
Преснова Г. В., Рубцова М. Ю., Егоров А. М. Электрохимические биосенсоры на основе пероксидазы хрена //Российский химический журнал. – 2008. – Т. 52. – №. 2. – С. 60-65. -
Ferapontova E. E. et al. Mediatorless biosensor for H2O2 based on recombinant forms of horseradish peroxidase directly adsorbed on polycrystalline gold //Biosensors and Bioelectronics. – 2001. – Т. 16. – №. 3. – С. 147-157. -
Ferri T., Poscia A., Santucci R. Direct electrochemistry of membrane-entrapped horseradish peroxidase.: Part II: Amperometric detection of hydrogen peroxide //Bioelectrochemistry and bioenergetics. – 1998. – Т. 45. – №. 2. – С. 221-226. -
Malhotra B. D., Chaubey A. Biosensors for clinical diagnostics industry //Sensors and Actuators B: Chemical. – 2003. – Т. 91. – №. 1-3. – С. 117-127. -
Полыгалина Г. В., Чередниченко В. С., Римарева Л. В. Определение активности ферментов. – 2003.