Файл: 1. Нефть и нефтяные месторождения. Гипотезы происхождения нефти. Современные представления об образовании нефти и газа.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.11.2023
Просмотров: 290
Скачиваний: 5
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Основные свойства газов
-
Молекулярная масса— масса молекулы.
Различают абсолютную молекулярную массу и относительную молекулярную массу — безразмерную величину, равную отношению массы молекулы к 1/12 массы атома углерода 12C.
-
Относительную плотность газа при нормальных условиях можно определить как частное его молекулярной массы на объем одного киломоля (22,414 м3/кмоль).
pг = М / 22,414, где М – молекулярная масса, кг/кмоль
Относительная плотность газов уменьшается с ростом температуры и растет с повышением давления и молекулярной массы.
-
Вязкость газа характеризует способность газа оказывать сопротивление перемещению одной части газа относительно другой.
Различают динамическую вязкость и кинематическую вязкость газов. Кинематическая вязкость учитывает влияние силы тяжести.
\
№12.Газообразные алканы. Классификация и номенклатура. Свойства. Применение.
Алканы и циклоалканы относятся к насыщенным предельным соединениям, молекулы которых представлены углеводородами с открытой цепью и в виде циклических структур
Классификация и номенклатура.
Различают моно-, би-, три и полициклические алканы
К моноциклическим алканам относятся:
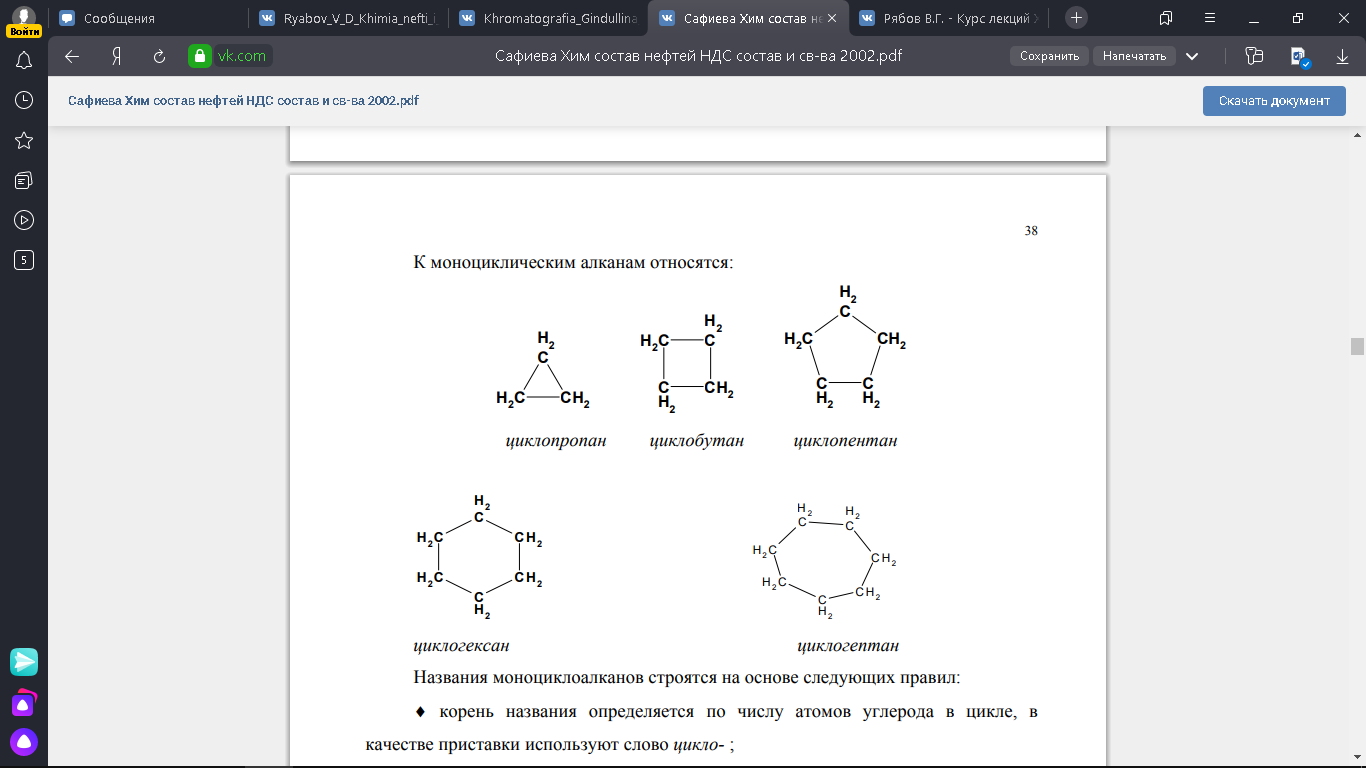
Бициклические алканы:
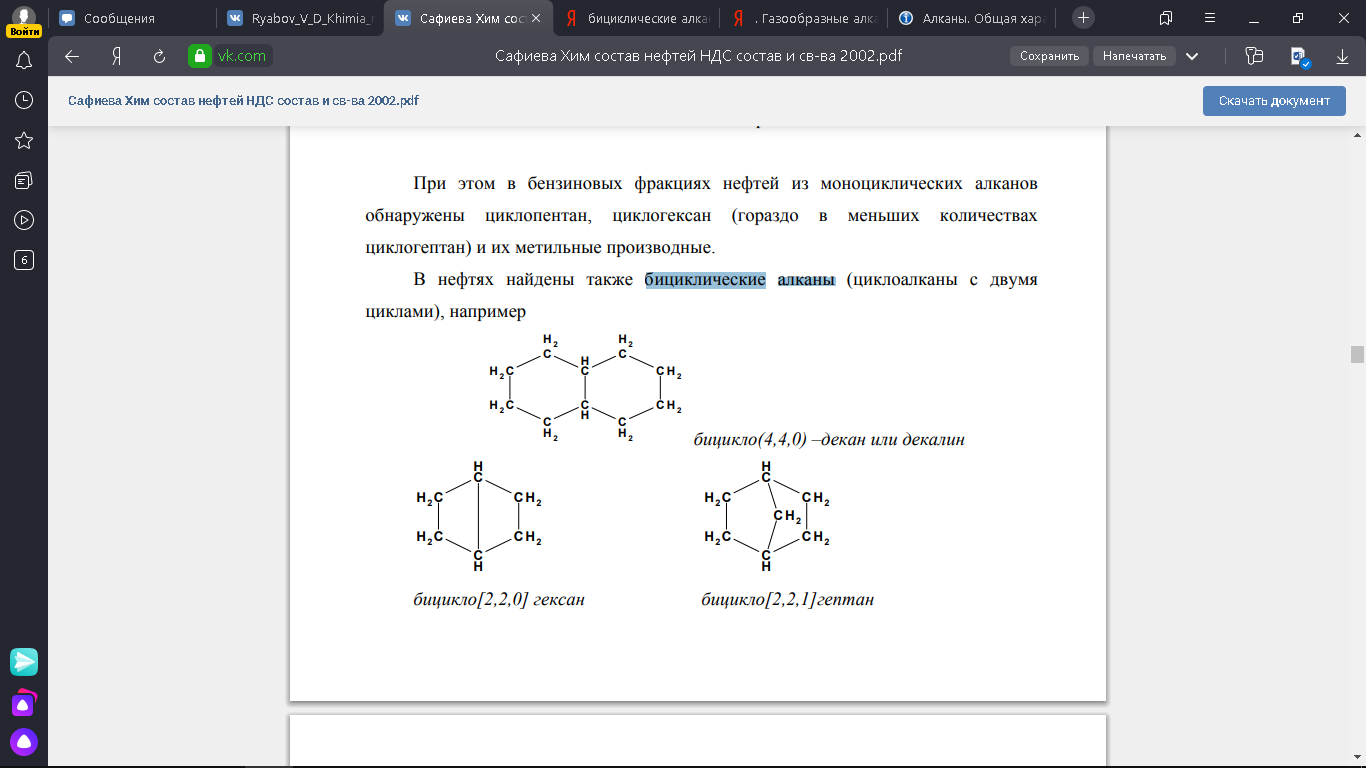
Трициклические алканы, примером которых служит адамантан
В зависимости от месторождений углеводородные газы подразделяют на природные, попутные и газы газоконденсатных месторождений.
Свойства
Газообразные алканы не пахнут. Все алканы бесцветны, легче воды и нерастворимы в ней. Алканы хорошо растворяются в органических растворителях.
Применение
Чистые газообразные алканы служат химическим сырьем, в частности, для получения алкенов, бутадиена, гало-гено - и нитропроизводных, кислородных соединений. Жидкие алканы, входящие в состав нефти, имеют ограниченное применение в органическом синтезе. Эти углеводороды, входя в состав бензина, керосина и др, используются, в первую очередь, как топливо, а также в качестве газа для приготовления пищи, в быту и для производства аэрозолей.
№13.Жидкие алканы линейного строения. Номенклатура. Свойства. Распределение по фракциям. Влияние на свойства топлив. Применение.
Жидкие алканы линейного строения – это предельные углеводороды, содержащие только одинарные связи межу атомами С-С в молекуле.
К жидким алканам относятся углеводороды С5 – С15. Среди них углеводороды С5 – С9 встречаются главным образом в бензиновых фракциях, а С10 – С15 – в керосино-газойлевых фракциях.
Номенклатура
названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь, при этом нумерация этой цепи начинается со стороны ближайшего к концу цепи заместителя. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающая группа или гетероатом, затем название группы или гетероатома и название главной цепи. Если группы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых групп указывают приставками ди-, три-, тетра-. Если группы неодинаковые, то их названия перечисляются в алфавитном порядке.
Свойства
Алканы имеют низкую химическую активность.
Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи
Галогенирование - Галогенирование алканов протекает по радикальному механизму.
Нитрование - Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных.
Реакции окисления - Окисление алканов в жидкой фазе протекает по свободно-радикальному механизму и приводит к образованию гидропероксидов, продуктов их разложения и взаимодействия с исходным алканом.
Горение - Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения.
Каталитическое окисление - Мягкое окисление СН4 в присутствии катализатора кислородом при 200 °C.
Термические превращения алканов (Разложение) - Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов.
Влияние на свойства топлив
-
Понижают октановое число -
Ухудшают моторные свойства -
Понижают плотность и нагарообоазование -
Повышают теплотворную способность и воспламеняемость
Применение алканов
Алканы используются как топливо и важное химическое сырьё для производства пластмасс, синтетических волокон, каучуков, синтетических моющих средств, растворителей. Метан является основным компонентом природного газа.
№14.Жидкие алканы разветвленного строения. Номенклатура. Свойства. Распределение по фракциям. Влияние на свойства топлив. Применение.
Жидкие алканы-алканы от С5до С15 в обычных условиях представляют собой жидкости, входящие в состав бензиновых (C5–C10) и керосиновых (С11–С15) фракций нефтей: жидкие алканы C5-C9 имеют в основном нормальное или слаборазветвленное строение.
Номенклатура
названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь, при этом нумерация этой цепи начинается со стороны ближайшего к концу цепи заместителя. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающая группа или гетероатом, затем название группы или гетероатома и название главной цепи. Если группы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых групп указывают
приставками ди-, три-, тетра-. Если группы неодинаковые, то их названия перечисляются в алфавитном порядке.
Физические свойства алканов
Все алканы нерастворимы в воде, но хорошо растворяются в неполярных органических растворителях. Легко смешиваются друг с другом. Разветвленные алканы имеют более низкие температуры кипения, чем нормальные. Имеют характерный бензиновый запах.
Химические свойства алканов
Реакция галогенирования-атом водорода замещается на атом галогена или какую-либо группу
Реакция дегидрирования-при пропускании алканов над катализатором под высокой температурой (400-600 °С) происходит отщепление молекулы водорода и образование алкена).
Распределение по фракциям:
Содержание в нефтях 20-50%
В парафинистых нефтях до 60% и более
В малопарафинистых 1-2%
Содержание алканов падает с увеличением темп кипения фракции. В парафино-нафтеновых нефтях алканы находятся в низкокипящих фракциях (до 300°С).
Влияние на свойства топлив.
Повышают теплотворную способность, воспламеняемость, понижают темп застывания, повышает октановое число, понижают нагарообразование, понижают плотность.
Приминение:
Применяются в качестве компонентов топлива, исходных веществ в синтезе лекарственных препаратов, смазочных материалов
№15.Твердые парафины. Свойства. Распределение по фракциям. Влияние на свойства топлив. Применение.
Твердые парафины – смесь твердых углеводородов предельного ряда (алканов), получаемых при переработке нефти, имеют преимущественно линейное строение с 19-35 атомов углерода в молекуле. Твердые парафины получают при очистке гача (сырой продукт депарафилизаций масляных фракций). Твердые Парафин- сложная смесь алканов нормального строения и твердых изоалканов 20%, с примесью нафтенов. Твердые алканы входят в состав Цезин. Твердые парафины присутствуют во всех нефтях, но содержание их обычно не превышает 5%. В типично парафиновых нефтях содержание их повышается до 7-12%
Химическая формула парафинаCnH2n+2, где значение n = от 18 до 35.
Свойства:
Химические:
Т. Парафины инертны к большинству химических веществ. Окисляются азотной кислотой, кислородом воздуха (при 140 °C и выше) и некоторыми другими окислителями с образованием различных жирных кислот, аналогичных жирным кислотам, содержащимся в жирах растительного и животного происхождения.
Реагирует с хлором с образованием хлорпарафинов.
Физические:
Кристаллическое строение, белый полупрозрачный цвет, без вкуса и запаха, температура плавления 40-60 С, молекулярная масса 500, твердое вещество жирное на ощупь, температура tкип =330 и выше, температура вспышки не ниже 160 С, температура самовоспламенения не ниже 300 С, плотность= 0,77-0,79, при застывании уменьшается в объеме на 15-17%. С увеличением молекулярной массы парафиновых углеводородов tпл их повышается.