Файл: 1. Стафилококки. Лабораторная диагностика стафилококковой инфекции.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 25.10.2023
Просмотров: 110
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
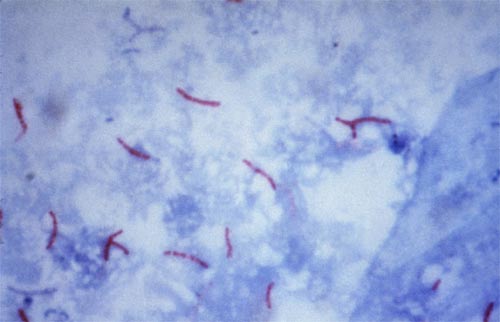
Морфология. Гр+, прямые или слегка изогнутые палочки длиной 2–8 и шириной 0,3 мкм. Высокое содержание липидов придает ряд характерных свойств: устойчивость к кислотам, щелочам и спирту, трудное восприятие анилиновых красителей (для окраски применяют метод Циля–Нильсена). В культурах встречаются зернистые формы, ветвящиеся, зерна Муха (шаровидные кислотоподатливые, легко окрашивающиеся по Грамму). Возможен переход в L-формы. Неподвижны, спор и капсул не образуют.
Для размножения используют сложные пит среды, содержащие яйца, глицерин, картофель. Стимулируют рост микобактерий АСП, соли NН4, альбумин, глюкоза, твин-80. Чаще всего применяют среду Левенштейна–Йенсена (яичная среда с добавлением картофельной муки, глицерина и соли) и среду, содержащую АСП, глицерин, цитрат Fe, фосфат калия. Размножаются медленно. Период генерации длителен – деление клеток в оптимальных условиях 1 раз в 14–15ч. Первые признаки роста обнаруживаются через 8–10 дней после посева. Затем на плотных средах появляются морщинистые, сухие с неровными краями колонии. В жидких средах – сначала нежная пленка на поверхности, затем утолщается и падает на дно. Среда при этом остается прозрачной.
АГ. Выделяют белковые, полисахаридные и липидные соединения. АТ образуются на туберкулиновые протеиды, на полисахариды, фосфатиды, корд-фактор. Специфичность АТ определяется в РСК, РНГА, преципитации в геле. АГ состав М.tuberculosis, М.bovis, M.leprae и других микобактерий (включая многие сапрофитические виды) сходен. Туберкулиновый протеин (туберкулин) обладает выраженными аллергенными свойствами.
Экология и распространение. В естественных условиях М tuberculosis вызывает туберкулез у человека, человекообразных обезьян. Из лабораторных животных высокочувствительными являются морские свинки, менее – кролики. К М.bovis – возбудитель туберкулеза у крупного рогатого скота, свиней и человека – высокочувствительны кролики и менее – морские свинки. М.africanus вызывает туберкулез в странах Африки. Путь заражения воздушно-капельный, возбудитель проникает через верхние дыхательные пути, иногда через слизистые оболочки ЖКТ или через поврежденную кожу.
В окружающей среде длительное время сохраняются (в высохшей мокроте – в течение нескольких недель, в воде – более года).
К действию дезинфицирующих веществ более устойчивы, чем другие бактерии Þ требуются более высокие концентрации и более длительное время воздействия. При кипячении погибают мгновенно, чувствительны к УФ.
Патогенез. Источник заражения – люди и животные с активно протекающим туберкулезом, с наличием воспалительных и деструктивных изменений, выделяющие микобактерии. В зоне проникновения и размножения возникает воспалительный очаг (первичный эффект – инфекционная гранулема), наблюдаются сенсибилизация и специфический воспалительный процесс в регионарных лимфоузлах – формируется первичный туберкулезный комплекс. При доброкачественном течении болезни первичный очаг может рассасываться, пораженный участок кальцинироваться и рубцеваться. Но этот процесс не завершается полным освобождением от возбудителя. В лимфоузлах и других органах туберкулезные бактерии сохраняются много лет, иногда в течение всей жизни. Такие люди, с одной стороны, обладают иммунитетом, а с другой – остаются инфицированными.
При сниженной сопротивляемости организма первичный туберкулезный процесс генерализуется. Диссеминация приводит к образованию в различных органах туберкулезных очагов. Характерна интоксикация. При генерализации – поражение органов мочеполовой системы, костей и суставов, мозговых оболочек, глаз.
Не синтезируют экзотоксин. Поражение тканей вызывает ряд веществ – липиды, мураминдипептид, фтионовые кислоты, сульфатиды, туберкулин, возникают специфические гранулемы и поражение тканей. Токсическое действие оказывает гликолипид, так называемый корд-фактор, разрушает митохондрии клеток, нарушает функцию дыхания.
Патогенетически важным является действие на организм инфицированного человека туберкулина. Очищенный от примесей туберкулин (PPD – очищенный протеиновый дериват) является белком. Внутрикожное введение туберкулина вызывает у инфицированных людей местную воспалительную реакцию в виде инфильтрата и покраснения (реакция Манту). Неинфицированные люди реакции на туберкулин не дают. Эту пробу применяют для выявления инфицированных, сенсибилизированных людей.
Иммунитет. Заражение не всегда приводит к развитию заболевания, это зависит от состояния микроорганизмов. Восприимчивость усиливается в неблагоприятных условиях (изнурительный труд, недостаточное и неполноценное питание, плохие жилищные условия и т.д.). Способствуют развитию туберкулезного процесса и эндогенные факторы – сахарный диабет; психические болезни и др. Значение АТ в формировании сопротивляемости к туберкулезной инфекции до сих пор неясно. Считается, что АТ являются «свидетелями» иммунитета и не оказывают ингибирующего действия на возбудитель.
Большое значение имеет клеточный иммунитет. По РБТЛ, цитотоксическому действию лимфоцитов на клетки-«мишени», содержащие АГ микобактерии, выраженности РТММ судят о течении заболевания. Т-лимфоциты после контакта с АГ синтезируют медиаторы, усиливающие фагоцитарную активность макрофагов. При подавлении функции Т-лимфоцитов туберкулезный процесс становится быстротечным и тяжелым.
Микобактерии туберкулеза разрушаются внутриклеточно в макрофагах. Фагоцитоз является одним из механизмов, приводящих к освобождению организма от микобактерии туберкулеза, но он часто незавершенный.
Другой важный механизм – фиксация микобактерий в очагах благодаря образованию инфекционных гранулем при участии Т-лимфоцитов, макрофагов и других клеток. В этом проявляется защитная роль ГЗТ.
Иммунитет при туберкулезе раньше называли нестерильным. Значение имеет не только сохранение живых бактерий, поддерживающих повышенную сопротивляемость к суперинфекции, но и явление «иммунологической памяти». При туберкулезе развивается реакция ГЗТ.
Лабораторная диагностика. Материалом для микробиологического исследования в зависимости от локализации процесса служат мокрота, гной, моча, спинномозговая жидкость, испражнения.
Бактериоскопическое исследование. Мокроту выливают в чашку Петри, ставят на черную поверхность стола, выбирают гнойные комочки, наносят их на предметное стекло и растирают между двумя стеклами. Спинномозговую жидкость для образования пленки фибрина и фиксации в ней микобактерии туберкулеза оставляют на сутки в холодном месте. Затем ее осторожно распределяют на предметном стекле. Мочу центрифугируют для получения осадка. Сделанные мазки окрашивают по Цилю–Нельсену. Микобактерии туберкулеза окрашиваются в ярко–красный (рубиновый) цвет. Если в материале находится небольшое количество микобактерии и в обычных мазках их нельзя обнаружить, применяют методы обогащения.
Метод гомогенизации. Суточную порцию мокроты выливают во флакон или банку, добавляют равный объем 1% водного раствора натрия гидроксида, плотно закрывают резиновой пробкой и энергично встряхивают до, полной гомогенизации (10–15 мин). Утратившую вязкость мокроту центрифугируют, жидкость сливают, осадок нейтрализуют добавлением 2–3 капель 10% соляной кислоты. Из осадка готовят мазки и окрашивают по Цилю–Нельсену.
Метод флотации. Подвергнутую щелочной гомогенизации мокроту для более полного растворения оставшихся слизистых комков помещают на 30 мин на водяную баню при температуре 55°С. Затем к ней добавляют 1–2 мл ксилола (бензола, бензина) и встряхивают в течение 10 мин, потом отстаивают 20 мин при комнатной температуре. Капельки ксилола с адсорбированными микобактериями всплывают, образуя сливкообразный слой, его снимают пипеткой и несколько раз наносят по мере высыхания на предметное стекло. Сделанные мазки тоже окрашивают по Цилю–Нельсену.
Бактериологический метод. Выделить культуру микобактерии туберкулеза удается при наличии в 1 мл исследуемого материала даже 20–100 микробных тел. При этом определяют ее устойчивость к лекарственным препаратам, для того чтобы разработать индивидуальную схему лечения больных.
Выделяя из мокроты культуру микобактерии туберкулеза, к ней в целях уничтожения кислотоподатливой микрофлоры добавляют двойной объем 6% серной кислоты, встряхивают в течение 10 мин, центрифугируют. Затем жидкость сливают, осадок нейтрализуют 1–2 каплями 3% натрия гидроксида или несколько раз отмывают изотоническим раствором натрия хлорида. Нейтрализованные осадки мокроты засевают на скошенную в пробирках яичную среду Левенштейна–Йенсена с малахитовым зеленым, который угнетает рост банальной микрофлоры.
Спинномозговая жидкость, экссудат, гной, кровь кислотно–щелочной обработке не подвергаются, их засевают на среду Левенштейна–Йенсена пипеткой с последующим втиранием бактериальной петлей. Ватные пробки, которыми закрывают засеянные пробирки, заливают парафином, чтобы избежать высыхания среды. Посевы помещают в термостат при температуре 37°С и выдерживают в течение 6–8 недель.
Биологический метод. Животных, чаще морских свинок, заражают для выделения чистых культур микобактерии туберкулеза и изучения патогенеза заболевания. Поскольку большинство изониазидустойчивых штаммов утратило к ним вирулентность, биологический эксперимент в настоящее время не находит широкого применения.
Аллергическая реакция Манту. Выполняют ее путем внутрикожного введения 0,1 мл альт–туберкулина в ладонную поверхность предплечья. Ее результат учитывают через 24–48 ч. В положительных случаях на месте введения туберкулина появляется инфильтрат с венчиком гиперемии диаметром 10 мм, который чаще всего свидетельствует об инфицированности туберкулезом, а у 2–3–летних детей может также являться диагностическим тестом активно развивающейся болезни.
Профилактика и лечение. Для специфической профилактики – живая вакцина БЦЖ-BCG (Bacille Calmette–Guerin). Штамм БЦЖ был получен при длительном пересеивании палочек на картофельно-глицериновой среде с добавлением желчи. За 13 лет была получена культура со сниженной вирулентностью. В нашей стране в настоящее время вакцинируют всех новорожденных на 5–7-й день жизни внутрикожно. Ревакцинация – лицам с отрицательной туберкулиновой пробой с интервалом в 5–7 лет до 30-летнего возраста. Создают т.о. инфекционный иммунитет, при котором возникает реакция ГЗТ. Для лечения –
АБ, химиотерапевтические препараты I ряда: тубазид, фтивазид, изониазид, дигидрострептомицин, ПАСК и II ряда: этионамид, циклосерин, канамицин, рифампицин, виомицин. Также проводится десенсибилизирующая терапия и стимуляция естественных защитных механизмов организма.
16. Бруцеллы. Лабораторная диагностика бруцеллёза.
Бруцеллы (род Brucella) – возбудители бруцеллеза человека и животных. В. melitensis, В. abortus и В. suis – вызывают заболевание у человека; B. ovis, B. canis, B. neotomae заболевания человека не вызывают.
Морфология, физиология. Мелкие Гр– коккобактерии размером 0,5-0,7х0,6-1,5 мкм. Также могут быть палочковидной формы; в мазках обычно расположены беспорядочно. Жгутиков не имеют. Спор не образуют. Свежевыделенные штаммы могут образовывать нежную капсулу при культивировании на средах, содержащих 10% иммунной сыворотки барана или лошади, а также при выращивании на куриных эмбрионах.
Требовательны к питательным средам. Для выращивания обычно применяют триптозный, триптозо-казеиново-соевый и кровяной (5% овечьей крови) агары; оптимальная среда для культивирования - печёночный агар Хеддльсона. Выделяемые из организма больных они размножаются очень медленно, рост может быть обнаружен только через 1–3 недели после посева исходного материала. Многократное пересевание в лабораторных условиях делает культуры способными расти в течение 1–2 дней. На плотных питательных средах образуют мелкие, выпуклые, бесцветные с перламутровым блеском колонии S-формы (жемчужины), легко переходят в мукоидную и шероховатую. В жидких средах возникает равномерное помутнение. Под влиянием антибиотиков образуют L-формы.
Бруцеллы строгие аэробы, а В. abortus в первых поколениях требует увеличенной концентрации (5–10%) СО2.
БХ: расщепляют глюкозу и некоторые другие углеводы, разлагать мочевину и аспарагин, гидролизовать белок, пептоны, аминокислоты, выделять каталазу, гиалуронидазу, пероксидазу, липазу, фосфатазу и другие ферменты. Внутри видов бруцелл различают биовары. Их дифференциация основана как на биохимических различиях, так и на способности расти на средах с фуксином и тионином, лизабельности фагом Т6, агглютинабельности моноспецифическими сыворотками.