ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.10.2023
Просмотров: 171
Скачиваний: 8
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Эксергетический и энтропийный методы дополняет энергетический, позволяя полнее оценить картину энергоиспользования. Эти методы приобретают особое значение при создании энерготехнологических систем.
15. Энтропийный метод анализа. Его преимущества и недостатки.
Энтропийный метод анализа осуществляется путем рассмотрения влияния изменения энтропии в отдельных процессах, на энтропию системы в целом.
Поскольку энтропия является параметром состояния рабочего вещества, то в замкнутом цикле с совершенным рабочим веществом его энтропия примет первоначальное значение в исходной точке цикла, независимо от прироста энтропии в отдельных процессах. Поэтому необратимые потери и рост энтропии цикла можно определить только сравнивая данные (анализируемые необратимый цикл), состоящие из необратимых процессов с эквивалентным обратимым циклом-образцом, состоящим из обратимых процессов.
Эквивалентность обратимого цикла-образца определяется тем, что он имеет одинаковые с анализируемым циклом температуры источников Тинт, Тивт и одинаковую холодопроизводительность (для теплового насоса – теплопроизводительность). Работа эквивалентного обратимого цикла будет минимальной для заданных условий (температур), что позволяет при сравнении с работой необратимого цикла определить коэффициент обратимости последнего.
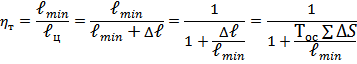
В общем случае цикл ХМ состоит из процесса сжатия рабочего вещества с более низкого давления до более высокого, расширения рабочего вещества и двух процессов теплообмена с источниками ИВТ и ИНТ.
Процессы сжатия и расширения обратимы если они проходят по изоэнтропе. Процессы теплообмена с источниками обратимы, если изменение температуры источника и рабочего вещества совпадают.
Рассмотрение энтальпийного метода позволяет перийти к следующим важным выводам.
1. Система коэффициентов эксергетических потерь универсальна для любой энергетической, холодильной или теплонаносной установки.
2. Основные показатели метода характеризуют термодинамическое совершенство установки (эксергетический КПД), а также суммарную потерю производимой и затрачиваемой в установке работы вследствие необратимости процессов (сумма абсолютных коэффициентов эксергетических потерь).
3. Недостатком метода является учет только относительных потерь эксергии отдельных элементов ХТС, которые не дают представления о термодинамической эффективности конкретного элемента как самостоятельного объекта.
16. Энергетический метод анализа. Его преимущества и недостатки.
В основе этого метода лежит первый закон термодинамики – закон сохранения энергии, в соответствии с которым в общем случае подведенные к установке теплота и работа должны равняться израсходованной теплоте и израсходованной работе :
работе :
+ = +
В печах = =0, поэтому уравнение энергетического баланса сводится к уравнению теплового баланса:
Для печей непрерывного действия составляющие теплового баланса относят к единице времени и измеряют в кДж/ч или в МДж/ч. Для печей периодического действия составляющие относят к периоду обработки материала.
В общем случае в входят следующие составляющие.
Теплота сжигания топлива или теплота , выделившаяся в результате преобразования электрической энергии:
где – часовой расход топлива, измеряемый для жидких и твердых топлив в кг/ч, а для газообразных топлив – в нм3/ч; – электрическая мощность, кВт. Для газообразного топлива вместо берется низшая теплота сгорания сухого газа , кДж/нм3.
Физическая теплота , вносимая подогретым воздухом:
Физическая теплота, вносимая подогретым топливом:
Ниже перечисляются составляющие тепловых потерь.
Теплота, уносимая уходящими газами:
где – объем продуктов сгорания 1 кг или 1 нм3 топлива, м3/кг или м3/нм3; – средняя объемная теплоемкость продуктов сгорания, кДж/(нм3К); – температура уходящих газов, С. Для электрических печей .
Потери теплоты от химической и механической неполноты сгорания топлива:
.
Для газообразного топлива вместо берется . Для электропечей .
Коэффициент полезного действия печи определяют так
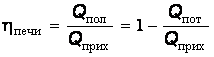
В соответствии с равенством снижение потерь теплоты приводит к повышению КПД печи и снижению расхода топлива.
Рассмотрение энергетического метода позволяет прийти к следующим важным выводам.
1. При определении суммарных количеств подведенной и отведенной энергии необходимо контролировать их равенство.
2. Метод позволяет оценить потери энергии в ХТС, определить потери энергии по всей ХТС и отдельным ее элементам, выявить те элементы, где теряется наибольшее количество энергии.
3. Это единственный метод термодинамического анализа, позволяющий определить потери тепловой энергии через внешнюю поверхность установки в окружающую среду.
4. Недостатком метода является то, что в нем не учитывается качество энергии т. е. ее превратимость в работу, так как из второго закона термодинамики следует, что одно и то же количество энергии может обладать разной работоспособностью (эксергией).
17. Эксергетический баланс ЭХТС, диаграмма Грассмана-Шаргута. Эксергетические показатели совершенства процессов в ЭХТС.
ЭХТС представляет собой комплекс взаимосвязанных технологических и энергетических устройств, в котором изменение термодинамического совершенства процессов, протекающих в любом из элементов, приводит к изменению показателей термодинамического совершенства ЭХТС в целом.
В ЭХТС структура потоков эксергии оказывается весьма сложной. Потоки эксергии могут поступать извне одновременно в несколько элементов. Часть потоков эксергии внутри системы оказываются замкнутыми вследствие циркуляции вещества и регенерации теплоты.
Под качеством энергии понимают возможность получения за счет нее работы, а количественной мерой качества энергии служит эксергия. Различают эксергию потока вещества, эксергию потока теплоты, химическую эксергию, эксергию вещества в замкнутом объеме, эксергию излучения и т. д. Для термодинамического анализа металлургических установок значение имеют в основном три первых вида эксергии.
Эксергию потока вещества, поступающего в установку или уходящего из нее за единицу времени, определяют по формуле
где , и , – соответственно значения энтальпии и энтропии вещества в потоке и при параметрах окружающей среды; – температура окружающей среды; – массовый расход вещества в потоке.
Эксергию потока теплоты, забираемой у тела с температурой , находят на основе того, что максимальная работа за счет нее может быть получена в обратимом цикле Карно, в котором приемником теплоты является окружающая среда. Умножая количество теплоты на КПД цикла Карно, получают

Химическую эксергию топлива находят приближенно по величине низшей теплоты сгорания:
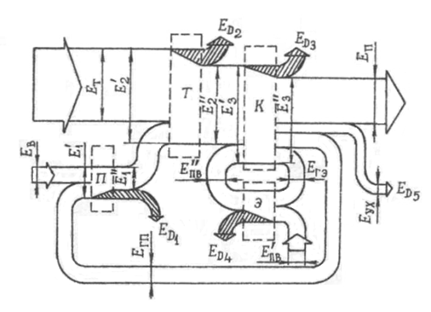
Диаграмма Грассмана-Шаргута
18. Потери эксергии вследствие необратимости. Закон Гюи-Стодолы.
Подчеркнем, что потери эксергии – результат необратимого протекания процессов и, чем выше степень необратимости, тем эти потери больше. Например, чем больше в нагревательных печах разница в температурах греющей среды и нагреваемого тела, тем больше при этом потеря эксергии. Напротив, чем меньше потери эксергии, тем полнее реализуется запас работоспособности потоков вещества и энергии, тем полнее выбранный способ использования энергии соответствует ее качеству. По этой причине надо стремиться
 к снижению потерь эксергии, если это не противоречит целям технологического процесса.
к снижению потерь эксергии, если это не противоречит целям технологического процесса.В эксергетическом методе эти потери находят, вычитая из величины эксергии на входе ее величину на выходе. При энтропийном методе определение потерь эксергии основано на законе Гюи–Стодолы. Согласно этому закону потери эксергии в любом необратимом процессе могут быть выражены произведением приращения энтропии вследствие необратимости процессов на температуру окружающей среды:
Эксергетический и энтропийный методы дополняет энергетический, позволяя полнее оценить картину энергоиспользования. Эти методы приобретают особое значение при создании энерготехнологических систем.
19. Определение газовой постоянной и кажущейся молярной массы смеси. Вычисление теплоемкости смеси.
Газовые смеси подчиняются тем же законам, что и чистые газы, поэтому при термодинамических расчётах необходимо умение находить газовую постоянную и среднюю (кажущуюся) молярную массу смеси.
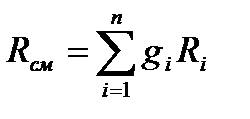
где gi – массовая доля компонента газовой смеси;
Ri - газовая постоянная компонента газовой смеси
Газовая постоянная смеси равна сумме произведений газовых постоянных компонентов смеси на их массовую долю.
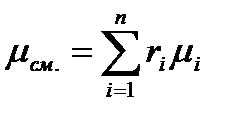
где ri – объёмная доля компонента газовой смеси;
mi – молярная масса компонента газовой смеси.
Молярная масса смеси равна сумме произведений молярных масс компонентов газовой смеси на их объёмную долю.
Надо также отметить, что зная молярную массу смеси можно легко найти газовую постоянную смеси и наоборот по соотношению:
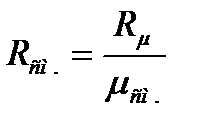
где Rm - универсальная газовая постоянная..
Теплоемкость газовой смеси может быть вычислена, если задан состав смеси и известны теплоемкости компонентов, входящих в смесь.
Для нагревания смеси массой Мсм на 1К необходимо температуру каждого из компонентов также повысить на 1К. При этом на нагревание i-го компонента смеси массой Мi затрачивается количество теплоты, равное ciMi. Для всей смеси количество теплоты ,
где ci и cсм - массовые теплоемкости i-го компонента и смеси.
Поделив последнее выражение на Мсм, получим расчетную формулу для массовой теплоемкости смеси:
где mi - массовая доля i-го компонента.
Рассуждая аналогично, найдем объемную c¢см и мольную cmсм теплоемкости смеси:
где c¢i - объемная теплоемкость i-го компонента, ri - объемная доля i-го компонента,
где cmi - мольная теплоемкость i-го компонента, ri - мольная (объемная) доля i-го компонента
20. Эксергетический КПД. Использование понятия транзитной эксергии для определения эксергетического КПД. Эксергетические КПД основных теплотехнических устройств, входящих в ЭХТС.
В ходе анализа эксергетическим и энтропийным методами составляется эксергетический баланс и на его основе определяется эксергетический КПД:
