Файл: Контрольная работа 1 по дисциплине стандартизация лекарственных средств Вариант 75 Студентки 6 курса группы.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.10.2023
Просмотров: 22
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ ДОНЕЦКОЙ НАРОДНОЙ РЕСПУБЛИКИ
ГОСУДАРСТВЕННАЯ ОБРАЗОВАТЕЛЬНАЯ ОРГАНИЗАЦИЯ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ДОНЕЦКИЙ НАЦИОНАЛЬНЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
ИМЕНИ М.ГОРЬКОГО»
Кафедра фармацевтической и медицинской химии
Контрольная работа № 1
по дисциплине: «стандартизация лекарственных средств»
Вариант 75
Студентки 6_курса группы _4_
заочного отделения
медико-фармацевтического факультета
Петренко Анастасия Игоревна
ВАРИАНТ 75
1. Показатели качества, по которым контролируются растворы для инъекций согласно Государственной Фармакопеи: определение рН, определение плотности, определение сопутствующих примесей, определение объема, который извлекается.
Определение рН
Потенциометрическое определение рН заключается в измерении электродвижущей силы электродной системы, где в качестве ионоселективного электрода используют чувствительный к ионам водорода электрод (обычно стеклянный), в качестве электрода сравнения – стандартный электрод с известной величиной потенциала (насыщенный каломельный или хлорсеребряный электроды) [2].
Прибор. В качестве прибора для потенциометрического определения рН используют иономеры или рН-метры с чувствительностью не менее 0,05 единиц рН или 3 мВ. Калибровка приборов производится по стандартным буферным растворам, приведенным в общей фармакопейной статье «Буферные растворы» [2].
Методика. Все измерения проводят при одной и той же температуре в интервале от 20 до 25 ºС, если нет других указаний в фармакопейной статье. Для приготовления растворов могут быть использованы стандарт-титры для приготовления буферных растворов — рабочих эталонов рН (фиксаналы) промышленного производства [2].
Определение плотности
Определение плотности проводят с помощью пикнометра.
Чистый сухой пикнометр взвешивают с точностью до 0,0002 г, заполняют с помощью маленькой воронки водой очищенной немного выше метки
, закрывают пробкой и выдерживают в течение 20 мин в термостате при температуре (20 ± 0,1) ºС. При этой температуре уровень воды в пикнометре доводят до метки, отбирая излишек воды при помощи пипетки или свернутой в трубку полоски фильтровальной бумаги. Пикнометр снова закрывают пробкой и выдерживают в термостате еще 10 мин. Затем пикнометр вынимают из термостата, проверяют положение мениска воды, который должен находиться на уровне метки. Вытирают фильтровальной бумагой внутреннюю поверхность горлышка и весь пикнометр снаружи, закрывают пробкой. Выдерживают пикнометр под стеклом аналитических весов в течение 10 мин и взвешивают с той же точностью [3].
Пикнометр освобождают от воды, высушивают, ополаскивая последовательно спиртом и эфиром (сушить пикнометр нагреванием не допускается), удаляют остатки эфира продуванием воздуха, заполняют пикнометр испытуемой жидкостью и проводят те же операции, что и с водой.
Плотность r20 (г/см3) вычисляют по формуле:
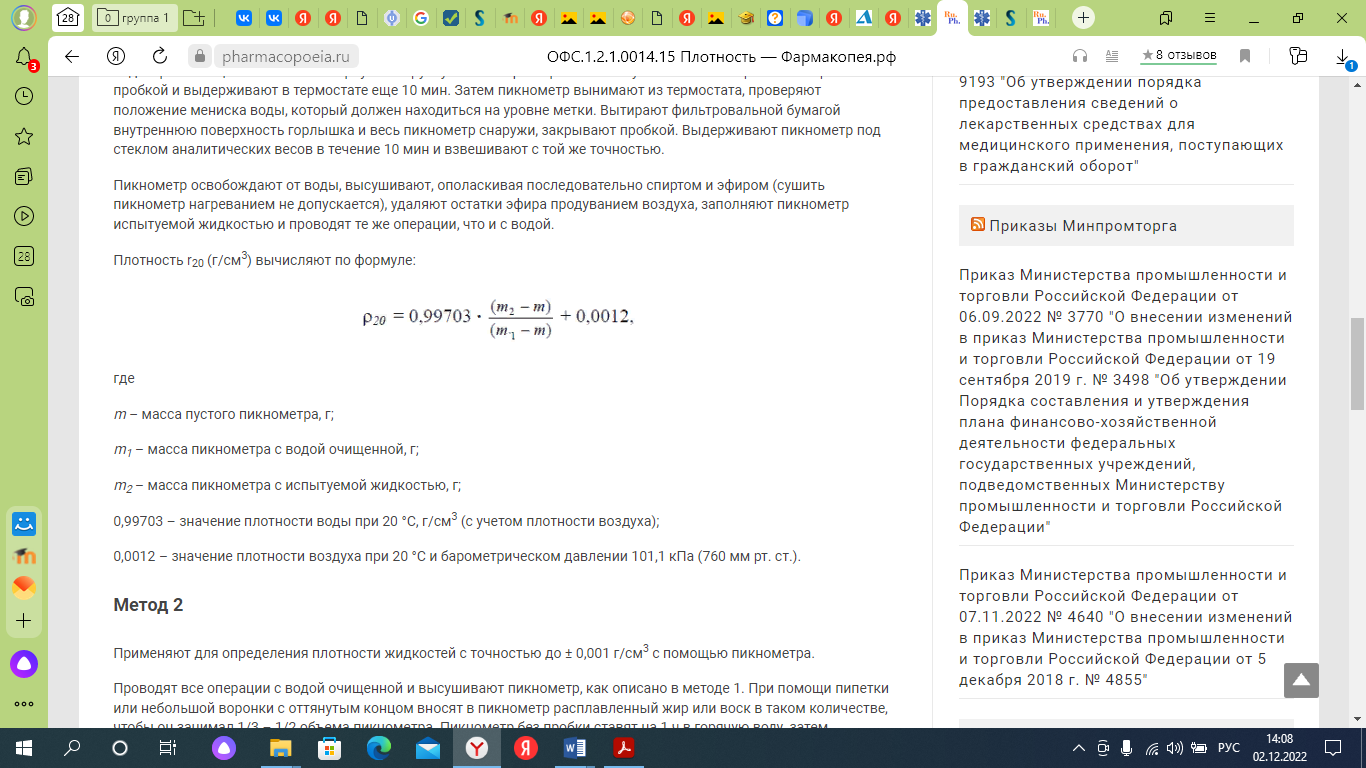
где
m – масса пустого пикнометра, г;
m1 – масса пикнометра с водой очищенной, г;
m2 – масса пикнометра с испытуемой жидкостью, г;
0,99703 – значение плотности воды при 20 °С, г/см3 (с учетом плотности воздуха);
0,0012 – значение плотности воздуха при 20 °С и барометрическом давлении 101,1 кПа (760 мм рт. ст.).
Определение сопутствующих примесей
Объективную оценку разложения лекарственного вещества в инъекционном растворе дает такой показатель качества, как «посторонние примеси», определяемые высокочувствительными хроматографическими методами (ТСХ или ВЭЖХ). Посторонние примеси в инъекционных лекарственных препаратах не допускаются. Если появление таких примесей неизбежно, особенно для термолабильных веществ, то они подлежат нормированию [4].
Ампульные растворы относятся к дозированным лекарственным формам. Дозирование осуществляется с помощью калиброванного шприца непосредственно перед введением раствора больному. Однако при отборе раствора в шприц часть его остается в ампуле, другая часть расходуется на вытеснение воздуха из иглы. Данное обстоятельство учитывается в технологии ампулированных растворов. Объем раствора, заключенный в ампулу, должен быть несколько больше номинального. В противном случае не будет обеспечиваться требуемая дозировка лекарственного вещества. Поэтому одним из показателей качества инъекционных растворов в ампулах является извлекаемый объем. Это испытание унифицировано и изложено в
ОФС «Извлекаемый объем лекарственных форм для парентерального применения». Для определения 16 объема раствора в ампулах вместимостью менее 10 мл отбирают пять ампул, вместимостью 10 мл и более – 3 ампулы. Извлекают содержимое каждой ампулы сухим шприцем, вместимость которого не более чем в три раза превышает измеряемый объем. Из шприца и иглы удаляют пузырьки воздуха и помещают содержимое, не выдавливая раствор из иглы, в сухой мерный цилиндр, калиброванный на заполнение. Вместимость мерного цилиндра должна быть такой, чтобы измеряемый объем занимал не менее 40% от номинального объема цилиндра. Для ампул с номинальным объемом 2 мл и менее содержимое нескольких ампул может быть объединено, чтобы получился объем, подходящий для измерения. Причем, для каждой ампулы используют отдельный сухой шприц. Объем раствора должен быть не меньше номинального, если ампулы исследуются индивидуально. Для ампул с номинальным объемом 2 мл и менее измеренный объем раствора должен быть не менее суммы номинальных объемов исследованных ампул [4].
2. Укажите, как количественно можно определить натрия хлорид в лекарственной форме, состоящей из раствора метазона и натрия хлорида. Приведите формулу расчета натрия хлорида.
Меркуриметрия, прямое титрование, индикатор-дифенилкарбазон [1]:
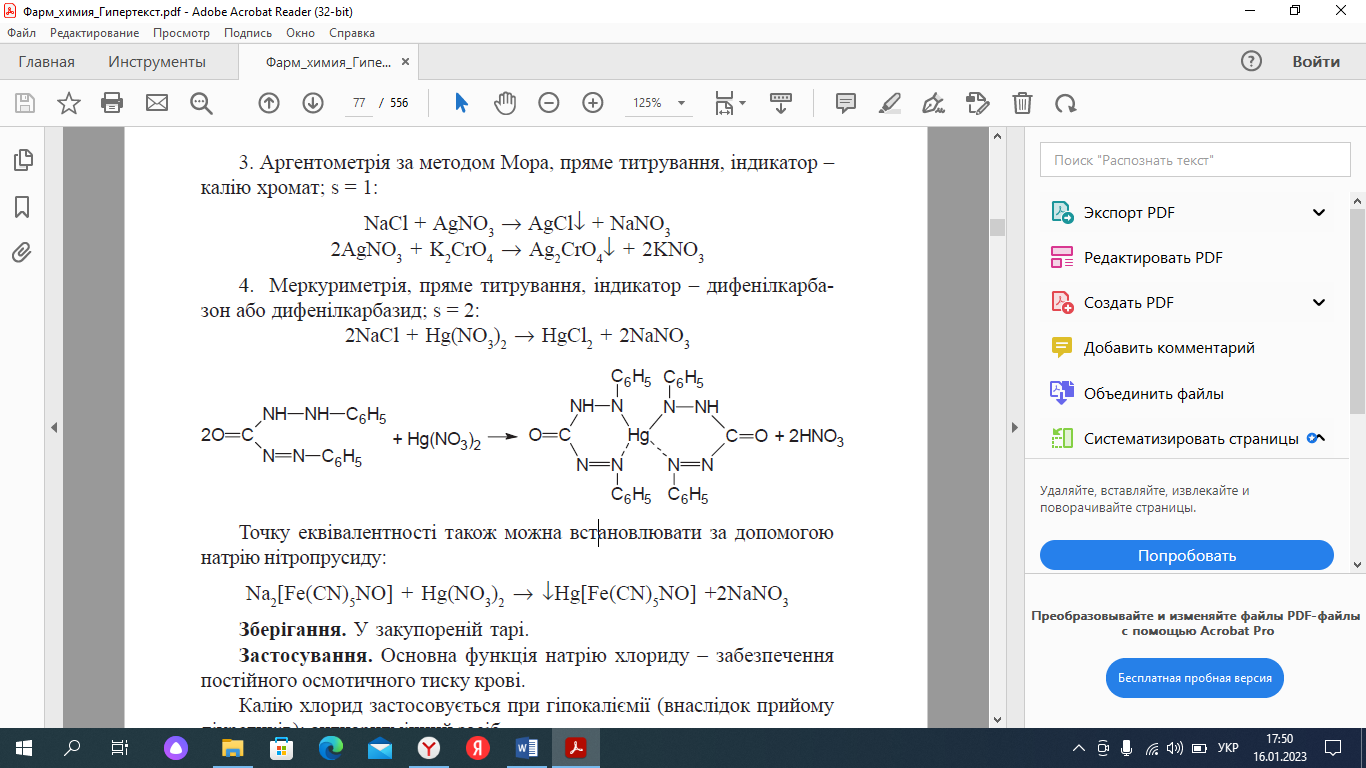
Меркуриметрическое определение NaCl проводят по следующей методике. В три колбы для титрования помещают по 5,00 мл анализируемого раствора, прибавляют в каждую колбу по 5 мл 0,1 М HNO3, 1 мл 10% раствора нитропруссида натрия и медленно титруют 0,1 М 1/2 Hg(NO3)2 до появления неисчезающей белой мути.
При использовании дифенилкарбазона в три колбы для титрования помещают по 5,00 мл анализируемого раствора NaCl, прибавляют в каждую колбу по 5 мл 0,1 М HNO3, 5 капель 0,5% спиртового раствора дифенилкарбазона и титруют стандартным раствором Hg(NO3)2 до появления светло-фиолетового окрашивания.
Расчёт массовой концентрации (г/л) NaCl в растворе проводят по формуле
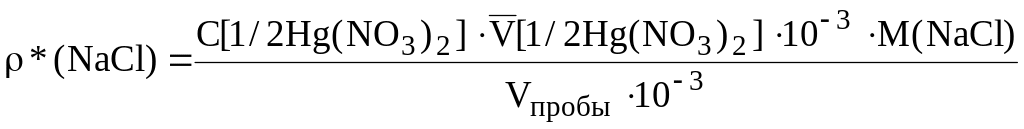
где М(NaCl) = 58,44 г/моль, Vпробы = 5,00 мл
3. Рассчитайте объем 0.1 М раствор аммония тиоцианата, который будет израсходован на титрование 0.2876 г серебра нитрата тиоцианометрическим методом, если содержание действующего вещества в субстанции – 99.8%. (Мсеребра нитрата = 169.87, К аммония тиоционата = 0.9950).
Решение:
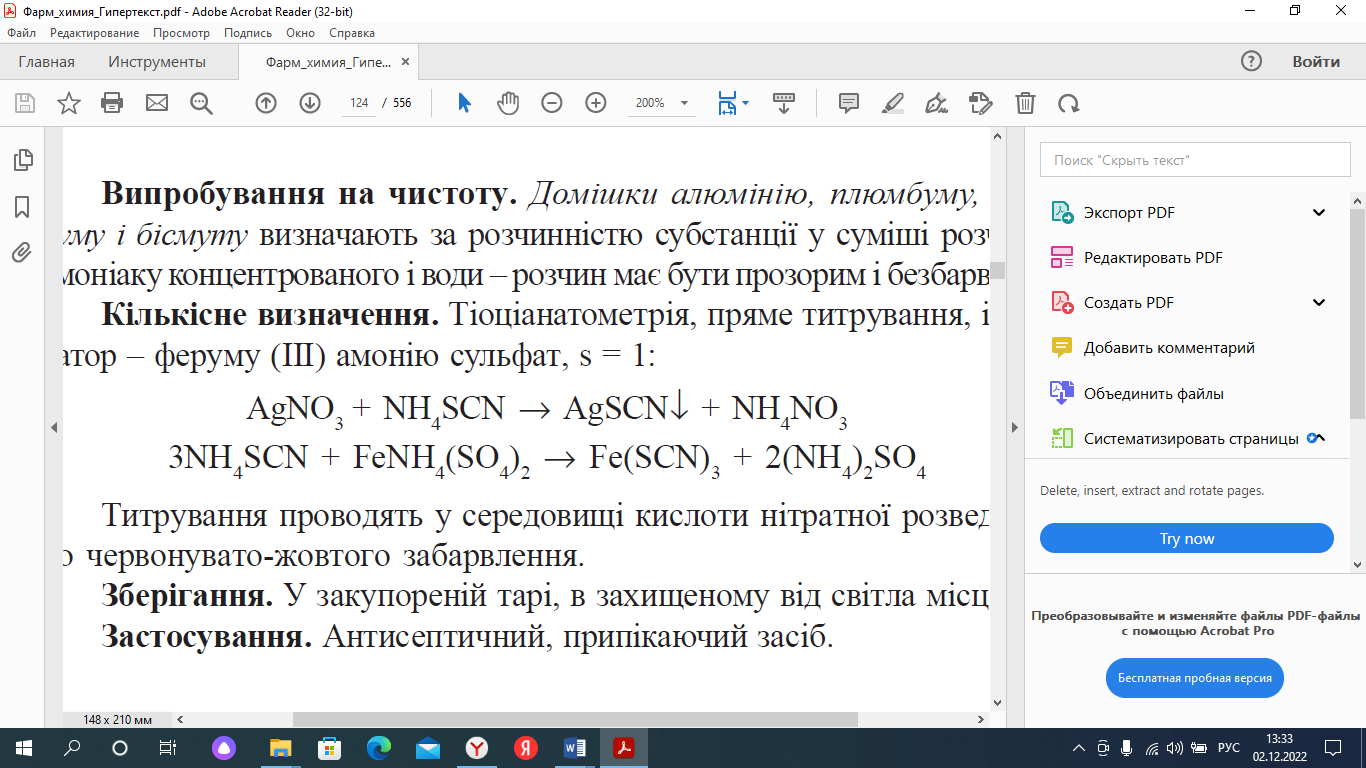
Исходя из уравнения реакции S=1 [2].
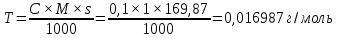
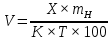
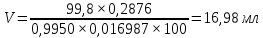
Ответ: 16,98 мл
4. Пропись: Раствора левомецитина 0.25% - 10 мл
Натрия хлорида 0.09
Рассчитайте содержание натрия хлорида в лекарственной форме, если на титрование 1 мл израсходовано 1.2 мл 0.1 М раствора серебра нитрата. (Мнатрия хлорида = 58.44, К серебра нитрата = 1.0000).
Исходя из уравнения реакции S=1 [2].
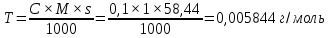
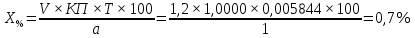
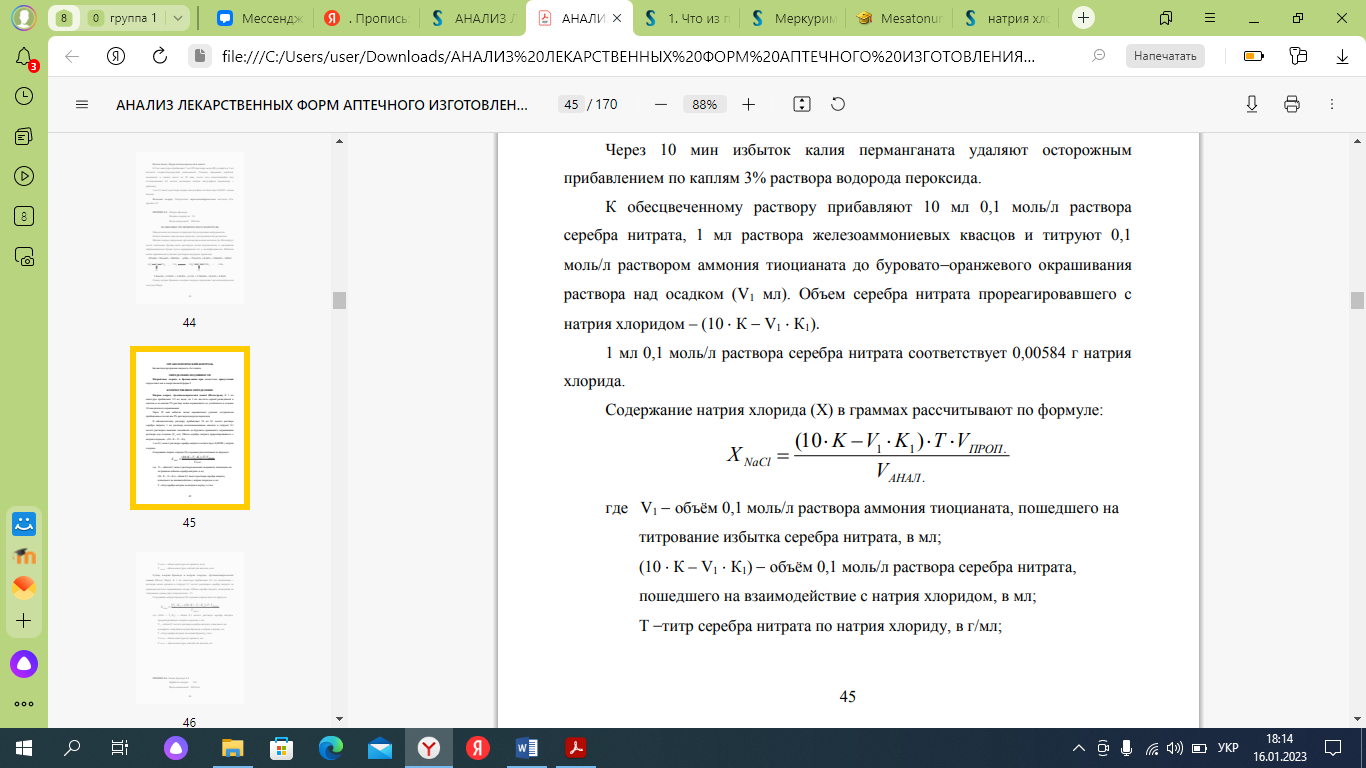
где V1 - объём 0,1 моль/л раствора аммония тиоцианата, пошедшего на титрование избытка серебра нитрата, в мл;
(10 К – V1 К1) - объём 0,1 моль/л раствора серебра нитрата, пошедшего на взаимодействие с натрия хлоридом, в мл;
Т - титр серебра нитрата по натрия хлориду
V ПРОП. - объем по прописи, в мл;
V АНАЛ. - объем, взятый для анализа, в мл.
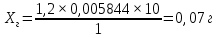 Ответ: 0,07 г
Ответ: 0,07 г 5. Дайте заключение о качестве лекарственной формы раствор калия йодида 3%-25мл, если на титрование 0,5 мл препарата пошло 0,9 мл раствора нитрата серебра с К=1,00604.
Решение:
Исходя из уравнения реакции S=1 [2].
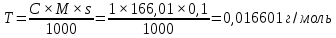
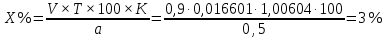
-
Заключение: данная лекарственная форма приготовлена удовлетворительно. (Пункт 10.2 Приказа МЗ ДНР от 08.05.2015 № 502 "Об утверждении Порядка изготовления в условиях аптеки и отпуска лекарственных препаратов для медицинского применения.")
Список использованной литературы:
-
Фармацевтическая химия: учеб. для студ. высш. фармац. учеб. заведений и фармац. ф-тов высш. мед. учеб. заведений III-IV уровней аккредитации / П. А. Безуглый [и др.]; под общ. ред. П. А. Безуглого; - Винница : Нова книга, 2017. – 464 -
ОФС «Ионометрия» [Электронный ресурс]. – Режим доступа: ОФС.1.2.1.0004.15 Ионометрия — Фармакопея.рф (pharmacopoeia.ru) - дата обращения: 06.12.2022 -
ОФС Лекарственные формы для парентерального применения [Электронный ресурс]. – Режим доступа: ОФС.1.4.1.0007.15 Лекарственные формы для парентерального применения — Фармакопея.рф (pharmacopoeia.ru) - дата обращения: 06.12.2022