Добавлен: 26.10.2023
Просмотров: 67
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Ш Чрезмерное выпадение волос у женщин.
Ш Небольшие расстройства процесса пищеварения, особенно в детском возрасте.
Ш Возможно, повышенное желание есть мороженое или пить охлажденные напитки.
Ш Ухудшение регуляции температуры тела.
Ш Повышенная утомляемость.
Здесь необходимо отметить, что все вышеприведенные симптомы могут также быть вызваны и рядом других причин, а также сочетанием нескольких таких причин. Поэтому точный диагноз может быть поставлен больному лишь на основании всестороннего медицинского обследования и анализа содержания питательных веществ в употребляемой им пище. Выявление латентной фазы анемии
Ш Концентрация железа в сыворотке крови (плазме)
Ш Уровень трансферрина и насыщение его железом
Ш Концентрация ферритина в сыворотке крови
Ш Содержание железа в крови составляет 0,2-0,5 % всего железа - «верхушка айсберга»
Ш Концентрация железа в сыворотке широко варьирует по различным причинам: возраст, пол, циркадные ритмы
Ферритин
Ферритин - основной показатель запасов железа в организме, играет важную роль в поддержании железа в биологически полезной форме. В то же время ферритин защищает организм от токсического действия ионов металлов. Помимо железа ферритин способен связывать и другие ионы, некоторые из которых токсичны (алюминий, бериллий). В составе ферритина содержится фосфаты железа. Ферритин содержится во всех клетках и жидкостях организма.
Анализ крови на ферритин используется для диагностики железодефицитной анемии и диагностики анемии, сопровождающей инфекционные, ревматические и опухолевые заболевания.
Норма ферритина в крови для взрослых мужчин - 20 - 250 мкг/л. Для женщин норма анализа крови на ферритин - 10 - 120 мкг/л.
На диагностическую значимость ферритина влияют следующие факторы:
Ш Неопластические процессы (опухоли), метастатические поражения костного мозга, печени вызывают «парадоксальное повышение ферритина». Ферритин приобретает характер опухолевого маркера.
Ш Воспаления, некрозы, ревматические процессы могут повышать уровень ферритина, так как он обладает свойствами белка острой фазы.
Избыток ферритина в крови может быть следствием следующих заболеваний:
· избыток железа при гемохроматозе
· алкогольный гепатит и другие заболевания печени
· лейкоз
· острые и хронические инфекционно-воспалительные заболевания (остеомиелит, инфекции легких, ожоги, ревматоидный артрит)
· рак молочной железы.
Повышение уровня ферритина происходит при приеме оральных контрацептивов и голодании.
Низкий ферритин - следствие дефицита железа (железодефицитной анемии).
Лечение низкого ферритина всегда назначается только врачом: необходимо точно выяснить, какие нарушения привели к снижению ферритина в анализе крови.
Трансферрин
Ш Трансферрин (ТФ) - единственный плазменный белок, участвующий в транспорте железа от места его абсорбции (тонкая кишка) до места его использования (костный мозг, печень, селезенка)
Ш Насыщение трансферрина железом в норме 15-45%
Ш При недостатке железа насыщение ТФ становится неполным, уменьшается % насыщения, что указывает на анемию, обусловленную недостатком поступления железа
Ш Трансферрину свойственны качества «отрицательного» белка острой фазы, острое воспаление способствует понижению уровня, диагностическое значение трансферрина может быть неоднозначным
Синтез трансферрина осуществляется в печени и зависит от функционального состояния печени, от потребности в железе и резервов железа в организме. При снижении концентрации железа синтез трансферррина возрастает. Железо, поступающее с пищей, накапливается в эпителиальных клетках слизистой оболочки тонкого кишечника.
При разрушении эритроцитов в селезёнке, печени и костном мозге железо, высвобождаемое из гема, трансферрин транспортирует в костный мозг; часть железа включается в состав ферритина и гемосидерина. Плазматический трансферрин, "нагруженный" железом, разносится с током крови по организму. При взаимодействии трансферрина со своим специфическим рецептором на поверхности клеточных мембран образуется эндоцитозная вакуоль, внутри нее происходит изменение рН, и железо, меняя степень окисления +3 на +2, освобождается от трансферрина. Белок вновь возвращается в кровеносное русло, а железо немедленно связывается низкомолекулярными хелаторами, такими как цитрат или аскорбиновая кислота. После этого железо может быть использовано для синтеза гемоглобина и железосодержащих ферментов или заключено для хранения в ферритин.Одна молекула трансферрина связывает два атома железа - иона Fe3+, а 1 г трансферрина соответственно около 1,25 мг железа. Зная это соотношение, можно рассчитать количество железа, которое может связать сывороточный трансферрин, оно приближается к величине общей железосвязывающей способности сыворотки (ОЖСС). В диагностике используется также расчётная величина - % насыщения трансферрина железом (отношение концентрации сывороточного железа к максимальной железосвязывающей способности трансферрина, выраженное в процентах). В норме процент насыщения трансферрина железом составляет около 30%. Снижение процента насыщения трансферрина железом (следствие снижения концентрации железа и роста концентрации трансферрина) указывает на анемию, обусловленную недостатком поступления железа. При значительном увеличении % насыщения трансферрина железом в плазме появляется низкомолекулярное железо, которое может откладываться в печени и поджелудочной железе, вызывая их овреждение. Оценка содержания трансферрина (и расчет % его насыщения железом) может производиться с использованием иммунометрического определения его концентрации или косвенно, по железосвязывающей способности сыворотки, измеренной с помощью насыщения сыворотки избытком железа. Иммунометрическое определение трансферрина является более точным. Содержание трансферрина у женщин на 10% выше, чем у мужчин. В третьем семестре беременности концентрация трансферрина в сыворотке может повыситься на 50%. Концентрация этого белка снижается у пожилых людей. При воспалении трансферрин проявляется как негативный белок острой фазы (его концентрация при острофазном ответе на воспаление уменьшается) (Таблица 3).
Таблица 3. Референсные значения
| Возраст | Женщины, г/л | Мужчины, г/л |
| 1 день - 12 месяцев | 1,33 - 3,32 | 1,33 - 3,32 |
| 12 месяцев - 5 лет | 2,04 - 3,66 | 2,04 - 3,66 |
| 5 - 10 лет | 1,77 - 3,71 | 2,17 - 3,21 |
| 10 - 14 лет | 2,00 - 3,67 | 1,81 - 3,53 |
| 14 - 20 лет | 1,93 - 4,21 | 1,83 - 3,63 |
| 20 - 60 лет | 2,5 - 3,8 | 2,15 - 3,66 |
| 60 - 90 лет | 1,9 - 3,75 | 1,9 - 3,75 |
| 90 - 120 лет | 1,86 - 3,47 | 1,86 - 3,47 |
Повышение уровня трансферрина
1. дефицит железа (повышение уровня может предшествовать развитию анемии в течение нескольких дней или месяцев);
2. приём эстрогенов и оральных контрацептивов.
Понижение уровня трансферрина
1. хронические воспалительные процессы;
2. гемохроматоз;
. цирроз печени;
. потери белка при ожогах, нефротическом синдроме и гастроэнтеропатиях (синдром мальабсорбции);
. злокачественные опухоли;
. приём андрогенов и глюкокортикоидов;
. наследственная атрансферринемия (редко);
. множественные гемотрансфузии (перегрузка организма железом);
. состояния, сопровождающиеся повышением онкотического давления (множественная миелома, гепатоцеллюлярное заболевание).
Перераспределение железа в организме
В организме человека происходит постоянное перераспределение железа.
В количественном отношении наибольшее значение имеет метаболический цикл
(1): плазма --» красный костный мозг --» эритроциты --» плазма.
(2): плазма --» ферритин, гемосидерин --» плазма
(3): плазма --» миоглобин, железосодержащие ферменты --» плазма.
Все эти три цикла взаимосвязаны через плазматический трансферрин. Единовременно он связывает лишь 3 мг железа, но ежедневный обмен железа через него в 10 раз больше. Трансферрин, таким образом, играет центральную роль в "круговороте" железа в организме (рис. 2).
Свободные ионы железа могут образовываться в клетке при переносе между трансферрином и низкомолекулярными хелаторами, ферритином и хелаторами, хелаторами и митохондриями, при деградации ферритина в лизосомах, при избыточном накоплении гемосидерина. Несвязанное железо вместе с супероксид-радикалом, который восстанавливает Fe(III), и перекисью водорода, образующейся в ходе реакции Фентона, поставляют высоко реакционноспособные гидроксильные радикалы. Суммой этих двух реакций является так называемая реакция Габера-Вейса. Fe(III), получающееся при реакции Фентона, также может быть восстановлено аскорбатом, что ведет к дальнейшей продукции радикалов. Обладающий высочайшей активностью гидроксильный радикал вызывает перекисное окисление липидов, разрывы нитей ДНК и деградацию других биомолекул.
Таким образом, ионы железа постоянно находятся в связанной форме. Главные органы, выполняющие функцию хранения железа, - это печень, которая содержит около 700 мг железа, селезенка и костный мозг. Мышцы также важны из-за их большой массы, хотя реальная концентрация хранимого в них железа низкая - 40 мг/кг.
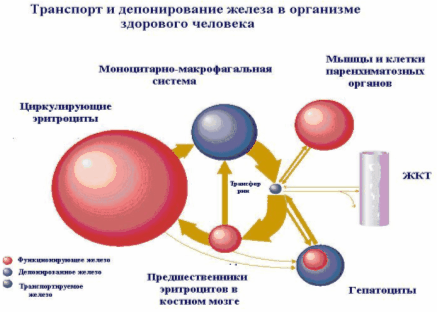
Рис. 2 Транспорт и депонирование железа в организме здорового человека.
Материалы и методы исследования
1)Определение уровня железа сыворотки крови, общей железосвязывающей способности и степени насыщения трансферрина, уровня ферритина сыворотки крови и растворимого sTfR рецептора к трасферрину.
Из многочисленных методов количественной оценки содержания железа в сыворотке крови наибольшее распространение получили методы определения железа по цветной реакции с батофенантролином. В основе этих методов лежит свойство двухвалентного восстановленного железа (Fe2+) образовывать яркоокрашенный комплекс с батофенантролином. Интенсивность окраски комплекса, соответствующую концентрации Fe2+ в сыворотке, определяют фотометрически. Предварительно белки сыворотки крови осаждают трихлоруксусной кислотой и восстанавливают сывороточное железо в двухвалентную его форму (Fe3+ в Fe 2+) с помощью гидразина или тиогликолевой кислоты.
В норме у мужчин в сыворотке крови содержится 13-30 мкмоль/л негеминового железа, у женщин - примерно на 10-15% меньше.
Общая железосвязывающая способность сыворотки (ОЖСС) отражает резервную «незаполненную» железом емкость транспортного белка - трансферрина. При ЖДА всегда наблюдается повышение ОЖСС в отличие других типов гипохромных анемий.
Рецептор sTfR трансферрина - альтернативный параметр, указывающий на функциональный недостаток железа. Транспорт железа в клетку происходит при взаимодействии комплекса железо-Tf со специфичным для Tf рецептором плазматической мембраны.
Структура рецептора: две одинаковые пептидные цепи, проходящие сквозь мембрану клетки, связаны несколькими дисульфидными мостиками. Молекула Tf, несущая два атома железа, «причаливает» на внешний конец рецептора, после чего поглощается клеткой путем эндоцитоза (Рис.3).
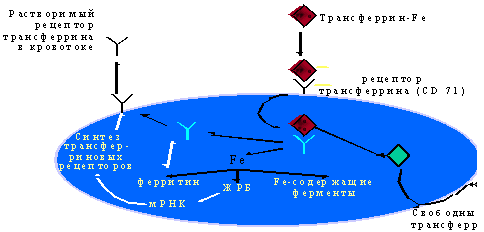
Рис.3 Работа растворимого sTfR рецептора к трансферрину.
Белковая часть Tf, освободившись от железа, вместе с рецептором выходит на поверхность клетки, где апо-трансферрин отделяется и весь цикл повторяется.
При повышенной потребности в железе, цикл рецептора Tf ускоряется и все больше рецепторов располагается на поверхности клетки. При этом все чаще внеклеточная часть рецептора подвергается воздействию протеаз, в результате чего от рецептора отделяется и попадает в кровь довольно стабильный фрагмент - пептид с молекулярным весом 95 кД, называемый «растворимым» рецептором трансферрина (sTfR), концентрацию которого в сыворотке крови можно определить при помощи иммунологических методов.
Т.о., уровень sTfR в крови отражает «железное голодание» клетки. Рассматривая диагностическое значение sTfR, следует помнить, что 80% рецептора ТФ находится на мембране эритропоэтических клеток, присутствует он в клетках плаценты, лимфоцитах, некоторых раковых клетках.
Чем ниже содержание Fe в клетке, тем выше экспрессия рецепторов трансферрина
При высокой скорости синтеза рецепторов трансферрина происходит угнетение синтеза молекул ферритина
При проведении исследования особые требования предъявляются к технике взятия крови, поскольку неизбежное при этом разрушение эритроцитов и увеличение содержания в сыворотке свободного гемоглобина может оказать существенное влияние на результаты.
) Мазок крови
Для правильной интерпретации СОЭ необходимо исследование мазка периферической крови (рис. 4; 5) поскольку:(1) одновременное наличие клеток малого и большого объема создает представление о нормальном размере эритроцитов;
(2) включение в подсчет ретикулоцитов, имеющих большие размеры, чем зрелые эритроциты, ведет к завышению СОЭ
(3) эритроидные клетки аномальных размеров могут присутствовать в столь малом количестве, что не влияют на вычисляемый СОЭ.Эритроцитометрическая кривая используется для оценки анизоцитоза(вариабельности размеров эритроцитов) и полезна в дифференциальной диагностике анемий с близкими значениями СОЭ. Для железодефицитной анемии характерен низкий СОЭ. Исследование мазка периферической крови имеет решающее значение в диагностике анемий. При приготовлении мазков не должно возникать артефактов. Морфологию эритроцитов лучше изучать в той части мазка, где они расположены в один слой и лишь соприкасаются друг с другом. Важно выявить специфические нарушения морфологии эритроцитов (обсуждаемые при рассмотрении отдельных типов анемии), а также изменения структуры и количества лейкоцитов и тромбоцитов. Исследование мазка периферической крови нередко позволяет установить окончательный диагноз или значительно сузить выбор из возможных нозологических форм, для разграничения которых используют дополнительные исследования. Д. Дополнительные исследования, по возможности, проводят до гемотрансфузии.