Файл: Дрістер жинаЫ 1 дріс Таырыбы кіріспе. Материалды нкте механикасы. аралатын мселелер.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 259
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Термодинамика – физикалық процестерді энергетикалық тұрғыдан қарастыратын сала. Термодинамика денелер мен табиғат құбылыстарының тек макроскопиялық қасиеттерін ғана зерттейді. Термодинамикаға негіз болатын заңдар термодинамика бастамалары деп аталады. Термодинамиканың бірінші бастамасы: Ішкі энергия - жүйе күйінің функциясы, ол негізінен екі түрлі процестің – дененің А жұмыс істеуі мен денеге берілген Q жылу мөлшерінің есебінен өзгереді. Жұмыс істеу жүйеге әсер етуші сыртқы денелердің орын ауыстыруымен қоса жүреді. Бір денеден екінші денеге энергияның берілуіне әкелетін макроскопиялық процестердің жиынтығы жылу берілу деп аталады.

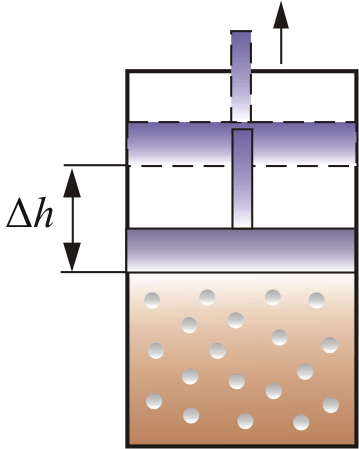
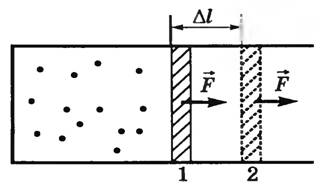
а) б) в)
7.1– сурет
Дененің ішкі энергиясын екі түрлі жолмен өзгертуге болады: Жылу беру арқылы және механикалық жұмыс жасау арқылы (7.1 – сурет).
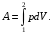
(
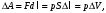
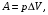 7.1)
7.1)А > 0 болса, жұмысты газ атқарады.
А < 0 болса, жұмыс сыртқы күштердің тарапынан жасалады.
Жылу берілу түрлері: жылу алмасу, конвекция, сәуле шығару.
Көлем тұрақты болса, онда жұмыс жасалмайды да, жылу мөлшері толығымен ішкі энергияны арттыруға жұмсалады.
Термодинамиканың бірінші бастамасы: жүйеге берілген жылу мөлшері жүйенің ішкі энергиясын өзгертуге және жүйенің сыртқы күштерге қарсы жұмыс атқаруына жұмсалады.
ТД-ның бірінші бастамасының дифференциалдық түрдегі теңдеуі:
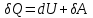 . (7.2)
. (7.2)Жұмыс пен жылу – термодинамикалық жүйе күйінің өзгеру процестерінің энергетикалық сипаттамасы. Идеал газ сыртқы күштерге қарсы жұмыс атқарса, элементар жұмыс оң болады:
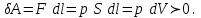
Жүйе бір күйден екіншіге ауысқанда (1→2) атқарылған жұмыс:
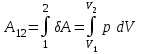 (7.3)
(7.3)Жүйе периодты түрде бастапқы күйіне қайтып оралып тұрса, оның ішкі энергиясы өзгермейді:
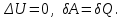
Яғни, қыздырғыштанберілетін энергиядан артық жұмыс атқаратын периодты түрде жұмыс істейтін жылу машинасының болуы мүмкін емес.
1 моль идеал газ үшін ТД-ның бірінші бастамасының теңдеуі:

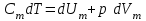 . (7.4)
. (7.4) Тұрақты көлемде берілген жылу ішкі энергияның артуына жұмсалады:
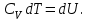 1 моль газдың ішкі энергиясының өзгеруі:
1 моль газдың ішкі энергиясының өзгеруі: 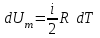 . (7.5)
. (7.5)Осыдан:
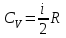 . Изобарлық қызу процесінде:
. Изобарлық қызу процесінде: 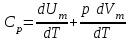 . (7.6)
. (7.6)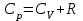 . (7.7)
. (7.7) Осы (73) формула Майер теңдеуі деп аталады: изобарлық
Осы (73) формула Майер теңдеуі деп аталады: изобарлық 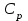 мольдік жылу сыйымдылығы изохорлық
мольдік жылу сыйымдылығы изохорлық 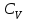 мольдік жылу сыйымдылығынан мольдік газ тұрақтысы R шамасына артық. Майер теңдеуінің еркіндік дәрежелерінің саны арқылы жазылуы:
мольдік жылу сыйымдылығынан мольдік газ тұрақтысы R шамасына артық. Майер теңдеуінің еркіндік дәрежелерінің саны арқылы жазылуы: 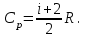
Адиабаттық және политроптық процестер
Термодинамикалық жүйеде оны қоршаған сыртқы ортамен жылу алмаспай
(
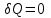 ) орындалатын процесті адиабаттық деп атайды.
) орындалатын процесті адиабаттық деп атайды.Адиабаттық процесс үшін Пуассон теңдеуі:
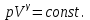 (7.8)
(7.8)Мұндағы
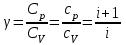 - адиабата көрсеткіші. Пуассон теңдеуінің:
- адиабата көрсеткіші. Пуассон теңдеуінің:температура мен көлем арқылы жазылуы:
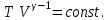 (7.8´)
(7.8´)температура мен қысым арқылы жазылуы:
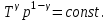 (7.9)
(7.9)Адиабаттық процесс үшін термодинамиканың бірінші бастамасы:
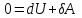 . (7.10)
. (7.10) 1)
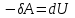 , сыртқы күштердің жұмысы есебінен газдың ішкі энергиясы артады, яғни
, сыртқы күштердің жұмысы есебінен газдың ішкі энергиясы артады, яғни 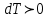 .
.2)
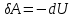
, газішкі энергиясының кемуі есебінен сыртқы күштерге қарсы жұмыс атқарады, яғни
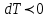 .
.Адиабаттық процесте атқарылатын жұмыс:

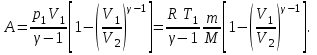 (7.11)
(7.11)ТД жүйенің тұрақты жылу сыйымдылығында (
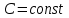 ) орындалатын процесс политроптық деп аталады. Политроптық процестің теңдеуі:
) орындалатын процесс политроптық деп аталады. Политроптық процестің теңдеуі: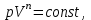 (7.12)
(7.12)мұндағы
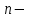 политропаның көрсеткіші:
политропаның көрсеткіші: 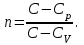
Политроптық процестің дербес жағдайлары:
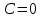 | 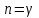 | 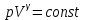 | Адиабата теңдеуі |
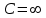 | 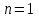 |  | Изотерма теңдеуі |
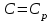 | 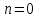 | 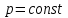 | Изобара теңдеуі |
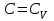 | 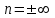 | 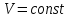 | Изохора теңдеуі |
Термодинамиканың екінші бастамасы Алдымен тура бағытта, сосын кері бағытта орындалатын процесте ТД жүйе және онымен әсерлесетін барлық сыртқы денелер алғашқы күйіне қайта оралатын процесті қайтымды деп атайды.
Энтропия. Газ молекулалардың жылулық қозғалысының ерекшелігі - оның ретсіздігінде. Изотермдік процесте жүйенің алған жылуының энергия көзінің температурасына қатынасы келтірілген
 жылу мөлшері деп аталады:
жылу мөлшері деп аталады: 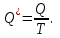 Процестің шексіз аз бөлігінде келтірілген
Процестің шексіз аз бөлігінде келтірілген жылу мөлшері
жылу мөлшері 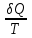 -ге тең, ал нақты екі бөлігінің арасында (
-ге тең, ал нақты екі бөлігінің арасында (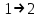 ):
): 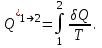
Кез келген қайтымды циклде:
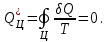 Толық дифференциалы процестің шексіз аз бөлігінде келтірілген жылу мөлшеріне тең күй функциясын энтропия (S) деп атайды:
Толық дифференциалы процестің шексіз аз бөлігінде келтірілген жылу мөлшеріне тең күй функциясын энтропия (S) деп атайды: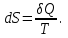 (7.13)
(7.13)Оқшауланған тұйық жүйедегі қайтымсыз процесте жүйенің энтропиясы әрқашан артады:
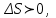 ал қайтымды процесте өзгермейді:
ал қайтымды процесте өзгермейді: 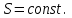 Осы екі жағдай Клаузиус теңсіздігіне біріктірілген:
Осы екі жағдай Клаузиус теңсіздігіне біріктірілген: 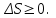 (7.14)
(7.14)ТД жүйе бір күйден екінші күйге (
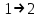 ) өткенде энтропияның өзгерісі осы күйлерге сәйкес энтропиялардың айырымына тең:
) өткенде энтропияның өзгерісі осы күйлерге сәйкес энтропиялардың айырымына тең: (7.15)
(7.15)Адиабаттық қайтымды процесте (
 ) энтропия тұрақты
) энтропия тұрақты 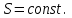 Сондықтан оны изоэнтропиялық процесс деп те атайды.
Сондықтан оны изоэнтропиялық процесс деп те атайды. Изотермдік процестегі (
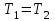 ) энтропияның өзгерісі:
) энтропияның өзгерісі: 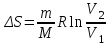 .
. Изохорлық процестегі (
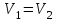
) энтропияның өзгерісі:
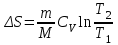 .
. Энтропия - аддитивті шама: термодинамикалық жүйенің энтропиясы жүйенің құрамдас бөліктерінің (жүйеге кіретін денелердің) энтропияларының қосындысына тең.
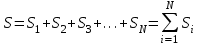 . (7.16)
. (7.16)Макрожүйенің қандай да бір нақты күйге келу әдістерінің саны жүйе күйінің термодинамикалық ықтималдығы деп аталады. Жүйенің энтропиясы мен термодинамикалық ықтималдық арасындағы байланыс Больцман формуласымен анықталады:
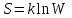 (7.17)
(7.17)Жүйе күйінің термодинамикалық ықтималдығы W жүйені құрайтын бөлшектердің координаттар және жылдамдықтар бойынша таралу санына тең (
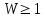 ). Оңашаланған тұйық жүйедегі қайтымды процестерде термо-динамикалық ықтималдық тұрақты болады (
). Оңашаланған тұйық жүйедегі қайтымды процестерде термо-динамикалық ықтималдық тұрақты болады (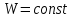 ), ал қайтымсыз процестерде ылғи артып отырады (
), ал қайтымсыз процестерде ылғи артып отырады ( 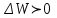 ). Осыдан шығатын қорытынды: қайтымсыз процестің нәтижесінде жүйе ең төменгі орнықсыз ықтимал күйден ең жоғарғы орнықты күйге (тепе-теңдікке) келеді.
). Осыдан шығатын қорытынды: қайтымсыз процестің нәтижесінде жүйе ең төменгі орнықсыз ықтимал күйден ең жоғарғы орнықты күйге (тепе-теңдікке) келеді.Больцман формуласы МКТ-ның негізінде энтропияның статистикалық мағынасын айқындайды: энтропияның анықтамасына сәйкес жүйе күйінің шексіз аз қайтымды өзгерісінде оған берілген жылу мөлшері
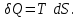 Сонда термодинамиканың бірінші бастамасы бойынша қайтымды процесте термодинамикалық тепе-теңдік орындалады:
Сонда термодинамиканың бірінші бастамасы бойынша қайтымды процесте термодинамикалық тепе-теңдік орындалады: 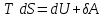 .
.Термодинамиканың екінші бастамасы жүйеде өтіп жатқан процестің бағытын анықтауға мүмкіндік береді. Клаузиус теңсіздігі мен энтропия ұғымы екінші бастаманы қайтымсыз процестер үшінтұйық жүйеэнтропиясының арту заңы түрінде тұжырымдайды.
Екінші бастаманың басқа қорытындылары:
1) Кельвин бойынша: нәтижесінде қыздырғыштан алынған жылу мөлшерін толығымен пара-пар жұмысқа айналдыратын циклдік процесті жүзеге асыруға болмайды;
2) Клаузиус бойынша:нәтижесінде температурасы төмен салқын денеден температурасы жоғары қызған денеге жылу берілетінциклдік процесті жүзеге асыруға болмайды;
ТД-ның алғашқы екі бастамасы температурасы абсолют нөлге жақын жүйенің күйі туралы айқын сипаттама бермейді. Бұл жағдай термоди-намиканың