Файл: Лекарственные формы с модифицированным высвобождением.doc
Добавлен: 08.11.2023
Просмотров: 879
Скачиваний: 23
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
3. Определить основные методы модификации высвобождения и доставки лекарственного вещества
4. Изучить технологию создания лекарственных форм с модифицируемым высвобождением.
3. Основные методы модификации высвобождения и доставки лекарственного вещества
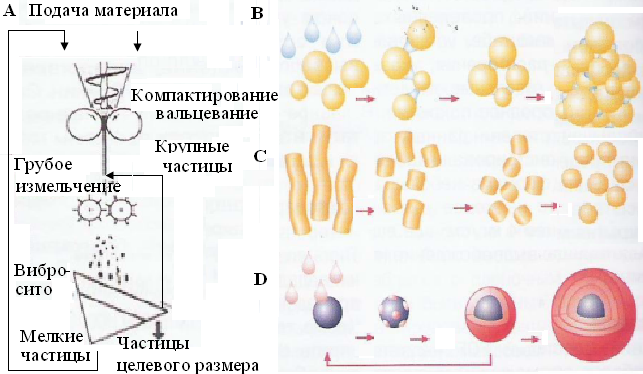
Рисунок 1. Технологические подходы к производству микрочастиц.
4. Технология создания лекарственных форм с модифицируемым высвобождением
Пролонгирование действия лекарственных веществ может быть обеспечено за счёт уменьшения скорости высвобождения их из лекарственной формы, депонирования лекарственного вещества в органах и тканях, снижения степени и скорости инактивации лекарственных веществ ферментами и скорости выведения из организма.
Таким образом, пролонгирования действия лекарств можно достигнуть с использованием физиологических, химических и технологических методов:
Основные методы модификации высвобождения и доставки лекарственного вещества:
1. Физические:
-
использование вспомогательных веществ, изменяющих растворимость, всасывание, распределение или элиминацию; -
использование физических сил – диффузия, осмос, гидродинамика, аэродинамика, электромеханические, магнитные, ультразвук и т. п.;
2. Химические:
-
образование солей, комплексов, добавление или замена функциональных химических групп в молекулу лекарственного вещества; -
конъюгация с веществом-носителем;
3. Технологические:
-
производство наноразмерных готовых лекарственных форм;
-
создание матриц, однослойных или многослойных оболочек, резервуаров, микросфер, липосом, наночастиц; -
микрогранулирование и микрокапсулирование; объединение частиц лекарственного вещества с разной скоростью высвобождения; -
иммобилизация, адсорбция, дисперсия в матриксах или на носителях; -
создание лекарственных терапевтических систем и т. п.); -
применение таргетных (направленных) инновационных препаратов, обеспечивающих наноразмерное воздействие на биомишень, что приводит к улучшенному терапевтическому эффекту.
Компактирование массы с последующей сепарацией необходимой фракции, влажная грануляция, как правило, в грануляторах с высоким усилием сдвига или экструзия-сферонизация массы, включающей активные фармацевтические ингредиенты и функциональные вспомогательные вещества.8
Нанесение функциональных оболочек на кристаллы активных фармацевтических ингредиентов или суспензии активных фармацевтических ингредиентов на сферы-плацебо, в коатерах, например, в условиях псевдоожиженного слоя с последующим нанесением функциональных оболочек. (Рисунок 1).
Впоследствии для получения мультипартикулярной системы микрочастицы смешивают со вспомогательными веществами и спрессовывают в таблетку.
Рисунок 1. Технологические подходы к производству микрочастиц.
Идеальная система доставки лекарственных средств должна быть инертной, биосовместимой, устойчивой, воспроизводимой, комфортной для пациента, безопасной, простой при использовании и удалении, пригодной для производства и стерилизации.4. Технология создания лекарственных форм с модифицируемым высвобождением
Как уже оговаривалось, различают три основных технологических приема:
1) монолитные (матриксные) системы;
2) резервуарные (мембранные) системы;
3) насосные (осмотические) системы.
Основу монолитной системы составляет матрикс (матричная или сетчатая структура), который может характеризоваться различными физико-химическими свойствами, быть растворимым или нерастворимым (рисунок 2).
Матрицы могут набухать и медленно растворятся или сохранять свою геометрическую форму в течение всего пребывания в организме и выводиться в неизменном виде. В последнем случае высвобождение лекарственного вещества происходит путемвымывания, при этом скорость его высвобождения не зависит ни от содержания ферментов, ни от величины рН и остается остаточно постоянной по мере прохождения таблетки через желудочно-кишечный тракт (ЖКТ).
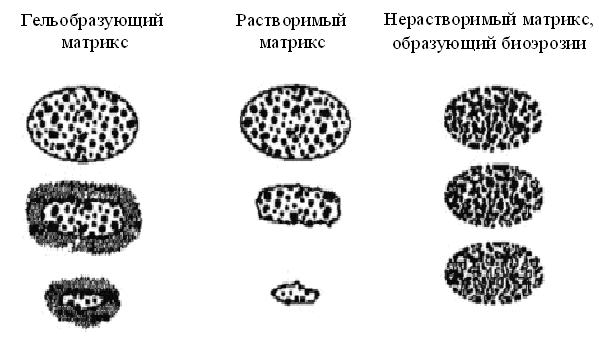
Рисунок 2. Матричная или сетчатая структура.
В зависимости от природы вспомогательных веществ матрицы могу быть:
гидрофильные (набухающие гидроколлойды): поливинол, производные целлюлозы – ГОПЦ, ГОПМЦ, ГОЭЦ, пектин, агар-агар, карбапол, альгиновая кислота и ее натриевая соль, хитозан, циклодекстрины. Хитозан получают из панцирей ракообразных после обработки раствором щелочи. Хитозан нетоксичен, неаллергенен. Циклодекстрины – циклические полимеры глюкозы, полученные из крахмала, под действием амилазы BACILLUS MACERENS. К ним относятся a,b,y – циклодекстрины, содержащие 6,7,8 остатков глюкозы и имеющие внутренний диаметр полости 0,6-0,8 и 1,0 нм.
У трех последних веществ (альгиновая кислота и ее соли, хитозан, циклодекстрины) регулируемая скорость высвобождения лекарственных веществ зависит от РН окружающей среды. Гидрофильные матрицы являются самыми перспективными, так как не раздражают слизистую ЖКТ и постепенно разрушаются. При контакте с биологической жидкостью на поверхности таблетки образуется гель, являющийся барьером для диффузии лекарственных веществ.
На основе хитозана и ГОПЦ изготавливают «плавающие» таблетки, содержащие АСК, индометацин натриевую соль, и рибофлавин-5-фосфат. Таблетки не повреждают слизистую оболочку желудка, так как в кислой среде лекарственные формы, содержащие хитозан, набухают и плавают в содержимом желудка 2-3 часа, постепенно высвобождаясь и равномерно высвобождая лекарственные вещества.
Преимущество этих лекарственных форм заключается в том, что не создается местная высокая концентрация лекарственных веществ, следовательно, уменьшается опасность побочных реакций. Кроме того, плавающие лекарственные формы перспективны в случае применения лекарств, растворимых в жирах.
На основе гелия из ГОПЦ создана «плавающая» таблетка, содержащая в одном слое смесь, выделяющая диоксид углерода (оптимальное количество кальция карбоната, натрия гидрокарбоната, лимонной кислоты, наполнителей и ГОПЦ) и в другом слое - натриевую соль рибофлавин 5-фосфата. Выделяющийся диоксид углерода включается в гель ГОПЦ, благодаря чему таблетка плавает в желудке. «Плавающая» таблетка продлевает время нахождения ЛВ в желудке, пролонгируя его действия, при использовании оптимального количества смеси, выделяющей диоксид углерода.9
1. Буккальные таблетки – Тринитролонг, содержащие нитроглицерин представляют матричную – набухающую систему слоистой структуры. Представляет собой пленки овальной формы защечного типа. Через две минуты после аппликации пленки образуется желеобразная масса, которая постепенно рассасывается. Нитроглицерин быстро поступает в систему кровообращения, минуя печень. По продолжительности действия (до 6 часов) тринитролонг сравним с таблетками сустак, но по выраженности действия превосходит их. Для замедления скорости высвобождения нитроглицерина и растворения полимера добавлено масло какао, которое введено во внутренние слои таблетки. В качестве биорастворимого полимера используют сополимер акриламида: этилакрилата/винилпирролидона в соотношении 3:1:1.
2. Гидрофобные матрицы изготавливают из натуральных восков, гидрированных растительных масел, ВЖС, моно- ди- и триглицеридов – эфиров органических кислот, таких как миристиновая, пальмитиновая и стеариновая.
3. Для изготовления матричных таблеток используют инертные матрицы, представляющие собой нерастворимые полимеры. К ним можно отнести этилцеллюлозу, ацетилцеллюлозу, поливинилхлорид, полиэтилен, сополимеры винилацетата и винилхлорида. Вспомогательные вещества нерастворимы в жидкостях ЖКТ, и поэтому создают барьер, регулирующий диффузию действующих веществ таблеток. После высвобождения ЛВ в организме таблетка не теряет своей формы, поэтому такие таблетки называют скелетными или дурулами. Таблетки – дурулы хинидина сульфата представляют собой пористую таблетку, состоящую из основы поливинилхлорида, в поры которой включен хинидин сульфат. Хинидин сульфат равномерно высвобождается из таблетки в течение 8-10 часов путем вымывания из таблетки с постоянной скоростью два раза в день.
4. Для изготовления таблеток с нерастворимым каркасом (скелетные таблетки) используют также неорганические матрицы: ди- или трикальций фосфат, бария или кальция сульфат, аэросил. Эти вещества не токсичны, не растворимы в воде, не набухают при контакте с жидкостями, имеют до 40% пористую структуру. Лекарственное вещество из скелетных таблеток высвобождается путем вымывания. Такая таблетка не распадается в ЖКТ и сохраняет свою геометрическую форму в течение всего пребывания в организме. Но главным недостатком является то, что эти таблетки нельзя назначать больным с нарушенной моторикой ЖКТ. Так как были описаны случаи некроза ЖКТ при назначении таблеток феррогард-фолик, содержащих сульфат железа и фолиевую кислоту.
Резервуарные системы состоят из двух частей: оболочки (мембраны), которая образует резервуар, и ядра, в котором находится лекарственное вещество.
Высвобождение активных компонентов обеспечивается свойствами оболочки. Механизмами высвобождения являются диффузия через поры мембраны, образующиеся после ее набухания или биодеградации. Если ее толщина не изменяется, то процесс высвобождения описывается кинетикой нулевого порядка в течение 80 % времени, если же в результате биодеградации оболочки толщина ее уменьшается, то скорость высвобождения со временем будет увеличиваться. Свойствами оболочки достигаются разные эффекты: замедленное высвобождение (в т. ч. с системой множественных пеллет), отсроченное высвобождение, целенаправленное высвобождение (например, кишечнорастворимые оболочки), а также с помощью многослойных оболочек – прерывистое (пульсирующее) высвобождение вещества.
В резервуарных системах лекарственные вещества могут находиться в виде множественных микрочастиц (пеллет), которые размещены в матриксе или капсуле, такая система получила название спансула. Следует отметить, что термином «пеллеты» называют частицы лекарственного вещества малого размера, к ним относятся микрогранулы, микросферы, мини-таблетки и др.10 (Рисунок 3).
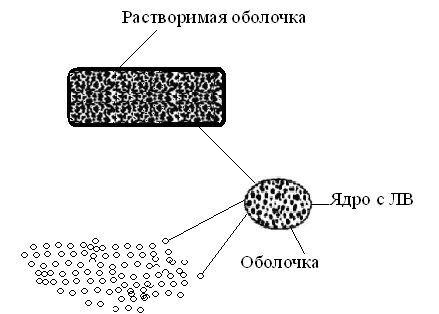
Рисунок 3. Строение пеллет.
Осмотические системы доставки и высвобождения лекарственных веществ предназначены для достижения кинетики нулевого порядка на протяжении ограниченного времени абсорбции в ЖКТ. Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Существует два типа осмотических систем доставки лекарственных средств: генерический осмотический насос и элементарный осмотический насос.
Генерическая осмотическая система представляет собой устройство с внутренним резервуаром, содержащим раствор или суспензию лекарственного вещества и окруженным непроницаемой оболочкой, и наружным резервуаром, содержащим осмотическое вещество и окруженным полупроницаемой оболочкой. Увеличение гидростатического давления ведет осмотические устройства, принуждая суспензию или раствор препарата к выходу из устройства через маленький порт доставки. Выпуск препарата независим от pH фактора и возможно смодулировать особенности выпуска, оптимизируя свойства покрытия полимера и препарата.
При погружении в водной среде гидростатическое давление в таблетке будет расти из-за селективного входа воды через полуводопроницаемую мембрану. Чтобы гарантировать, что покрытие в состоянии сопротивляться давлению в пределах устройства доставки, толщина мембраны обычно колеблется между 200 и 300 мкм. Мембрана нерасширяема, и увеличение объема, вызванное впитыванием воды, поднимает гидростатическое давление. Растворение препарата происходит в изоляции от окружающей среды ЖКТ. Давление уменьшено интенсивным потоком раствора из устройства доставки через маленькое отверстие.
Когда внутреннее осмотическое давление повысилось достаточно, то раствор или суспензия лекарственного препарата удаляется согласно предопределенной норме через отверстие доставки, процесс продолжается, пока весь твердый препарат не удаляется, и остается заполненная раствором оболочка. Первоначально 60-80 % препарата высвобождается при шкале нулевого порядка. Остаточный растворенный препарат продолжает доставляться, но по исчерпанной норме, пока осмотические давления внутри и снаружи таблетки не равны между собой.
Стимул, чтобы вовлечь воду в устройство доставки является различие между осмотическими давлениями внешней окружающей среды и раствора препарата. Осмотическое давление раствора лекарственного препарата должно быть относительно высоко, чтобы преодолеть осмотическое давление клеток тела. Следовательно, система часто содержит дополнительные осмотически активные материалы, такие как сахар или соли в пределах ядра, поскольку АФК может не всегда быть растворимым в воде вплоть до того, чтобы быть способным проявить адекватное осмотическое давление, чтобы запустить механизм устройства высвобождения.
В состав лекарственного средства могут также входить солюбилизаторы, которые делают растворимым препарат, поддерживая pH микроокружения, что помогает при высвобождении и поглощении препарата. Осмотические системы доставки препарата осуществляют высвобождение препарата по норме, которая зависит pH фактора и гидродинамики внешней среды-растворителя. Система также применима для доставки лекарственных препаратов с широким диапазоном водной растворимости. Следовательно, препарат может или быть высвобожден как раствор или как суспензия. Однако если препарат высвобожден как суспензия, то он должен быть растворим in vivo, прежде чем он станет систематически доступным.