ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 20.11.2021
Просмотров: 194
Скачиваний: 2
План.
ВВЕДЕНИЕ.
1.БИОЧИПЫ В БИОЛОГИИ И МЕДИЦИНЕ XXI ВЕКА.
1.2. Биочипы определение.
1.3. Виды, свойства и функции биочипов.
2.Основная часть.
2.1. Гелевые биочипы, их свойства, производство и анализ.
2.2. Олигонуклеотиды и ДНКовые микрочипы.
2.3. Клеточные микрочипы.
ЗАКЛЮЧЕНИЕ.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ .
БИОЧИПЫ В БИОЛОГИИ И
МЕДИЦИНЕ XXI ВЕКА.
Биологические микрочипы являются одним из наиболее быстро развивающихся экспериментальных направлений современной биологии. Существует два основных типа биочипов. Первый рассматриваемый тип - это микроматрицы различных соединений, главным образом биополимеров, иммобилизованных на поверхности стекла, в микрокаплях геля, в микрокапиллярах. Другим типом биочипов являются миниатюризованные "микролаборатории". Эффективность биочипов обусловлена возможностью параллельного проведения огромного количества специфических реакций и взаимодействий молекул биополимеров, таких как ДНК, белки, полисахариды, друг с другом и низкомолекулярными лигандами. Удается в достаточно простых параллельных экспериментах собрать и обработать на отдельных элементах биочипа огромное количество биологической информации. В этом заключается фундаментальное информационное сходство биочипов с электронными микрочипами. Однако между ними имеется и ряд принципиальных различий.
На рис. 1 показан принцип действия ячейки ДНК или олигонуклеотидного биочипа, основанный на комплементарных взаимодействиях основания аденина (А) с тимином (Т) и гуанина (G) с цитозином (С) в двух нитях ДНК. Если последовательность оснований в одной нити ДНК (или олигонуклеотида) полностью комплементарна последовательности другой нити, то образуется стабильная совершенная двухнитчатая спираль - дуплекс. Однако присутствие в дуплексе даже одной неправильной пары, например G-G, предотвращает образование дуплекса. Если иммобилизовать в одном из элементов микрочипа специфическую одноцепочечную ДНК или, положим, 20-мерный олигонуклеотид (пробу), то при добавлении к микрочипу меченных флюоресцентными красителями фрагментов ДНК, например генома человека, будет происходить их высокоспецифичное взаимодействие. Заданный олигонуклеотидный элемент биочипа специфически свяжет только одну комплементарную последовательность из 420 = 1.09 х 1012 всех возможных последовательностей этой длины в ДНК. В результате флюоресцентное свечение наблюдается только на этом комплементарном элементе биочипа. Таким образом, один элемент биочипа производит одну выборку примерно из триллиона возможных вариантов, в отличие от элемента электронного чипа, где происходит двоичная выборка: ДА или НЕТ.
Рис. 1. Схема образования двойной спирали ДНК на биочипе
Олигонуклеотид фиксирован на одном из элементов биочипа и избирательно связывает из многих флуоресцентно меченых фрагментов ДНК только комплементарный. В результате только этот элемент начинает светиться. Это происходит благодаря высоко-специфичным взаимодействиям комплементарных пар нуклеотидов А с Т и G с С. Присутствие некомплементарной пары, например G-G, предотвращает взаимодействие и оставляет элемент микрочипа темным
Стремительное развитие биологии во второй половине прошлого века тесно связано с появлением молекулярной и клеточной биологии, которая основана на концепции о редукционизме -сводимости сложных биологических процессов к процессам, протекающим на уровне отдельных молекул биополимеров, прежде всего белков и нуклеиновых кислот и их различных клеточных комплексов и структур. Редукционизму противопоставлялась концепция интегратизма о необходимости комплексного изучения структуры и функционирования в клетке всей совокупности макромолекул. В последние годы появились такие новые интегративные подходы, как геномика, протеомика и селломика, развиваемые большими коллективами или часто целыми "научными фабриками". Эти направления позволяют устанавливать структуру и изучать процессы на уровне генов всего генома, белков всей клетки или клеток всей ткани. Развиваемые в последние годы биологические микрочипы позволяют реализовать в доступной форме весьма сложные интегративные подходы геномики, протеомики и селломики. Например, олигонуклеотидные и ДНКовые микрочипы, выпускаемые рядом фирм, позволяют в достаточно простых, доступных отдельным исследователям экспериментах изучать экспрессию большинства генов различных бактерий и многих генов человека. На очереди создание белковых чипов, содержащих большое количество иммобилизованных клеточных белков или специфичных к ним антител.
Макроматрицы ДНК и белков иммобилизованных на фильтре, или фиксированных в лунках планшет, были известны достаточно давно. Однако первая работа по ДНКовым микрочипам и одна из первых по белковым микрочипам в современном формате были опубликованы нашей лабораторией в Институте молекулярной биологии им. В.А. Энгельгардта РАН (ИМБ). Этот принципиальный скачок был предложен для использования в новом методе секвенирования ДНК гибридизацией. В 1968 г. Советский Союз, а вслед за ним США и другие страны приняли государственные программы установления полной последовательности всех 3 миллиардов нуклеотидов генома человека. Широко дискутировался вопрос, должна ли эта задача решаться масштабированием существующих подходов или должны быть разработаны новые, более эффективные методы. В связи с временными ограничениями, ученые пошли по пути существенного улучшения и гигантского масштабирования уже существующего метода, основанного на считывании одного нуклеотида за другим с конца коротких фрагментов ДНК. Этот метод в химическом и ферментативном варианте был предложен В. Гилбертом и Ф. Сенгером, которые и разделили Нобелевскую премию за 1967 г. В развитии химического метода большую роль сыграли академики Е.Д. Свердлов и А.Д. Мирзабеков. В своей Нобелевской речи В. Гилберт отметил, что "идея метода пришла только после второго визита А. Мирзабекова" в его лабораторию.
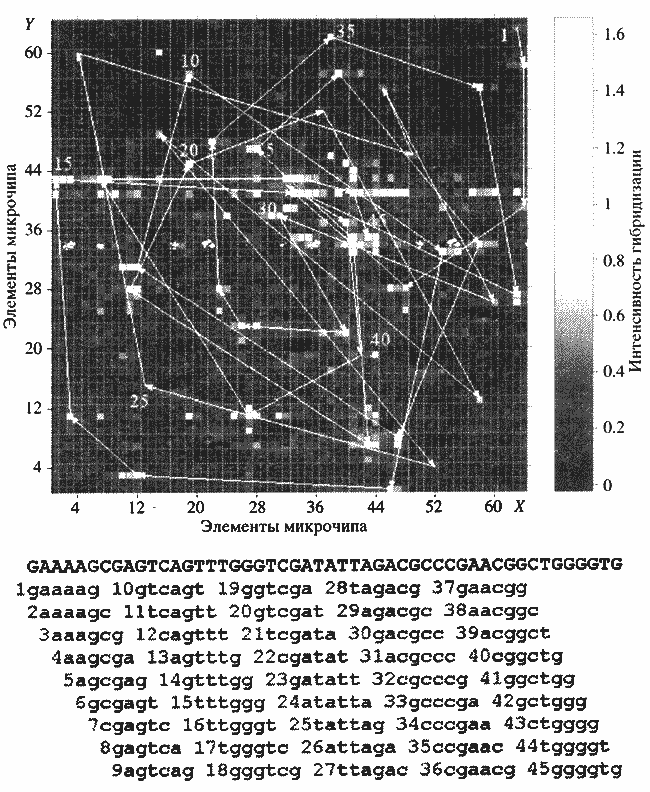
Рис. 2. Секвенирование фрагмента ДНК гибридизацией с полным олигонуклеотидным микрочипом, содержащим все 4096 6-меров
6-меры микрочипа, образующие при гибридизации с флуоресцентно меченым фрагментом ДНК совершенные дуплексы, интенсивно светятся. Такие соседствующие 6-меры перекрываются на пять нуклеотидов; это перекрывание позволяет однозначно восстановить нуклеотидную последовательность ДНК
В поисках новых подходов к секвенированию ДНК нами, а также независимо двумя другими группами в Англии и Сербии было предложено в 1988 г секвенирование гибридизацией. В этом методе секвенирование проводится не отдельными нуклеотидами, а словами в составе полного "словаря" нуклеотидных слов определенной величины. Такой словарь может содержать все возможные 4096 гексануклеотидов, т.е. шестибуквенных генетических слов. Для нас стала очевидной необходимость создания микрочипов, и в следующем году появилась первая статья, описывающая приготовление и свойства предложенных нами гелевых микрочипов. Позднее нами были созданы полные микрочипные гексануклеотид-ные словари. С этого момента и по настоящее время наша группа сконцентрировалась на развитии биочипов: создании ДНКовых, белковых и клеточных биочипов, на развитии технологий их производства и на их применении в фундаментальных исследованиях и их различных приложениях в медицине, биотехнологии и др. областях. Эти исследования рассмотрены в обзорной работе.
Рис. 2 показывает такой полный 6-мерный олигонуклеотидный микрочип и секвенирование на нем 50-нуклеотидного фрагмента ДНК . Для приведенного случая идентификация всех 6-меров, комплементарных к ДНК, и перекрывание соседних 6-меров на пять нуклеотидов позволяет восстановить полную нуклеотидную последовательность ДНК. В действительности метод в данном варианте работает только в части случаев, его широкому применению должно предшествовать решение ряда экспериментальных проблем, которые будут рассмотрены далее. .
ГЕЛЕВЫЕ БИОЧИПЫ, ИХ СВОЙСТВА, ПРОИЗВОДСТВО И АНАЛИЗ
Своеобразием и отличием развиваемых нами биочипов является то, что они представляют собой полусферические капли гидрогеля, фиксированные химической связью на поверхности стекла, пластика или силикона. Различные биомолекулы равномерно распределяются и иммобилизуются химическими связями в объеме геля. Иммобилизация не на двумерной поверхности, а в трехмерном объеме геля дает ряд существенных преимуществ. В десятки и сотни раз увеличивается емкость биочипа на единицу поверхности и соответственно увеличивается чувствительность измерений. Иммобилизованные макромолекулы как бы фиксированы в гомогенной водной среде, составляющей около 95% объема геля. Это исключает их взаимодействие как друг с другом, так и с твердой поверхностью, где гетерофазные процессы с участием фиксированных на ней биомолекул протекают более сложным образом. Это особенно существенно для белковых чипов, поскольку молекулы белков имеют тенденцию денатурации в интерфазе, образованной между твердой поверхностью и водной средой. Наконец, гелевые элементы на воздухе или под маслом превращаются как бы в изолированные микро- и нанолитровые пробирки, в каждой из которых можно проводить индивидуально различные специфические взаимодействия, химические и ферментативные реакции. Благодаря этому гелевые биочипы объединяют в себе свойства и микроматриц и микролабораторий.
Технология производства гелевых биочипов прошла три этапа развития.
Громоздкая и малоэффективная технология первого поколения состояла из пяти стадий и была разработана и запатентована в ИМБ в 1989-1993 гг. Она была перенесена в совместную биочипную лабораторию, организованную ИМБ и Аргонской национальной лабораторией (АНЛ, США) в 1994-2000 гг. и стала технологией первого поколения, была лицензирована американскими фирмами "Моторолой" и "Пакардом". Однако из-за ее несовершенства фирмы стали производить биочипы не как микроматрицы гелевых элементов, а как сплошную поверхность полиакриламидного геля.
В ИМБ за последние три года разработаны технологии производства биочипов второго и третьего поколения. Технология второго поколения состоит из трех этапов: модификация иммобилизуемых биополимеров мономерными группами геля, нанесение раствора этих веществ в смеси с мономерными звеньями геля с помощью игольчатого или пьезоэлектрического робота и, наконец, фотоиндуцированная сополимеризация свободных и связанных с биополимерами молекул мономера. Это приводит к равномерной иммобилизации веществ во всем объеме геля. В еще более простой двухэтапной технологии третьего поколения первая и третья стадии получения биочипов объединены с помощью своеобразной химической реакции.
Достаточно простая, универсальная и дешевая технология третьего поколения позволяет производить даже в лабораторных условиях сотни и в скором будущем тысячи олигонуклеотидных, ДНКовых или белковых микрочипов в день. Разработан также метод получения сополимеризацией микрочипов с размерами гелевых микроячеек до 5х5х5 мкм. Биочипы содержат от десятков до нескольких тысяч гелевых элементов с иммобилизованными в них соединениями. Элементы микрочипа представляют собой гидрогелевые полусферы (диаметром около 100 мкм), находящиеся на расстоянии 250 мкм друг от друга на гидрофобизованной поверхности стекла. Одноцепочечные ДНК длиной до 200-300 нуклеотидов и белки с массой до 150 кД легко и достаточно быстро диффундируют в гидрогелевые элементы микрочипов специально разработанного состава. Сам биочип помещен в реакционную камеру с капиллярным входом и выходом, в которой можно проводить различные процессы в строго контролируемых условиях.
АНАЛИЗ БИОЧИПОВ
Регистрация происходящих на биочипах процессов осуществляется с помощью флюоресцент-ных, а также в некоторых случаях хемилюминис-центных и масс-спектрометрических методов. Для количественного флюоресцентного анализа нами были разработаны совместно с РНЦ "Государственный оптический институт им. С.И. Вавилова" флюоресцентные широкопольные высоко-апертурные микроскопы, снабженные ПЗС-камерой и компьютером. Прибор позволяет проводить в реакционной камере количественный анализ в реальном времени сразу всех элементов биочипа в автоматическом режиме, одновременно при четырех длинах волн, при заданной или меняющейся температуре. Более 20 таких достаточно дорогих исследовательских анализаторов биочипов поставлены в лаборатории России и США. Для клиник нами разработан более простой и дешевый лазерный анализатор. Он позволяет проводить количественную регистрацию флюоресценции одновременно со всего биочипа с помощью более простой ПЗС-камеры и обрабатывать результаты на прилагаемом портативном компьютере с помощью специально созданных программ.
Хемилюминисцентные методы, хотя и уступают по чувствительности люминесцентным, позволяют значительно упростить и удешевить регистрирующую аппаратуру. Кроме того, разработан специальный метод прямого анализа соединений непосредственно в гелевых элементах с помощью MALDI-TOF масс-спектрометрии. Этот важный в протеомике метод позволяет проводить дополнительную идентификацию взаимодействующих с биочипами соединений по их массе.
ОЛИГОНУКЛЕОТИДНЫЕ И ДНКовые МИКРОЧИПЫ
Процесс комплементарных взаимодействий двух нитей ДНК (гибридизация) осложняется существенно меньшей стабильностью совершенного дуплекса А-Т по сравнению с G-C дуплексом и неодинаковым дестабилизирующим эффектом различных неправильных пар оснований. Поэтому в некоторых типах экспериментов была введено измерение кривых плавления, то есть количественной регистрации флюоресценции параллельно во всех ячейках микрочипа в градиенте повышающейся температуры. Это позволяет вычислить термодинамические параметры образования дуплексов: свободную энергию, энтропию и энтальпию. Проведение таких исследований на производимых нами микрочипах, содержащих всевозможные 6-мерные нуклеотиды (всего их 4096), открывает уникальные возможности. Сейчас измеряются термодинамические параметры для 4096 совершенных гексамерных дуплексов и 73728 дуплексов, содержащих всевозможные неправильные пары оснований во всех положениях гексануклеотидов. Составление полного каталога термодинамических параметров гексамерных дуплексов позволит создать более точную теорию гибридизации и оценить влияние на гибридизацию первичной и вторичной структур в ДНК. Эта теория необходима для практических работ с ДНК и, в свою очередь, будет способствовать завершению развития метода секвенирования ДНК гибридизацией.
Для широкого применения секвенирования ДНК гибридизацией с полными, например 6-мерными или более сложными, микрочипами требуется решение ряда проблем. Важной задачей является надежная дискриминация совершенных и неправильных дуплексов, образующихся на био-чипе, что затруднено различиями в стабильности А-Т и G-C пар оснований. Измерение кривых плавлений дуплексов и применение алгоритмов, вычисляющих поверхность под кривой плавления для каждого дуплекса, увеличивают надежность анализа. Другим серьезным препятствием является частое присутствие в ДНК повторяющихся гексануклеотидных и более длинных последовательностей. Эту частоту можно оценить количественно, измеряя и сравнивания интенсивности флуоресценции различных элементов биочипа.
Гибридизация с полным 6-мерным биочипом становится привлекательным методом для выявления известных и открытия новых мутаций и нуклеотидного полиморфизма в участках ДНК с известной структурой. Последовательная гибридизация с одним и тем же полным биочипом двух фрагментов одного и того же участка генома с известной и анализируемой структурой позволяет выявить различия во флюоресцентной картине и установить структуру и положение измененного основания в ДНК. Таким методом можно выявлять присутствие патогенных мутантов в стандартном штамме полиовируса, используемого как полиомиелитная вакцина.