Файл: Катионы iii аналитической группы. Катионы iv аналитической группы.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 22.11.2023
Просмотров: 380
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Схема систематического анализа смеси катионов V аналитической группы:
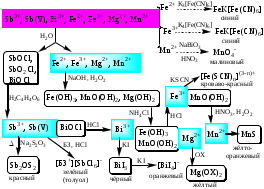
Предварительные испытания заключаются в определении цвета раствора (растворы Fe3+ окрашены в светло-бурый цвет), рН раствора и проведение пробы на легкогидролизуемые ионы Sb (III), Sb (V), Bi3+. В предварительных испытаниях дробным методом в отдельных пробах анализируемого раствора открывают ионы, окисляющиеся в ходе систематического анализа: Fe2+; Mn2+; Sb (III) реакциями с гексацианоферратом (III) калия, с висмутатом натрия и с металлическим железом соответственно.
Систематический анализ основан на использовании группового реагента NaOH в присутствии H2O2, на особенностях химических свойств метасурьмяной кислоты HSbO3; различной окислительно-восстановительной активности Mn2+ и Fe3+, Mg2+, Bi3+, а также на способности гидроксида магния растворяться в солях аммония.
2 Общая характеристика. Свойства катиона меди II. Реакции комплексообразования. Использование их в открытии катионов VI группы. Групповой реактив. Его действие. Применение соединений меди в медицине.
Все катионы VI аналитической группы являются простыми катионами d-элементов, которые расположены в периодической таблице Д. И. Менделеева в IB (Cu), IIB (Cd, Hg), VIIIB (Co, Ni) группах.
Характеристика катионов VI аналитической группы:
-
К шестой аналитической группе относятся Cu2+, Co2+, Cd2+, Ni2+ и Hg2+. -
Растворы солей меди (II) окрашены в синий, голубой цвет, кобальта (II) - в розовый, никеля – в зеленый; кадмия и ртути - бесцветные. -
Хлориды, сульфаты и нитраты этих катионов хорошо растворимы в воде. -
Гидроксиды катионов этой группы - слабые трудно растворимые электролиты. Гидроксиды катионов этой группы не растворимы в воде, щелочах, но растворимы в избытке концентрированного раствора аммиака. -
Гидроксиды меди (II) и ртути (II) неустойчивы и разлагаются на соответствующий оксид и воду: Cu(OH)2 при нагревании, а Hg(OH)2 при обычной температуре. -
Для катионов шестой группы характерны реакции комплексообразования. -
Групповым реактивом является раствор аммиака. Растворы аммиака осаждают Co, Ni, Cd, Cu в виде гидроксидов. Действие группового реактива. Групповым реактивом на катионы шестой группы является раствор гидроксида аммония. При взаимодействии эквивалентных количеств гидроксида аммония с солями катионов VI группы образуются осадки различного состава:
2CuSO4 + 2NH4OH → (CuOH)2SO4↓ + (NH4)2SO4 (фармакопейная реакция)
HgCl2 + 2NH4OH → [HgNH2]Cl↓ + NH4Cl + 2H2O
NiCl2 + NH4OH → NiOHCl↓ + NH4Cl
CoCl2 + NH4OH → CoOHCl↓ + NH4Cl
-
Все катионы VI аналитической группы, за исключением Cd2+, имеют переменную степень окисления, поэтому для них характерны окислительно-восстановительные реакции. Ионы Hg2+ и Cu2+ проявляют себя как окислители, ионы Co2+ и Ni2+ - как восстановители.
Таблица 2.
Продукты реакции катионов шестой аналитической группы
Реактив
Катион
Cu2+
Hg2+
Co2+
Ni2+
Cd2+
NH4OH
Гидроксид аммония
(CuOH)2SO4 зелено-синий
осадок
HgNH2Cl белый осадок
CoOHCl
синий осадок
NiOHCl зеленый
осадок
Cd(OH)2 белый осадок
NH4OHизб.
Гидроксид аммония
[Cu(NH3)4]2+
синий
[Hg(NH3)4]2+
бесцветный в присутст-вии NH4+
[Со(NH3)6]2+
желтый в присутствии NH4+
[Ni(NH3)6]2+
сине-фиолето-вый
[Cd(NH3)4]2+
бесцвет-ный
NaOH
Натрия гидроксид
Cu(OH)2
голубой
осадок
HgO
желтый
осадок
Co(OH)An
синий ↓,
переходящий в Cо(OH)2 розового цвета
Ni(OH)2
зеленый
осадок
Cd(OH)2
белый осадок
Na2S
Натрия сульфид
CuS
черный
осадок
HgS черный
осадок,
растворим в
«царской
водке»
CoS
черный
осадок
NiS
черный
осадок
CdS
желтый осадок
K4[Fe(CN)6]
Гексациа-ноферрат (II) калия
Cu2[Fe(CN)6]
красно-бурый
осадок
Hg2[Fe(CN)6]
коричнево-
черный
осадок
Co2[Fe(CN)6]
серо-зеленый
осадок
Ni2[Fe(CN)6]
зеленоватый
осадок
Cd2[Fe(CN)6]
Белый аморфный
KI
Калия йодид
Cu2I2+I2 бурова-тый
осадок
HgI2 красный осадок,
растворим в KI
-
Применение в медицине и значение для организма катионов VI аналитической группы:
| катион | Применение в медицине и значение для организма |
| Co2+ | Биологическая роль. В организме человека содержится очень мало кобальта (всего 1,2 мг). Как незаменимый микроэлемент (суточная потребность 300 мкг) он входит в состав металлопротеинов, которые находятся в тканях внутренних органов: печенки, почек, поджелудочной железы, а также в эритроцитах крови. Кобальт принимает участие в синтезе гормонов щитовидной железы - тироксина и трииодтиронина. Выявлено позитивное влияние ионов Co2+ на обмен витаминов, особенно аскорбиновой кислоты, а также на белковый, углеводный, липидный и минеральный обмены и синтез витамина РР. |
| Применение в медицине. Кобальт применяется в виде комплексных соединений препаратов «Коамид» и «Цинкобаламин» (В12) назначают для заболеваний системы крови – анемий, улучшения синтеза гемоглобина, усвоения препаратов железа. Этот витамин применяют также при многих заболеваниях нервной системы, кожных болезнях и ряде других патологических процессов. Хлористый кобальт в виде 20% раствора используется при лечении гипертонической болезни. Радиоактивные изотопы кобальта применяются в радиоизотопной диагностике и для лучевой терапии (Со-60). | |
| Ni2+ | Биологическая роль. Считается, что биологическая роль никеля заключается в участии в структурной организации и функционировании основных клеточных компонентов – ДНК, РНК и белка. Никель играет определенную роль и в гормональной регуляции организма. Никель угнетает действие адреналина, снижает артериальное давление, оказывает успокаивающее действие на центральную нервную систему. |
| Применение в медицине.Применяется при изготовлении брекет-систем, протезировании. | |
| Cd2+ | Биологическая роль. Кадмий относится к токсичным (иммуно-токсическим) ультрамикроэлементам, являясь одним из основных поллютантов окружающей среды. Его отрицательное действие на организм человека проявляется уже при очень низких концентрациях (3–300 мг в сутки). А при дозе 1–9 г возможны случаи с летальным исходом. Предполагается, что кадмий влияет на углеводный обмен, активирует ряд ферментов, играет роль в синтезе в печени гиппуровой кислоты, участвует в обмене в организме цинка, меди, железа и кальция. |
| Применение в медицине. Кадмий используется в гомеопатической медицине. В последние годы кадмий стал применяться при создании новых противоопухолевых нано-медикаментов. | |
| Cu2+ | Биологическая роль. Ионы меди, которые входят в состав ферментов, принимают участие в процессах дыхания тканей, роста и кроветворения, влияют на синтез в организме гемоглобина, а также усиливают действие гормонов гипофиза и инсулина, влияя таким образом на обмен сахаров и жиров. Медь необходима для нормальной жизнедеятельности растений и животных, так как входит в состав ферментов, влияет на белковый и углеводный обмен. |
| Применение в медицине. Сульфат меди CuSO4•5H2O обладает антисептическим вяжущим действием. В малых дозах раствор применяется для лечения анемии. Cu2С6Н4О8∙5H2O цитрат меди назначают в виде мазей при глазных заболеваниях. Медьсодержащие препараты и БАДП используются также в лечении и профилактике заболеваний опорно-двигательного аппарата, гипотиреоза. | |
| Hg2+ | Биологическая роль. Содержание ртути в организмах составляет около 10-6%. Ионы ртути и её соединения, связываясь с сульфгидрильными группами ферментов, могут инактивировать их. Попадая в организм, ртуть влияет на поглощение и обмен микроэлементов - Си, Zn, Cd, Se. |
| Применение в медицине. HgO является антисептическим веществом и входит в состав мазей для лечения кожных и глазных болезней. HgCl2 (сулема) применяют в растворе 1:1000 как дезинфицирующее средство для дезинфекции белья, одежды, стен, лечения кожных заболеваний. HgI2 используют в виде микстур для лечения некоторых венерических заболеваний, входит в состав мазей для лечения кожных заболеваний. Hg(СN)2•HgO – оксицианид ртути используется для лечения глазных и урологических заболеваний. |
Систематический анализ смеси катионов
VI аналитической группы.
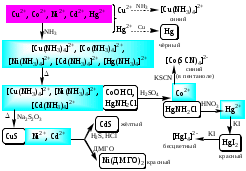
Анализируемый раствор может быть окрашенным или бесцветным. Предварительные испытания заключаются в определении цвета раствора и рН раствора. В прозрачном растворе смеси катионов шестой группы могут присутствовать ионы ртути (II) и кадмия, при наличии голубого цвета – ионы меди (II), светло-зеленого – никеля (II), розового – кобальта (II). Систематический анализ основан на использовании группового реагента раствора аммиака, а также на различной способности ионов к действию тиосульфата натрия в кислой среде.