Файл: Контрольные задания по дисциплине общая химическая технология для студентов заочной формы обучения.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 23.11.2023
Просмотров: 118
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
A, селективность SR, выход продукта ER, если на выходе из реактора CA=1 кмоль/м3, CR=7 кмоль/м3, СS=4 кмоль/м3.
Вариант 13
N2(г) + 3H2(г) ↔ 2NН3(г)
С6Н6(г) ↔ С6Н12(г) + Н2(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=1 кмоль/м3, CR=6 кмоль/м3, СS=2 кмоль/м3.
Вариант 14
4С2Н4(г) ↔ С5Н10(г) + С3Н6 (г)
С6Н14(г) ↔ С6Н6 (г) + 4Н2(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=7 кмоль/м3, СS=4 кмоль/м3.
Вариант 15
2СО(г) + О2(г) ↔ 2СO2(г)
С6Н5–СН3(ж) + Н2(г) ↔ С6Н6(г) + СН4(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=2 кмоль/м3, CR=6 кмоль/м3, СS=2 кмоль/м3.
Вариант 16
С6Н6(г) ↔ С6Н12(г) + Н2(г)
4С2Н4(г) ↔ С5Н10(г) + С3Н6 (г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=8 кмоль/м3, СS=5 кмоль/м3.
Вариант 17
С2Н6(г) ↔ С2Н4(г) + Н2(г)
N2(г) + 3H2(г) ↔ 2NН3(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=9 кмоль/м3, СS=2 кмоль/м3.
Вариант 18
С2Н6(г) ↔ С2Н4(г) + Н2(г)
CuS(т) + O2(г) ↔ Cu(т) + SO2(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=1 кмоль/м3, CR=5 кмоль/м3, СS=4 кмоль/м3.
Вариант 19
С2Н4(г) ↔ С2Н2(г) + Н2(г)
СН2О(г) + Н2(г) ↔ СН3ОН(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=5 кмоль/м3, CR=12 кмоль/м3, СS=3 кмоль/м3.
Вариант 20
С6Н14(г) ↔ С6Н6 (г) + 4Н2(г)
2СО(г) + О2(г) ↔ 2СO2(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=12 кмоль/м3, СS=4 кмоль/м3.
Вариант 21
2С4Н8(г) ↔ С8Н16(ж)
2СО(г) + О2(г) ↔ 2СO2(г)
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=7 кмоль/м3, СS=2 кмоль/м3.
Рекомендуемая литература.
1.Бесков В.С., Сафронов В.С. Общая химическая технология и основы промышленной экологии: Учебник для вузов. – М.:Химия, 1999. 472 с.: ил.
2.Общая химическая технология: Учебник для химико-техн. вузов/Под ред. И.П. Мухленова. – 4-е изд., перераб. и доп. – М: Высш. шк., 1984. – 256 с.: ил.
3.Краткий справочник физико-химических величин. Издание девятое/ Под ред. А.А. Равделя и А.М.Пономаревой. – СПб.: Специальная Литература, 1998. – 232 с.: ил.
ВОПРОСЫ К ЭКЗАМЕНУ
по дисциплине «Общая химическая технология»
1.Химическая технология. Основные стадии химико-технологического процесса.
2.Основные технико-экономические показатели химико-технологических процессов.
3.Классификация химических реакций по механизму, молекулярности и порядку.
4.Классификация химических реакций по зонам протекания и тепловому эффекту.
5.Понятие о конверсии, селективности и выходе товарной продукции.
6. Материальный и энергетический балансы.
7. Скорость химических реакций. Зависимость скорости реакции от концентрации реагентов. Кинетическое уравнение.
8.Зависимость константы равновесия химических реакций от температуры. Энергия активации.
9.Равновесие химических реакций. Закон действующих масс.
10.Константа равновесия и энергия Гиббса.
11.Способы смещения химического равновесия.
12.Понятие о катализе.
13.Основные механизмы катализа.
14.Технологические характеристики твердого катализатора: активность, температура зажигания, селективность.
15.Технологические характеристики твердого катализатора: структура, промотирование и отравление катализатора.
16.Стадии взаимодействия газообразных реагентов на поверхности твердых катализаторов.
17.Химические реакторы. Классификация.
18.Модель реактора идеального вытеснения (РИВ-н).
19.Модель реактора идеального смешения (РИС-н).
20.Сырьевая база химической промышленности.
21.Энергетическая база химической промышленности.
22.Химическая технология и очистка промышленных выбросов.
23.Классификация промышленных загрязнений биосферы.
24.Методы очистки отработанного воздуха и химзагрязненной воды.
Вариант 13
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
N2(г) + 3H2(г) ↔ 2NН3(г)
С6Н6(г) ↔ С6Н12(г) + Н2(г)
-
Описать физико-химические основы и аппаратурное оформление процесса очистки обжигового газа от контактных ядов. -
Представить и описать технологическую схему синтеза аммиака при среднем давлении. -
Протекают параллельные реакции: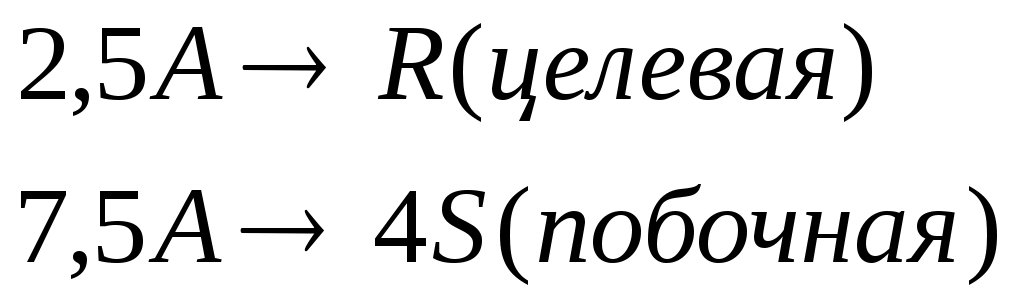
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=1 кмоль/м3, CR=6 кмоль/м3, СS=2 кмоль/м3.
Вариант 14
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
4С2Н4(г) ↔ С5Н10(г) + С3Н6 (г)
С6Н14(г) ↔ С6Н6 (г) + 4Н2(г)
-
Описать технологическую схему и оборудование очистного отделения современного производства контактной серной кислоты из колчедана. -
Изложить влияние различных факторов на процесс окисления аммиака в производстве азотной кислоты. -
Протекают последовательные реакции: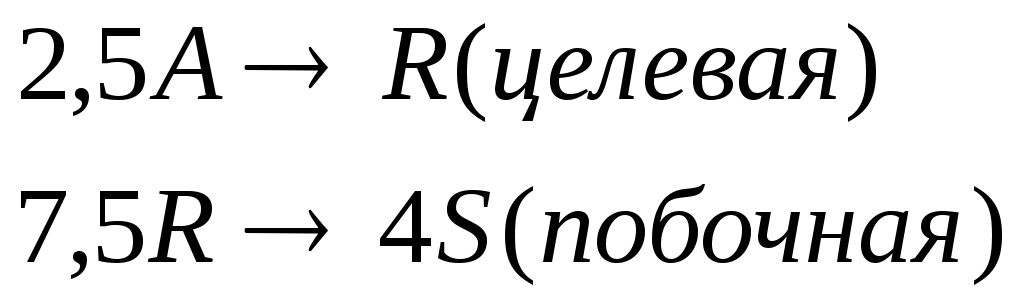
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=7 кмоль/м3, СS=4 кмоль/м3.
Вариант 15
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
2СО(г) + О2(г) ↔ 2СO2(г)
С6Н5–СН3(ж) + Н2(г) ↔ С6Н6(г) + СН4(г)
-
Охарактеризовать катализаторы, применяемые в производстве серной кислоты контактным методом. -
Изложить физико-химические основы процесса абсорбции диоксида азота водой в производстве разбавленной азотной кислоты. -
Протекают параллельные реакции: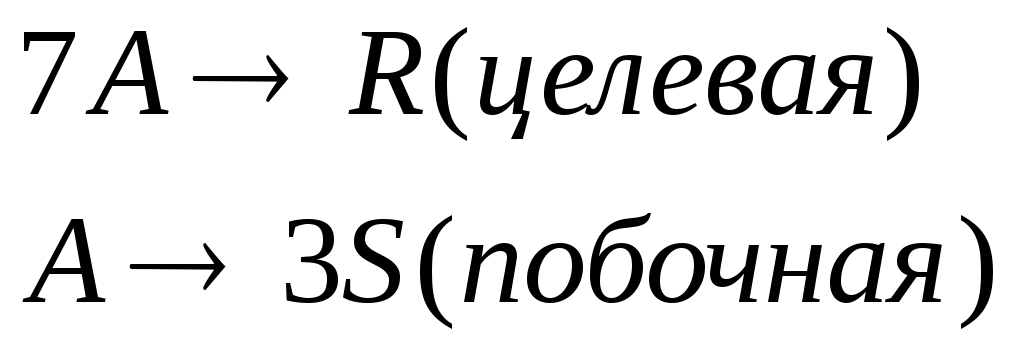
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=2 кмоль/м3, CR=6 кмоль/м3, СS=2 кмоль/м3.
Вариант 16
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
С6Н6(г) ↔ С6Н12(г) + Н2(г)
4С2Н4(г) ↔ С5Н10(г) + С3Н6 (г)
-
Описать физико-химические основы нитрозного процесса получения серной кислоты. -
Изложить теоретические основы разделения жидкого воздуха на азот и кислород методом ректификации. -
Протекают последовательные реакции: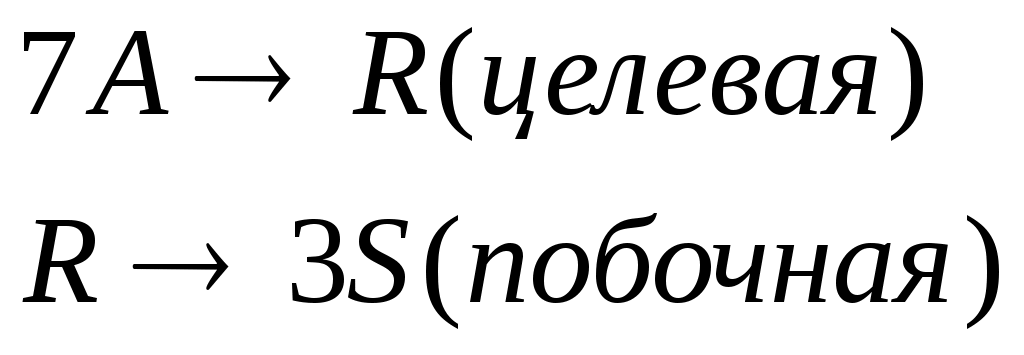
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=8 кмоль/м3, СS=5 кмоль/м3.
Вариант 17
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
С2Н6(г) ↔ С2Н4(г) + Н2(г)
N2(г) + 3H2(г) ↔ 2NН3(г)
-
Описать оборудование башенных систем производства серной кислоты нитрозным методом. -
Провести характеристику сырья для азотной промышленности. -
Протекают параллельные реакции: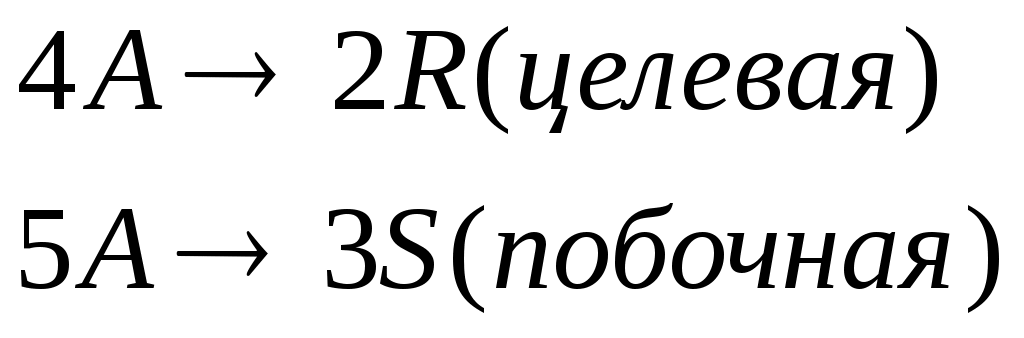
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=9 кмоль/м3, СS=2 кмоль/м3.
Вариант 18
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
С2Н6(г) ↔ С2Н4(г) + Н2(г)
CuS(т) + O2(г) ↔ Cu(т) + SO2(г)
-
Описать значение и область применения промышленного катализа. Сущность и виды катализа. -
Описать технологию получения азотоводородной смеси методом паровоздушной конверсии метана. -
Протекают последовательные реакции: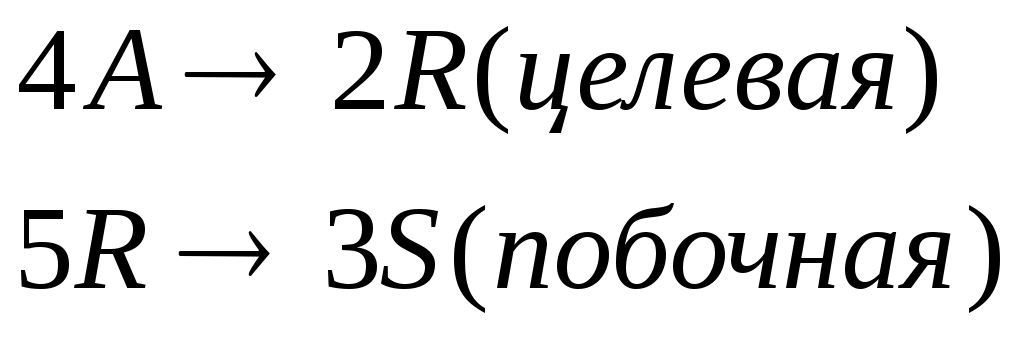
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=1 кмоль/м3, CR=5 кмоль/м3, СS=4 кмоль/м3.
Вариант 19
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
С2Н4(г) ↔ С2Н2(г) + Н2(г)
СН2О(г) + Н2(г) ↔ СН3ОН(г)
-
Описать методы производства водорода конверсией углеводородных газов. Привести сравнительный анализ этих методов. -
Описать методы очистки азотоводородной смеси от диоксида углерода и сероводорода. -
Протекают параллельные реакции: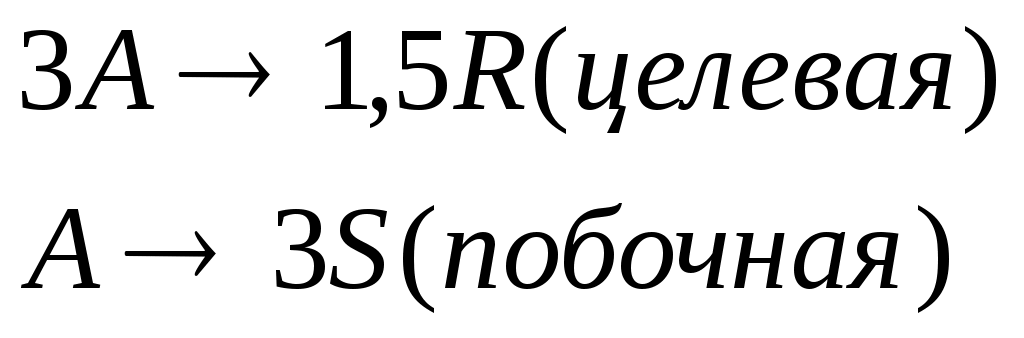
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=5 кмоль/м3, CR=12 кмоль/м3, СS=3 кмоль/м3.
Вариант 20
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
С6Н14(г) ↔ С6Н6 (г) + 4Н2(г)
2СО(г) + О2(г) ↔ 2СO2(г)
-
Описать производство водорода (азотоводородной смеси) разделением коксового газа. -
Описать процесс переработки нитрозных газов в разбавленную азотную кислоту. -
Протекают последовательные реакции: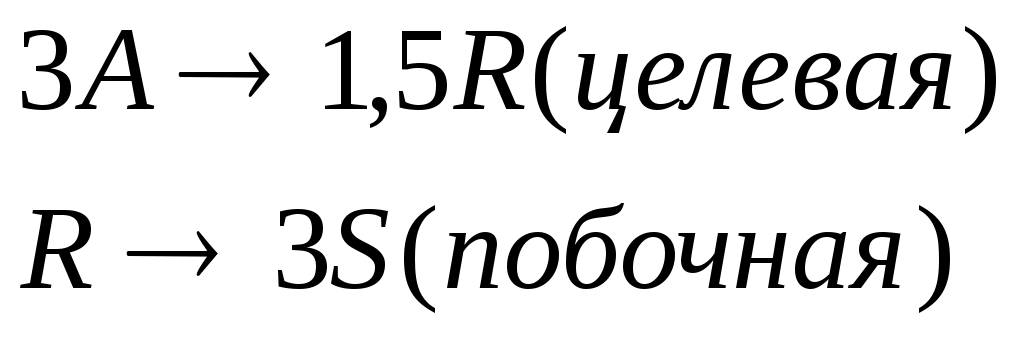
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=12 кмоль/м3, СS=4 кмоль/м3.
Вариант 21
-
Используя принцип Ле-Шателье, проанализируйте все возможные способы смещения равновесия реакции вправо для получения максимального количества целевого продукта (ΔН реакции рассчитывается по табличным данным):
2С4Н8(г) ↔ С8Н16(ж)
2СО(г) + О2(г) ↔ 2СO2(г)
-
Изложить особенности сернокислотного разложения фосфоритов Каратау. Изобразить технологическую схему производства из них экстракционной фосфорной кислоты. -
Охарактеризовать виды серосодержащего сырья для производства серной кислоты. Получение серы из руд, очистка серы. Привести схему установки для комплексной переработки серных руд. -
Протекают параллельные реакции:
Определить: степень превращения XA, селективность SR, выход продукта ER, если на выходе из реактора CA=3 кмоль/м3, CR=7 кмоль/м3, СS=2 кмоль/м3.
Рекомендуемая литература.
1.Бесков В.С., Сафронов В.С. Общая химическая технология и основы промышленной экологии: Учебник для вузов. – М.:Химия, 1999. 472 с.: ил.
2.Общая химическая технология: Учебник для химико-техн. вузов/Под ред. И.П. Мухленова. – 4-е изд., перераб. и доп. – М: Высш. шк., 1984. – 256 с.: ил.
3.Краткий справочник физико-химических величин. Издание девятое/ Под ред. А.А. Равделя и А.М.Пономаревой. – СПб.: Специальная Литература, 1998. – 232 с.: ил.
ВОПРОСЫ К ЭКЗАМЕНУ
по дисциплине «Общая химическая технология»
1.Химическая технология. Основные стадии химико-технологического процесса.
2.Основные технико-экономические показатели химико-технологических процессов.
3.Классификация химических реакций по механизму, молекулярности и порядку.
4.Классификация химических реакций по зонам протекания и тепловому эффекту.
5.Понятие о конверсии, селективности и выходе товарной продукции.
6. Материальный и энергетический балансы.
7. Скорость химических реакций. Зависимость скорости реакции от концентрации реагентов. Кинетическое уравнение.
8.Зависимость константы равновесия химических реакций от температуры. Энергия активации.
9.Равновесие химических реакций. Закон действующих масс.
10.Константа равновесия и энергия Гиббса.
11.Способы смещения химического равновесия.
12.Понятие о катализе.
13.Основные механизмы катализа.
14.Технологические характеристики твердого катализатора: активность, температура зажигания, селективность.
15.Технологические характеристики твердого катализатора: структура, промотирование и отравление катализатора.
16.Стадии взаимодействия газообразных реагентов на поверхности твердых катализаторов.
17.Химические реакторы. Классификация.
18.Модель реактора идеального вытеснения (РИВ-н).
19.Модель реактора идеального смешения (РИС-н).
20.Сырьевая база химической промышленности.
21.Энергетическая база химической промышленности.
22.Химическая технология и очистка промышленных выбросов.
23.Классификация промышленных загрязнений биосферы.
24.Методы очистки отработанного воздуха и химзагрязненной воды.