Файл: Емтихан тест тапсырмалары пн бейорганикалы химия Оу курсы 1 курс фармация факультеті.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 23.11.2023
Просмотров: 922
Скачиваний: 12
СОДЕРЖАНИЕ
ЕМТИХАН ТЕСТ ТАПСЫРМАЛАРЫ Пән: бейорганикалық химия Оқу курсы: 1 курс фармация факультеті
*+ негіздің эквиваленттік факторын
*ХИМИЯЛЫҚ БАЙЛАНЫС. МОЛЕКУЛА ҚҰРЫЛЫСЫ *1*25*1*
*ХИМИЯЛЫҚ РЕАКЦИЯНЫҢ ЖЫЛУ ЭФФЕКТІСІ*1*22*2*
*ЭЛЕКТРОЛИТИКАЛЫҚ ДИССОЦИАЦИЯ *1*39*2*
*КОЛЛИГАТИВТІК ҚАСИЕТТЕР*1*16*1*
*КОМПЛЕКСТІҚОСЫЛЫСТАР *1*20*1*
*ТОТЫҒУ-ТОТЫҚСЫЗДАНУ РЕАКЦИЯЛАР *1*27*2*
* IА-IIA ТОП ЭЛЕМЕНТТЕРІ*1*25*1*
*ТЕМІР, КОБАЛЬТ , НИКЕЛЬ ТОПШАСЫ*2*35*2*
*ХРОМ ЖӘНЕ ОНЫҢ ҚОСЫЛЫСТАРЫ 2*30*2*
*КӨМІРТЕК ПЕН КРЕМНИЙ ТОПШАСЫ*2*32*1*
*ЕРІТІНДІЛЕРДІҢ КОЛЛИГАТИВТІК ҚАСИЕТТЕРІ *2*12*1
*КОМПЛЕКСТІК ҚОСЫЛЫСТАР*2*10*1*
ЕКІ ЖАУАПТЫ ТЕСТЕР *ХИМИЯЛЫҚ РЕАКЦИЯЛАРДЫҢ ЭНЕРГЕТИКАСЫ*4 *17*1*
* ЭЛЕКТРОЛИТТЕР ДИССОЦИАЦИЯ*4*16*1*
*ХИМИЯЛЫҚ КИНЕТИКА*4*12*1* #611
* IА-IIA ТОП ЭЛЕМЕНТТЕРІ*1*25*1*
#246
*!Химиялық реакцияларда тотықтырғыш ретінде қолданатын зат
*+ K2Сr2O7
#247
*! Калий дихроматы қай ортада тотықтырғыш қасиетін көрсетеді
* + қышқылды
#248
*!Төменгі схема бойынша 2МеNO3 →600 M2O + 2NO2 + ½O2 қай элементтің нитраты ыдырайды
*+Li
#249
*!Натрий ионын ашуға қолданатын калий дигидроантимонатынқосқанда қандай зат пайда болады
*+NaH2SbO4
#250
*! Калий ионын ашуға қолданатын натрийдің гексанитрокобальтатын (III) қосқанда қандай зат пайда болады
*+K2Na[Co(NO2)6]
#251
*!Калий ионын ашуға қолданатын натрийдің гексанитрокобальтаты (III) қандай түсті тұңба береді
*+сары
#252
*!Калий иондары жалынды қай түске бояйды
-
+күлгін
#253
*!Натрий иондары жалынды қай түске бояйды
-
+сары
#254
*!Асқазан қышқылы жоғарлағанда натрийдің қай тұзын қолданады *+NaHCO3
#255
*!Қорғасын, барий тұздарымен уланғанда беретін және іш айдағыш глаубер тұзының формуласы
#256 *!Жүрек жұмысы бұзылғанда калийдің қай тұзын қолданады *+KCl
#257
*!Калий хроматы барий- ионымен сары түсті кристалдық тұңба, ал аммоний сульфаты –ақ түсті түңба береді . Осы тұңбалардың формулалары
*+BaCrO4, BaSO4
#258
*!Комплексті қосылыстың Na2[Cu(OH)4] түсі қандай
*+ көк
#259
*! Амфотерлық қасиеті бар негіз
*+ Be(OH)2
#260
*!Берилий гидроксиді ериді
*+NaOH
#261
*!Ca(OH)2ериді *+HCl
#262
*!Кальций карбонаты ериді
-
+HCl
#263
*!Кальций ионы жалын түсін қай түске бояйды
*+ қызыл
#264
*!Аммоний оксалатын кальций- иондарына қосқанда қандай тұңба түзіледі
-
+CaC2O4
#265
*!Тіс ұнтағын дайындағанда кальцийдің қай тұзын қолданады * +CaCO3
#266
*!Стенокардия ауруында тамырды кеңіту үшін натрийдің қай тұзын қолданады
*+ NaNO3
#267 *!Суда аз еритін және ортакүшті негіз қай элементтің гидроксиді *+ Mg
#268
*!Іш айдатқыш тұзы ( ашты немесе ағылшын тұзы)
*+ MgSO4 •7H2O
#269
*!Сүйекте кальций иондарының сіңіруіне және шығуына әсер ететін дәрумен
*+Д
#270
*!Қай металдың оксиді асқазан қышқылдығын төмендетеді,қышықлдармен уланғанда ем ретінде пайдаланады , тіс ұнтағының құрамына кіреді
*+MgO
-
ДЕҢГЕЙДІ ТЕСТЕР *БУФЕРЛІК ЖҰЙЕЛЕР *2*36*2*
#271
*!Күшті бір негізді қышқылдың сутек иондарының концентрациясын есептейтін формула
*+[H+] = Cк-ты
#272
*!Бейтарап орта үшін дұрыс
*+[H+] = [OH-]
#273
*!Аз мөлшерде хлорлы сутек қышқылын гидрокарбонатты буферлік ерітіндіге қосқанда қай компоненті онымен әрекеттеседі
*+NaHCO3
#274
*!Ацетатты буферлік жұйеде сутек иондарының концентрациясын есептейтін теңдеу
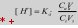
#275
*!Гидрокарбонатты буфердің құрамына кіретін қосылыстар
*+H2CO3и NaHCO3
#276
*!Фосфатты буфердің құрамына кіретін қосылыстар
*+Na2HPO4и NaH2PO4
#277
*!Аммиакты буфердің құрамына кіретін қосылыстар
*+NH4Cl и NH4OH
#278
*!Қай ерітіндіде мына қатынас сақталады [H+] < [OH-]
*+NaOH
#279
*!Қай ерітіндіде мына қатынас сақталады [H+] > [OH-]
*+HCl
#280
*!25°С таза суда сутек иондарының концентрация [H+] тең (моль/л) *+10-7
#281
*! Сон– концентрациясы нешеге тең , егер Сн+ = 10-4моль/л болса
*+10-10
#282
*!Сулы ерітінділерде сутектік көрсеткіш рН-ты анықтауға болады
* + –lg Cн+
#283
*!Сүйық ерітінділерде рН пен рОН- тың қосындысы тең *+14
#284
*! Бейтарап сулы ерітінділерге қандай талап қойылады *+[Н+] = 10-7
#285
*!Реакция орталығы қышқыл жаққа ығысуы аталады
*+ацидоз
#286
*! Реакция орталығы сілтілік жаққа ығысуы аталады
*+алколоз
#287
*!Сулы ерітіндіде рОН-ы тең 11, ал сутек иондарының концентрациясы тең болады (моль/л)
*+10-3
#288
*!Қышқылды буфердің компоненттері ол
*+әлсіз қышқыл және әлсіз қышқылдың күшті негізбен тұзы
#289
*!Негіздік буферге жатады *+NH4ОH, NH4Cl
#290
*!Ерітіндінің рОН-ы тең 13, реакция орталығы қандай
*+қышқылды
#291
*!Натрий гидроксидінің концентрациясы СNаОН = 0,001 моль/л , сонда рН-ы тең
*+11
#292
*! HClерітіндісінің концентрациясы 0,1 моль/л, сонда рН-ы тең *+ pH = 1
#293
*!Қышқылды ерітінділерде сутектік көрсеткіші тең * +рН< 7
#294
*!Қай сулы ерітіндіде мынадай талап бар [H+] > [OH-
]
*+ CH3COOH
#295
*!Сірке қышқылының ерітіндісінде сутек иондарының концентрациясының есептеуге болады формуламен
 *+[H+] = К к− ты Ск− ты
*+[H+] = К к− ты Ск− ты #296
*!Аммоний гидроксидінің ерітіндісінде сутек иондарының концентрациясының есептеуге болады формуламен
10−14
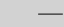
*+[H+] = [OH − ]
#297
*!Концентрациясы 0,01 моль/л калий гидроксидінің ерітіндісінде қай теңдеу дұрыс *+[H+] [OH-]
#298
*!Концентрациясы 0,001 моль/л калий гидроксидінің ерітіндісінде қай теңдеу дұрыс *+рОН = 3
#299
*!Концентрациясы 0,1 моль/л және иондану дәрежесі =0,001 әлсіз бір қышқылды негіздің иондану константасы тең
*+10-7
#300
*!Иондану константасы Kb тең 10-7 және концентрациясы 0,1 моль/л әлсіз бір қышқылды негіздің иондану дәрежесі тең
*+0,001
#301
*! Кв = Сн+. Сон- қалай аталады *+судың иондық көбейтіндісі
#302
*! 25 оС таза судың иондық қөбейтіндісі Кв тең
*+1014
#303
*!Буферлік ерітіндіге аз мөлшерде күшті қышқыл немесе аз мөлшерде күшті негіз қосқанда қай зат өзінің шамасын өзгертпейді
*+рН-ы
#304
*!Ағзада реакция орталығының рН –ының тұрақтылығы немен анықталады
*+буферлік жүйемен
#305
*!100мл қан плазмасында химиялық байланысқан СО2 көлемімен анықталатын шама аталады
*+қанның сілтілік резерві,
#306
*!Ерітіндіде Сн+ = Сон- = 10-7 ,бұл ерітінді қалай аталады
*+бейтарап
*ТЕМІР, КОБАЛЬТ , НИКЕЛЬ ТОПШАСЫ*2*35*2*
#307
*!Темір атомының электрондық конфигурациясы
*+…3d64s2
#308
*!Кобальт атомының электрондық конфигурациясы
*+…3d74s2
#309
*!Никель атомының электрондық конфигурациясы
*+ …3d84s2
#310
*!Магнитті теміртас минералының формуласы
*+ Fe3O4
#311
*! Сидерит минералының формуласы
*+ FeCO3
#312
*!Лимонит минералының формуласы *+ Fe2O3 ·nH2O
#313
*!Темір пассивтенеді *+ H2SO4 конц
#314
*!Үй температурасында темір әрекеттеседі
*+H2SO4 разб
#315
*!Темір суйық H2SO4 ерігенде түзіледі *+FeSO4
#316
*!Темір концентрлі H2SO4 ерігенде түзіледі
*+Fe2(SO4)3
#317
*!Қыздырғанда темір концентрлі HNO3 ерігенде түзіледі
*+ Fe(NO3)3
#318
*!Темір суйық HNO3 ерігенде түзіледі
*+Fe(NO3)3
#319
*!Темір (II) иондарын қанда ашуға қолданатын реагент
*+ K3[Fe(CN)6]
#320
*!Темір (III ) иондарын қанда ашуға қолданатын реагент
*+ K4[Fe(CN)6]
#321
*! “Берлин көгі”-нің формуласы
*+Fe4[Fe(CN)6]3
#322
*!“Турнбуль көгі ”-нің формуласы
*+Fe3[Fe(CN)6]2
#323
*!Сары қан тұзы Fe(III) иондарымен әрекеттескеде тұңбаның түсі
*+ көк
#324
*!Темір (II) қосылысының қайсысы ауаға тұрақты
*+(NH4)2SO4 •FeSO4 •6 H2O
#325
*!Темірдің координациялық саны *+6
#326
*!Пиритті қыздырғанда түзіледі
*+Fe2O3
#327
*!Темір (III) хлориді ерітіндісінен H2S жібергенде түзіледі
*+Fe2S3
#328
*!Темір (III) гидроксиді ериді
*+NaOH конц
#329
*!FeCl3 тұзының гидролизін үлғайту үшін қосады *+NH4Cl
#330
*!Темір карбонилі
*+Fe(CO)5
#331
*!Ең күшті гидролизденетін тұз
*+NaFeO2
#332
*!Fe2O3 калий карбонатымен балқытқанда түзіледі
*+KFeO2
#333
*!Fe2O3бертолет тұзымен сілтілік ортада балқытқанда түзіледі
*+K2FeO4
#334
*!Калий ферраты қышқылымен әрекеттескенде түзіледі
*+H2FeO4
#335
*!Темір роданидінің түсі *+ кан-қызыл түсті
#336
*!Дезинфициялау және қан тоқтатқыш темір тұзы
*+FeCl3 • 6H2O
#337
*!ВитаминаВ12қай элементтіңкомплексі
*+Co
#338
*!Кобальт (II)гидроксиді неде ерімейді
*+NaOH(cүйық)
#339
*!Ең тұрақты комплексті ион
*+[Co(CN)6]3- Kн=1*10-64
#340
*!Никель (II) гидроксиді ерімейді
*+NaOHсүйық
#341
*!Ерітіндіде Fe(III)иондарын төменгі реактивпен ашуға болады
*+KCNS