Файл: Тема 5 Коррозия металлов и сплавов Коррозия процесс разрушения металла под воздействием внешней среды.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 50
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Тема 5 Коррозия металлов и сплавов
Коррозия – процесс разрушения металла под воздействием внешней среды.
27.Виды коррозионных разрушений.
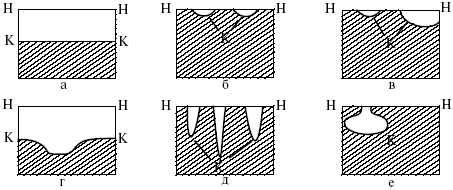 Рис. 11. Схематическое изображение различных видов коррозии: а – равномерная коррозия;
Рис. 11. Схематическое изображение различных видов коррозии: а – равномерная коррозия; б – коррозия пятнами; в, г – коррозия язвами; д – точечная коррозия (питтинг);
е – подповерхностная коррозия; НН – исходная поверхность металла; КК – рельеф поверхности, измененный вследствие коррозии.
28.Виды коррозии по механизму взаимодействия с окружающей среды.
Химическая коррозия металлов бывает газовой и жидкостной.
Газовая коррозия металлов – это результат действия агрессивных газовых или паровых сред на металл при высоких температурах, при отсутствии конденсации влаги на поверхности металла. Это, например, кислород, диоксид серы, сероводород, пары воды, галогены. Такая коррозия в одних случаях может привести к полному разрушению металла (если металл активный), а в других случаях на его поверхности может образоваться защитная пленка (например, алюминий, хром, цирконий).
Жидкостная коррозия металлов– может протекать в таких неэлектролитах, как нефть, смазочные масла, керосин и др. Этот тип коррозии при наличии даже небольшого количества влаги, может легко приобрести электрохимический характер.
При химической коррозии скорость разрушения металла пропорциональна скорости химической реакции и той скорости с которой окислитель проникает сквозь пленку оксида металла, покрывающую его поверхность. Оксидные пленки металлов могут проявлять или не проявлять защитные свойства, что определяется сплошностью.
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
-
Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде. -
Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e— = Fe2+
K: O2 + 4H+ + 4e— = 2H2O
Катодом является та поверхность, где больше приток кислорода.
29.Химическая коррозия. Условия её возникновения.
Химическая коррозия - это вид коррозионного разрушения металла, связанный с взаимодействием металла и коррозионной среды, при котором одновременно окисляется металл и происходит восстановление коррозионной среды. Химическая коррозия не связана с образованием, а также воздействием электрического тока.
соприкосновение разных видов металлов, сплавов;
- частые перепады температуры;
- трение между металлическими поверхностями;
- длительное воздействие влаги;
- влияние кислот, щелочей, химических элементов;
- использование некачественных жидкостей при механической обработке материала;
- жировые пятна, остающиеся на металлических поверхностях после прикосновения к ним.
30.Виды коррозионных разрушений.
На 27 вопрос – ответ
31.Способы защиты металлов и сплавов от коррозии.
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
Покрытие краской, лаками, смазками.
Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Тема 6 Реакционная способность веществ
32.Открытия, подтверждающие сложность строения атома. Модели атома. Квантово-механическая модель атома
Сложность строения атома доказана фундаментальными открытиями, сделанными в конце XIX и начале XX в. в результате изучения природы катодных лучей (Дж. Томсон, 1897 г.), открытия явления фотоэффекта (А. Г. Столетов, 1889 г.), открытия радиоактивности химических элементов (А. Беккерель, М. Склодовская-Кюри, 1896—1899 гг.), определения природы α-частиц (эксперименты Э. Резерфорда, 1889—1900 гг.). Ученые пришли к заключению о том, что атомы обладают собственной структурой, имеют сложное строение.
В квантово-механическая модель атома предполагает, что оно образовано центральным ядром, состоящим из протонов и нейтронов. Отрицательно заряженные электроны окружают ядро в диффузных областях, известных как орбитали.
Форма и размер электронных орбиталей определяется различными величинами: потенциалом ядра и квантованными уровнями энергии и углового момента электронов.
33.Теория четырёх квантовых чисел. Их физический смысл.
У электрона в атоме четыре квантовых числа.
1. Главное квантовое число (обозначается n) означает номер орбиты. Орбиты с бОльшим номером имеют бОльший радиус. (n = 1, 2, 3, ..)
2. Орбитальное квантовое число (обозначается L) характеризует вращение электрона - его орбитальный момент. Т. е. ту часть момента импульса электрона, которая обусловлена с его вращением во круг ядра. Орбитали с разным L имею разную форму. (L = 0, 1, 2, ..n-1)
3. Магнитное квантовое число (обозначется m) обозначает проекцию орбитального момента импульса на некоторую ось (т. е. зависит от выбора этой оси), характеризует ориентацию орбитали в пространстве.
m = -L, -(L-1), ..(L-1), L
4. Спиновое квантовое число s обозначает проекцию спинового момента на некоторую выбранную ось. Спиновый момент не связан с вращением электрона. (Это момент импульса электрона в системе отсчета, в которой электрон покоится, так называемый собственный момент.) (s=-1/2, 1/2)
34.Порядок заполнения уровней, подуровней. Правило Гунда, Паули. Валентность.
Правила заполнения электронных орбиталей. Электроны занимают уровни последовательно, в порядке увеличения их энергии (принцип наименьшей энергии). Число энергетических уровней в атоме равно номеру периода, в котором находится элемент. В этом заключается физический смысл номера периода в таблице Д.И. Менделеева.
Общий принцип распределения электронов такой, что энергетические подуровни заполняются в порядке суммы главного и орбитального квантовых чисел, то есть: 1S, 2S, 2P, 3S, 3P, 4S, 3D и так далее, если сумма одинакова, то сначала заполняется уровень с меньшим главным квантовым числом N.
Правило Хунда: в основном (невозбужденном) состоянии атома на подуровнях np, nd и nf всегда имеется максимальное количество неспаренных электронов (максимальный неспаренный спин).
Подуровни p, d и f состоят из нескольких орбиталей, энергия которых одинакова, поэтому эти подуровни называются “вырожденными”: p подуровень вырожден трехкратно, d пятикратно и f семикратно. Для электронов этих подуровней соблюдается правило Хунда.
Валентность – способность образовывать химические связи.
Принцип Паули (запрет): у атомов, имеющих больше одного электрна не может быть двух электронов с одинаковыми значениями всех четырех квантовых чисел. Или так: на одной орбитали могут находится только два электрона, причем с противоположенными спинами.
35.Периодический закон и периодическая система элементов Д.И. Менделеева в свете строения атома.
Периодический закон Менделеева, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов и величин их атомных весов.
Заряд ядра атома каждого хим-го элемента в табл. Менделеева возрастает на единицу по сравнению с зарядом ядра атома предыдущего хим-го элемента. Заряд атомного ядра совпадает с порядковым номером элементов в таблице Менделеева.
36.Ядро атома. Электрон. Параметры атома (радиус, заряд, электроотрицательность).
В центре атома находится положительно заряженное ядро. Весь положительный заряд и почти вся масса атома сосредоточена в его ядре. Ядра атомов состоят из нейтронов и протонов(нуклонов). Вокруг ядра по замкнутым орбитам вращаются электроны. Общее число электронов и распределение электронов. Общее число электронов определить несложно: оно равно порядковому номеру, т. е. заряду ядра атома. Электроны имеют отрицательный заряд.
Заряд ядра увеличивается, радиус атома уменьшается, притяжение электронов увеличивается, возрастает электроотрицательность, увеличивается кол-во электронов во внешнем уровне.
Электроотрицательность — это способность атома в соединениях притягивать к себе валентные электроны, то есть электроны, посредством которых образуются химические связи между атомами. Это свойство обусловлено тем, что атомы стремятся завершить внешний электронный слой и получить энергетически выгодное конфигурацию инертного газа — 8 электронов.
Электроотрицательность зависит от способности атомного ядра притягивать электроны внешнего энергетического уровня. Чем сильнее это притяжение, тем электроотрицательность больше.
37.Химическая связь. Основные типы и характеристики связи. Ковалентная и ионная связь.
Химическая связь - это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому.
Ковалентная связь — это образование общей электронной пары у двух атомов вещества при сближении ядер этих атомов.
Ковалентная полярная связь – это ковалентная связь, которая возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией).
Чем больше различие в электроотрицательностях атомов, тем выше полярность связи и тем больше дипольный момент. HCl, CO2
Ковалентная неполярная (симметричная) связь – это ковалентная связь, образованная атомами с равной элетроотрицательностью (как правило, одинаковыми неметаллами) и, следовательно, с равномерным распределением электронной плотности между ядрами атомов. H2 (H-H), O2 (O=O)
Ионная связь– это связь между атомами резко отличающимися по электроотрицательности: у одного она очень высокая, у другого – низкая. В этом случае, атом с меньшей электроотрицательностью полностью отдает свои валентные электроны атому с большей электроотрицательностью. Ионная связь образуется между металлами и неметаллами. Такой тип связи в NaCl, CsBr, NH 4 Cl
38.Агрегатное состояние вещества. Металлическая связь. Химическая связь в полупроводниках и диэлектриках. Зонная теория.
Тема 7. Химическая идентификация и анализ вещества.
39.Идентификация катионов и анионов. Количественный анализ, гравиметрический
Количественный анализ.
Определение содержания (концентрации, масс и т.п.) компонентов в анализируемом веществе называется количественным анализом. С помощью количественного анализа выявляют массовые соотношения компонентов в анализируемом образце, концентрация вещества в растворе или в газе. При количественном анализе измеряют те или иные химические, физико-химические и физические параметры анализируемого образца, которые зависят от его состава или содержания того или иного компонента. В большинстве методов полученные при анализе результаты сравнивают со свойствами известных веществ. Результаты анализа обычно выражают в массовых долях, в %.
Количественный анализ проводят в определенной последовательности, в которую входит отбор и подготовка проб, проведения анализа, обработка и расчет результатов анализа. Как и в качественном анализе различают макрометоды, полумикрометоды, микро- и ультрамикрометоды.
Количественный анализ широко используется для изучения состава руд, металлов, неорганических и органических соединений. В последние годы особое внимание обращается на определение содержания токсичных веществ в воздухе, водоемах, почвах, в продуктах питания, различных товарах.
Гравиметрический метод. Сущность метода заключается в получении труднорастворимого соединения, в которое входит определяемый компонент. Для этого навеску вещества растворяют в том или ином растворителе, обычно в воде,