Файл: Практическая работа6 Получение водорода и изучение его свойств.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 32
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Практическая работа№6
«Получение водорода и изучение его свойств».
Цель работы: научиться использовать лабораторное оборудование и посуду для получения, собирания и доказательства наличия водорода, исследовать свойства водорода.
1. Способ получения водорода – взаимодействие активных металлов с кислотами.
Zn + 2HCl = ZnCl2 + Н2↑ + Q - при обычных условиях
Наблюдения:
-
реакция взаимодействия гранул цинка с соляной кислотой идет сначала медленно, затем очень бурно, пробирка разогревается -
из газоотводной трубки выделяется бесцветный газ -
при упаривании полученного раствора на стеклянной пластинке остается белый порошок
2. Приборы для получения и собирания водорода
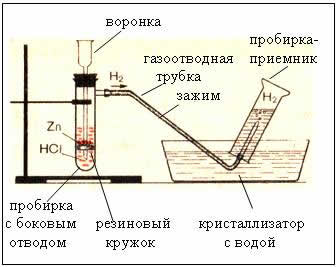
Рис1. Прибор для получения водорода – автоматический, который позволяет в любой момент остановить реакцию с помощью зажима (прибор Кирюшкина).
Собирание газа методом вытеснения воды – возможно, т.к. водород малорастворим в ней.
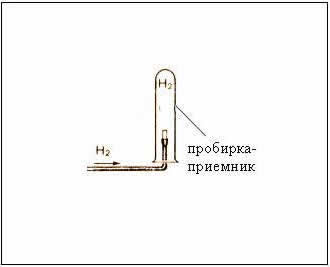
Рис2. Собирание газа методом вытеснения воздуха – держа пробирку-приемник вверх дном, т.к.
3. Обнаружение водорода – проверка его на чистоту
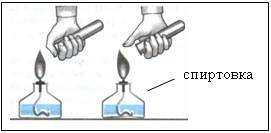
Рис. 3.
Наблюдения:
-
при сжигании первой порции газа раздается резкий лающий звук -
при сжигании второй порции газа слышен легкий хлопок
4. Свойство водорода – активный восстановитель
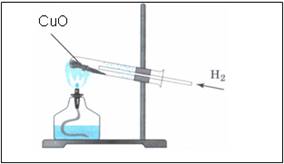
Рис.4.
Наблюдения:
-
порошок меняет цвет с черного на медный -
на стенках пробирки появляются бесцветные капельки жидкости
Вывод:
Одним из способов получения водорода в лаборатории является взаимодействие цинка с разб. соляной кислотой, при этом образуется соль (хлорид цинка) и водород. Водород – бесцветный газ, без запаха, малорастворим в воде, легче воздуха, в смеси с воздухом взрывоопасен, восстанавливает металлы из их оксидов.
Оформите результаты практической работы в виде таблицы.
| № п/п, название опыты | Что делаю? | Уравнения реакции, выводы. |
| 1. Способ получения водорода | Собираю прибор (рис. 1) и т. д. | |
| 2. Приборы для получения и собирания водорода | | |
| 3. Обнаружение водорода – проверка его на чистоту | | |
| 4. Свойство водорода – активный восстановитель | | |