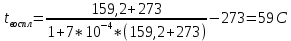Файл: Теоретические основы процессов горения и тушения курсовая работа исследование пожаровзрывоопасности горючих жидкостей на примере пропилбензола.docx
Добавлен: 06.12.2023
Просмотров: 414
Скачиваний: 35
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
3. ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИК ГОРЕНИЯ
3.2 Теоретический и практический расход воздуха на горение
3.3. Объем и состав продуктов полного сгорания
3.5 Стехиометрическая концентрация в паровоздушной смеси
3.6 Расчет температуры горения
4. ОПРЕДЕЛЕНИЕ ПОКАЗАТЕЛЕЙ ПОЖАРНОЙ ОПАСНОСТИ
4.3 Температура самовоспламенения
4.4 Концентрационные пределы распространения пламени
4.5 Температурные пределы распространения пламени
4.6 Нормальная скорость распространения пламени
4.7 Критический диаметр огнегасящего канала и безопасного экспериментального максимального зазора
4.8 Минимальная энергия зажигания
4.11 Минимальное взрывоопасное содержание кислорода
4.12 Максимальное давление взрыва
Определим температуру вспышки пропилбензола:
1.Запишем структурную формулу (

2.Определим виды и количество связей:
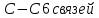
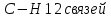
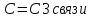 3.Определим температуру вспышки:
3.Определим температуру вспышки: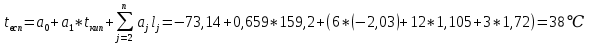 ;
;4.1.2 Расчёт температуры вспышки для некоторых классов соединений
Для перечисленных в таблице 6 классов веществ температуру вспышки:
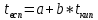
а, b — эмпирические коэффициенты.
Таблица 6 – Эмпирические коэффициенты для расчета температуры вспышки
| Класс веществ | Коэффициенты | ||
| а, С | b | , С | |
| Алканы | 73,22 | 0,693 | 1,5 |
| Спирты | 41,69 | 0,652 | 1,4 |
| Алкиланилины | 21,94 | 0,533 | 2,0 |
| Карбоновые кислоты | 43,57 | 0,708 | 2,2 |
| Алкилфенолы | 38,42 | 0,623 | 1,4 |
| Ароматические углеводороды | 67,83 | 0,665 | 3,0 |
| Альдегиды | 74,76 | 0,813 | 1,5 |
| Бромалканы | 49,56 | 0,665 | 2,2 |
| Кетоны | 52,69 | 0,643 | 1,9 |
| Хлоралканы | 55,70 | 0,631 | 1,7 |
Рассчитаем температуру вспышки пропилбензола.
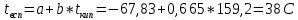
4.1.3 Расчёт температуры вспышки по формуле Блинова
Одним из наиболее распространенных из них является полуэмпирический метод, предложенный В.И. Блиновым:
tвс=
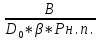
tвс – температура вспышки (воспламенения), К;
Рн.п. – парциальное давление насыщенного пара жидкости при температуре вспышки (воспламенения), Па;
Dо – коэффициент диффузии паров жидкости, с/м2,
β – количество молекул кислорода, необходимое для полного окисления одной молекулы горючего:
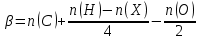
n(C), n(H), n(X), n(O) – число атомов углерода, водорода, галойдов и кислорода в молекуле горючего;
В – константа метода определения.
При расчете температуры вспышки в замкнутом сосуде рекомендуется принимать В = 28, в открытом сосуде В = 45, а для расчета температуры воспламенения принимают В = 53.
Таблица 7 - Зависимость давления от температуры для некоторых веществ
| Вещество | Давление, Па | |||||||||
| 1333,3 | 1333,2 | 2666,4 | 5332,9 | 7999,3 | 1333,2 | 2666,4 | 5332,9 | 1013,25 | ||
| Температура, К | ||||||||||
| 1 | Альдегид уксусный | 191,5 | 216,2 | 225,2 | 235,2 | 241,6 | 250,4 | 263,0 | 277,9 | 293,2 |
| 2 | Ангидрид уксусный | 274,7 | 309,0 | 325,0 | 335,1 | 343,8 | 355,2 | 373,0 | 392,8 | 412,6 |
| 3 | Акриловая кислота | 312,0 | 325,0 | 339,2 | 348,0 | 359,1 | 376,3 | 395,0 | 414,0 | 276,5 |
| 4 | Аллиловый спирт | 253,0 | 283,5 | 294,7 | 305,4 | 313,3 | 323,0 | 337,5 | 353,2 | 369,5 |
| 5 | Амиловый спирт | 286,0 | 317,9 | 328,8 | 244,0 | 348,5 | 358,8 | 375,0 | 392,8 | 410,8 |
| 6 | Бензиловый спирт | 331,0 | 365,6 | 378,8 | 392,8 | 402,3 | 414,7 | 433,0 | 456,0 | 477,7 |
| 7 | Бензол | 236,3 | 261,5 | 270,4 | 286,0 | 288,4 | 299,1 | 315,2 | 333,6 | 353,1 |
| 8 | Бутиловый спирт | 271,8 | 303,2 | 314,5 | 326,4 | 333,3 | 343,1 | 357,3 | 373,8 | 390,5 |
| 9 | Бутиловый спирт (вторичный) | 260,8 | 289,9 | 300,3 | 311,1 | 318,2 | 327,1 | 340,9 | 356,9 | 372,5 |
| 10 | Бутиловый спирт (третичный) | 252,6 | 278,5 | 287,3 | 297,5 | 304,0 | 312,8 | 325,7 | 314,0 | 355,9 |
| 11 | Диэтиловый эфир | 198,7 | 224,9 | 234,5 | 245,2 | 251,2 | 261,5 | 275,2 | 290,9 | 307,0 |
| 12 | Изобутиловый спирт | 264,0 | 294,7 | 307,3 | 317,1 | 324,7 | 334,5 | 348,9 | 364,4 | 381,0 |
| 13 | Бромистый этил | 198,7 | 225,5 | 235,2 | 246,3 | 253,5 | 263,0 | 287,5 | 294,0 | 311,4 |
| 14 | Бутилбензол | 295,7 | 335,0 | 349,3 | 365,4 | 275,6 | 389,2 | 409,4 | 432,2 | 456,1 |
| 15 | Бутилформиат | 246,6 | 279,1 | 291,0 | 304,6 | 312,8 | 324,0 | 340,9 | 359,2 | 379,0 |
| 16 | Метилэтилкетон | 224,2 | 255,3 | 266,5 | 279,0 | 287,0 | 298,0 | 314,6 | 333,0 | 352,6 |
| 17 | Метилциклогексан | 237,1 | 269,8 | 281,7 | 295,0 | 303,5 | 315,1 | 332,6 | 352,6 | 373,9 |
| 18 | 3-метил-2-бутинол | 253,1 | 281,3 | 291,3 | 302,6 | 309,2 | 318,5 | 332,0 | 348,6 | 361,9 |
| 19 | Метиловый спирт | 229,0 | 256,8 | 267,0 | 278,0 | 285,1 | 294,2 | 307,8 | 322,9 | 337,7 |
| 20 | Пропилбензол | 259,0 | 281,3 | 304,5 | 318,1 | 326,8 | 338,7 | 356,6 | 377,0 | 398,6 |
| 21 | Пропилбензол | 279,3 | 316,4 | 329,8 | 344,6 | 354,1 | - | 386,5 | 408,7 | 432,2 |
| 22 | Пропиловый спирт (вторичный) | 299,1 | 275,4 | 285,7 | 296,8 | 303,5 | 312 | 326,0 | 340,8 | 355,5 |
| 23 | Стирол | 266,0 | 303,8 | 317,6 | 332,8 | 424,5 | 355,0 | 374,3 | 395,5 | 418,2 |
| 24 | Сероуглерод | 199,2 | 228,3 | 238,7 | 250,5 | 257,7 | 267,9 | 283,4 | 301,0 | 319,5 |
| 25 | Толуол | 246,3 | 279,4 | 291,4 | 304,8 | 313,3 | 324,9 | 342,5 | 262,5 | 383,6 |
| 26 | Уксуснометиловый эфир | 215,8 | 243,7 | 253,9 | 265,1 | 272,5 | 282,4 | 279,0 | 313,0 | 330,8 |
| 27 | Уксуснопропиловый эфир | 246,3 | 278,4 | 289,0 | 301,8 | 310,0 | 320,8 | 337,0 | - | 374,8 |
| 28 | Уксусноэтиловый эфир | 229,6 | 257,12 | 270,0 | 282,1 | 289,6 | 300,0 | 315,0 | 332,3 | 350,1 |
| 29 | Этиловый спирт | 241,7 | 270,7 | 281,0 | 292,0 | 299,0 | 307,9 | 321,4 | 336,5 | 351,4 |
| 30 | Этилциклопентан | 240,8 | 272,9 | 284,7 | 298,0 | 306,4 | 318,0 | 335,4 | 355,3 | 318,4 |
| 31 | Этиленбензол | 263,2 | 298,2 | 311,6 | 325,8 | 334,8 | 347,1 | 365,7 | 386,8 | 409,2 |
Рассчитаем температуру вспышки пропилбензола, находящегося навоздухевоткрытомтигле.
Исходные данные:
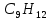 – пропилбензол;
– пропилбензол;В = 45 (константа метода определения для определения температуры вспышки в открытом тигле);
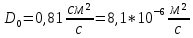
1.Запишем уравнение реакции горения пропилбензола:
C9H12 +12(О₂ + 3,76 N₂) = 9СО₂ +6Н₂О + 12· 3,76 N₂
β=12
2.Подставляем имеющиеся значения в формулу
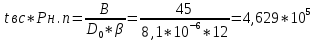
3.Предположим, что tвсп1 = 259,0 К, тогда Pн.п.1 = 1333,3 Па, тогда соотношение:
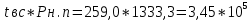
– полученное значение меньше расчетного.
Выбираем следующее значение tвсп2 = 281,3 К, тогда Pн.п.2 = 1333,2 Па.
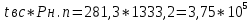
-полученное значение также меньше расчетного.
Выбираем следующее значение tвсп3 = 304,5 К, тогда Pн.п.3 = 2666,4 Па.
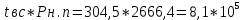
– полученное значение больше расчетного.
4.Температура вспышки бутилового спирта находится между 281,3 и 304,5К.
5.Рассчитаем температуру вспышки пропилбензола:
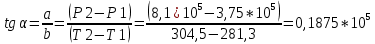
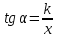
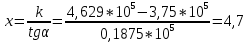
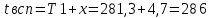 K
K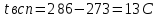
4.2 Температура воспламенения
Температура воспламенения – наименьшая температура вещества, при которой в условиях специальных испытаний вещество выделяет горючие пары и газы с такой скоростью, что при воздействии на них источника зажигания наблюдается воспламенение.
Температура воспламенения обычно на 1–30 ºС выше температуры вспышки.
4.2.1 Расчёт температуры воспламенения жидкости
Температура воспламенения рассчитывается по той же формуле, что и температура вспышки, но со своими коэффициентами
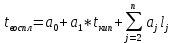
 – размерный коэффициент, равный -47,78
– размерный коэффициент, равный -47,78 ;
; - безразмерный коэффициент, равный 0,882;
- безразмерный коэффициент, равный 0,882; – температура кипения исследуемой жидкости,
– температура кипения исследуемой жидкости,  ;
; – эмпирические коэффициенты;
– эмпирические коэффициенты; – количество химических связей всегда j в молекуле исследуемой жидкости.
– количество химических связей всегда j в молекуле исследуемой жидкости.Таблица 8. Коэффициенты
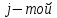 химической связи.
химической связи.| Вид связи |  |
 | 0,027 |
 Химические связи между атомами C внутри бензольного кольца | -2,069 |
 | -0,826 |
 | -8,980 |
 | -2,118 |
 | -0,111 |
 | -5,876 |
 | -0,261 |
 | 8,216 |
Определим температуру воспламенения пропилбензола:
1.Запишем структурную формулу (

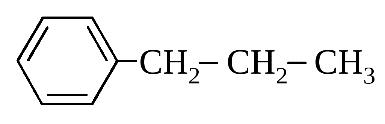
2.Определим виды и количество связей:

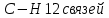
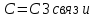
3.Определим температуру воспламенения:
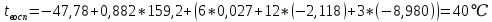
4.2.2 Расчёт температуры воспламенения алифатических спиртов и сложных эфиров
Температуру воспламенения алифатических спиртов и сложных эфиров вычисляют по формуле
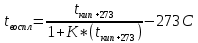
К эмпирический коэффициент, равный 6·10-4 для спиртов и 7·10-4 для сложных эфиров.
Рассчитаемтемпературупропилбензола.tкип=159,2С