ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.12.2023
Просмотров: 76
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, визуализировать взаимоотношение фронта опухолевой инвазии с мезоректальной клетчаткой и собственной фасцией прямой кишки, определить степень распространенности процесса относительно фасциальномышечных структур тазового дна. Кроме того, при этом исследовании возможно определение степени поражения лимфатических узлов. Для этого используют вещества с парамагнетической активностью. Непосредственно над зубчатой линией в подслизистый слой, после предварительного введения лидазы вводят Gd (гадолиний) – содержащий препарат «Omniscan» (Nycomed). Данная методика позволяет с высокой точностью (до 70 %) оценить состояние лимфатических узлов таза.
Т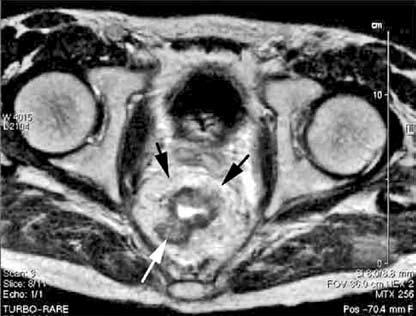 аким образом, пальцевое исследование прямой кишки, реьсгороманоскопия, ирригоскопия и колоноскопия являются основными методами первичной диагностики рака прямой кишки, а УЗИ, КТ и МРТ в комплексе с вышеперечисленными методами играют незаменимую роль в уточнении распространенности опухолевого процесса, что позволяет выбрать для каждого конкретного больного оптимальный метод лечения.
аким образом, пальцевое исследование прямой кишки, реьсгороманоскопия, ирригоскопия и колоноскопия являются основными методами первичной диагностики рака прямой кишки, а УЗИ, КТ и МРТ в комплексе с вышеперечисленными методами играют незаменимую роль в уточнении распространенности опухолевого процесса, что позволяет выбрать для каждого конкретного больного оптимальный метод лечения.
Рис. 4. Магнитнорезонансная томография (аксиальная проекция). Рак среднеампулярного отдела прямой кишки. На снимке видна инвазия опухоли в мезоректум на значительном протяжении –13 мм (белая стрелка), черными стрелками отмечена собственная фасция прямой кишки
Р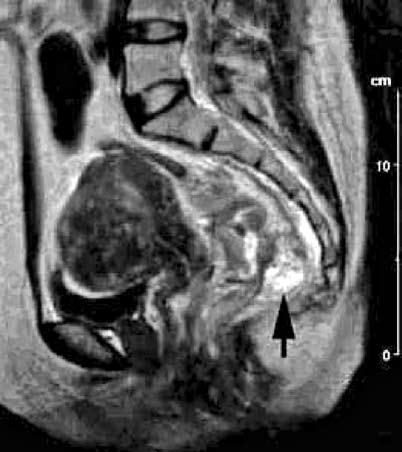 ис. 5. Магнитнорезонансная томография (сагиттальная проекция).
ис. 5. Магнитнорезонансная томография (сагиттальная проекция).
Рак нижнеампулярного отдела прямой кишки. Непрямая магнитнорезонансная лимфография. На снимке виден увеличенный, метастатически пораженный лимфоузел в мезоректуме (черная стрелка). Неравномерное распределение парамагнетика в лимфоузле.
Лечение рака прямой кишки
Основным методом лечения рака прямой кишки является хирургический.
В ряде случаев применяют комбинированное лечение – хирургическое и лучевое. Химиотерапии при раке прямой кишки отводится вспомогательная роль, поскольку эти опухоли относительно резистентны к воздействию цитостатиков (эффективность химиотерапии остается в пределах 20–30 %).
Радикальное лечение В 1826 г. J. Lisfranc впервые удалил опухоль нижних отделов прямой кишки из промежностного доступа. В 1882 г. М. Konig, начав операцию из промежностного доступа, вынужденно выполнил лапаротомию, удалил прямую кишку с опухолью из комбинированного доступа и закончил операцию формированием сигмостомы. В дальнейшем, в 1896 г. R. Quenu и в 1908 г. W.E. Miles, развили и усовершенствовали методики брюшнопромежностной экстирпации прямой кишки (их имена носит эта операция). Н. Hartman в 1920 г. выполнил резекцию сигмовидной кишки с опухолью, с последующим формированием одноствольной колостомы на передней брюшной стенке и ушиванием наглухо дистального участка с погружением его под тазовую брюшину (операция Гартмана). В 1939 г. W. W. Babcock предложил низведение мобилизованной толстой кишки через сфинктер заднего прохода (первый вариант брюшноанальной резекции).
Из радикальных операций в настоящее время чаще всего применяют:
• переднюю резекцию прямой кишки;
• брюшноанальную резекцию с низведением сигмовидной кишки;
• операцию Гартмана;
• брюшнопромежностную экстирпацию прямой кишки.
Подготовка кишки к операции Очень большое значение имеет подготовка толстой кишки к операции. С первого дня поступления из питания исключаются продукты, содержащие клетчатку (овощи, фрукты, как в сыром, так и в вареном виде). Назначается внутрь 25 % раствор сернокислой магнезии по 30 мл три раза в день. За три дня до операции рекомендуется употребление жидкой пищи (бульон, молоко, сливки, сметана, кефир, простокваша, соки без мякоти). Накануне операции утром натощак пациент выпивает 100 мл 25 % раствора сернокислой магнезии, то есть всю дневную дозу препарата. В дальнейшем прием любой пищи, а также сернокислой магнезии, запрещен. В течение этого дня можно пить только воду. Накануне операции вечером делают очистительные клизмы с промежутками в 20–30 минут до полного эффекта очистки.
Наиболее универсальным методом подготовки кишки следует считать использование растворов на основе комплексных препаратов полиэтиленгликоля (ПЭГ) молекулярной массой 3000–5000 и электролитов (лаваж). Концентрация ПЭГ в 5–6 % водном растворе сохраняет качество полимера, который способен удерживать от всасывания объем воды в кишечнике, желудке, а водноэлектролитный баланс и компенсация потерь ионов с кишечным секретом полностью корригируется введением электролитов с осмотическим давлением изотонического раствора (NaCI, KCI, NaHC03, KHC03, Na2S04, Mg S04). Наличие в растворе электролитов, соответствующих осмотическому давлению физиологического раствора, восполняет кишечную секрецию калия, натрия, хлора бикарбоната, в связи с чем не происходит изменения состава жидких сред организма. Питание не ограничено до операции или исследования, дополнительных клизм не требуется. Препарат в объеме 2–4 л пациент принимает самостоятельно по 200 мл через 20 мин. С этой целью применяются различные препараты: «Golytely», «Nulytely» фирмы «Brantree Laboratories» (США), «Fortrans» фирмы «Beaufour Ipsen» (этот препарат на практике применяется чаще всего) (Франция) и др. Методом кишечного лаважа удается в 92–95 % случаях добиться полной очистки толстой кишки от калового содержимого и вымывания условнопатогенных микроорганизмов в процессе ортоградного прохождения жидкости по кишке при значительном уменьшении объема раствора, что приводит к быстрому восстановлению нормальной микрофлоры кишки.
Основными противопоказаниями к проведению кишечного лаважа являются:
• острая кишечная непроходимость;
• подозрение на перфорацию полого органа;
• кишечное или внутрибрюшное кровотечение;
• токсическая дилатация толстой кишки.
Передняя (чрезбрюшная) резекция прямой кишки. Современным стандартом в хирургии рака прямой кишки является сфинктеросохраняющая операция с полным иссечением параректальной клетчатки – мезоректумэктомия.
Чрезбрюшная резекция прямой кишки показана при расположении нижнего полюса опухоли в 7–8 см от анального кольца и проксимальнее. При этом вмешательстве от нижнего края опухоли необходимо отступить не менее чем на 5 см, а от верхнего полюса – на 12–15 см. После удаления пораженного сегмента прямой и части сигмовидной кишки формируется колоректальный анастомоз по типу конец в конец. При «высоких» передних резекциях обычно формируется двухрядный или однорядный анастомоз нитями на атравматичной игле. При «низких» передних резекциях анастомоз удобнее формировать с помощью сшивающих аппаратов. Исключительно надежны аппараты фирм «Autosuture» и «Ethicon». При использовании техники двойного прошивания (doublestapling anastomosis), заключающейся в ушивании культи прямой кишки линейным аппаратом, а затем наложения колоректального анастомоза по типу конец в конец циркулярным сшивающим аппаратом, возможно выполнить низкую переднюю резекцию даже с расположением анастомоза на 1–2 см выше зубчатой линии.
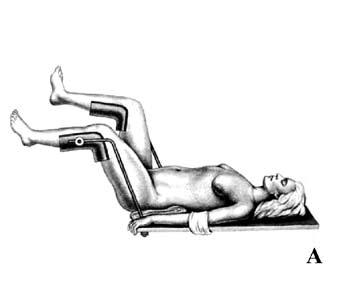
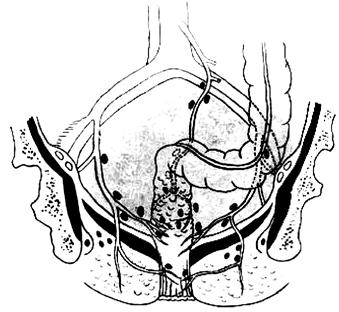
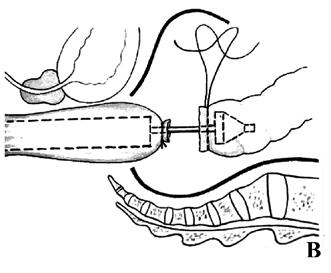

Рис. 6.
Т
 аким образом, пальцевое исследование прямой кишки, реьсгороманоскопия, ирригоскопия и колоноскопия являются основными методами первичной диагностики рака прямой кишки, а УЗИ, КТ и МРТ в комплексе с вышеперечисленными методами играют незаменимую роль в уточнении распространенности опухолевого процесса, что позволяет выбрать для каждого конкретного больного оптимальный метод лечения.
аким образом, пальцевое исследование прямой кишки, реьсгороманоскопия, ирригоскопия и колоноскопия являются основными методами первичной диагностики рака прямой кишки, а УЗИ, КТ и МРТ в комплексе с вышеперечисленными методами играют незаменимую роль в уточнении распространенности опухолевого процесса, что позволяет выбрать для каждого конкретного больного оптимальный метод лечения.Рис. 4. Магнитнорезонансная томография (аксиальная проекция). Рак среднеампулярного отдела прямой кишки. На снимке видна инвазия опухоли в мезоректум на значительном протяжении –13 мм (белая стрелка), черными стрелками отмечена собственная фасция прямой кишки
Р
 ис. 5. Магнитнорезонансная томография (сагиттальная проекция).
ис. 5. Магнитнорезонансная томография (сагиттальная проекция). Рак нижнеампулярного отдела прямой кишки. Непрямая магнитнорезонансная лимфография. На снимке виден увеличенный, метастатически пораженный лимфоузел в мезоректуме (черная стрелка). Неравномерное распределение парамагнетика в лимфоузле.
Лечение рака прямой кишки
Основным методом лечения рака прямой кишки является хирургический.
В ряде случаев применяют комбинированное лечение – хирургическое и лучевое. Химиотерапии при раке прямой кишки отводится вспомогательная роль, поскольку эти опухоли относительно резистентны к воздействию цитостатиков (эффективность химиотерапии остается в пределах 20–30 %).
Радикальное лечение В 1826 г. J. Lisfranc впервые удалил опухоль нижних отделов прямой кишки из промежностного доступа. В 1882 г. М. Konig, начав операцию из промежностного доступа, вынужденно выполнил лапаротомию, удалил прямую кишку с опухолью из комбинированного доступа и закончил операцию формированием сигмостомы. В дальнейшем, в 1896 г. R. Quenu и в 1908 г. W.E. Miles, развили и усовершенствовали методики брюшнопромежностной экстирпации прямой кишки (их имена носит эта операция). Н. Hartman в 1920 г. выполнил резекцию сигмовидной кишки с опухолью, с последующим формированием одноствольной колостомы на передней брюшной стенке и ушиванием наглухо дистального участка с погружением его под тазовую брюшину (операция Гартмана). В 1939 г. W. W. Babcock предложил низведение мобилизованной толстой кишки через сфинктер заднего прохода (первый вариант брюшноанальной резекции).
Из радикальных операций в настоящее время чаще всего применяют:
• переднюю резекцию прямой кишки;
• брюшноанальную резекцию с низведением сигмовидной кишки;
• операцию Гартмана;
• брюшнопромежностную экстирпацию прямой кишки.
Подготовка кишки к операции Очень большое значение имеет подготовка толстой кишки к операции. С первого дня поступления из питания исключаются продукты, содержащие клетчатку (овощи, фрукты, как в сыром, так и в вареном виде). Назначается внутрь 25 % раствор сернокислой магнезии по 30 мл три раза в день. За три дня до операции рекомендуется употребление жидкой пищи (бульон, молоко, сливки, сметана, кефир, простокваша, соки без мякоти). Накануне операции утром натощак пациент выпивает 100 мл 25 % раствора сернокислой магнезии, то есть всю дневную дозу препарата. В дальнейшем прием любой пищи, а также сернокислой магнезии, запрещен. В течение этого дня можно пить только воду. Накануне операции вечером делают очистительные клизмы с промежутками в 20–30 минут до полного эффекта очистки.
Наиболее универсальным методом подготовки кишки следует считать использование растворов на основе комплексных препаратов полиэтиленгликоля (ПЭГ) молекулярной массой 3000–5000 и электролитов (лаваж). Концентрация ПЭГ в 5–6 % водном растворе сохраняет качество полимера, который способен удерживать от всасывания объем воды в кишечнике, желудке, а водноэлектролитный баланс и компенсация потерь ионов с кишечным секретом полностью корригируется введением электролитов с осмотическим давлением изотонического раствора (NaCI, KCI, NaHC03, KHC03, Na2S04, Mg S04). Наличие в растворе электролитов, соответствующих осмотическому давлению физиологического раствора, восполняет кишечную секрецию калия, натрия, хлора бикарбоната, в связи с чем не происходит изменения состава жидких сред организма. Питание не ограничено до операции или исследования, дополнительных клизм не требуется. Препарат в объеме 2–4 л пациент принимает самостоятельно по 200 мл через 20 мин. С этой целью применяются различные препараты: «Golytely», «Nulytely» фирмы «Brantree Laboratories» (США), «Fortrans» фирмы «Beaufour Ipsen» (этот препарат на практике применяется чаще всего) (Франция) и др. Методом кишечного лаважа удается в 92–95 % случаях добиться полной очистки толстой кишки от калового содержимого и вымывания условнопатогенных микроорганизмов в процессе ортоградного прохождения жидкости по кишке при значительном уменьшении объема раствора, что приводит к быстрому восстановлению нормальной микрофлоры кишки.
Основными противопоказаниями к проведению кишечного лаважа являются:
• острая кишечная непроходимость;
• подозрение на перфорацию полого органа;
• кишечное или внутрибрюшное кровотечение;
• токсическая дилатация толстой кишки.
Передняя (чрезбрюшная) резекция прямой кишки. Современным стандартом в хирургии рака прямой кишки является сфинктеросохраняющая операция с полным иссечением параректальной клетчатки – мезоректумэктомия.
Чрезбрюшная резекция прямой кишки показана при расположении нижнего полюса опухоли в 7–8 см от анального кольца и проксимальнее. При этом вмешательстве от нижнего края опухоли необходимо отступить не менее чем на 5 см, а от верхнего полюса – на 12–15 см. После удаления пораженного сегмента прямой и части сигмовидной кишки формируется колоректальный анастомоз по типу конец в конец. При «высоких» передних резекциях обычно формируется двухрядный или однорядный анастомоз нитями на атравматичной игле. При «низких» передних резекциях анастомоз удобнее формировать с помощью сшивающих аппаратов. Исключительно надежны аппараты фирм «Autosuture» и «Ethicon». При использовании техники двойного прошивания (doublestapling anastomosis), заключающейся в ушивании культи прямой кишки линейным аппаратом, а затем наложения колоректального анастомоза по типу конец в конец циркулярным сшивающим аппаратом, возможно выполнить низкую переднюю резекцию даже с расположением анастомоза на 1–2 см выше зубчатой линии.




Рис. 6.
Передняя резекция прямой кишки: А – положение больного на операционном столе; Б – мобилизация прямой кишки (указаны границы резекции); В – формирование сигморектального аппаратного анастомоза; Г – аппарат фирмы «Autosuture» для формирования циркулярного анастомоза
Брюшноанальная резекция с низведением сигмовидной кишки. При расположении опухоли на расстоянии 6–7 см от края заднего прохода может быть выполнена и брюшноанальная резекция с низведением сигмовидной кишки в анальный канал и формированием колоанального анастомоза. У данной методики существует и ряд недостатков. В первую очередь, возможно развитие такого грозного раннего послеоперационного осложнения, как некроз низведенной ободочной кишки.
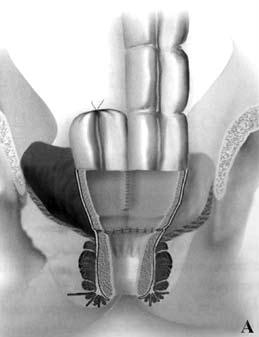
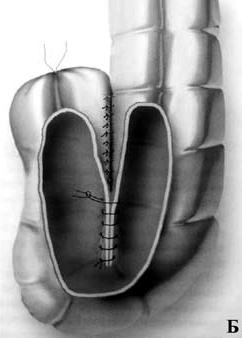
Рис. 7. Брюшноанальная резекция с формированием Jобразного резервуара: А – сформирован резервуароанальный анастомоз; Б – Jобразный толстокишечный резервуар
Кроме того, удаление прямой кишки влечет за собой потерю ее резервуарноэвакуаторной функции. Это обстоятельство приводит к ухудшению функциональных результатов операции – частые (до 6 и более раз в сутки) дефекации; многомоментное, длительное и неполное опорожнение кишечника; императивные позывы на дефекацию; различной степени выраженности явления анальной инконтиненции (недержания кала) с подтеканием кишечного содержимого. Данный симптомокомплекс получил в мировой литературе название «синдром низкой передней резекции». Ведущим патогенетическим звеном подобных нарушений является удаление ампулы прямой кишки с потерей ее резервуарной и эвакуаторной функций. Для решения данной проблемы было предложено формирование толстокишечного резервуара в форме латинской буквы «J». Но наряду с положительной оценкой резекций прямой кишки с формированием толстокишечного резервуара, существуют и функциональные недостатки таких операций: эвакуаторные нарушения, проявляющиеся запорами в отдаленном периоде и специфические осложнения (несостоятельность колоанального анастомоза, некроз и воспаление резервуара).
Операция Гартмана заключается в резекции кишки (по онкологическим правилам), ушивании культи прямой кишки наглухо и формировании одноствольной колостомы (снгмостомы) на передней брюшной стенке. Эту операцию выполняют при осложнениях рака прямой кишки, в частности обтурационной толстокишечной непроходимости, кровотечении, перфорации опухоли или при тяжелых сопутствующих заболеваниях.
Брюшнопромежностная экстирпация прямой кишки (операция КенюМайлса) – показана при низколокализованном раке прямой кишки (ниже 5–7 см от ануса) и невозможности выполнения сфинктеросохраняющей операции. Операция заключается в удалении всей прямой кишки вместе со сфинктерным аппаратом, клетчаткой, лимфатическими узлами, дистальной частью сигмовидной кишки и формировании постоянной одноствольной колостомы (сигмостомы) на передней брюшной стенке.
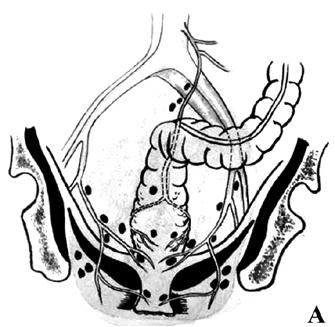
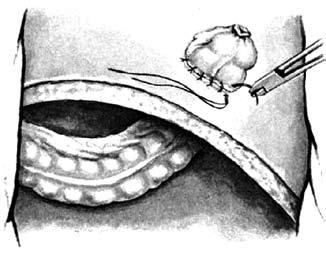
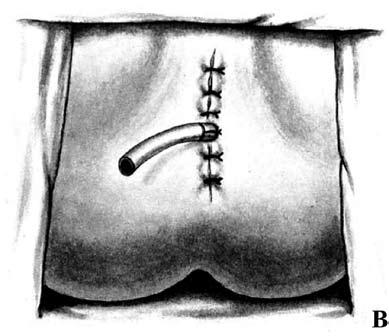
Рис. 8. Брюшнопромежностная экстирпация прямой кишки: А – границы резекции;
Б – сформирована одноствольная колостома;
В – ушитая промежностная рана с дренажем в полости малого таза
Принципы радикальной операции Дистальный и проксимальный края отсечения кишки должны быть на достаточном расстоянии от опухоли, чтобы при микроскопическом исследовании они не содержали опухолевых клеток. Проксимальная граница резекции должна располагаться на 12–15 см от опухоли. Дистальная граница резекции зависит от локализации опухоли. Для опухолей верхней трети прямой кишки (12–16 см выше зубчатой линии) актуальным является «правило 5–6 сантиметров» (с обязательной резекцией такого же отрезка мезоректума). При локализации опухоли ниже 12 сантиметров это расстояние может и должно быть ограничено двумя сантиметрами. Объясняется это тем, что интрамуральное (внутри стенки прямой кишки) распространение опухоли в дистальном направлении является исключительной редкостью и возможно только в запущенных стадиях, приводящих к блокаде лимфооттока. Но даже в этих случаях внутристеночная инвазия не превышает одного сантиметра. Именно поэтому почти все опухоли прямой кишки могут быть резецированы с сохранением сфинктера, что обуславливает значительное улучшение качества жизни пациентов с раком прямой кишки.
Вместе с опухолью должны быть удалены все регионарные лимфатические узлы. Поскольку практически все дренирующие среднюю и нижнюю треть прямой кишки лимфоузлы находятся в пределах мезоректума, то удаление и резекция прямой кишки должны выполняться без нарушения целостности ее висцеральной фасции, «в футляре» – т. н. «мезоректумэктомия».
Лучевая терапия Предоперационная лучевая терапия рака прямой кишки преследует следующие цели: а) сокращение массы опухоли и перевод ее в операбельное состояние; б) резорбцию или инактивацию метастазов в регионарных лимфоузлах; в) снижение потенции раковых клеток к приживлению в отдаленных органах (профилактика отдаленных метастазов).
Лучевая терапия проводится по двум программам:
Обычное (классическое) фракционирование дозы по 2 Гр (Грэй) за сеанс до суммарной дозы 46–48 Гр. Операция выполняется через 2–3 недели после окончания курса лучевой терапии.
Крупное фракционирование – по 5 Гр за сеанс ежедневно до суммарной дозы в 25 Гр, что по биологическому действию и терапевтическому эффекту равноценно 44 Гр обычного фракционирования. Больного оперируют через 24–48 часов после завершения курса, до развития лучевой реакции.
Брюшноанальная резекция с низведением сигмовидной кишки. При расположении опухоли на расстоянии 6–7 см от края заднего прохода может быть выполнена и брюшноанальная резекция с низведением сигмовидной кишки в анальный канал и формированием колоанального анастомоза. У данной методики существует и ряд недостатков. В первую очередь, возможно развитие такого грозного раннего послеоперационного осложнения, как некроз низведенной ободочной кишки.


Рис. 7. Брюшноанальная резекция с формированием Jобразного резервуара: А – сформирован резервуароанальный анастомоз; Б – Jобразный толстокишечный резервуар
Кроме того, удаление прямой кишки влечет за собой потерю ее резервуарноэвакуаторной функции. Это обстоятельство приводит к ухудшению функциональных результатов операции – частые (до 6 и более раз в сутки) дефекации; многомоментное, длительное и неполное опорожнение кишечника; императивные позывы на дефекацию; различной степени выраженности явления анальной инконтиненции (недержания кала) с подтеканием кишечного содержимого. Данный симптомокомплекс получил в мировой литературе название «синдром низкой передней резекции». Ведущим патогенетическим звеном подобных нарушений является удаление ампулы прямой кишки с потерей ее резервуарной и эвакуаторной функций. Для решения данной проблемы было предложено формирование толстокишечного резервуара в форме латинской буквы «J». Но наряду с положительной оценкой резекций прямой кишки с формированием толстокишечного резервуара, существуют и функциональные недостатки таких операций: эвакуаторные нарушения, проявляющиеся запорами в отдаленном периоде и специфические осложнения (несостоятельность колоанального анастомоза, некроз и воспаление резервуара).
Операция Гартмана заключается в резекции кишки (по онкологическим правилам), ушивании культи прямой кишки наглухо и формировании одноствольной колостомы (снгмостомы) на передней брюшной стенке. Эту операцию выполняют при осложнениях рака прямой кишки, в частности обтурационной толстокишечной непроходимости, кровотечении, перфорации опухоли или при тяжелых сопутствующих заболеваниях.
Брюшнопромежностная экстирпация прямой кишки (операция КенюМайлса) – показана при низколокализованном раке прямой кишки (ниже 5–7 см от ануса) и невозможности выполнения сфинктеросохраняющей операции. Операция заключается в удалении всей прямой кишки вместе со сфинктерным аппаратом, клетчаткой, лимфатическими узлами, дистальной частью сигмовидной кишки и формировании постоянной одноствольной колостомы (сигмостомы) на передней брюшной стенке.



Рис. 8. Брюшнопромежностная экстирпация прямой кишки: А – границы резекции;
Б – сформирована одноствольная колостома;
В – ушитая промежностная рана с дренажем в полости малого таза
Принципы радикальной операции Дистальный и проксимальный края отсечения кишки должны быть на достаточном расстоянии от опухоли, чтобы при микроскопическом исследовании они не содержали опухолевых клеток. Проксимальная граница резекции должна располагаться на 12–15 см от опухоли. Дистальная граница резекции зависит от локализации опухоли. Для опухолей верхней трети прямой кишки (12–16 см выше зубчатой линии) актуальным является «правило 5–6 сантиметров» (с обязательной резекцией такого же отрезка мезоректума). При локализации опухоли ниже 12 сантиметров это расстояние может и должно быть ограничено двумя сантиметрами. Объясняется это тем, что интрамуральное (внутри стенки прямой кишки) распространение опухоли в дистальном направлении является исключительной редкостью и возможно только в запущенных стадиях, приводящих к блокаде лимфооттока. Но даже в этих случаях внутристеночная инвазия не превышает одного сантиметра. Именно поэтому почти все опухоли прямой кишки могут быть резецированы с сохранением сфинктера, что обуславливает значительное улучшение качества жизни пациентов с раком прямой кишки.
Вместе с опухолью должны быть удалены все регионарные лимфатические узлы. Поскольку практически все дренирующие среднюю и нижнюю треть прямой кишки лимфоузлы находятся в пределах мезоректума, то удаление и резекция прямой кишки должны выполняться без нарушения целостности ее висцеральной фасции, «в футляре» – т. н. «мезоректумэктомия».
Лучевая терапия Предоперационная лучевая терапия рака прямой кишки преследует следующие цели: а) сокращение массы опухоли и перевод ее в операбельное состояние; б) резорбцию или инактивацию метастазов в регионарных лимфоузлах; в) снижение потенции раковых клеток к приживлению в отдаленных органах (профилактика отдаленных метастазов).
Лучевая терапия проводится по двум программам:
Обычное (классическое) фракционирование дозы по 2 Гр (Грэй) за сеанс до суммарной дозы 46–48 Гр. Операция выполняется через 2–3 недели после окончания курса лучевой терапии.
Крупное фракционирование – по 5 Гр за сеанс ежедневно до суммарной дозы в 25 Гр, что по биологическому действию и терапевтическому эффекту равноценно 44 Гр обычного фракционирования. Больного оперируют через 24–48 часов после завершения курса, до развития лучевой реакции.