ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 129
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
14) Оттегі тасымалдаудың биохимиялық негіздері
Оттектің гемоглобинге байланысуы үшін мына шарттар орындалады:
1. Оттектің жоғары парциалды қысымда болуы (100мм сынап бағанасынан төмен болмауы.).
2. Көмірқышқыл газының төмен парциалды қысымда болуы
3. Әлсіз қышқылдық орта.
4. Өте төмен температура.
5. 2,3-дифосфоглицераттың еңтөменгіконцентрациясы.
Осы шарттардың бәрі өкпеде орындалады және гемоглобинніңоксигенденуіне мүмкіндік тудырады.
Гемоглобинніңоттекпенөкпедебайланысуыкезіндегемоглобинніңпротондарғаынтықтығытөмендейді. Бөлініп шыққан протондар бикарбонат иондарыменбайланысады да көмірқышқылытүзіледі, ол көмірқышқыл газы мен суға дейін ыдырайды. Көмірқышқыл газы деммен шығады(Бор эффектісі):
-
HbH + O2 HbO2 + H+ -
H+ + HCO3- H2CO3 ↔H2O+CO2
Артериалдықандағы эритроциттердің оксигемоглобині 95-98% дықұрайды. Қалған бөлігін бос гемоглобин құрайды. Көктамырдағыэритроциттердіңоксигемоглобині 67-75% болады.
Тіндерде оксигемоглобин бос гемоглобин мен оттеккедейіныдырауыүшінтөмендегішарттарорындалуыкерек:
1. Оттектің төмен парциалдықысымдаболуы.
2. Көмірқышқыл газының жоғары парциалдықысымдаболуы.
3. Жоғары қышқылдық орта
4. Жоғары температура.
5. 2,3 – дифосфоглицераттыңжоғары концентрациясы
Тіндерде протондар мен СО2 концентрациялары артқанда оксигемоглобиннің деоксигенденуі жүреді, себебі гемоглобиннің оттекке ынтықтығы төмендейді. Осы уақытта гемоглобиннің протондарға ынтықтығы артады да гемоглобин протондармен және көмірқышқыл газымен байланысады. Осылай гемоглобин тынысалу қызметін ғана атқарып қоймайды, ол тіндерде протондар мен көмірқышқыл газының мөлшерін азайту арқылы буфер рөлін де атқарады. Сонымен, заттардың ыдырауының қарқындылығы артқан сайын , мысалы, физикалық жұмыс істегенде, СО2 мен протондардың концентрациялары артады және осы уақытта гемоглобиннің оттекке деген ынтықтығы төмендегендіктен, тіндердің оттекті қабылдауы жоғарылайды:
-
H2O+CO2↔ H2CO3 H+ + HCO3- -
HbO2 + H+ O2 + HbH
1лқанқалыптыжағдайдаорташамамен 200-210 млоттекті байланыстырады. Бұл шама қанның оттектік белсенділігі деп аталады.
Оксигенденукезіндегемоглобинмолекуласы бета –тізбектерінің жақындауынан қысылады, ал HbО2 – нің ыдырауында кеңейеді. Бұл құбылысты байқау нәтижесіндебиохимикПерутцгемоглобинмолекуласына "тынысалушы" деп атады.
15) Көмірқышқылгазынтасымалдаудыңбиохимиялықнегіздері
Зат алмасуы кезінде көмірқышқыл газы тін жасушаларынан көктамырқан плазмасына түседі. Аздаған бөлігі еріген күйде қалады, ешқандай өзгеріссіз қан айналымымен бірге жүреді. СО2 нің негізгі бөлігі эритроциттергетүседі, онда карбангидразаферментініңәсеріненкөмірқышқылытүзіледі:
СО2+Н2О↔Н2СО3↔НСО-3 + Н+
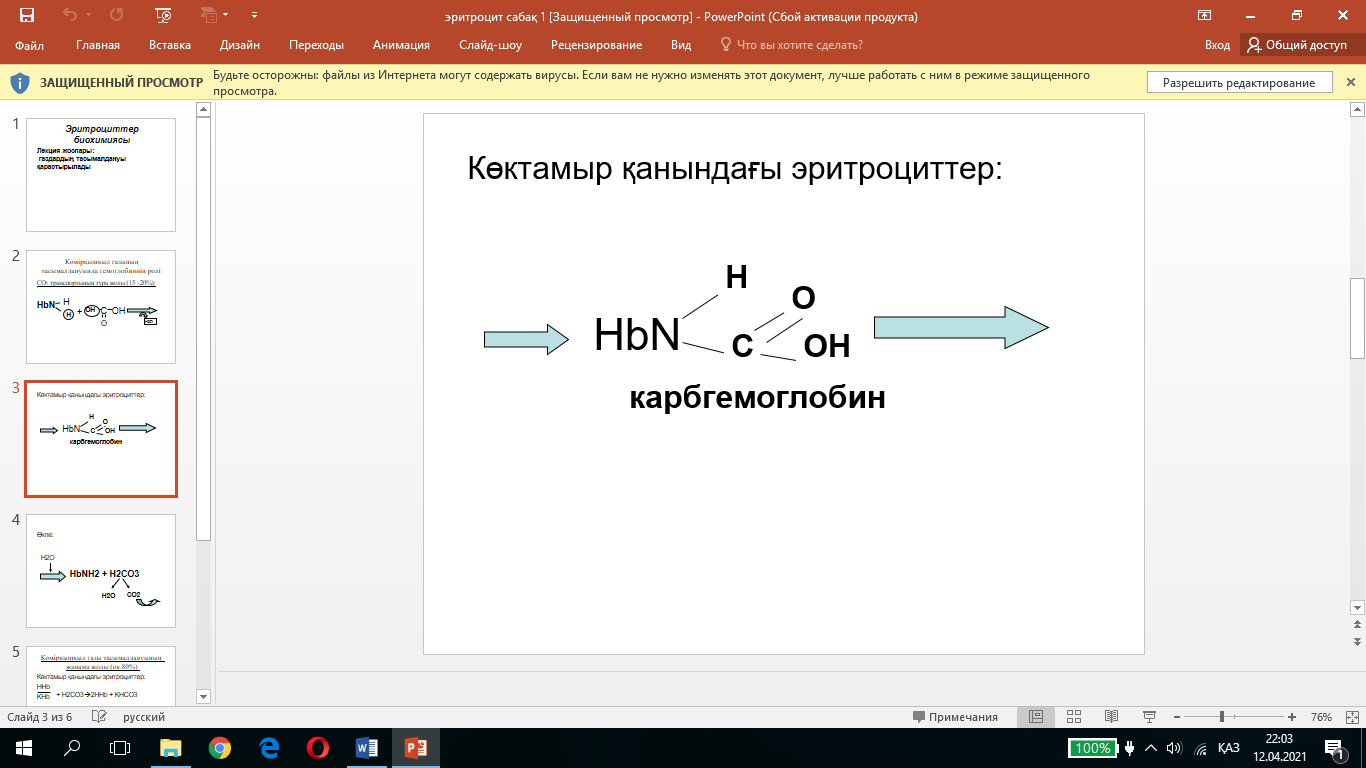
Көмір қышқылының 5-10% диссоцияцияланып гидрокарбонат-анио-нын(НСО-3 ) түзеді де қан плазмасына түседі. Гидрокарбонат-ион белок буферімен әрекеттесіп бикарбонат буферлік жүйесінің компоненті NaHCO3 -ті түзеді. Қалған көмір қышқылы 90-95% өкпеге тасымалданады да, деммен шығып кетеді. Көмір қышқылының 10-15% карбгемоглобин түзу арқылы тікелей жолмен тасымалданады.
Карбгемоглобиннің түзілуі мен ыдырау шарттары оксигемоглобиннің түзілуі мен ыдырауына қарама қарсы жүреді:
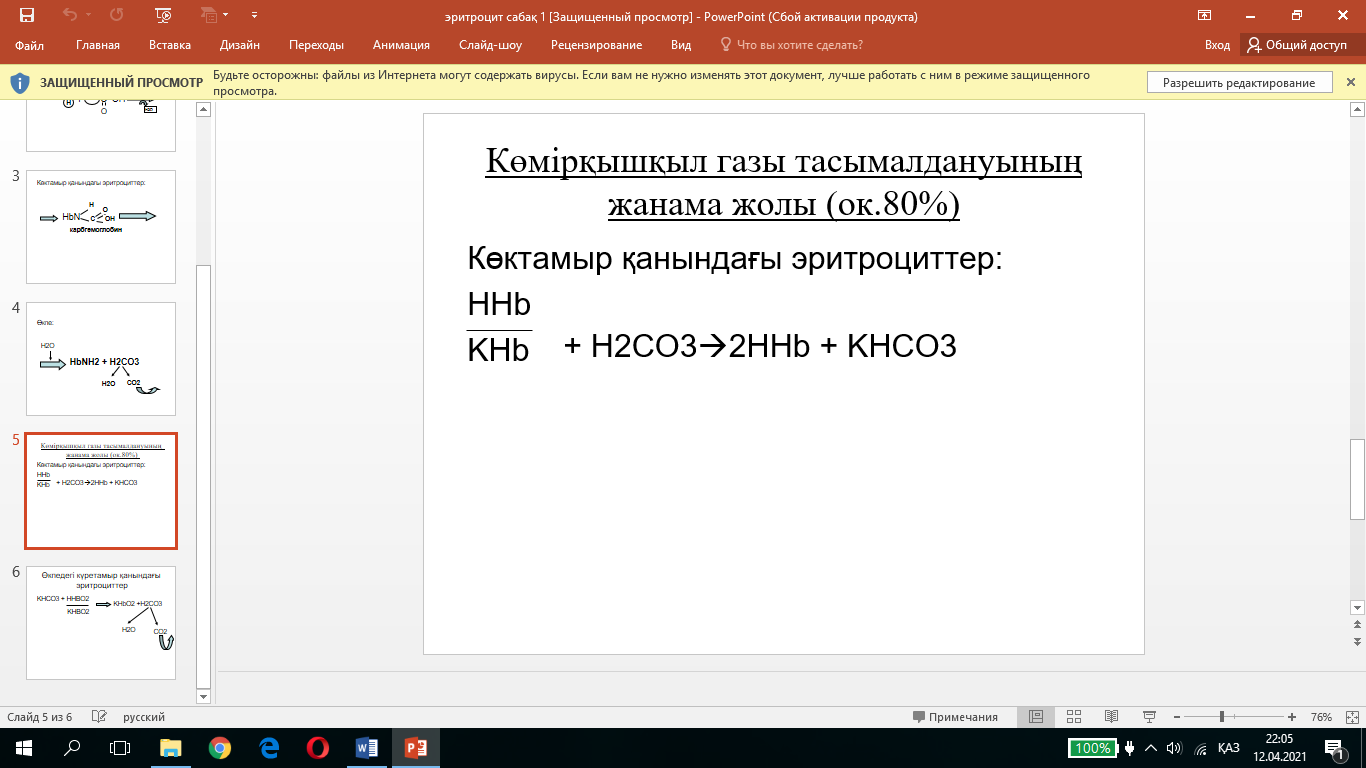
Көмір қышқылының негізгі массасы 80% ға жуығы гемоглобинмен тасымалданады, ол бұл уақытта буферлік жүйе қызметін атқарады. Көктамыр қанының эритроциттерінде гемоглобин буфері ННb/КНb бар, ол көмір қышқылын бөлімімен әрекеттестіріп көмір қышқылын бейтараптайды, себебі көмірқышқылы ННb ге қарағанда күштірек, сондықтан КНb нен К+ ионын ығыстырып шығаратын реакция жүреді.
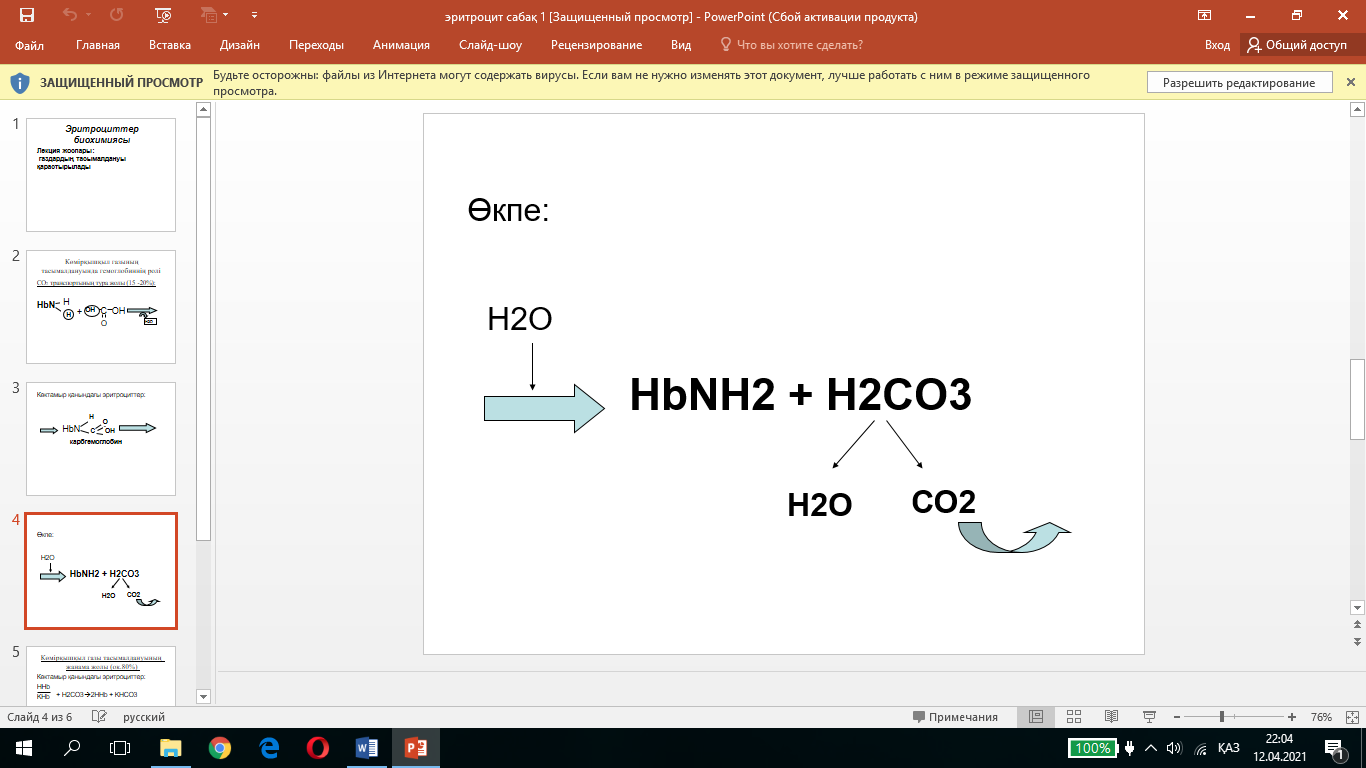
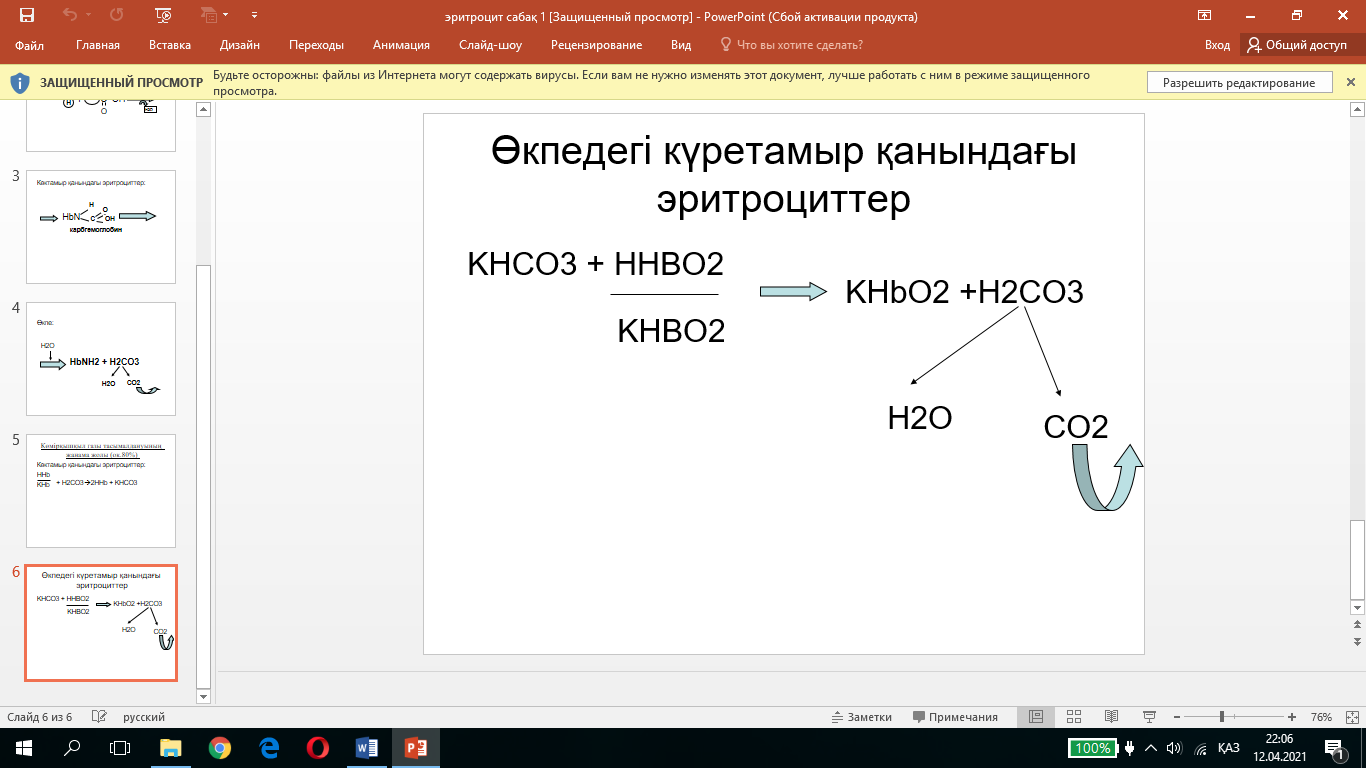
Өкпеге түскенде гемоглобин оксигенденеді де оксигемоглобин буферлік жүйесін түзеді : ННbO2/КНbO2. Оксигемоглобин қышқылы көмір қышқылына қарағанда күштірек, сондықтан ол түскен тұздан көмір қышқылын ығыстырып шығарады.
Көмір қышқылы ыдырайды да көмірқышқыл газы деммен ауаға шығып кетеді.

16) Гемоглобинніңфизиологиялықтуындылары, түзілушарттары. Жұтылуспектрлері
-
Оксигемоглобин– өкпеде гемоглобиннің оксигендену процесі кезінде түзіледі.Артерия қанының құрамындаболып,оксигемоглобині бар қанның түсі ашық қызыл түсті болады. Боялған түсті заттар ерітінділерілерінің белгілі бір ұзындықтағы күн сәулелерінің спектрлерін арнайылықты тежеп, сіңіретін қабілеттері бар.Күн сәулесі спектрінің сәйкес жерінде қара жолақтар түзіледі (жұтылу спектрі). Гемоглобин және оның туындылары арнайылықты жұтылу спектрлерлеріне ие болады, олар әртүрлі ауруларға диагноз қоюға қолданылады. Оксигемоглобиннің жұтылу спектрі- жасыл сары спектрдің бөлігінде фраунгофердің Д мен Е сызықтарының аралығында екі жіңішке қара сызықты түзеді. -
Карбгемоглобин – көктамыр қаны эритроциттерінде түзіледі, оның ертіндідегі мөлшеріне қарай қошқыл- қызыл түске ие болады. Арнайылықты спектрі болмайды, себебі СО2 гемге емес гемоглобиннің глобиніне байланысады. Көктамыр қанын спектроскопиялық әдіспен зерттегенде спектрдің жасыл сары аймағында бір кең жолақ байқалады,ол НЬ-нің жұтылу спектрі.
17) Гемоглобиннің патологиялық туындылары, пайда болу себептері. Жұтылу спектрлері.
1.Карбоксигемоглобин (НbCO) – гемоглобин иісті газбен әрекеттескенде түзіледі. Карбоксигемоглобин – бұл мықты байланысты қосылыс, әлсіз диссоцияцияланады, оттекті қосып ала алмайды. Сонымен қатар карбоксигемоглобин бар уақытта оксигемоглобиннің дезоксигенденуі қиындайды (Холден эффектісі). Жұтатын ауада иісті газдың концентрациясы 0,1% ге жуық болғанда гемоглобиннің 50% онымен 1/130 секунд ішінде байланысады (гемогло¬биннің иісті газға ынтықтығы оттекке қарағанда жоғары болады). Егер гемоглобиннің 70% иісті газбен байланысса гипоксиядан адам ағзасы өледі. Қан күлгін түсті болады ("ит бүлдіргені -(брусника) шырыны түсті"). Карбоксигемоглобиннің жұтылу спектрі оксигемоглобиннің жұтылу спектріне өте ұқсас - спектрдің жасыл сары аймағында екі жіңішке сызық, бірақ олар аздап күлгін түсті жаққа ығысқан. Оксигемоглоби¬н мен карбоксигемоглобинді бір бірінен толық ажырата білу үшін зерттелетін ерітіндіге Стокс реактивін қосу керек ( темірдің шараптасты аммиактағы ерітіндісі). Бұл реактив күшті тотықсыздандырғыш болғандықтан, осы реактивті оксигемоглобин ерітіндісіне қосқанда ол бір қара жолақ - жұтылу спектрі бар гемоглобинге дейін тотықсызданады.Стокс реактивін қосқанда карбоксигемоглобиннің жұтылу спектрі өзгермейді, себебі бұл реактив оған әсер етпейді.
2.Метгемоглобин (НbОН) – қалыпты жағдайда (1-2%) азот оксидін пайдаланғанда түзіледі. Метгемоглобин физиологиялық жағдайда тынысалу ферменттерін активтендіру арқылы тек азот окидін ғана емес, цианидтерді де байланыстыра алады. Цианидтер физиологиялық жағдайда үздіксіз түзіледі ( альдегидтердің, кетондардың және альфа-оксиқышқылдардың циангидринмен әрекеттесулері нәтижесінде, сонымен қатар нитрилдердің метаболизмі нәтижесінде). Метгемоглобин күкіртті сутекті, натрий азитін, роданидтерді, натрий фторидін, формиатты, мышьякты қышқылын және басқа да уларды байланыстыра алады. Метгемоглобин сутек пероксидінің артық мөлшерін су мен атомдық оттекке дейін ыдыратуға қатысады да оксигемоглобинге айналады Қалыпты жағдайда метгемоглобин эритроциттерде жинақталмайды, себебі онда оны тотықсыздандыратын ферментті жүйе (НАДФ-редуктаза), ферментсіз (С витамині – 12-16% және тотықсызданған глутатион – 9-12%) бар.
Метгемоглобин көп мөлшерде күшті тотықтырғыштардың әсерінен түзіледі (бертолет тұзы , қызыл қанды тұз, нитробензол, анилин, көптеген органикалық еріткіштер және басқалары). Бұл уақытта темір тотығып үш валентті түрге айналады. Үш валентті темірге атомдық оттек байланысып гидроксил тобы түзіледі. Мұндай гемоглобин оттекті тасымалдау қабілетін жоғалтады да, ағзада оттек жетіспеушілігі туады. Қан қызыл-қоңыр түске айналады (кірпіш түсті). Метгемоглобин бүйрек арқылы шыға алатындықтан зәр қоңыр түске боялады. Метгемоглобиннің жұтылу спектрі – үш жолақ, екеуі спектрдің жасыл сары аймағында, біреуі қызыл бөлігінде болады.
Нитриттер мен нитраттар – суды негізгі ластайтын заттар, ал су көп мөлшерде жаңа туған нәрестелер мен емшектегі нәрестелерге ішу үшін керек. Ересектер үшін мұндай су онша әсер етпейді, бірақ, нитриттер мен нитратты сулар жасөспірімдердің ағзаларына қатты әсер етеді. Нитраттар мен нитриттер ағзада метгемоглобинанің түзілуіне мүмкіндік туғызады. Метгемоглобин-емияның белгісі дистилденген суды пайдаланғанда кетеді. Метгемоглобин-емияның бар екендігін дәлелдеу үшін қанның газдарын зерттейді (қалыпты рО2), лактат деңгейін (жоғарылаған) және метгемоглобин деңгейін (жоғарылаған). Метгемоглобин оксиметрмен өлшенеді. Метгемоглобин-анемиядан емдеу үшін оттекпен демалдырады
, тотықтырғыш агенттерін кетіреді, метилен көгін пайдаланады (қорғау жолының бірінші антидоты). Метилен көгі метгемоглобиннің тотықсыздануын тездетеді және оның ағзадағы мөлшерін төмендетеді. Бұдан басқа гипербариялық оксигенотерапия, активтелген көмірді пайдалану ұсынылады .
3.Гликозилденген (гликирленген) гемоглобин (HbA1c) гемоглобиннің бета –тізбегіне глюкоза байланысқанда түзіледі. Глюкозаның карбонил тобы глобиннің бета-тізбегіндегі валиннің амин тобымен әрекеттеседі, нәтижесінде Шифф негізі түзіледі. Бұл ферментсіз гликирленудің бірінші сатысы, ол тез және қайтымды жүреді. Екінші сатысы - баяу және қайтымсыз жүреді, осы жағдайда тұрақты кетоамин түзіледі (қараңыз - 94 бет, Данилова бойынша). Сонымен, гликирленген гемоглобин бос глюкозаның валиннің бета –тізбегіндегі шеткі амин тобымен комплекс түзуін көрсетеді. Гемоглобин А дан басқа гликирленуге гемоглобиннің басқа түрлері де ұшырайды, мысалы, HbA2. Гемоглобиннің гликирленуі оның құрылысын және қызметін өзгертеді, алдымен оның оттекке ынтықтығы өзгереді. Бұл дезоксигенденудің бұзылуына әкеледі. Гликирленуге басқа нәруыздар да ұшырауы мүмкін – инсулин, ферменттер, альбуминдер, фибриноген, липопротеидтер және басқалары. Гемоглобиннің гликирленуі қалыпты жағдайда 2-4% және патологияда (более 7%) болуы мүмкін, ұзақ гипергликемия (бір айдан көбірек), мысалы, қант диабеті болған жағдайда кездеседі. Бұл қосылыс өте мықты, дезоксигенденуге нашар беріледі, ол қантты диабет кезінде тіндердің оттекке жетіспеушілігін тудырады.Гликирленген гемоглобинді анықтаудың диагностикалық маңызы зор, әсіресе ерте пайда болған қантты диабет пен диабеттің алдынғы түрін анықтауда.
4.Нитрозогемоглобин(S-NO-HbO2) NO цистеиннің тиотобымен немесе гемнің темір ионымен байланысады. Нитрозогемоглобин тамырлардың тонусын жақсартады.
18) Бор эффектісі
Гемоглобиннің оттекті тасымалдауға қатысуы. Гемоглобиннің оттекпен өкпеде байланысуы кезінде гемоглобиннің протондарға ынтықтығы төмендейді. Бөлініп шыққан протондар бикарбонат иондарымен байланысады да көмір қышқылы түзіледі, ол көмірқышқыл газы мен суға дейін ыдырайды. Көмірқышқыл газы деммен шығады,бұл-Бор эффектісі:
-
HbH + O2 HbO2 + H+ -
H+ + HCO3- H2CO3 ↔H2O+CO2
Тіндерде протондар мен СО2 концентрациялары артқанда оксигемоглобиннің деоксигенденуі жүреді ( себебі гемоглобиннің оттекке ынтықтығы төмендейді). Осы уақытта гемоглобиннің протондарға ынтықтығы артады да гемоглобин протондармен және көмірқышқыл газымен байланысады. Осылай гемоглобин тынысалу қызметін ғана атқарып қоймайды, ол тіндерде протондар мен көмірқышқыл газының мөлшерін азайту арқылы буфер рөлін де атқарады. Сонымен, заттардың ыдырауының қарқындылығы артқан сайын,мысалы, физикалық жұмыс істегенде, СО2 мен протондардың концентрациялары артады және осы уақытта гемоглобиннің оттекке деген ынтықтығы төмендегендіктен (