Файл: Физика изучение спектра излучения атома водорода Методические указания к лабораторной работе Электронный учебный материал Минск 2020.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.01.2024
Просмотров: 152
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
Белорусский национальный технический университет
Кафедра "ТЕХНИЧЕСКАЯ ФИЗИКА"
Изучение спектра излучения атома водорода
Методические указания к лабораторной работе
Электронныйучебныйматериал
Минск 2020
Составители: доктор физ.-мат. наук, профессор Зенькевич Э.И. канд. физ.-мат. наук, доцент Качан С.М.
канд. физ.-мат. наук, доцент Митькина Н.Н.
Рецензент: доктор физ.-мат. наук, профессор кафедры "Лазерная физика и спектроскопия " БГУ Воропай Е.С.
В издании представлены методические указания к выполнению лабораторной работы по физике в разделе "Оптика и атомная физика" для студентов технических специальностей университетов, включающие в себя теоретическую часть, контрольные вопросы и порядок выполнения работы, заключающейся в наблюдении серии Бальмера в спектре излучения атома водорода с помощью призменного монохроматора и определении длин волн наблюдаемой серии как экспериментально, так и теоретически.
Белорусский национальный технический университет. Факультет информационных технологий и робототехники. ул. Б.Хмельницкого, 9, г. Минск, Республика Беларусь
Тел.: (017) 292-71-53
E-mail: tf@bntu.by http://www.bntu.by/fitr.html
Регистрационный № БНТУ/ФИТР47-74.2020
Содержание
Контрольные вопросы 4
-
Введение 5 -
Постулаты Бора 8 -
Атом водорода по Бору 10 -
Спектральные серии атома водорода 13 -
Атом водорода в квантовой механике 14 -
 Определение длин волн спектральных линий в серии Бальмера спектра излучения атома водорода 17
Определение длин волн спектральных линий в серии Бальмера спектра излучения атома водорода 17
Описание установки 17
 Порядок проведения измерений и обработка
Порядок проведения измерений и обработкарезультатов 19
Градуировка монохроматора 20
Определение длин волн в серии Бальмера с помощью призменного монохроматора 21
Список литературы 23
Цельработы.
-
Изучить теорию атома водорода в модели Бора и в рамках квантовой механики. -
Экспериментально определить длины волн в видимой области спектра излучения атома водорода и сопоставить их с теоретическими значениями.
Приборыипринадлежности
-
Водородная лампа -
Ртутная лампа -
Призменный монохроматор УМ-2 -
Миллиметровая бумага формата А4
Порядоктеоретическойподготовкиквыполнениюработы
Изучить теоретический материал и законспектировать в тетрадь ответы на контрольные вопросы.
Контрольныевопросы
-
Атом водорода по Резерфорду. Постулаты Бора. -
Атом водорода по Бору. Какие физические величины, определяющие состояние электрона в атоме, принимают дискретные значения? -
Энергия электрона в атоме водорода. Схема энергетических уровней атома водорода. Основное и возбужденные состояния атома водорода. -
Определение энергии ионизации атома водорода и формула для ее оценки. -
Определение спектральных серий в спектрах излучения атома водорода. Какая серия в спектре атома водорода расположена в видимой части спектра? -
Стационарное уравнение Шредингера для электрона в атоме водорода. -
Квантовые числа, их связь с физическими величинами. -
Принципиальная схема призменного монохроматора. -
В чем заключается градуировка монохроматора?-
Введение
-
Согласно философскому учению древних греков, все материальные вещи состоят из химически неделимых частиц – атомов. Сами атомы греки считали мельчайшими, невозникающими и неисчезающими, качественно однородными, непроницаемыми частицами, обладающими определённой формой. В XVIII веке А. Лавуазье, М.В. Ломоносов, М. Фарадей, Д.И. Менделеев и другие ученые доказали реальность существования атомов. Однако вопрос об их внутреннем устройстве даже не возникал. Прошли века и вплоть до XIX века ученые предполагали, что атом является неделимым.
Первые модели строения атома появились лишь в конце XIX - начале XX веков. Так, в 1897 г. молодой английский физик Дж. Дж. Томсон, исследуя поведение катодных лучей под воздействием магнитного и электрического полей открыл электрон и измерил отношение заряда электрона к массе e/m. После этого открытия стало ясно, что электроны должны существовать в составе атомов, но несмотря на присутствие отрицательно заряженных электронов, атом в целом должен быть электронейтральным.
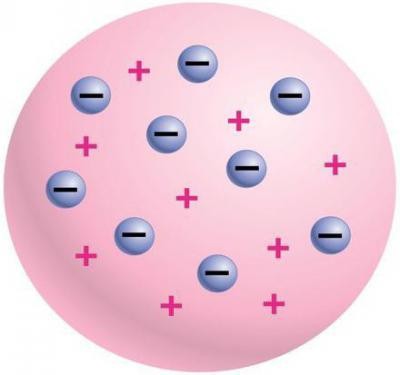
Рисунок 1. Модель атома Томсона
В 1898-1903 г.г. Дж. Дж. Томсон разработал ипредложилмодельатомав виде положительно заряженного шара, в котором плавают электроны, нейтрализующие положительный заряд. Другое неофициальное название модели – «Пудинг с изюмом». Согласно классическим представлениям атом в рамках такой модели может испускать монохроматическую световую волну (регистрируемую как спектральную линию в видимом диапазоне спектра) в том случае, когда
электрон в излучающем атоме совершает гармонические колебания и, следовательно, удерживается около положения равновесия квазиупругой силой. Расчеты в рамках этой модели позволили оценить радиус атома как R
310-10 м. Следует, однако, отметить, что модель атома Томсона (см. рисунок 1) имела два существенных недостатка: 1) она не могла объяснить дискретный характер испускания света атомами и 2) с ее помощью невозможно объяснить причины устойчивости атомов как единого целого. Вместе с тем, модель атома Томсона имела не меньшую ценность для науки
того времени, чем другие гипотезы. В настоящее время она имеет лишь исторический интерес как одно из звеньев в цепи развития представлений о строении атомов.
 В1909–1911гг.первыепрямыеэкспериментыпоисследованиюстроенияатомовбыли выполненыЭ. Резерфордоми его сотрудниками Э. Марсденом и Х. Гейгером. В этих экспериментах атомы мишени (тонкой фольги из тяжелого металла - золота, серебра, меди и др.) бомбардировались α- частицами с кинетической энергией около 5 МэВ (скорость
В1909–1911гг.первыепрямыеэкспериментыпоисследованиюстроенияатомовбыли выполненыЭ. Резерфордоми его сотрудниками Э. Марсденом и Х. Гейгером. В этих экспериментах атомы мишени (тонкой фольги из тяжелого металла - золота, серебра, меди и др.) бомбардировались α- частицами с кинетической энергией около 5 МэВ (скорость 107 м/с). Отметим, что α-частицы – это дважды ионизированные атомы гелия, масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду.
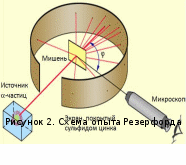
В экспериментах Резерфорда исследовались закономерности рассеяния, то есть изменения
направления движения α-частиц при их столкновении с мишенью (схема опыта приведена на рисунке 2). Вылетая из источника, находящегося в защитном свинцовом контейнере, α-частицы достигали мишени (тонкая металлическая фольга). Рассеянные от мишени α- частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться в виде коротких вспышек под ударами быстрых частиц. Эти вспышки (сцинтилляции) на экране наблюдались глазом с помощью микроскопа, который устанавливался под различными углами φ к первоначальному направлению пучка α-частиц. В ходе этих экспериментов были установлены следующие принципиальные факты: 1) большинство α- частиц проходит через тонкий слой металла, практически не испытывая отклонения; 2) небольшая часть частиц отклоняется на значительные углы, превышающие 30°; 3) в очень редких случаях (приблизительно один на десять тысяч наблюдений) α-частицы испытывали отклонение на углы, близкие к 180°, т.е. практически рассеивались назад.
Эти результаты были объяснены следующим образом. Электроны, входящие в состав атомов, из-за малой собственной массы (по сравнению с массой α-частиц) не могут заметно изменить траекторию α-частицы. Поэтому рассеяние положительных α-частиц на мишенях (т.е. изменение направления движения) способна вызвать только тяжелая положительно заряженная часть атома. В модели Томсона положительный заряд распределен по всему объему атома (см. рисунок 1) и не может создать сильное электрическое поле, способное отбросить
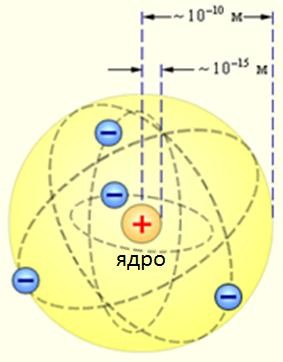 Рисунок 3. Планетарная модель атома Резерфорда
Рисунок 3. Планетарная модель атома Резерфорда