ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.01.2024
Просмотров: 75
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Кешенді қосылыстар, координациялық теория
Біздер химиялық байланысты оқығанда тарту күші тек атомдар арасында ғана емес, сонымен қатар молекула аралық та болатынын қарастырғанбыз.
Д.И.Менделеев пен В.А Каблуковтың ерітінділер жайындағы теориясы бойынша иондар сулы ерітіндіде гидратталған күйде жүреді. Егер натрий хлориді ерітіндісін қарастырсақ, онда Na+ ионын судағы ерітіндіде 6 моль су қоршап жүре алады. [Na(H2O)6]+, Cu2+ ионы аммиактағы ерітіндісінде 4 моль аммиак қоршайды – [Cu(NH3)4]2+ болады. Мұндай күрделі бейорганикалық қосылыстардың құрамы мен құрылысын валенттіліктің классикалық теориясы арқылы түсіндіруге келмейді. Бұл қосылыстарға былай анықтама беруге болады:
Бейтарап молекулаларды не иондарды қосып алып, кристалл тор түйіндерінде және ерітіндіде де жүре алатын иондарды кешенді деп, ал құрамында осындай иондары бар қосылыстарды кешенді қосылыстар деп атайды.
Кешенді қосылыстар құрылысы және қасиеттерін 1893 жылы швейцария ғалымы, Нобель сыйлығының лауреаты А. Вернер ұсынған координациялық теория түсіндіреді.
Бұл теорияның негізгі қағидалары төмендегідей:
-
кешенді қосылыстарда бір ион не атом орталықтан орын алады, оны кешен түзушідеп атайды;
ә) орталық ион (атом) айналасында қарама-қарсы зарядты ион не полярлы молекулалар орналасады, оларды лигандтар деп атайды. “Лиганд” деген сөз латынның “ligo” – байланысқан деген мағына береді;
б)орталық ион (атом) лигандтармен бірге кешенді қосылыстың ішкі координациялық сферасын құрады, оны квадрат жақшаға алып жазады;
в) кешен түзішумен байланысқан бөлшектердің жалпы санын координациялық сан деп атайды, оның сан мәні көп жағдайда 2, 4, 6, 8, болады;
г) орталық ионнан едәуір қашықтықта орналасқан иондар кешенді қосылыстың сыртқы сферасын құрады;
д) орталық ионның (атом) өзінің айналасындағы бөлшектерімен байланыс беріктілігі әртүрлі болады.
А.Вернердің координациялық теориясын орыс ғалымдары Л.А.Чугаев, И.Л.Черняев, А.А.Гринберг т.б. ғалымдар толықтырды.
Кешенді қосылыстардың құрылысын төмендегідей сызбанұсқамен көрсетуге болады:
[NH4]Cl [Cu(NH3)4]SO4
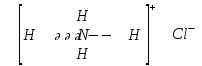




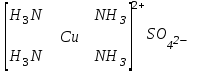
N-3 – комплекс түзуші Сu2+– комплекс түзуші
[NH4]+– ішкі сфера NH3– лиганд
Cl-– сыртқы сфера [Cu(NH3)4]2+– ішкі сфера
Координациялық сан – 4 SO42-– сыртқы сфера
координациялық саны – 4
Кешен түзуші бола алатындар:
-
Оң зарядты иондар (көбінде қосымша топша металдарының иондары).
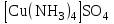
-
Теріс зарядты иондар:
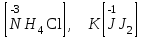
-
Бейтарап атомдар:
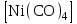
Лиганд бола алатындар:
-
теріс тотығу дәрежесін көрсететін иондар: Cl-, OH-, CN-, NO3-, Br- -
полярлы молекулалар: H2O, NH3, CO, NO, N2H4, μ ≠ 0 -
полярсыз, бірақ оңай поляризацияланатын молекулалар:
H2N – CH2 – CH2 – NH2 (этилендиамин)
Координациялық сан мәндері 2, 3, 4, 5, 6, 7, 8, 9, 12 болуы мүмкін, көптеген қосылыстарда бұл сан 2, 4, 6-ға тең, негізінен кешен түзуші зарядына екі еселі болып келеді.
Кешен түзуші жанынан лигандтардың алатын орнының санына байланысты оларды бір дентантты: J-, Cl-, OH-, NH3-, т.т. және көп дентантты: SO42-, CO32-, PO43- деп бөледі.
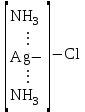
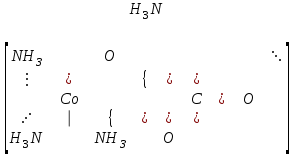
Ag(NH3)2Cl [Co(NH3)4CO3]
Координациялық сан кешен түзуші ионның
а) зарядына:
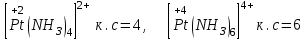
ә) лиганд зарядына:
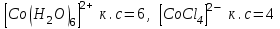
б) орталық ион мен лиганд радиустарының арақатынасына тәуелді.
Коссель-Магнус тәсілі
| rо.и/rлиг | < 0,15 ≥ 0,18 ≥ 0,22 ≥ 0,41 ≥ 0,73 |
| к.с | 2 3 4 6 8 |
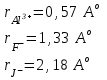
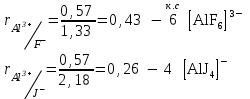
§5 Кешенді қосылыстың құрамдас бөліктерінің зарядтарын анықтау, формулаларын құру алгоритмдері
Кешенді ион зарядын екі тәсілмен анықтайды
1.Сыртқы сферадағы ион зарядына таңбасы жөнінен қарама-қарсы, ал абсолюттік мәндері бірдей болады, себебі қосылыс электробейтарап.
Мысалы:
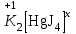
2· (+1) + х = 0
+2 + х = 0
х = -2
2. Ішкі сфераға кіретін иондар зарядтарының алгебралық қосындысына тең болады.
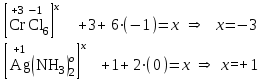
Кешен түзушінің зарядын да екі тәсілмен анықтайды
1.Егер кешенді қосылыс формуласы берілсе, мына ережеге сүйенеді:
Кешенді қосылысты құрайтын бөлшектер зарядының алгебралық қосындысы нольге тең.
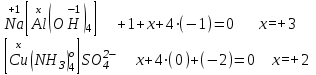
2.Егер кешенді ион заряды белгілі болса, ол құрамдас бөліктерінің зарядтарының қосындысына тең болады деп есептеп анықтауға болады.
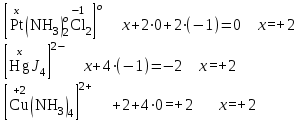
Кешенді қосылыстар формуласын құру алгоритмі
1. Кешен түзушілер таңбаларын, тотығу дәрежелерін көрсетіп жазу.
Pt2+ Cu2+ Fe3+
2.Кешен түзушінің координациялық санын ескеріп, ішкі сфераның формуласын құру:
а) бейтарап кешен формуласын құру үшін кешен түзуші зарядын бейтараптағанша теріс зарядты лигандтарды жазып, соңынан координациялық санын қанықтырғанша бейтарап лигандтар жазу;
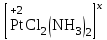
ә) катионды кешен үшін кешен түзуші жанына координациялық санын қанықтырғанша бейтарап лигандтарды жазу;

б) анионды кешен үшін кешен түзуші жанына координациялық санын қанықтырғанша теріс зарядты лигандтарды жазу;
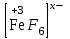
3. Кешенді ионның зарядтарын анықтау:
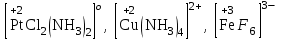
4. Кешенді қосылыстың сыртқы сферасын жазу:

5. Кез келген қосылыс электрбейтарап екендігін ескеріп, қосылыстардың формуласын жазу:
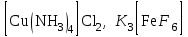
§6 Кешенді қосылыстардың жіктелуі
1)Электр өткізгіштігіне байланысты
а) электролиттер: K4[Fe(CN)6], NH4Cl, т.б.
ә) электролит еместер: [PtCl4(NH3)2]o
2) Кешенді ионның зарядына байланысты.
а) катионды кешенді қосылыстар: [Zn(NH3)4]Cl2
ә) анионды кешенді қосылыстар: K3[FeF6], K3[Al(OH)6]
б) бейтарап кешенді қосылыстар: [Pt(NH3)2Cl2]o, [Fe(CO)5]o
в) бикешенді қосылыстар екі кешенді ионның бірігуінен түзіледі:
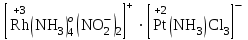
г) көп ядролы кешенді қосылыстар: [(NH3)5Cr – O – Cr(NH3)5]Cl4
3) Функционалдық белгілеріне байланысты.
а) қышқылдар H[BF4], H2[SO4]
ә) негіздер: [Cu(NH3)4](OH)2
б) тұздар: К3[FeF6]
4) Лиганд табиғатына байланысты
а) акво кешенді қосылыстар (L – H2O)
ә) ацидокешенді қосылыстар (L – қышқыл қалдықтары)
б) гидроксокешенді қосылыстар (L – OH-)
в) аммиакаттар (L – NH3)
г) карбонилдер (L – CO)
ғ) полигалидтер (L –
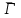 )
)5) Ішкі кешенді қосылыстар (хелаттар)
Мұндай кешенді қосылыстарда лиганд кешен түзушімен екі түрлі механизммен байланыс (алмасу және донорлы-акцепторлы) түзу арқылы топтасады.
H
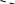 2C – NH2 H2N – CH2
2C – NH2 H2N – CH2 
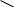
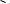 | Cu |
| Cu |
 C –– O O –– C
C –– O O –– C O O
Мыс (ІІ) гликоляты
Ішкі кешенді қосылыстың алынуы және қасиеттерін зерттеуде көп еңбек еткен ғалым – Л.А.Чугаев.
6)Түзілу тәсіліне байланысты
а) қосылу арқылы:
Al(OH)3 + NaOH → Na[Al(OH)
4]
NH3 + HCl → [NH4]Cl
ә) арасына кіру арқылы:
AgCl + 2NH3 → [Ag(NH3)2]Cl
CuSO4 + 4NH3 → [Cu(NH3)4]SO4
§7 Кешенді қосылыстардың изомерлері, аталуы, қолданылуы
Бейорганикалық қосылыстардың ішіндегі күрделі қосылыс болуына байланысты органикалық қосылыстардағы сияқты да әр түрлі изомерлер береді.
-
Кеңістік изомерия -
Сольваттық (гидраттық) изомерия -
Иондық изомерия -
Координациялық изомерия -
Оптикалық изомерия
1.Кеңістік изомерия лигандтар әр түрлі кешенді қосылыстарда лигандтардың кеңістікте орналасуына байланысты болады.
[Pt(NH3)2Cl4]
Cl



Pt




Pt

Cl
NH3
Cl
NH3
Cl
Cl
NH3
Cl
Cl
NH3
Cl
цис-изомер (қызыл сары) транс-изомер (сары)
2.Сольваттық (гидраттық) изомерия кезінде су молекуласының ішкі және сыртқы сфераға таралып орналасуына байланысты.
[Cr(H2O)6]Cl3[Cr(H2O)5Cl]Cl2· H2O [Cr(H2O)4Cl2]Cl· 2H2O
күлгін түсті ашық жасыл түсті жасыл түсті
3.Иондық изомерия кешенді қосылыс құрамында иондардың орналасуына тәуелді болады.

4.Координациялық изомерия бикешенді қосылыстарда байқалады:
[Co(NH3)6][Cr(CN)6], [Cr(NH3)2][Co(CN)6]
5.Оптикалық изомерия органикалық заттар үшін белгілі болған (Л.Пастер), ал кешенді қосылыстардың изомерлі қосылыстарының алғашқы өкілін 1907 жылы А.Вернер зертеулерінен белгілі болды, олар жарықтың поляризациялану жазықтығын әр түрлі бұрады.