Файл: Учебнометодическое пособие Тюмень, 2018 удк 54 н 24. 1 Рецензенты.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.01.2024
Просмотров: 292
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
vоб равна нулю (рис. 3).
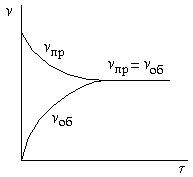
Рисунок 3 – Зависимость скоростей прямой и обратной реакций от времени τ. При равенстве этих скоростей наступает химическое равновесие.
По мере протекания реакции исходные вещества расходуются, и их концентрации падают. Одновременно появляются продукты реакции, их концентрации возрастают. Вследствие этого начинает идти обратная реакция, причем ее скорость постепенно увеличивается. Когда скорости прямой и обратной реакций становятся одинаковыми, наступает химическое равновесие. Оно является динамическим, т.к., хотя концентрации веществ в системе остаются постоянными, реакция продолжает протекать как в прямом, так и в обратном направлении.
При равенстве vпр и vоб можно приравнять их выражения согласно закону действия масс *. Например, для обратимого взаимодействия водорода с иодом:
kпр·[H2]·[I2]=kоб·[HI]2
или
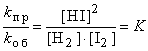
Отношение констант скорости прямой и обратной реакций (K) называется константой равновесия. При постоянной температуре константа равновесия представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов и исходных веществ, которое устанавливается при равновесии. Величина K зависит от природы реагирующих веществ и от температуры.
Система находится в состоянии равновесия до тех пор, пока внешние условия сохраняются постоянными. При увеличении концентрации какого-либо из веществ, участвующих в реакции, равновесие смещается в сторону расхода этого вещества; при уменьшении концентрации какого-либо из веществ равновесие смещается в сторону образования этого вещества.
Когда в реакции участвуют газы, равновесие может нарушаться при изменении давления:
2NO + O2 ⇄ 2NO2
vпр=kпр·[NO]2·[O2]; vоб=kобр·[NO2]2
В связи с этим равновесие при возрастании давления сдвигается в сторону уменьшения числа молекул газов, т.е. в сторону понижения давления. При возрастании температуры равновесие эндотермической реакции смещается вправо, а экзотермических реакций – влево. Оказывается также, что катализатор * не влияет на константу равновесия
, так как он снижает энергию активации * прямой и обратной реакций на одну и ту же величину.
Закономерности, которые проявляются в рассмотренных примерах, представляют собою частные случаи общего принципа, определяющего влияние различных факторов на равновесие системы. Это принцип Ле-Шателье: если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате протекающих в ней процессов равновесие смещается в таком направлении, что оказанное воздействие уменьшится.
Пример: укажите, как повлияет:
а) повышение давления;
б) повышение температуры;
в) увеличение концентрации кислорода на равновесие системы:
2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
Решение:
а) Изменение давления смещает равновесие реакций с участием газообразных веществ (г). Определим объёмы газообразных веществ до и после реакции по стехиометрическим коэффициентам:
По принципу Ле Шателье, при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём, следовательно равновесие сместится вправо, т.е. в сторону образования СО2, в сторону прямой реакции (→).
б) По принципу Ле Шателье, при повышении температуры, равновесие смещается в сторону эндотермической реакции (-Q), т.е. в сторону обратной реакции – реакции разложения СО2 (←), т.к. по закону сохранения энергии:
Q - 2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
в) При увеличении концентрации кислорода равновесие системы смещается в сторону получения СО2 (→) т.к. увеличение концентрации реагентов (жидких или газообразных) смещает в сторону продуктов, т.е. в сторону прямой реакции.
5.3.Вопросы для самоконтроля:
1. Дайте определение понятию скорости химической реакции.
2. Сформулируйте закон действующих масс.
3. Сформулируйте правило Вант-Гоффа.
4. Сформулируйте принцип Ле-Шателье.
5. Факторы, влияющие на смещение химического равновесия.
5.4. Контрольные задания
51-55. Дайте определение понятию скорость химической реакции. Опишите количество (где это можно), как влияют на скорость реакции внешние условия (концентрация, температура, давление). Рассчитайте, во сколько раз изменится скорость реакции при изменении указанных в таблице 7 условий.
Таблица 7
56-60. Чем характеризуется состояние химического равновесия? От каких факторов зависит константа равновесия, положение равновесия? Предскажите в соответствии с принципом Ле-Шателье смещение равновесия при изменении температуры и давления в реакции, соответствующей номеру вашего задания (табл. 8).
Таблица 8
Глава 6.Растворы.
Электролитическая диссоциация. Гидролиз солей.
6.1. Растворы
Растворами называются гомогенные системы, содержащие не менее двух веществ.
В зависимости от агрегатного состояния растворителя различают газообразные, жидкие и твердые растворы.
Газообразными растворами являются воздух и другие смеси газов. К жидким растворам относят гомогенные смеси газов, жидкостей и твердых тел с жидкостями. Твердыми растворами являются многие сплавы, например, металлов друг с другом, стёкла.
Способы выражения концентрации растворов
Концентрацию веществ в растворах можно выразить разными способами. Наиболее часто используют массовую долю растворённого вещества, молярную и нормальную концентрацию.
Массовая доля растворенного вещества w(B) – это безразмерная величина, равная отношению массы растворённого вещества к общей массе раствора m:
w(B)= m(B) / m
Массовую долю растворенного вещества w(B) обычно выражают в долях единицы или в процентах. Например, массовая доля растворённого вещества – CaCl2 в воде равна 0,06 или 6%. Это означает, что в растворе хлорида кальция массой 100 г содержится хлорид кальция массой 6 г и вода массой 94 г.
Пример: Сколько грамм сульфата натрия и воды нужно для приготовления 300 г 5% раствора?
Решение:
m(Na2SO4) = w(Na2SO4) / 100 = (5 · 300) / 100 = 15 г
где w(Na2SO4) – массовая доля в %,
m – масса раствора в г
m(H2O) = 300 г – 15 г = 285 г.
Таким образом, для приготовления 300 г 5% раствора сульфата натрия надо взять 15 г Na2SO4 и 285 г воды.
Молярная концентрация C(B) показывает, сколько моль растворённого вещества содержится в 1 литре раствора.
C(B) = n(B) / V = m(B) / (M(B) · V),
где М(B) - молярная масса растворенного вещества г/моль.
Молярная концентрация измеряется в моль/л и обозначается «M». Например, 2 M NaOH – двухмолярный раствор гидроксида натрия. Один литр такого раствора содержит 2 моль вещества или 80 г (M(NaOH) = 40 г/моль).
Пример: Какую массу хромата калия K2CrO4 нужно взять для приготовления 1,2 л 0,1 М раствора?
Решение:
M(K2CrO4) = C(K2CrO4) · V · M(K2CrO4) = 0,1 моль/л · 1,2 л · 194 г/моль » 23,3 г.
Таким образом, для приготовления 1,2 л 0,1 М раствора нужно взять 23,3 г K2CrO4 и растворить в воде, а объём довести до 1,2 литра.
Концентрацию раствора можно выразить количеством молей растворённого вещества в 1000 г растворителя. Такое выражение концентрации называют моляльностью раствора.
Нормальность раствора обозначает число грамм-эквивалентов данного вещества в одном литре раствора или число миллиграмм-эквивалентов в одном миллилитре раствора.
Грамм – эквивалентом вещества называется количество граммов вещества, численно равное его эквиваленту. Для сложных веществ – это количество вещества, соответствующее прямо или косвенно при химических превращениях 1 грамму водорода или 8 граммам кислорода.
Эоснования = Моснования /число гидроксильных групп
Экислоты = Мкислоты / число атомов водорода
Эсоли = Мсоли / произведение числа катионов на его заряд
Пример: Вычислите значение грамм-эквивалента (г-экв.) серной кислоты, гидроксида кальция и сульфата алюминия.
Э H2SO4 = М H2SO4 / 2 = 98 / 2 = 49 г
Э Ca(OH)2 = М Ca(OH)2 / 2 = 74 / 2 = 37 г
Э Al2(SO4)3 = М Al2(SO4)3 / (2· 3) = 342 / 2= 57 г
Величины нормальности обозначают буквой «Н». Например, децинормальный раствор серной кислоты обозначают «0,1 Н раствор H2SO4». Так как нормальность может быть определена только для данной реакции, то в разных реакциях величина нормальности одного и того же раствора может оказаться неодинаковой. Так, одномолярный раствор H2SO4 будет однонормальным, когда он предназначается для реакции со щёлочью с образованием гидросульфата NaHSO4, и двухнормальным в реакции с образованием Na2SO4.
Пример: Рассчитайте молярность и нормальность 70%-ного раствора H2SO4 (r = 1,615 г/мл).
Решение:
Для вычисления молярности и нормальности надо знать число граммов H2SO4 в 1 л раствора. 70%-ный раствор H2SO4 содержит 70 г H2SO4 в 100 г раствора. Это весовое количество раствора занимает объём:
V = 100 / 1,615 = 61,92 мл
Следовательно, в 1 л раствора содержится 70 · 1000 / 61,92 = 1130,49 г H2SO4
Отсюда молярность данного раствора равна: 1130,49 / М (H2SO4) =1130,49 / 98 =11,53 M
Нормальность этого раствора (считая, что кислота используется в реакции в качестве двухосновной) равна 1130,49 / 49 =23,06 H
Пример:
Какова молярная и нормальная концентрация 12%-ного раствора серной кислоты, плотность которого р = 1,08 г/см3?
Решение:
Мольная масса серной кислоты равна 98. Следовательно,
m (H2SO4) = 98 и э(H2SO4) = 98: 2 = 49.
Подставляя

Рисунок 3 – Зависимость скоростей прямой и обратной реакций от времени τ. При равенстве этих скоростей наступает химическое равновесие.
По мере протекания реакции исходные вещества расходуются, и их концентрации падают. Одновременно появляются продукты реакции, их концентрации возрастают. Вследствие этого начинает идти обратная реакция, причем ее скорость постепенно увеличивается. Когда скорости прямой и обратной реакций становятся одинаковыми, наступает химическое равновесие. Оно является динамическим, т.к., хотя концентрации веществ в системе остаются постоянными, реакция продолжает протекать как в прямом, так и в обратном направлении.
При равенстве vпр и vоб можно приравнять их выражения согласно закону действия масс *. Например, для обратимого взаимодействия водорода с иодом:
kпр·[H2]·[I2]=kоб·[HI]2
или
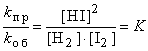
Отношение констант скорости прямой и обратной реакций (K) называется константой равновесия. При постоянной температуре константа равновесия представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов и исходных веществ, которое устанавливается при равновесии. Величина K зависит от природы реагирующих веществ и от температуры.
Система находится в состоянии равновесия до тех пор, пока внешние условия сохраняются постоянными. При увеличении концентрации какого-либо из веществ, участвующих в реакции, равновесие смещается в сторону расхода этого вещества; при уменьшении концентрации какого-либо из веществ равновесие смещается в сторону образования этого вещества.
Когда в реакции участвуют газы, равновесие может нарушаться при изменении давления:
2NO + O2 ⇄ 2NO2
vпр=kпр·[NO]2·[O2]; vоб=kобр·[NO2]2
В связи с этим равновесие при возрастании давления сдвигается в сторону уменьшения числа молекул газов, т.е. в сторону понижения давления. При возрастании температуры равновесие эндотермической реакции смещается вправо, а экзотермических реакций – влево. Оказывается также, что катализатор * не влияет на константу равновесия
, так как он снижает энергию активации * прямой и обратной реакций на одну и ту же величину.
Закономерности, которые проявляются в рассмотренных примерах, представляют собою частные случаи общего принципа, определяющего влияние различных факторов на равновесие системы. Это принцип Ле-Шателье: если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате протекающих в ней процессов равновесие смещается в таком направлении, что оказанное воздействие уменьшится.
Пример: укажите, как повлияет:
а) повышение давления;
б) повышение температуры;
в) увеличение концентрации кислорода на равновесие системы:
2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
Решение:
а) Изменение давления смещает равновесие реакций с участием газообразных веществ (г). Определим объёмы газообразных веществ до и после реакции по стехиометрическим коэффициентам:
По принципу Ле Шателье, при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём, следовательно равновесие сместится вправо, т.е. в сторону образования СО2, в сторону прямой реакции (→).
б) По принципу Ле Шателье, при повышении температуры, равновесие смещается в сторону эндотермической реакции (-Q), т.е. в сторону обратной реакции – реакции разложения СО2 (←), т.к. по закону сохранения энергии:
Q - 2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
в) При увеличении концентрации кислорода равновесие системы смещается в сторону получения СО2 (→) т.к. увеличение концентрации реагентов (жидких или газообразных) смещает в сторону продуктов, т.е. в сторону прямой реакции.
5.3.Вопросы для самоконтроля:
1. Дайте определение понятию скорости химической реакции.
2. Сформулируйте закон действующих масс.
3. Сформулируйте правило Вант-Гоффа.
4. Сформулируйте принцип Ле-Шателье.
5. Факторы, влияющие на смещение химического равновесия.
5.4. Контрольные задания
51-55. Дайте определение понятию скорость химической реакции. Опишите количество (где это можно), как влияют на скорость реакции внешние условия (концентрация, температура, давление). Рассчитайте, во сколько раз изменится скорость реакции при изменении указанных в таблице 7 условий.
Таблица 7
| № задания | Реакция | Изменение температуры | Температурный коэффициент | Изменение давления |
| 1 | 2 | 3 | 4 | 5 |
| 51 | – | уменьшение на 40° | 3 | – |
| 52 | – | увеличение на 30° | 2 | – |
| 53 | H2+Cl2=2HCl | – | – | увеличение в 2 раза |
| 54 | 2Fe+O2=2FeO | – | – | уменьшение в 3 раза |
| 55 | CaO+CO2=CaCO3 | – | – | увеличение в 3 раза |
56-60. Чем характеризуется состояние химического равновесия? От каких факторов зависит константа равновесия, положение равновесия? Предскажите в соответствии с принципом Ле-Шателье смещение равновесия при изменении температуры и давления в реакции, соответствующей номеру вашего задания (табл. 8).
Таблица 8
| № задания | Реакция |
| 1 | 2 |
| 56 | CO2+CaCO3+H20 (пар)⇄Ca(HCO3)2-Q |
| 57 | NH3+H2O⇄NH4OH+Q |
| 58 | N2O4⇄2NO2-Q |
| 59 | 4NH3+5O2⇄4NO+6H2O (пар)+Q |
| 60 | 2CO+O2⇄2CO2+Q |
Глава 6.Растворы.
Электролитическая диссоциация. Гидролиз солей.
6.1. Растворы
Растворами называются гомогенные системы, содержащие не менее двух веществ.
В зависимости от агрегатного состояния растворителя различают газообразные, жидкие и твердые растворы.
Газообразными растворами являются воздух и другие смеси газов. К жидким растворам относят гомогенные смеси газов, жидкостей и твердых тел с жидкостями. Твердыми растворами являются многие сплавы, например, металлов друг с другом, стёкла.
Способы выражения концентрации растворов
Концентрацию веществ в растворах можно выразить разными способами. Наиболее часто используют массовую долю растворённого вещества, молярную и нормальную концентрацию.
Массовая доля растворенного вещества w(B) – это безразмерная величина, равная отношению массы растворённого вещества к общей массе раствора m:
w(B)= m(B) / m
Массовую долю растворенного вещества w(B) обычно выражают в долях единицы или в процентах. Например, массовая доля растворённого вещества – CaCl2 в воде равна 0,06 или 6%. Это означает, что в растворе хлорида кальция массой 100 г содержится хлорид кальция массой 6 г и вода массой 94 г.
Пример: Сколько грамм сульфата натрия и воды нужно для приготовления 300 г 5% раствора?
Решение:
m(Na2SO4) = w(Na2SO4) / 100 = (5 · 300) / 100 = 15 г
где w(Na2SO4) – массовая доля в %,
m – масса раствора в г
m(H2O) = 300 г – 15 г = 285 г.
Таким образом, для приготовления 300 г 5% раствора сульфата натрия надо взять 15 г Na2SO4 и 285 г воды.
Молярная концентрация C(B) показывает, сколько моль растворённого вещества содержится в 1 литре раствора.
C(B) = n(B) / V = m(B) / (M(B) · V),
где М(B) - молярная масса растворенного вещества г/моль.
Молярная концентрация измеряется в моль/л и обозначается «M». Например, 2 M NaOH – двухмолярный раствор гидроксида натрия. Один литр такого раствора содержит 2 моль вещества или 80 г (M(NaOH) = 40 г/моль).
Пример: Какую массу хромата калия K2CrO4 нужно взять для приготовления 1,2 л 0,1 М раствора?
Решение:
M(K2CrO4) = C(K2CrO4) · V · M(K2CrO4) = 0,1 моль/л · 1,2 л · 194 г/моль » 23,3 г.
Таким образом, для приготовления 1,2 л 0,1 М раствора нужно взять 23,3 г K2CrO4 и растворить в воде, а объём довести до 1,2 литра.
Концентрацию раствора можно выразить количеством молей растворённого вещества в 1000 г растворителя. Такое выражение концентрации называют моляльностью раствора.
Нормальность раствора обозначает число грамм-эквивалентов данного вещества в одном литре раствора или число миллиграмм-эквивалентов в одном миллилитре раствора.
Грамм – эквивалентом вещества называется количество граммов вещества, численно равное его эквиваленту. Для сложных веществ – это количество вещества, соответствующее прямо или косвенно при химических превращениях 1 грамму водорода или 8 граммам кислорода.
Эоснования = Моснования /число гидроксильных групп
Экислоты = Мкислоты / число атомов водорода
Эсоли = Мсоли / произведение числа катионов на его заряд
Пример: Вычислите значение грамм-эквивалента (г-экв.) серной кислоты, гидроксида кальция и сульфата алюминия.
Э H2SO4 = М H2SO4 / 2 = 98 / 2 = 49 г
Э Ca(OH)2 = М Ca(OH)2 / 2 = 74 / 2 = 37 г
Э Al2(SO4)3 = М Al2(SO4)3 / (2· 3) = 342 / 2= 57 г
Величины нормальности обозначают буквой «Н». Например, децинормальный раствор серной кислоты обозначают «0,1 Н раствор H2SO4». Так как нормальность может быть определена только для данной реакции, то в разных реакциях величина нормальности одного и того же раствора может оказаться неодинаковой. Так, одномолярный раствор H2SO4 будет однонормальным, когда он предназначается для реакции со щёлочью с образованием гидросульфата NaHSO4, и двухнормальным в реакции с образованием Na2SO4.
Пример: Рассчитайте молярность и нормальность 70%-ного раствора H2SO4 (r = 1,615 г/мл).
Решение:
Для вычисления молярности и нормальности надо знать число граммов H2SO4 в 1 л раствора. 70%-ный раствор H2SO4 содержит 70 г H2SO4 в 100 г раствора. Это весовое количество раствора занимает объём:
V = 100 / 1,615 = 61,92 мл
Следовательно, в 1 л раствора содержится 70 · 1000 / 61,92 = 1130,49 г H2SO4
Отсюда молярность данного раствора равна: 1130,49 / М (H2SO4) =1130,49 / 98 =11,53 M
Нормальность этого раствора (считая, что кислота используется в реакции в качестве двухосновной) равна 1130,49 / 49 =23,06 H
Пример:
Какова молярная и нормальная концентрация 12%-ного раствора серной кислоты, плотность которого р = 1,08 г/см3?
Решение:
Мольная масса серной кислоты равна 98. Следовательно,
m (H2SO4) = 98 и э(H2SO4) = 98: 2 = 49.
Подставляя