Файл: Отчет по лабораторной работе 3 По дисциплине Физика.docx
Добавлен: 12.01.2024
Просмотров: 47
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Министерство науки и высшего образования Российской Федерации

Федеральное государственное бюджетное образовательное учреждение высшего образования
Санкт-Петербургский горный университет
Отчет по лабораторной работе № 3
По дисциплине: Физика____________________________
(наименование учебной дисциплины согласно учебному плану)
Тема: Термодинамика. Политропный процесс
Автор: студент гр. ПЭ-22 ________________ /Пономарев Л.С. /
(подпись) (Ф.И.О.)
Дата: ___________________
Проверил: ____________ / /
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2022
Цель работы – изучить законы идеального газа, основные положения классической теории теплоёмкости и определить показатель адиабаты методом Клемана-Дезорма.
Краткое теоретическое содержание
Явление, изучаемое в работе – Адиабатический процесс
Определения:
Адиабатическим называется процесс, протекающий без теплообмена с внешней средой.
Адиабата - график зависимости между параметрами состояния идеального газа при ∆Q=0.
Молярной теплоёмкостью называется скалярная физическая величина, характеризующая количество теплоты, которое нужно затратить для изменения температуры одного моля вещества на один Кельвин.
Законы и соотношения, на основании которых выведена расчетная формула:
Уравнение состояния идеального газа (уравнение Менделеева
-Клапейрона)
PV=vRT,
где P(Па) - давление, V – (
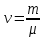 (моль) – количество вещества
(моль) – количество вещества 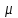 (кг/моль)– молярная масса газа. R – универсальная газовая постоянная,R = 8,31 Дж /(мольК), T(K) - температура.
(кг/моль)– молярная масса газа. R – универсальная газовая постоянная,R = 8,31 Дж /(мольК), T(K) - температура.Уравнение Пуассона
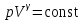 ,
,где γ – показатель политропы.
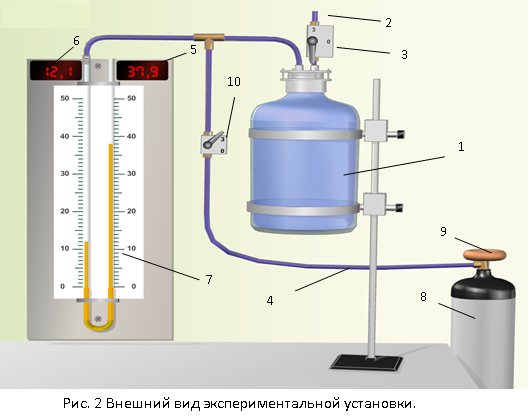 Схема установки:
Схема установки:Установка состоит из стеклянного сосуда 1, баллона 8 с редуктором 9, U–образного жидкостного манометра 7 с цифровыми табло 5 и 6. Баллон заполнен сжатым воздухом. Имеется также два крана – впускной кран 10, служащий для напуска газа в сосуд 1 из баллона 8 по магистрали 4, и выпускной кран 3 для соединения сосуда с атмосферой через магистраль 2.
Основная расчётная формула:
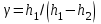 ,
,где h1 и h2 -разности уровней манометра в первом и третьем состоянии.
Формулы для расчета погрешностей косвенных измерений:
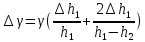
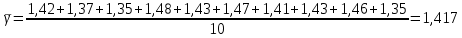
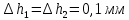
Погрешность прямых измерений:
∆l=0,0001 (м)
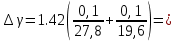 0,01235 мм
0,01235 мм| Физ. величина | h1 | h2 | h1-h2 | γ |
| Ед. измер-я Номер опыта | мм | мм | мм | |
| 1 | 27,8 | 8,2 | 19,6 | 1,46 |
| 2 | 27,4 | 7,4 | 20 | 1,37 |
| 3 | 26,8 | 7 | 19,8 | 1,35 |
| 4 | 26,6 | 8,6 | 18 | 1,43 |
| 5 | 26,7 | 8 | 18,7 | 1,39 |
| 6 | 26,4 | 8,4 | 18 | 1,38 |
| 7 | 27 | 7,8 | 19,2 | 1,38 |
| 8 | 26,4 | 7,2 | 19,2 | 1,40 |
| 9 | 26,8 | 8,4 | 18,4 | 1,34 |
| 10 | 27 | 7 | 20 | 1,47 |
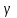 | 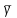 | 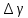 |
| 1,46 | 1.4 | 0,022659806 |
| 1,37 | | 0,014263571 |
| 1,35 | | 0,014118903 |
| 1,43 | | 0,0193 |
| 1,39 | | 0,018521817 |
| 1,38 | | 0,018423029 |
| 1,38 | | 0,018591938 |
| 1,40 | | 0,019 |
| 1,34 | | 0,01767033 |
| 1,47 | | 0,020926068 |
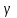 | 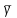 | 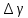 |
| 1,42 | 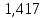 | 0,01235 |
| 1,37 | 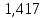 | 0,01185 |
| 1,35 | 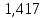 | 0,01254 |
| 1,48 | 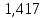 | 0,01379 |
| 1,43 | 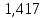 | 0,013 |
| 1,47 | 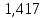 | 0,01373 |
| 1,41 | 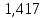 | 0,01257 |
| 1,43 | 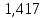 | 0,01286 |
| 1,46 | 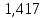 | 0,01338 |
| 1,35 | 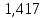 | 0,01175 |
Окончательный результат:
 =1,417±0,013 мм
=1,417±0,013 ммВывод:
В ходе лабораторной работы я рассчитала значение показателя политропы, γ=1,417, что удовлетворяет значению, приведённому в справочнике для двухатомного газа, равному γ теор = 1,4. Результат подтверждает, что методика измерения показателя адиабаты точна.