ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.11.2019
Просмотров: 7159
Скачиваний: 16
86
вода
проходит
через
мембрану
.
Эта
сила
называется
"
осмотическим
давлением
".
Таким
образом
,
осмотическое
давление
возникает
в
растворах
с
разной
концентрацией
,
разделенных
полупроницаемой
мембраной
,
градиент
осмотического
давления
направлен
из
раствора
меньшей
концентрации
в
сторону
раствора
с
большей
концентрацией
1
.
Проделаем
следующий
опыт
.
В
воронку
,
раструб
которой
затянут
бычьим
пузырем
(
бычий
пузырь
обладает
полупроницаемыми
свойствами
–
пропускает
молекулы
воды
и
не
пропускает
молекулы
сахара
),
нальем
слабый
водный
раствор
сахара
и
опустим
в
сосуд
с
чистой
водой
так
,
чтобы
уровни
жидкостей
в
воронке
и
сосуде
совпали
.
Через
некоторое
время
уровень
раствора
в
воронке
начнет
медленно
повышаться
(
см
.
рисунок
34).
Процесс
продолжится
до
тех
пор
,
пока
гидростатическое
давление
столба
жидкости
высотой
h
не
будет
препятствовать
дальнейшему
поступлению
воды
из
сосуда
.
Величина
гидростатического
давления
,
создаваемого
столбом
жидкости
высотой
h,
равна
gh
,
где
g
–
ускорение
свободного
падения
,
−
плотность
жидкости
.
Давление
,
уравновешивающее
гидростатическое
,
называется
осмотическим
давлением
.
Повышение
уровня
раствора
в
воронке
происходит
по
следующей
причине
:
так
как
концентрация
молекул
воды
в
сосуде
больше
концентрации
молекул
воды
в
воронке
,
то
через
полупроницаемую
перегородку
диффундируют
молекулы
воды
из
сосуда
в
воронку
.
Молекулы
же
сахара
не
могут
перейти
из
воронки
в
сосуд
.
Пусть
молярная
концентрация
молекул
сахара
в
сосуде
равна
нулю
,
а
в
воронке
С
.
Избыточная
концентрация
молекул
сахара
и
создаст
парциальное
давление
растворенного
вещества
,
уравновешиваемое
гидростатическим
давлением
ρ
gh
.
Так
как
осмотическое
давление
есть
результат
бомбардировки
полупроницаемой
мембраны
молекулами
растворенного
вещества
(
рисунок
35),
то
величина
осмотического
давления
может
быть
рассчитана
по
формуле
идеального
газа
:
RT CRT
V
,
где
−
число
молей
растворенного
вещества
,
V
–
1
Здесь
термин
«
градиент
осмотического
давления
»
используется
в
нетрадиционной
,
медицинской
трактовке
(
пояснения
см
.
в
разделе
«
Простая
диффузия
»).
87
объем
раствора
,
С
–
молярная
концентрация
раствора
.
Применение
теории
идеального
газа
к
растворам
позволило
химику
Вант
-
Гоффу
получить
прекрасные
результаты
для
растворов
многих
веществ
.
Однако
для
растворов
некоторых
веществ
полученные
результаты
между
измеренными
и
расчетными
значениями
осмотических
давлений
давали
расхождение
в
2
и
более
раз
.
Осмысление
возможных
причин
такого
расхождения
между
теорией
и
практикой
привело
ученого
С
.
Аррениуса
к
открытию
явления
диссоциации
.
Единомышленник
Вант
-
Гоффа
шведский
исследователь
С
.
Аррениус
догадался
,
что
если
измеренное
осмотическое
давление
раствора
поваренной
соли
в
два
раза
больше
расчетного
,
то
и
число
частиц
в
растворе
в
два
раза
больше
,
чем
молекул
NaCl.
Следовательно
,
величина
осмотического
давления
прямо
пропорциональна
молярной
концентрации
растворенного
в
растворителе
вещества
,
которое
лишено
возможности
участвовать
в
диффузии
вследствие
наличия
полупроницаемой
мембраны
,
и
температуре
раствора
:
iCRT
,
где
множитель
i
учитывает
процессы
возможного
распада
(
диссоциации
)
молекул
в
растворе
.
Для
растворов
неэлектролитов
i = 1
,
при
диссоциации
молекул
электролитов
на
ионы
i > 1
,
при
ассоциации
i < 1
.
Растворы
с
одинаковыми
осмотическими
давлениями
называют
изотоническими
.
Физиологические
растворы
должны
быть
изотоническими
относительно
внутренних
жидкостей
организма
−
в
противном
случае
происходит
либо
обезвоживание
,
либо
пересыщение
организма
водой
.
Если
один
раствор
по
сравнению
с
другим
имеет
более
высокое
осмотическое
давление
,
его
называют
гипертоническим
,
а
имеющий
меньшее
давление
−
Рисунок
35.
Бомбарди
-
ровка
мембраны
моле
-
кулами
растворённого
вещества
88
гипотоническим
.
Осмотическое
давление
крови
человека
составляет
7,6 10
5
– 7,8 10
5
Па
.
Такое
же
осмотическое
давление
имеет
физиологический
раствор
,
т
.
е
.
0,86%
раствор
NaCl
.
Для
сравнения
нормальное
атмосферное
давление
равно
10
5
Па
.
Осмотическое
давление
в
клетках
с
/
х
животных
составляет
(6,8-
7,3)10
5
Па
,
и
оно
создает
так
называемый
тургор
клетки
,
придает
ей
определенную
форму
.
Основная
часть
осмотического
давления
обусловлена
растворенными
в
плазме
крови
или
в
цитоплазме
солями
,
но
часть
его
определяется
содержащимися
в
них
белками
(
альбумин
,
глобулин
и
др
.)
и
называется
онкотическим
давлением
.
Несмотря
на
его
малую
величину
,
оно
играет
важную
роль
в
распределении
воды
между
тканями
и
кровью
.
Если
клетка
организма
граничит
с
концентрированным
водным
раствором
вещества
,
для
которого
мембрана
клетки
непроницаема
,
то
вода
переходит
из
клетки
в
этот
раствор
.
Происходит
осмотическое
высасывание
воды
из
клетки
.
Им
,
в
частности
,
обусловлено
чувство
жажды
,
возникающее
при
приеме
сладкой
пищи
.
В
крови
позвоночных
животных
находится
специальный
белок
–
сывороточный
альбумин
,
который
поддерживает
постоянное
осмотическое
давление
в
кровеносной
системе
.
Шок
при
сильных
кровотечениях
обусловлен
не
столько
потерей
крови
,
сколько
резким
падением
осмотического
давления
,
ведущим
к
клеточному
коллапсу
.
Поэтому
при
больших
потерях
крови
необходимо
ввести
заменители
крови
,
благодаря
которым
восстанавливается
осмотическое
давление
.
6.
Активный
транспорт
ионов
.
Механизм
активного
транспорта
вещества
на
примере
натрий
-
калиевого
насоса
Пассивный
транспорт
стремится
выровнять
величины
осмотических
давлений
,
концентраций
,
электрических
потенциалов
по
разные
стороны
мембраны
,
т
.
е
.
свести
к
нулю
величины
этих
градиентов
.
Если
бы
в
клетках
существовал
89
только
пассивный
транспорт
,
то
рано
или
поздно
концентрации
,
давления
и
другие
величины
вне
и
внутри
клетки
сравнялись
бы
.
Следовательно
,
существует
другой
механизм
,
работающий
в
направлении
против
электрохимического
градиента
и
происходящий
с
затратой
энергии
клеткой
.
Перенос
молекул
и
ионов
против
электрохимического
градиента
,
осуществляемый
клеткой
за
счет
энергии
метаболических
процессов
,
называют
активным
транспортом
.
Активный
транспорт
присущ
только
биологическим
мембранам
.
Активный
перенос
вещества
через
мембрану
против
соответствующих
градиентов
происходит
за
счет
свободной
энергии
,
высвобождающейся
в
ходе
химических
реакций
внутри
клетки
.
У
высших
организмов
(
например
у
человека
)
такие
активные
процессы
используют
значительную
часть
потребляемой
организмом
энергии
–
примерно
30-40%
.
Активный
транспорт
в
организме
создает
градиенты
концентраций
,
электрических
потенциалов
,
давлений
и
т
.
д
.,
то
есть
поддерживает
жизнь
в
организме
.
В
настоящее
время
более
или
менее
изучены
три
основные
системы
активного
транспорта
,
которые
обеспечивают
перенос
ионов
натрия
,
калия
,
кальция
и
водорода
через
мембрану
.
Существует
также
активный
перенос
ионов
кальция
,
сахаров
,
аминокислот
,
нуклеотидов
,
но
кинетика
этих
процессов
исследована
недостаточно
.
Не
обнаружено
активного
переноса
анионов
,
которые
,
очевидно
,
попадают
внутрь
клетки
путем
пассивного
переноса
.
Тем
не
менее
,
анионы
,
в
особенности
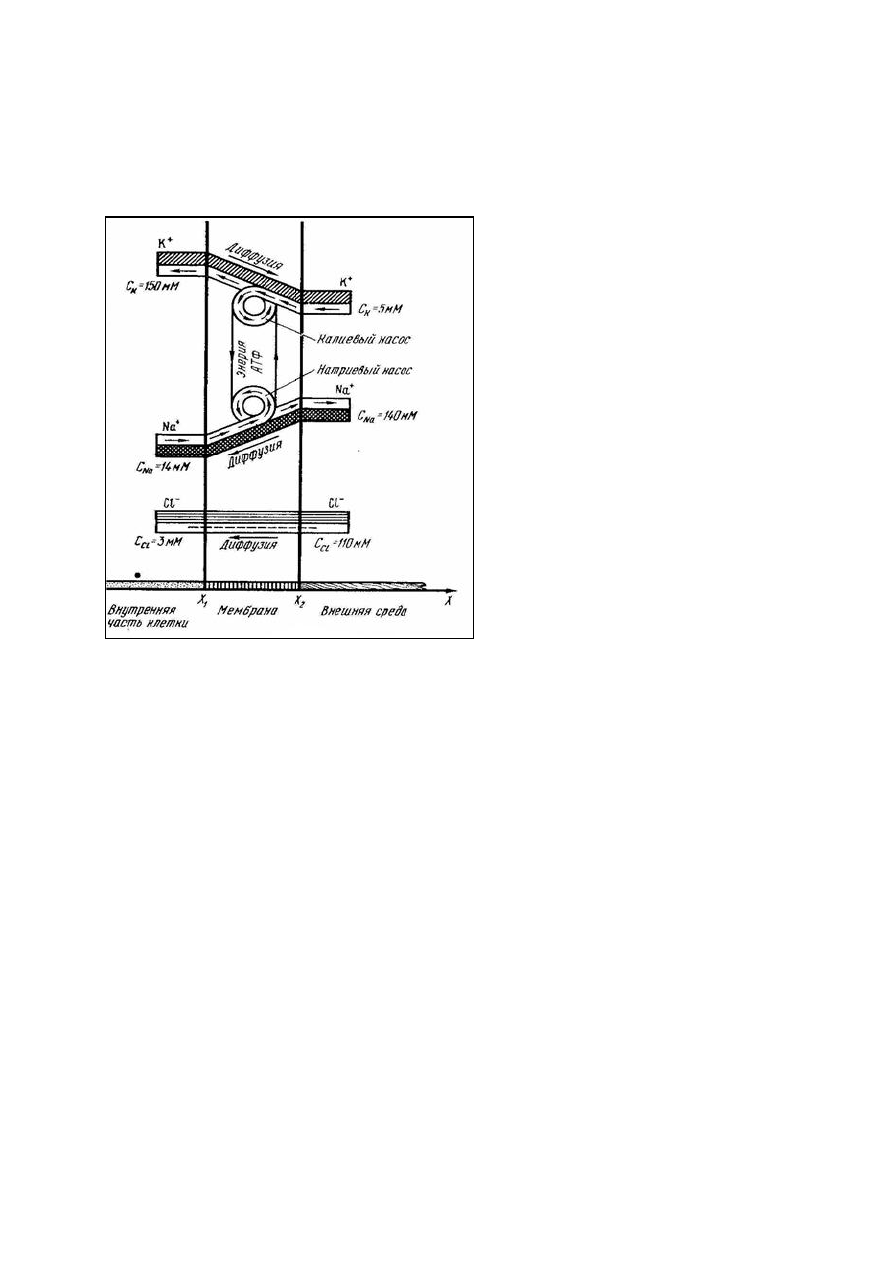
Рисунок
36.
Механизм
работы
Na-K
насоса
90
ионы
хлора
,
играют
значительную
роль
в
жизни
клетки
.
Рассмотрим
механизм
активного
транспорта
на
примере
натрий
-
калиевого
насоса
.
Ионы
К
+
и
Na
+
неравномерно
распределены
по
разные
стороны
мембраны
:
концентрация
ионов
Na
+
снаружи
больше
,
чем
концентрация
ионов
К
+
,
тогда
как
внутри
клетки
концентрация
ионов
К
+
больше
,
чем
ионов
Na
+
(
см
.
рисунок
36).
Эти
ионы
диффундируют
через
мембрану
по
направлению
электрохимического
градиента
,
что
приводит
к
его
выравниванию
.
Очевидно
,
что
если
бы
не
было
противодействия
этим
процессам
со
стороны
механизма
натрий
-
калиевого
насоса
,
то
по
разные
стороны
мембраны
создалась
бы
обратная
разность
концентраций
.
Натрий
-
калиевые
насосы
входят
в
состав
цитоплазматических
мембран
и
работают
за
счет
энергии
гидролиза
молекул
АТФ
с
образованием
молекул
АДФ
и
неорганического
фосфата
Ф
н
:
АТФ
=
АДФ
+
Ф
н
Натрий
-
калиевый
насос
работает
обратимо
:
градиенты
концентраций
ионов
способствуют
синтезу
молекул
АТФ
из
молекул
АДФ
и
Ф
н
:
АДФ
+
Ф
н
=
АТФ
Натрий
-
калиевый
насос
переносит
из
клетки
во
внешнюю
среду
три
иона
натрия
в
обмен
на
перенос
двух
ионов
калия
внутрь
клетки
.
На
кинетику
натрий
-
калиевого
насоса
могут
оказывать
влияние
некоторые
вещества
.
Например
,
под
действием
цианистого
калия
натрий
перестает
откачиваться
из
клетки
,
его
концентрация
внутри
нервных
клеток
и
волокон
возрастает
,
клетки
перестают
проводить
нервные
импульсы
и
это
приводит
к
смерти
живого
организма
.
7. C
пособы
проникновения
веществ
через
биологические
мембраны
Одной
из
важнейших
характеристик
клеточных
мембран
является
избирательная
проницаемость
.
КМ
избирательно
снижает
скорость
передвижения
молекул
в
клетку
и
из
нее
.
Она
определяет
,
каким
молекулам
можно
проникнуть
в
клетку
,
а