ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 02.12.2019
Просмотров: 881
Скачиваний: 1
Реализация того или иного агрегатного состояния вещества зависит главным образом от температуры и давления, при которых оно находится.
Т.о. можно отметить, что в газообразном состоянии атомы расположены хаотически, в жидком состоянии имеют близкий порядок в расположении атомов, а в кристаллическом состоянии имеется и ближний и дальний порядок в расположении атомов.
П
Рисунок
1- Кристаллографическая плоскость
Это обуславливает то, что в кристалле каждый атом имеет одно и тоже ближайшее количество атомов – соседей, расположенных на Одинаковом расстоянии.
Кристаллическая решетка – это неоднократное повторение кристаллографической плоскости во всех направлениях.
Кристаллическую решетку можно «построить», выбрав для этого определенный «строительный блок» (аналогично постройке стены из кирпичей) и многократно смещая этот блок по трем непараллельным направлениям. Такая «строительная» единица кристаллической решетки имеет форму параллелепипеда и называется элементарной ячейкой. Все элементарные ячейки, составляющие кристаллическую решетку, имеют одинаковую форму и объемы. Атомы могут располагаться как в вершинах элементарной ячейки, так и в других ее точках (в узлах кристаллической решетки). В первом случае элементарные ячейки называются простыми (примитивными), во втором — сложными. Если форма элементарной ячейки определена и известно расположение всех атомов внутри нее, то имеется полное геометрическое описание кристалла, т.е. известна его атомно-кристаллическая структура.
В кристаллографии рассматривают 14 типов элементарных ячеек. Их называют пространственными решетками Бравэ. Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки а, Ь, с и три угла между ними. Эти величины называются параметрами элементарной ячейки (кристаллической решетки). Все 14 решеток Бравэ распределены по семи кристаллическим системам (сингониям) в соответствии с ориентацией и относительными величинами параметров решетки (рис. 2). Каждая кристаллическая система включает одну или несколько типов пространственных кристаллических решеток. В простой решетке атомы располагаются только по вершинам решетки, в объемноцентри-рованной еще один атом в центре решетки, в гранецентрированной еще по одному атому в центре каждой грани, и в базоцентрированной еще по одному атому в центрах пары параллельных граней.
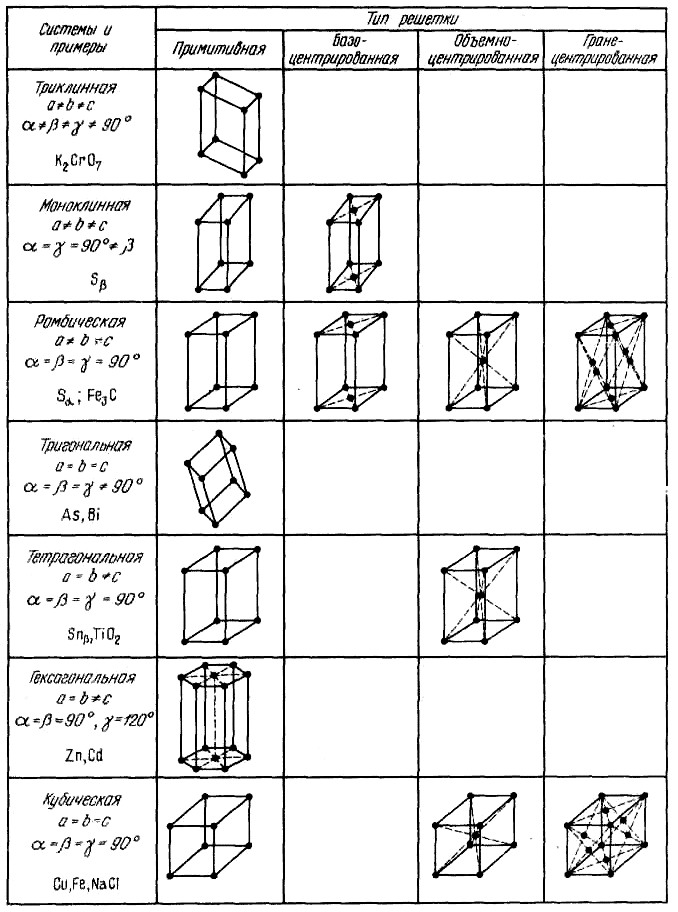
Рисунок 2 – Основные типы кристаллических решеток и их характеристики
Наиболее распространенными среди металлов являются гексагональная плотноупакованная решетка (ГПУ) –Mg, Zn, Co, Ti; гранецентрированная кубическая решетка (ГЦК) – Fe, Ni, Cu, Al, Pb, Ag, Au; объемно-центрированная кубическая решетка (ОЦК) – Fe, Cr, W, V, Mo (рисунок 3).
Компактность структуры является одним из факторов, уменьшающим свободную энергию твердого тела, т. е. обеспечивающим его равновесное состояние и следствием особенностей электронной структуры металлов и характером их межатомного взаимодействия. Поэтому основной характеристикой кристаллической решетки является координационное число. За координационное число принято число ближайших соседей данного атома, находящихся от него на одинаково близком расстоянии.
Рисунок 3- Основные виды кристаллических решеток и расположение в них атомов.
Точечное расположение атомов в кристаллических решетках, приведенных на рисунке 3, является условным, так как в действительности атомы имеют определенный размер и могут соприкасаться друг
с другом. Для характеристики величины атома служит атомный радиус, под которым понимается половина расстояния между ближайшими соседними атомами. Параметры элементарной ячейки а, Ь, с и атомные радиусы измеряются в ангстремах (1Å – 10-8 см). Параметры решетки металлов (их также называют периодами решетки) находятся в пределах 0,2—6,7 Å и определяются методом рентгеноструктурного анализа с точностью до третьего, а при необходимости и до четвертого или даже пятого знака после запятой.
Реальное строение металлических кристаллов
Обычно кусок металла состоит из скопления большого числа маленьких кристаллов неправильной формы, называемых зернами. Кристаллические решетки в отдельных зернах ориентированы относительно друг друга случайным образом (в некоторых случаях, например, при холодной прокатке, наблюдается преимущественная ориентировка зерен — текстура. Поверхности раздела зерен называются границами зерен. Такой кусок металла является поликристаллом. При определенных условиях, обычно при очень медленном контролируемом отводе тепла при кристаллизации (затвердевании металла), может быть получен кусок металла, представляющий собой один кристалл, его называют монокристаллом. В настоящее время в лабораториях выращивают монокристаллы массой в несколько сот грамм и более.
Встречающиеся в природе кристаллы, как монокристаллы, так и зерна в поликристаллах, никогда не обладают такой строгой периодичностью в расположении атомов, о которой говорилось выше, т. е. не являются «идеальными» кристаллами. В действительности «реальные» кристаллы содержат те или иные несовершенства (дефекты) кристаллического строения.
Дефекты в кристаллах принято классифицировать по характеру их измерения в пространстве на точечные (нульмерные), линейные (одномерные), поверхностные (двухмерные), объемные (трехмерные). Точечными дефектами называются такие нарушения периодичности кристаллической решетки, размеры которых во всех измерениях сопоставимы с размерами атома. К точечным дефектам относят вакансии (узлы в кристаллической решетке, свободные от атомов), межузельные атомы (атомы, находящиеся вне узлов кристаллической решетки), а также примесные атомы, которые могут или замещать атомы основного металла (примеси замещения), или внедряться в наиболее свободные места решетки (поры или междоузлия) аналогично межузельным атомам (примеси, внедрения) (рисунок 4).
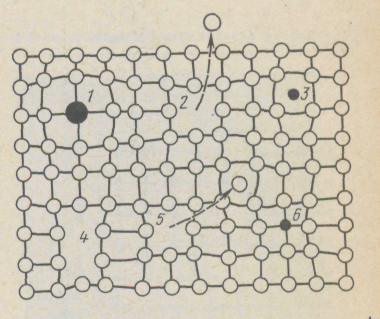
Рисунок 4 – Точечные дефекты: 1 – примесный атом замещения;
2 – вакансия по Шоттки;
3 – примесный атом внедрения;
4 – дивакансия;
5 – вакансия по Френкелю;
6 – примесный атом замещения
При переходе атома из равновесного положения (узла) в междоузлие возникает пара вакансия — межузельный атом, которая называется дефектом Френкеля, а если атом из своего узла выходит на поверхность кристалла, то образующийся дефект называется дефектом Шоттки, Точечные дефекты являются центрами локальных искажений в кристаллической решетке. Однако заметные смещения атомов, окружающих вакансию или межузельный атом создаются только на расстоянии нескольких атмоных диаметров от центра дефекта и быстро убывают по мере удаления от дефекта.
Точечные дефекты, хотя и требуют определенной затраты энергии для образования, являются термодинамически равновесными, т. е. всегда присутствуют в кристалле. Это связано с тем, что точечные дефекты повышают энтропию системы.
Линейные дефекты в кристаллах характеризуются тем, что их поперечные размеры не превышают нескольких межатомных расстояний, а длина может достигать размера кристалла. К линейным дефектам относятся дислокации — линии, вдоль и вблизи которых нарушено правильное периодическое расположение атомных плоскостей кристалла. Различают краевую и винтовую дислокации (рисунок 5). Краевая дислокация представляет собой границу неполной атомной плоскости (экстраплоскости). Винтовую дислокацию можно определить как сдвиг одной части кристалла относительно другой.
Рисунок 5 – Схема краевой (линейной дислокации)
Дислокации не могут обрываться внутри кристалла — они должны быть либо замкнутыми, либо выходить на поверхность кристалла. Дислокации создают в кристалле вокруг себя поля упругих напряжений, убывающих обратно пропорционально расстоянию от них. Наличие упругих напряжений вокруг дислокаций приводит к их взаимодействию, которое зависит от типа дислокаций. Под действием внешних напряжений дислокации двигаются (скользят), что определяет дислокационный механизм пластической деформации. Перемещение дислокации в плоскости скольжения сопровождается разрывом и образованием вновь межатомных связей только у линии дислокации, поэтому пластическая деформация может протекать при малых внешних напряжениях, гораздо меньших тех, которые необходимы для пластической деформации идеального кристалла путем разрыва всех межатомных связей в плоскости скольжения. Обычно дислокации возникают при образовании кристалла из расплава.
Под поверхностными (двумерными) дефектами понимают такие нарушения в кристаллической решетке, которые обладают большой протяженностью в двух измерениях и протяженностью лишь в нескольких межатомных расстояниях в третьем измерении. К ним относятся дефекты упаковки, двойниковые границы, границы зерен и внешние поверхности кристалла. Под дефектами упаковки подразумевают локальные изменения расположения плотноупакованных плоскостей в кристалле.
Полиморфизм (аллотропия)
Как видно из первого раздела лекции некоторые металлы могут иметь несколько видов кристаллических решеток (железо, кобальт, олово, титан) Такое явление называется полиморфизмом или аллотропией.
Более точно можно сказать, что полиморфизм это способность металла менять тип кристаллической решетки при изменении температуры или давления.
Полиморфизм дает возможность кардинально изменять свойства металла при изменении внешних факторов, что позволяет в частности проводить для этих металлов термическую обработку. Аллотропические формы металлов приведены в таблице 1.
Таблица 1 – Аллотропические формы металлов
|
Металл |
Тип решетки |
Температурный интервал |
Аллотропическая форма |
|
Fe |
ОЦК ГЦК ОЦК |
Менее 911°С 911 – 1392°С 1392 - 1539°С |
α γ δ |
|
Co |
ГПУ ГЦК |
Менее 477°С 477 - 1490°С |
α β |
|
Sn |
Алмазная Тетрагональная |
Менее 13°С 13 - 232°С |
α β |
|
Ti |
ГПУ ОЦК |
Менее 882°С 882 - 1668°С |
α β |
ЛЕКЦИЯ 4
ПРОЦЕСС КРИСТАЛЛИЗАЦИИ МЕТАЛЛОВ ИСПЛАВОВ
При переходе из жидкого состояния в твердое образуется кристаллическая решетка, возникают кристаллы. Такой процесс называется кристаллизацией.
Чем объясняется существование при одних температурах жидкого, а при других температурах твердого состояния и почему превращение происходит при строго определенных температурах?
В природе все самопроизвольно протекающие превращения, а следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии.
Поясним примером.
Тяжелый шарик из положения 1 (рисунок 4.1) стремится попасть в более устойчивое положение 2, так как потенциальная энергия в положении 2 меньше, чем в положении 1.
Рисунок 4.1 – Перемещение шарика из неустойчивого в энергетически устойчивое состояние.
Энергетическое состояние системы, имеющей огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией F, называемой свободной энергией (свободная энергия F = V — TS, где U — внутренняя энергия системы; Т — абсолютная температура; S — энтропия). Можно сказать, что чем больше свободная энергия системы, тем система менее устойчива, и если имеется возможность, то система переходит в состояние, где свободная энергия меньше («подобно» шарику, который скатывается из положения 1 в положение 2, если на пути нет препятствия).
С изменением внешних условий, например температуры, свободная энергия системы изменяется по сложному закону, но различно для жидкого и кристаллического состояний. Схематически характер изменения свободной энергии жидкого и твердого состояний с температурой показан на рисунке 4.2.
Выше температуры Ts меньшей свободной энергией обладает вещество в жидком состоянии, ниже Ts — вещество в твердом состоянии. Следовательно, выше Ts вещество должно находиться в жидком состоянии, а ниже Тs, — в твердом, кристаллическом.
Очевидно, что при температуре, равной Ts, свободные энергии жидкого и твердого состояний равны, металл в обоих состояниях находится в равновесии. Эта температура Ts и есть равновесная или теоретическая температура кристаллизации.
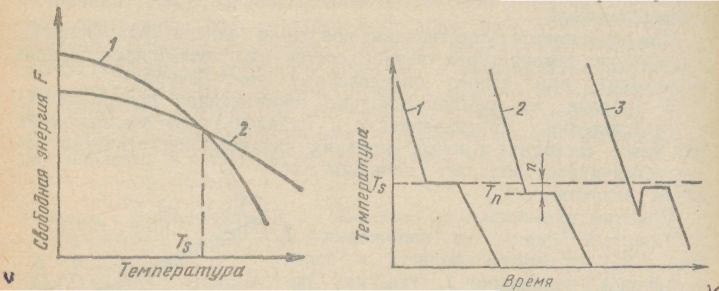
Рисунок 4.2 – Изменение свободной энергии жидкого (1) и кристаллического (2) состояния в зависимости от температуры (а); кривые охлаждения при кристаллизации (б).
Однако при Ts не может происходить процесс кристаллизации (плавление), так как при данной температуре Fж = Fтв и процесс охлаждения при кристаллизации (плавления) не может идти, так как при равенстве обеих фаз это не будет сопровождаться уменьшением свободной энергии.
Для начала кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Из кривых, приведенных на рисунке 4.2 видно, что это возможно только тогда, когда жидкость будет охлаждена ниже точки Тs. Температура, при которой практически начинается кристаллизация, может быть названа фактической температурой кристаллизации.
Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением.
Указанные причины обусловливают и то, что обратное превращение из кристаллического состояния в жидкое может произойти только выше температуры Тs - это явление называется перенагреванием.
Величиной или степенью переохлаждения называют разность между теоретической и фактической температурами кристаллизации.
Если, например, теоретическая температура кристаллизации сурьмы равна 631°С, а до начала процесса кристаллизации жидкая сурьма была переохлаждена до 590°С и при этой температуре закристаллизовалась, то степень переохлаждения определяется разностью 631 —590 =41°С.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время — температура (рисунок 4.2.б).
Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры и может быть названо простым охлаждением, так как при этом нет качественного изменения состояния.
При достижении температуры кристаллизации на кривой температура — время появляется горизонтальная площадка (кривая 1, рисунок 4.2.б.), так как отвод тепла компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации. По окончании кристаллизации, т. е. после полного перехода в твердое состояние, температура снова начинает снижаться, и твердое кристаллическое вещество охлаждается. Теоретически процесс кристаллизации изображается кривой 1. Кривая 2 показывает реальный процесс кристаллизации. Жидкость непрерывно охлаждается до температуры переохлаждения Тn, лежащей ниже теоретической температуры кристаллизации Тs. При охлаждении ниже температуры Тs создаются энергетические условия, необходимые для протекания процесса кристаллизации.
У некоторых металлов из-за большого переохлаждения скрытая теплота плавления выделяется в первый момент кристаллизации настолько бурно, что температура скачкообразно повышается, приближается к теоретической (кривая 3, рисунок 4.2.б.). Так кристаллизуется, например, сурьма.
Чем больше скорость охлаждения, тем больше величина переохлаждения. Для того, чтобы полностью переохладить металл в жидком состоянии требуются большие скорости охлаждения (миллионы и даже миллиарды градусов в секунду), охлаждение жидкого металла до комнатной температуры следует проводить так, чтобы получить переохлажденный жидкий металл (т. е. металл, не имеющий кристаллического строения) за ничтожную долю секунды. Такой металл называется аморфным или металлическим стеклом, который начинает применяться на практике.
Механизм процесса кристаллизации
Еще в 1878 г. Д. К. Чернов, изучая структуру литой стали, указал, что процесс кристаллизации состоит из двух элементарных процессов. Первый процесс заключается в зарождении мельчайших частиц кристаллов, которые Чернов называл «зачатками», а теперь их называют зародышами, или центрами кристаллизации. Второй процесс состоит в росте кристаллов из этих центров.
Систематическое исследование процесса образования центров кристаллизации и их роста вначале на прозрачных органических веществах, а затем и металлах было проведено Г. Тамманом. Им установлена в общем виде зависимость между числом центров кристаллизации, скоростью роста и степенью переохлаждения. Однако более поздние исследования процессов кристаллизации, особенно исследования А. А. Бочвара, К. П. Бунина и др., показали ограниченное значение схемы Г. Таммана для процесса кристаллизации реальных жидких металлов, поскольку они содержат нерастворенные (взвешенные) частицы, служащие центрами кристаллизации. Все же многие закономерности, установленные Тамманом на основе его опытов, нашли качественное подтверждение в последующих работах и оказываются полезными при анализе процессов кристаллизации.
Процесс
образования кристаллов путем зарождения
центров кристаллизации и их роста можно
изучать с помощью рассмотрения моделей
(схем),
что с успехом применялось И. Л. Миркиным.
Подобная модель кристаллизации
представлена на рисунке 4.3. Предположим,
что на площади, изображенной на рисунке
4.3. за секунду возникает пять зародышей,
которые растут с определенной скоростью.
К концу первой

Рисунок 4.3 - Модель процесса кристаллизации
секунды образовалось пять зародышей, к концу второй секунды они выросли и одновременно с этим возникло еще пять новых зародышей будущих кристаллов. Так, в результате возникновения зародышей и их роста происходит процесс кристаллизации, который, как видно в данном примере, заканчивается на седьмой секунде.
Качественная схема процесса кристаллизации, изображенная на рисунке 4.3, может быть представлена количественно кинетической кривой (рисунок 4.4).
Рассмотрение подобных схем кристаллизации позволяет объяснить два важных момента:
1. По мере развития процесса кристаллизации в нем участвует все большее и большее число кристаллов. Поэтому процесс вначале ускоряется, пока в какой-то момент взаимное столкновение растущих кристаллов не начинает заметно препятствовать их росту; рост кристаллов замедляется, тем более, что и жидкости, в которой образуются новые кристаллы, становится все меньше.
2. В процессе кристаллизации, пока кристалл окружен жидкостью, он часто имеет правильную форму, но при столкновении и срастании кристаллов их правильная форма нарушается, внешняя форма кристалла оказывается зависимой от условий соприкосновения растущих кристаллов. Вот почему кристаллы металла, зерна (кристаллиты) не имеют правильной формы.
Скорость всего процесса кристаллизации количественно определяется двумя величинами: скоростью зарождения центров кристаллизации и скоростью роста кристаллов. Обе эти величины можно измерить для разных условий кристаллизации.
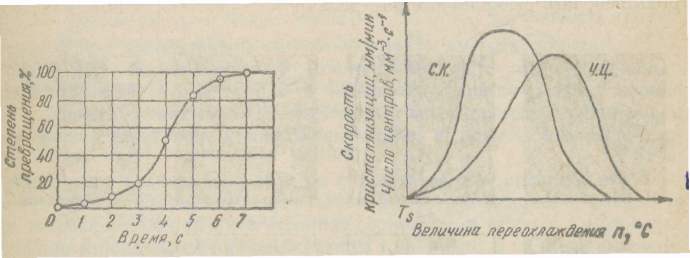
Рисунок 4.4 – Кинетическая кривая кристаллизации (а); Скорость роста кристаллов (с.к.) и скорость хзарождения центров кристаллизации (ч.ц.) в зависимости от степени переохлаждения (б).
Число зарождающихся в единицу времени кристаллов, которые в дальнейшем мы будем обозначать буквами ч. ц., имеет размерность 1/мм3-с (число центров кристаллизации, возникших в 1 мм3 за одну секунду). Скорость роста кристаллов, обозначаемая в дальнейшем через с. к., есть скорость увеличения линейных размеров кристалла, выраженная в миллиметрах в единицу времени. Размерность этой величины — мм/с; мм/мин.
Исследуя кристаллизацию прозрачных органических веществ при разных температурах, Г. Тамман установил, что ч.ц. и с.к. определяются степенью переохлаждения. Графически изменения величин ч.ц. и с.к. в зависимости от переохлаждения представлены на рисунке 4.4.б. Зависимость ч.ц. и с.к. от переохлаждения выражается кривой с максимумом. При теоретической температуре кристаллизации (n = 0) значения с.к. и ч.ц. равны нулю и процесс кристаллизации идти не может, что находится в полном соответствии с изложенным выше положением о необходимости переохлаждения для протекания процесса. С увеличением переохлаждения значения с.к. и ч.ц. возрастают, достигают максимума и затем понижаются; при больших величинах переохлаждения практически падают до нуля.
Увеличение с.к. и ч.ц. при малых степенях переохлаждения обусловлено тем, что вблизи равновесной точки (Ts) подвижность атомов велика и ускорение кристаллизации с увеличением степени переохлаждения вызывается увеличением разности свободных энергий жидкого и кристаллического состояний. Снижение с.к. и ч,ц. при больших степенях переохлаждения вызвано тем, что при больших переохлаждениях и, следовательно, при низких температурах подвижность атомов уменьшена, а тем самым уменьшена и способность системы к превращению. При больших степенях переохлаждения с.к. и ч.ц. становятся равными нулю, так как подвижность атомов уже недостаточна для того, чтобы осуществилась перестройка их из хаотического расположения в жидкости в правильное в кристалле.
Размер образовавшихся кристаллов зависит от соотношения величин с.к. и ч.ц. при температуре кристаллизации, при данной степени переохлаждения. При большом значении с.к. и малом значении ч.ц. (например, при малых степенях переохлаждения, рисунке 4.4.б), образуются немногочисленные крупные кристаллы; при малых значениях с.к. и больших ч.ц. (большое переохлаждение) образуется большое число мелких кристаллов. Наконец, в соответствии с кривыми Таммана, если удается очень сильно переохладить жидкость без кристаллизации, то с.к, и ч.ц. становятся равными нулю, жидкость сохраняется непревращенной, неза-кристаллизовавшейся. Соли, силикаты, органические вещества весьма склонны к переохлаждению. Для металлов же требуется переохладить жидкость до температуры, когда подвижность атомов станет мала и такое состояние окажется достаточно устойчивым.
Обычное прозрачное «твердое» стекло представляет собой переохлажденную загустевшую жидкость. Такое состояние, как указывалось выше, является аморфным и характеризуется отсутствием определенной температуры плавления и отсутствием правильного расположения атомов в виде определенной кристаллической решетки.
Было показано, что не только в жидких расплавах, но и при превращении в твердом состоянии новая форма также образуется путем зарождения и роста кристаллов; скорость этих процессов зависит от переохлаждения. В отличие от кристаллизации из жидкости процесс превращения в твердом состоянии (перекристаллизация) обычно протекает при сильном переохлаждении, и таммановская зависимость с.к. и ч.ц. для этого случая даже более приемлема, чем для случая первичной кристаллизации из жидкого состояния.
Учитывая изложенное, можно отметить, что переход из одного состояния в другое, например из жидкого в твердое, возможен тогда, когда твердое состояние более устойчиво, имеет более низкое значение свободной энергии. Но сам переход из одного состояния в другое требует затраты энергии на образование поверхности раздела жидкость — кристалл.
Превращение произойдет тогда, когда выигрыш в энергии от перехода в более устойчивое состояние будет больше потери энергии, идущей на образование поверхности раздела.
Форма кристаллических образований
Реально протекающий процесс кристаллизации усложняется действием различных факторов, в столь сильной степени влияющих на процесс, что роль степени переохлаждения может стать в количественном отношении второстепенной.
При кристаллизации из жидкого состояния для скорости течения процесса и для формы образующихся кристаллов первостепенное значение приобретают такие факторы, как скорость и направление отвода тепла, наличие нерастворившихся частиц (которые могут служить готовыми центрами кристаллизации), конвекционных токов жидкости и т. д.
В направлении отвода тепла кристалл растет быстрее, чем в другом направлении.
Если на боковой поверхности растущего кристалла возникает бугорок, то кристалл приобретает способность расти и в боковом направлении. В результате образуется древовидный кристалл, так называемый дендрит, схематическая структура которого, впервые изображенная Д. К. Черновым, показана на рисунке 4.5.
Дендритное строение типично для литого металла. Если условия благоприятны, охлаждение медленное, то могут вырасти огромного размера, дендриты. В усадочной раковине 100-т слитка один из учеников Д. К. Чернова нашел дендрит (точнее два дендрита, сросшиеся своими основаниями) длиной в 39 см. Фотография этого дендрита, который обычно называют «Кристаллом Чернова», приведена на рисунке 4.6.
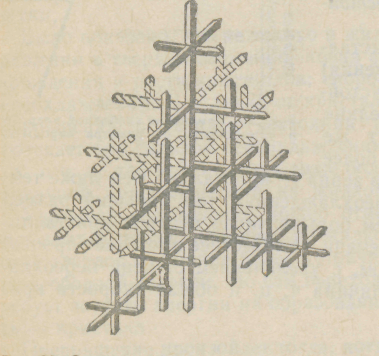
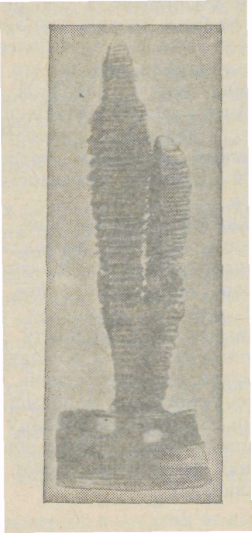
Рисунок 4.5 – Схема дендрита Рисунок 4.6 – Кристалл Чернова
Согласно схеме (рисунок 4.5) дендрит состоит из ствола (ось первого порядка), от которого идут ветви (оси второго и последующего порядка).
Чем быстрее было охлаждение при кристаллизации, тем меньше размеры (высота) дендрита и меньше расстояния между ветвями второго порядка.
При очень большой скорости охлаждения, например, при распылении жидкого металла в отдельные гранулы (круглые частицы диаметром 0,01—0,1мм) дендриты имеют размеры порядка 100мкм, а расстояние между осями второго порядка 1—5 мкм.
В обычных слитках массой в сотни килограмм или несколько тонн дендриты имеют размеры несколько десятков миллиметров и меньше. В момент своего образования дендрит является монокристаллом, но при последующем охлаждении в результате полиморфных превращений или внутренних напряжений могут внутри ветвей дендрита образоваться зерна равноосной, полиэдрической формы, вероятно, не сильно различающиеся ориентировкой.
Строение слитка
Ранее было отмечено, что реальный процесс кристаллизации осложняется влиянием побочных факторов. Сочетание влияния этих привнесенных факторов (часто не поддающихся точному учету) с общими законами кристаллизации и определяет особенности строения стального слитка.
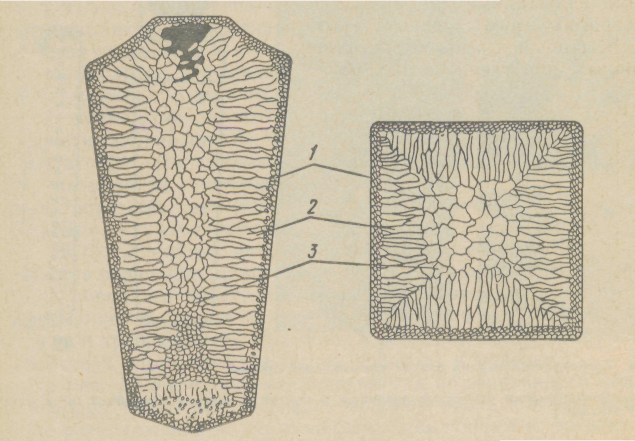
Рисунок 4.7 - Схема строения стального слитка
Описание строения стального слитка впервые дано в 1878 г. Д. К. Черновым. Остальные характерные черты в строении литого металла были отмечены тогда Д. К. Черновым, хотя многочисленные последующие исследования вскрыли много новых деталей.
Структура литого слитка состоит из трех основных зон. Первая зона — наружная мелкозернистая корка 1, состоящая из дезориентированных мелких кристаллов — дендритов. При первом соприкосновении со стенками изложницы в тонком прилегающем слое жидкого металла возникает резкий градиент температур и явление переохлаждения, ведущее к образованию большого количества центров кристаллизации. В результате корка получает мелкозернистое строение.
Вторая зона слитка — зона столбчатых кристаллов 2. После образования самой корки условия теплоотвода меняются (из-за теплового сопротивления, из-за повышения температуры стенки изложницы и других причин), градиент температур в прилегающем слое жидкого металла резко уменьшается и, следовательно, уменьшает степень переохлаждения стали. В результате из небольшого числа центров кристаллизации начинают расти нормально ориентированные к поверхности корки (т. е. в направлении отвода тепла) столбчатые кристаллы.
Третья зона слитка — зона равноосных кристаллов 3. В центре слитка уже нет определенной направленности отдачи тепла, «Температура застывающего металла успевает почти совершенно уравниваться в различных точках и жидкость обращается как бы в кашеобразное состояние, вследствие образования в различных ее точках зачатков кристаллов. Далее зачатки разрастаются осями — ветвями по различным направлениям, встречаясь друг с другом» (Чернов Д. К.). В результате этого процесса образуется равноосная структура. Зародышами кристалла здесь являются обычно различные мельчайшие включения, присутствующие в жидкой стали, или случайно в нее попавшие, или не растворившиеся в жидком металле.
В зоне столбчатых кристаллов металл более плотный, он содержит меньше раковин и газовых пузырей. Однако места стыка столбчатых кристаллов обладают малой прочностью.
Кристаллизация, приводящая к стыку зон столбчатых кристаллов, носит название транскристаллизации.
Степень развития столбчатых кристаллов будет варьироваться главным образом в зависимости от химического состава металла, степени его перегрева, от размера слитка, скорости разливки, формы изложницы и толщины, а также температуры ее стенок. Эти факторы будут влиять на скорость теплоотвода и образование больших или меньших градиентов температур внутри объема кристаллизующейся стали и т. д. Повышение степени перегрева и увеличение скорости охлаждения слитка способствует увеличению доли столбчатых кристаллов и может привести к полной транскристаллизации; при несколько замедленном охлаждении в центре слитка образуется зона равноосных кристаллов
Жидкий металл имеет больший объем, чем закристаллизовавшийся, поэтому залитый в форму металл в процессе кристаллизации сокращается в объеме, что приводит к образованию пустот, называемых усадочными раковинами; усадочные раковины могут быть сконцентрированы в одном месте, либо рассеяны по всему объему слитка или по его части. Они могут быть заполнены газами, растворимыми в жидком металле, но выделяющимися при кристаллизации. В хорошо раскисленной так называемой спокойной стали, отлитой в изложницу с утепленной надставкой, усадочная раковина образуется в верхней части слитка, и в объеме всего слитка содержится малое количество газовых пузырей и раковин.
Форма первичных кристаллов (дендритов) после горячей механической обработки давлением (ковка, прессовка, прокатка и т. д.) видоизменяется. Дендриты вытягиваются вдоль направления течения металла и превращаются в волокна. В результате возникает различие в свойствах вдоль проката (вдоль волокна) и поперек.
ЛЕКЦИЯ № 4
СТРОЕНИЕ СПЛАВОВ. ДИАГРАММЫ СОСТОЯНИЯ ДВОЙНЫХ СПЛАВОВ.
Диаграмма состояния - это графическое изображение состояния сплавов изучаемой системы в зависимости от их химического состава и температуры.
Диаграммы состояния показывают устойчивые, равновесные, состояния сплавов, т.е такие, которые при данных условиях обладают минимальной свободной энергией. Поэтому их называют также и диаграммами фазового равновесия. Зная диаграмму состояния, можно представить полную картину формирования структуры любого сплава, определить температуры литья и обработки давлением, установить возможность проведения и режимы термической обработки металлоизделий.
Закономерности всех изменений в многофазной системе подчиняются правилу фаз Гиббса. Оно дает возможность предсказать и проверить процессы, происходящие в сплавах при нагреве V. охлаждении; показывает, происходит ли кристаллизация при постоянной температуре или в определенном температурном интервале, указывает, какое количество фаз может одновременно находиться в равновесии. Правило фаз устанавливает следующую зависимость между числом степеней свободы С ( вариантностью) системы, числом компонентов К и числом фаз Ф , находящихся в равновесии:
С=К-Ф+2
Числом степеней свободы С называется число независимых внешних и внутренних факторов С температура, давление, концентрация), которые можно изменять, не изменяя числа фаз, находящихся в равновесии.
При построении диаграмм состояния металлических сплавов давление принимают постоянным, тогда:
С=К-Ф+1
Диаграммы состояния строят экспериментально, используя наиболее часто термический метод, с помощью которого получают кривые охлаждения отдельных сплавов системы в координатах время-температура. По остановкам и перегибам на этих кривых определяют температуры превращений.
Температуры, соответствующие фазовым превращениям, называются критическими точками.
Точки, отвечающие началу кристаллизации, называются точками ликвидуса, а концу кристаллизации - точками солидуса.
По полученным кривым охлаждения (критическим точкам)строят диаграмму состояния в координатах: по оси абсцисс - концентрация компонентов, по оси ординат - температура.
ДИАГРАММА. СОСТОЯНИЯ СПЛАВОВ С НЕОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ В ТВЕРДОМ СОСТОЯНИИ
Полная взаимная растворимость в твердом состоянии возможна лишь для металлов с однотипными (изоморфными) и близкими по периодам кристаллическими решетками, образующих при сплавлении непрерывный ряд твердых растворов замещения. Соответствующая этому случаю диаграмма представлена на рис. I.
Имеем: компоненты А ( например, Сu ) и В (например, Ni); фазы - жидкий раствор Ж и твердый раствор б.
Поле диаграммы разделено на три области фазового состояния, разделяемые линиями tACtB и tADtB. Линия tACtb представляет собой геометрическое место то ликвидус и называется линией ликвидуса.
Выше этой линии все сплавы находятся в жидком состоянии. Линия tADtB - геометрическое место точек солидус - называется линией солидуса, ниже которой все сплавы находятся в твердом состоянии. Область между этими линиями соответствует равновесию жидкости и кристаллов твердой фазы.
Вначале получают кривые охлаждения для чистых компонентов, а затем для сплавов различного состава.
Кривая I получена при охлаждении компонента А ( Сu ). Выше температуры tА (для меди - 1086°С ) металл находится в жидком состоянии. Кристаллизация начинается при этой температуре через промежуток времени ф1 и заканчивается в момент ф2 . Согласно правилу фаз, имеем: компонент I ( металл А ), фазы 2 ( жидкий металл и кристаллы А ), следовательно,
С = К - Ф + 1 = 1 - 2 + 1= 0,
т.е. кристаллизация должна происходить при постоянной температуре. Ниже температуры tA происходит только охлаждение образовавшихся кристаллов компонента А. Аналогичные процессы происходят и при охлаждении компонента B.
Сплав II, содержащий, например, 60 % компонента B ( Ni ) и 40 % компонента A ( Сu ) выше температуры t1 ( точка l1 на линии ликвидуса ) находится в состоянии однородного жидкого раствора. При этой температуре жидкий раствор становится насыщенным по отношению к б-фазе и начинается кристаллизация, сопровождающаяся уменьшением скорости охлаждения. В интервале температур t1-t2 находятся две фазы: насыщенные жидкий и твердый растворы. Поскольку в данном случае количество компонентов К = 2, то С = 2 - 2+1 = 1, из чего следует, что кристаллизация сплава должна происходить в интервале температур. В этом состоит существенное отличие процесса кристаллизации двухкомпонентных сплавов от процесса кристаллизации чистых компонентов, происходящего при постоянной температуре.
При температуре t2 ( точка S2 на линии солидуса ) кристаллизация сплава заканчивается, и ниже ее никаких превращений не происходит.
Аналогичные процессы происходят и при охлаждении всех других сплавов, образованных компонентами А и В.
Следует усвоить, что в процессе кристаллизации изменяются химический состав (концентрация) фаз и количество каждой фазы. Пользуясь диаграммой состояния, можно в той области диаграммы, где существует две фазы, определить их состав и относительные количества при любой температуре. Для этого необходима использовать правила отрезков.
Первое правило отрезков применяют для определения состава фаз. Так, например, для того, чтобы в сплаве 2 (рис. I) определить составы жидкой и твердой фазы при температуре Ь черв» точку К характеризующую состояние сплава при этой температуре, надо пролети горизонтальную линию - коноду до пересечения с линями, ограничивающими данную двухфазную область. Проекция точки пересечения коноды с линией ликвидус l на ось концентраций – точка I - показывает состав жидкой фазы, а проекция точки пересечения S к он оды с линией солидус на эту ось - точка S` состав твердой фазы.
Из рис. I видно, что состав первых кристаллов твердого раствора б, образовавшихся при температуре t1 , отвечает точке S`1 , а последних г при температуре t2 - точке S`2 , т.е. вменяется в соответствии с линией солидус на участке l1- l2. Состав жидкой фазы изменяется при этом от l1- в начале кристаллизации до l2. в конце, т.е. в соответствии с линией ликвидус на участке l1- l2.
Это может быть записано в виде:
Для
определения количеств ( массы или
объема ) каждой на фаз в двухфазной
области при какой-либо температуре
следует применять второе правило
отрезков. Так, например, для сплава
2(рис. I) с этой целью также надо использовать
коноду, проведенную до границ двухфазной
об-ласги через точку К, характеризующую
состояние сплава при температуре.
Количество твердой фазы определяется
при этом отношением длины отрезка,
примыкающего к области жидкой фазы, по
всей длине коноды , т.е.
а
количество жидкой фазы - отношением
отрезка, примыкающего к области твердой
фазы, также к длине этой коноды:
Индексы при буквах указывают состав твердой и жидкой фаз соответственно при заданной температуре .
ДИАГРАММА. СОСТОЯНИЯ СПЛАВОВ С ОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ В ТВЕРДОМ СОСТОЯНИИ С ЭВТЕКТИКОЙ
Д
иаграмма
представлена на рис. 2.
Имеем: компоненты А и B, фазы - жидкий раствор Ж, твердые растворы б и в. Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений.
На приведенной диаграмме tACtB – линия ликвидус, линия tAECFtB – линия солидус.
Твердый раствор б образован на базе компонента А. Область его существования ограничена линией tAES, часть которой ES вертикальна, что указывает на постоянную растворимость компонента и в решетке компонента А во всем интервале температур ниже tэ (в приведенном примере 10 %).
В отличие от этого, состав твердого раствора В, образованного на базе компонента О, при понижении температуры изменяется. Обратите внимание на то, что растворимость компонента А в решетке компонента В максимальна при температуре, т.е. отвечает точке г (в нашем примере 20 % ), и с понижением температуры уменьшается в соответствии с ходом линии FK до 5 %, что отвечает 95 % компонента B).
В отличие от сплавов, лежащих левее линии ES и правее FК , являющихся однофазными, сплавы, лежащие между этими линиями, находятся за пределами растворимости и являются двухфазными, состоящими из кристаллов, образующих разные структуры.
Линия ECF называется линией "эвтектического превращения», которое состоит в одновременном выделении из жидкости кристаллов твердого раствора состава точки F. Запомните, что механическая смесь двух ( или более) разнородных кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой. Эвтектическую реакцию можно записать в следующем виде:
Эвтектическое
превращение протекает при постоянной
температуре tЭ,
так как при этом в двухкомплектном
сплаве одновременно сосуществуют три
фазы: одна жидкая и две твердых, в связи
с чем число степеней свободы при
этой температуре равно нулю
(реакция нонваривнтая) :
С = К – Ф + 1 = 2-3+1 = 0.
Следует усвоить, что количества каждой из фаз в эвтектической смеси могут быть определены с помощью второго правила отрезков:
Сплав I называется эвтектическим ( наиболее легкоплавким ). Сплавы, лежащие левее точки С , называются доэвтектичеокими ,а правее заэвтектическими.
При температурах выше tЭ эвтектический сплав находится в жидком состоянии, а при достижении этой температуры вся его масса претерпевает эвтектическое превращение по описанной выше . схеме. Обратите внимание, что на кривой охлаждения ( рис. 2 ) этому превращению отвечает температурная остановка ( т.к.C=О), длительность которой определяется массой кристаллизующейся жидкости. Последующее охлаждение сплава продолжается только после . полного завершения эвтектической реакции. Конечная структура сплава - пластинчатая эвтектика ( может быть и другое ее строение ) изображена на рис. 2.
В отличие от сплава | ,в заэвтекгическом сплаве || эвтектическому превращению предшествует выделение из жидкого раствора в интервале точек 1-2 кристаллов в , обогащенных компонентом О , в результате чего жидкая фаза обедняется этим компонентом.
Уясните, что при охлаждении до эвтектической температуры ( точка 2 ) состав кристаллов в изменяется в соответствии с линией МF , а жидкости - в соответствии с линией 1C . При достижении этой температуры количество первичных кристаллов ft состава точки F определяется отрезком С2 , а количество оставшейся жидкости состава точки С - отрезком 2F. Эго количество жидкости, составляющее часть массы сплава ( а не всю массу, как в сплаве I ),при температуре точки 2 превращается в эвтектику (б+в).
При дальнейшем охлаждении сплава II вследствие, уменьшения растворимости компонента A в решетке компонента B по линии FK будет происходить распад твердого раствора в с выделением в этой фазе вторичных кристаллов б состава точки S. (Необходимо уяснить, что это относится как к в-фазе, выделившейся из жидкости выше линии ECF, так и к находящейся в эвтектике).
Конечная структура сплава II в+эвтектика (б+.в)+б||
В сплаве ||| первичная кристаллизация, происходящая в интервале температур между точками 4 и 5 , сопровождается изменением состава твердой фазы по линии L5 , а жидкой - по линии 4N . Она заканчивается образованием в - твердого раствора", состав которого соответствует составу сплава. Такая однофазная структура сохраняется до температуры точки 6 . . •
При охлаждении сплава ||| ниже точки 6 , по мере уменьшения концентрации в твердом растворе в , избыточное количество компонента А выделяется из этой фазы в виде кристаллов б||. состава точки S, как и в предыдущем случае. Таким образом, конечная структура рассматриваемого сплава - кристаллы В -твердого раствора с выделениями в них вторичных кристаллов б||.
Кристаллизация доэвтектических сплавов (т.е. лежащих между точками E и C ) начинается на линии tAC выделением из жидкости кристаллов б-твердого раствора. При температуре tЭ остаток жидкости превращается в эвтектику (б+в),и конечная их структура состоит из этой эвтектики, количество которой тем больше, чем ближе состав сплава к эвтектическому, и кристаллов б -твердого раствора без выделений вторичных кристаллов.
Заканчивая изучение диаграммы, обратите внимание на го, что при одинаковом фазовом составе сплавов в диапазоне концентраций от точки 5 до точки К (б и в -твердые растворы ) их конечные структуры различны, чем определяется различие их свойств.
Уясните также, что протяженность областей существования твердых растворов б и в зависит от взаимной растворимости компонентов А и В . При полном отсутствии растворимости эти области отсутствуют и диаграмма имеет вид, изображенный на рис. 3.
Рис.3
ЛЕКЦИЯ №5
ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО - УГЛЕРОД
В сплавах при охлаждении и нагреве происходят изменения и образуются новые фазы и структуры. Эти изменения можно определить по диаграмме состояния. Диаграммой состояния называется графическое изображение, показывающее фазовый состав и структуру сплавов в зависимости от температуры и химической концентрации компонентов в условиях равновесия.
Фаза — однородная часть системы, отделенная от других частей поверхностью раздела, при переходе через которую свойства сплава изменяются скачкообразно. Большое практическое значение имеет диаграмма состояния железоуглеродистых сплавов (рис. 2).
Структурные составляющие железоуглеродистых сплавов. В зависимости от температуры и концентрации углерода железоуглеродистые сплавы имеют следующие составляющие:
аустенит — твердый раствор углерода в -железе с предельной концентрацией углерода 2,14 % при температуре 1147°С; с понижением температуры до 727 °С концентрация углерода уменьшается до 0,8 %; сталь со структурой аустенита немагнитна и имеет высокие пластичность и вязкость;
феррит — твердый раствор углерода в -железе с предельной концентрацией углерода 0,02 % при температуре 727 0С; феррит имеет малую твердость и высокую пластичность;
цементит — химическое соединение железа с углеродом Fe3С (6,67 % С); имеет большие твердость и хрупкость;
перлит — механическая смесь (эвтектоид) феррита и цементита, образующаяся при эвтектоидном распаде аустенита (0,8 % С); сталь, имеющая структуру перлита, обладает большими прочностью
и твердостью;
ледебурит (4,3 % С) — механическая смесь (эвтектика) аустенита или перлита и цементита; ниже 727 °С аустенит превращается в перлит, при этом образуется смесь перлита и цементита;
графит — углерод в свободном состоянии, располагается в основной массе металла и имеет развитую объемную форму в виде пластинок; кроме пластинчатого графита можно получить графит компактных форм (шаровидный или хлопьевидный), образующийся в результате распада цементита или выделяющийся из пересыщенных твердых растворов железа с углеродом. В железоуглеродистом сплаве графит образуется при содержании Si 1,5 % и при очень медленном охлаждении. Графит мягок и обладает низкой прочностью.
Диаграмма состояния железоуглеродистых сплавов.
Основные свойства сплава определяются содержанием главной примеси – углерода. Взаимодействие углерода с - или -модификациями железа приводит к образованию железоуглеродистых сплавов, различных по строению и свойствам. Построение диаграммы состояния железо— углерод (цементит) дает представление о температурных и концентрационных границах существования этих сплавов.
На диаграмме состояния железо—цементит (рис. 2) линия ACD — линия ликвидуса, выше нее сплав находится в жидком состоянии; линия AECF — линия солидуса, ниже нее сплав находится в твердом состоянии. При температурах, соответствующих линии AECF заканчивается первичная кристаллизация. В точке С при концентрации углерода 4,3 % образуется эвтектика, которая носит название ледебурит. Линия PSK — эвтектоидная линия, на которой заканчивается .процесс вторичной кристаллизации. Линия PS— линия нижних критических точек А1. Линия GSE — начало процесса вторичной кристаллизации твердого раствора. Линия GS — линия верхних критических точек Л3; она показывает температуру выделения феррита из аустенита. Линия SE — линия верхних критических точек Ат; она показывает температуру начала выделения вторичного цементита и является линией предельной растворимости углерода в аустените. Сплавы, содержащие до 2,14 % С, условно называют сталями, более 2,14 % С — чугунами. Сталь, содержащая 0,8 % С, называется эвтектоидной сталью; сталь, содержащая менее 0,8 % С — доэвтектоидной. Сталь, содержащая более 0,8 % С — заэвтектоидной.
СПЛАВЫ ДИАГРАММЫ ЖЕЛЕЗО – УГЛЕРОД.
СТАЛИ.
Вуглецеві сталі – сплави заліза з вуглецем, у яких міститься до 2,14 % вуглецю.
Залізо – метал сріблистого кольору. Температура плавлення 1539°С (± 5°С). Технічне залізо – має високу пластичність ( = 50 %, = 85 %), малу міцність (В = 250 МН/м2), твердість - 80 НВ.
Залізо може знаходитися в двох модифікаціях: -залізо і -залізо.
Модифікація -заліза існує в інтервалі температур до 911°С і від 1392 до 1539°С (високотемпературна модифікація іноді називається -залізом). Залізо даної модифікації має обємноцентровану кубічну гратку.
Модифікація -заліза існує в інтервалі температур від 911 до 1392°С, має граньоцентровану кубічну гратку.
До температури 7680С залізо зберігає феромагнітні властивості, при нагріванні вище цієї температури залізо переходить у парамагнітний стан.
Вуглець – є неметалічним елементом, важкість 2,5 г/см3, температура плавлення 3500°С. Вуглець є поліморфним матеріалом. У звичайних умовах він знаходиться у виді модифікації графіту, але може існувати й у виді метастабільної модифікації алмаза. Вуглець розчинний у залізі в рідкому і твердому станах. У сталях може знаходитися у виді хімічно зв'язаних зєднань – карбідів заліза (FeС, Fe2C і Fe3C), найбільш стійким з яких є Fe3C.
Взаємодіючи з вуглецем, залізо утворює тверді розчини проникання – ферит і аустеніт або хімічне зєднання (карбід заліза Fe3C, тобто цементит).
Ферит (Ф) – твердий розчин проникання атомів вуглецю в -залізо. Ферит має обємноцентровану кубічну гратку. Розрізняють низькотемпературний ферит (-ферит) і високотемпературний ферит (-ферит). Максимальна розчинність вуглецю в -залізі складає 0,025 % при температурі 7270С. Зі зниженням температури розчинність знижується і при кімнатній температурі складає 0,006 % вуглецю. Високотемпературний -ферит має граничну розчинність вуглецю 0,1 % при температурі 14990С. У мікроструктурі, після травлення, ферит має вигляд світлих зернин. Ферит має низьку міцність (В = 250 МПа) і твердість (НВ 80 – 90), але високу пластичність ( = 50%; = 80%), підвищені магнітні і корозійні властивості.
Аустеніт (А) – твердий розчин проникання атомів вуглецю в -залізо. Аустеніт має граньоцентровану кубічну гратку (рис. 1, а). Гранична розчинність вуглецю в -залізі складає 2,14% при температурі 11470С. Зі зниженням температури розчинність вуглецю знижується і при 7270С складає 0,8 %. Рівноважний аустеніт може існувати тільки при високих температурах (вище 727°С). При більш низькій температурі він розпадається з утворенням інших структур. Аустеніт є немагнітною фазою, володіє високою хімічною стійкістю, гарною опірністю стиранню і великою в'язкістю. Аустеніт має невисокі твердість (НВ 160 – 200) і міцність (В = 600 – 800 МПа), але високу пластичність (відносне подовження = 40 – 50 %).
Цементит (Ц) – хімічна сполука заліза з вуглецем – карбід заліза Fe3C; у який міститься 6,67 % вуглецю. Цементит має складну ромбічну ґратку з щільним упакуванням атомів (рис. 1, б). Температура плавлення цементиту точно не визначена в зв'язку з можливістю його розпаду при нагріванні і приймається 12500С. Цементит має дуже високу твердість (800 НВ), але надзвичайно низьку, практично нульову, пластичність. При звичайних температурах цементит має низькі феромагнітні властивості, які губляться при нагріванні вище 217°С.
Ферит, аустеніт, цементит – це однофазні структури, але в сплавах можуть утворюватися і двофазні структури, як, наприклад, перліт.
Перліт (П) – це механічна суміш фериту і цементиту. Перліт містить 0,8 % вуглецю й утворюється при охолодженні нижче температури 7270С з аустеніту в результаті евтектоїдного перетворення:
АS ФР + Ц.
У залежності від форми часточок цементиту перліт може мати пластинчасту і зернисту будову (рис. 5).
С
таль
із зернистим перлітом має більш низьку
твердість, границю міцності і, відповідно,
більш високі значення щодо подовження
і звуження. Наприклад, евтектоїдна
сталь із пластинчастим перлітом має
твердість НВ 228, а з зернистим перлітом
– НВ 163; відповідно границя міцності
820 і 630 МПа і відносне подовження 15 і 20
%.
Утворення тих чи інших фаз і структур у залізовуглецевих сплавах можна вивчити, розглядаючи процеси, що відбуваються в них відповідно до діаграми стану залізо – цементит (рис. 2).
Залізовуглецеві сплави з концентрацією вуглецю до 0,025 % називають технічним залізом, з концентрацією вуглецю від 0,025 до 2,14 % – сталями.
Сталі по змісту вуглецю поділяються на:
– доевтектоїдні зі змістом вуглецю від 0,025 до 0,8 %;
– евтектоїдні зі змістом вуглецю 0,81 %;
– заевтектоїдні зі змістом вуглецю від 0,82 до 2,14 %.
Технічно чисте залізо – зі змістом вуглецю менш 0,006 % має однофазну структуру, що складається з одного фериту. При змісті вуглецю більш 0,006 %, але менш 0,025 % структура технічно чистого заліза складається з фериту і цементиту третинного (Ц III), що виділяється по границях зернин фериту.
Виділення третинного цементиту при охолодженні відбувається внаслідок зменшення розчинності вуглецю у фериті по лінії PQ (рис. 2). Включення третинного цементиту по границях зерен різко знижує пластичність фериту. Мікроструктура технічно чистого заліза показана на рис. 3.
Хімічно чисте залізо через труднощі його одержання застосовують тільки при лабораторних дослідженнях. У техніці найчастіше застосовують так називані технічні сорти чистого заліза.
Доевтектоїдні сталі – мають структуру, що складається з фериту і перліту (рис. 4). До доевтектоїдних сталей відносять сплави, що містять від 0,025 до 0,8 % вуглецю.
У доевтектоїдних сталях після травлення 5 % розчином HNO3 ферит виділяється у виді світлих зернин, а перліт – у виді темних зернин, що мають пластинчасту будову.
По змісту вуглецю доевтектоїдні сталі можна підрозділити на:
– маловуглецеві зі змістом вуглецю від 0,025 до 0,25 % (рис. 4, а);
– середньовуглецеві зі змістом вуглецю від 0,25 до 0,6 % (рис. 4, б);
–
вуглецеві
(високовуглецеві) зі змістом вуглецю
більш 0,6 % (рис. 4, в).
Кількість фериту і перліту в доевтектоїдній сталі залежить від змісту вуглецю. Зі збільшенням змісту вуглецю кількість фериту зменшується, а кількість перліту збільшується. Так, у доевтектоїдних маловуглецевих сталях у структурі переважає надлишковий ферит, перліту – значно менше (рис. 4, а). У середньовуглецевих доевтектоїдних сталях кількість фериту і перліту приблизно однаково (рис. 4, б), у високовуглецевих – значно більше перліту (рис. 4, в).
Звичайно при рисуванні структур доевтектоїдних сталей студент натрапляє на труднощі в зображенні перліту. У сталях перліт часто має пластинчасту будову: складається з пластинок, фериту і цементиту, що чергуються, співвідношення товщин яких дорівнює 7:1. Тому, навіть у тих випадках, коли через недостатнє збільшення оптики мікроскопа пластинки фериту і цементиту роздільно не розрізняються, і перліт виглядає суцільним, однорідним по фарбуванню зерном, схематично цю структурну складову прийнято зображувати пластинчастою (рис. 4).
У доевтектоїдних сталях по співвідношенню площ, займаних у досліджуваній сталі – перлітом і феритом, можна приблизно оцінити зміст у ній вуглецю. У зв'язку з тим, що у фериті розчинена дуже невелика кількість вуглецю, практично можна вважати, що в доевтектоїдних сталях весь вуглець знаходиться в перліті. Таким чином, визначивши площу, займану в структурі перлітом, і знаючи, що в структурі, що складається з 100 % перліту, міститься 0,81 вуглецю, можна визначити зміст вуглецю в досліджуваній сталі користуючись формулою:
;
де FП – площа, зайнята перлітом у %.
Наприклад, якщо на розглянутому полі шліфа перліт займає, приблизно, 30 % площі мікроструктури, то зміст вуглецю стали дорівнює близько 0,24%:
.
Знаючи процентний зміст вуглецю можна визначити марку сталі.
Евтектоїдна сталь – містить 0,81 % вуглецю. Її структура складається з перліту (100 %). Поверхня мікрошліфа має перламутровий відлив, у зв'язку з чим перліт і одержав свою назву. Труднощі зображення структури полягають у тому, що як і в доевтектоїдних сталях, при середніх і малих збільшеннях оптики мікроскопа, у перліті не розрізняються окремо пластинки фериту і цементиту, і, крім того, важко розрізнити границі між окремими перлітними зернинами (колоніями). У цьому випадку потрібно області в структурі з однорідним фарбуванням зображувати у виді окремих перлітних колоній, що примикають одна до одної, з характерною для кожної пластинчастою будовою (рис. 5, а).
Крім пластинчастої перліт може мати і зернисту будову (рис. 5, б). У такому перліті цементит у виді глобул розташований у феритних зернинах. Така структура називається зернистим перлітом. Крім евтектоїдної сталі зернистий перліт може бути в заевтектоїдних сталях.
Заевтектоїдна сталь – містить вуглецю від 0,82 % до 2,14 %. Структура заевтектоїдних сталей складається з перліту і цементиту вторинного (рис. 6).
Вторинний цементит виділяється з аустеніту при охолодженні від температури лінії SE до лінії евтектоїдної рівноваги (PSK) унаслідок зменшення розчинності вуглецю в аустеніті (рис. 2).
При повільному охолодженні вторинний цементит виділяється у виді сітки (оболонки) по границях зернин аустеніту, що при охолодженні нижче температури 727°С (лінія PSK) перетворюється в перліт.
Зміст цементиту вторинного в структурі заевтектоїдної сталі зростає зі збільшенням концентрації вуглецю від 3,4 % при (1 % С) до 20,4 % при (2,0 % С).
Вторинний цементит досить чітко виявляється при звичайному травленні в 4 %-вому спиртовому розчині азотної кислоти.
У доевтектоїдних сталях, що містять трохи менше 0,8 % С, надлишковий ферит також може виділятися у виді сітки по границях зернин перліту: дана сітка при травленні вищезгаданим реактивом також виходить світлою. Якщо викликає сумнів, чи є сталь доевтектоїдною чи заевтектоїдною, тобто чи є світла сітка феритною чи цементитною, прибігають до контрольного травлення пікратом натрію. Пікрат натрію офарблює цементит у темнокоричневий колір. Тому, якщо сітка після травлення пікратом натрію залишилася світлою, значить це ферит і сталь доевтектоїдна, якщо ж сітка стала темною – сталь заевтектоїдна.
Підводячи підсумки мікроструктурного аналізу вуглецевих сталей, необхідно відзначити наступне – технічне залізо і всі вуглецеві сталі при кімнатних температурах складаються з двох фаз: фериту і цементиту.
При збільшенні змісту вуглецю кількість фериту в структурі поступово зменшується, а цементиту навпаки – збільшується. Так, технічне залізо при змістах вуглецю менш 0,006 % складається тільки з фериту, а при більш високих – з фериту і цементиту третинного. У доевтектоїдних сталях крім цементиту третинного є присутнім цементит перлітний, кількість якого зі збільшенням змісту вуглецю в сталях безупинно росте аж до евтектоїдної концентрації (0,81 % С). У заевтектоїдних сталях подальший ріст кількості цементитної фази забезпечується за рахунок цементиту вторинного.
О
скільки
уже відомо, що ферит є дуже м'якою
маломіцною і пластичною фазою, а цементит
– дуже твердою і крихкою фазою, логічно
припустити, що зі збільшенням змісту
вуглецю твердість і міцність вуглецевих
сталей повинна збільшуватися, а
пластичність знижуватися. Це, в основному,
підтверджується механічними випробуваннями
сталей (рис. 7). Зниження границі міцності
сталей при змістах вуглецю понад 1,0 %
пояснюється прогресуючим підвищенням
крихкості заевтектоїдних сталей за
рахунок утворення карбідної сітки з
крихкої цементитної фази в їхній
структурі.
ЛЕКЦИЯ 6
ФОРМИРОВАНИЕ СТРУКТУР ЧУГУНОВ. ВИДЫ ЧУГУНОВ
Чугун отличается от стали по составу — более высоким содержанием углерода, по технологическим свойствам — лучшими литейными качествами, малой способностью к пластической деформации (в обычных условиях не поддается ковке). Чугун дешевле стали. В зависимости от состояния углерода в чугуне различают: белый чугун, в котором весь углерод находится в связанном состоянии в виде;
серый чугун, в котором углерод в значительной степени или полностью находится в свободном состоянии в форме пластинчатого графита.
Пластинчатая форма графита ухудшает свойства чугуна, поэтому разработаны методы плавки или последующей обработки, при которой изменяется форма графита и улучшаются свойства. В настоящее время получают серый чугун с волокнистой (червеобразной) формой графита. Такой графит получил название вермикулярный (vermicu-lus (лат.) червь, отсюда и вермишель);
высокопрочный чугун, в котором углерод в значительной степени или полностью находится в свободном состоянии в форме шаровидного графита;
ковкий чугун, получающийся в результате отжига отливок из белого чугуна. В ковком чугуне весь углерод, или значительная часть его находится в свободном состоянии в форме хлопьевидного графита (углерода отжига).
Таким образом, чугун (кроме белого) отличается от стали наличием в структуре графитовых включений, а между собой чугуны различаются формой этих включений.
Естественно, что важнейший вопрос теории чугуна — выяснение условий образования графита, так называемой графитизации.
1. Процесс графитизации
Углерод может существовать в двух аллотропических формах алмаз и графит. Алмаз — редкая форма существования углерода и в сплавах не встречается.
В железоуглеродистых сплавах в свободном виде углерод находится в форме графита. Кристаллическая структура графита слоистая.
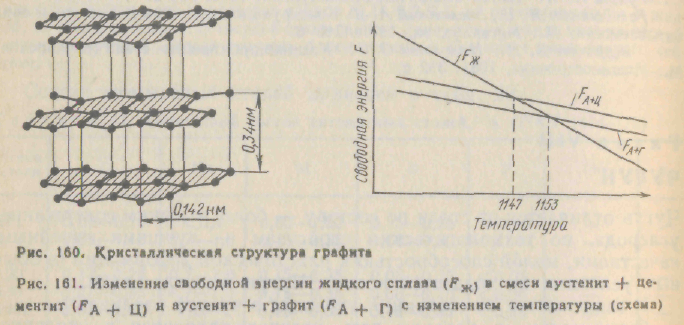
Расстояние между атомами углерода, лежащими в одной плоскости, составляет 0,142 нм, а расстояние между плоскостями равно 0,34 нм. Из четырех валентных электронов атома углерода только один поступает в электронный газ, что обусловливает некоторые, правда, слабо выраженные, металлические свойства графита (например, его электропроводность).
Прочность и пластичность графита весьма низкая.
Высокоуглеродистой фазой в железоуглеродистых сплавах может быть и цементит.
Рассматривая кристаллическую структуру и состав аустенита, цементита и графита, следует сделать следующий вывод: кристаллические структуры цементита и аустенита близки, тогда как кристаллические структуры аустенита и графита существенно различны. По составу аустенит и цементит ближе друг к другу, чем аустенит и графит (так, аустенит содержит до 2,14 % С, цементит 6,67 % С, а графит 100 % С). Поэтому образование цементита из аустенита, а также и из жидкости происходит легче, работа образования зародыша, как и необходимые диффузионные изменения, меньше в случае кристаллизации цементита, чем кристаллизации графита. Следовательно, кинетически из твердого раствора (аустенита) и из жидкости более выгодна кристаллизация цементита, а не графита (точнее, смеси феррит + цементит или аустенит - цементит, а не смеси феррит + графит или аустенит+ графит).
Вместе с тем графит — более устойчивая фаза, а цементит — менее устойчивая; это значит, что смесь феррит + графит или аустенит + графит обладает меньшей свободной энергией, чем смесь феррит + цементит или аустенит + цементит. Следовательно, термодинамические факторы способствуют образованию не цементита, а графита.
Эти два обстоятельства необходимо учитывать при изучении условий образования графита. Если кинетические условия позволяют, то образуются структуры с графитом, если нет, то с цементитом, несмотря на то, что более устойчивой является структура графита; в этом случае образование графита является вторичной реакцией, и графит будет продуктом распада цементита.
Переход из одного агрегатного состояния в другое, например, из жидкого состояния в твердое, вызван тем, что при изменившихся условиях новое состояние оказывается более устойчивым, обладает меньшим запасом свободной энергии.
Точка перехода жидкости в смесь аустенит + цементит при 1147°С (линия ECF на диаграмме железо — углерод. Следовательно, схематически линии изменения свободной энергии жидкого расплава и смеси аустенит + цементит при изменении температуры пересекаются при температуре 1147°С (рис. 161). Ниже этой температуры протекает процесс кристаллизации, выше — плавление.
Ранее было указано, что аустенито-графитная смесь является термодинамически более устойчивой, чем аустенито-цементитная смесь. Это значит, что если на схеме рис. 161 провести линию, которая будет характеризовать свободную энергию смеси аустенит + графит, то она должна располагаться при всех температурах выше линии, характеризующей свободную энергию смеси аустенит + цементит. Следовательно, линия свободной -энергии аустенит + графит пересечет линию свободной энергии жидкости при температуре более высокой, чем 1147°С, т.е. при 1153°С.
Исходя из этого, можем сделать следующие выводы.
Ниже точки равновесия (1147°С) кристаллизация протекает с образованием цементита, так как кинетически это легче осуществимо. Графит в металле будет вторичным продуктом, он может образоваться в результате распада цементита.
В интервале 1147—1153°С образование из жидкости аустенито-цементитной смеси термодинамически неосуществимо, и в данных -температурных условиях кристаллизации происходит с образованием аустенито-графитной смеси непосредственно из жидкости.
Совершенно аналогично следует рассматривать возможность рас пада аустенита на феррито-цементитную или феррито-графитную смесь. Температура 727°С есть температура фазового равновесия А = Ф + Ц, а температура фазового равновесия лежит выше (по экспериментальным данным при 738°С), следовательно в интервале 738—727°С возможен распад аустенита не на феррито- цементитную смесь (перлит), а на феррито-графитную смесь. Приведенные термодинамические соображения должны найти отражение и в диаграмме фазового равновесия.
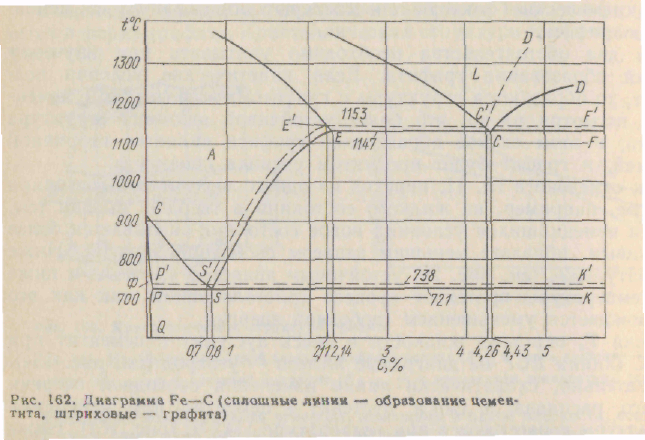
Диаграмма железо — углерод, приведенная на рис. 162, соответствует образованию аустенито-цементитных или феррито-цементитных смесей. Образование аустенито-графитных или феррито-графитных смесей происходит при более высоких температурах, а линии фазовых равновесий лежат при более высоких температурах. Таким образом, получается диаграмма железо — углерод с двойными линиями (см. рис. 162). Сплошные линии показывают температуру фазового равновесия аустенит (феррит) — цементит, а штриовые — аустенит (феррит) — графит.
Меньшая способность аустенита и жидкости растворять графит. чем цементит, приводит к тому, что линии S'E' и CD' располагаются левее соответствующих линий SE и CD.
Образование графита из жидкости или аустенита происходит при охлаждении в узком интервале температур между линиями стабильной и метастабильной диаграмм, т. е. в условиях малых переохлаждений или, следовательно, при малых скоростях охлаждения.
Образование структур серого чугуна непосредственно из жидкости или аустенита происходит при медленном охлаждении, тогда как образование структур белого чугуна происходит при более быстром охлаждении, что многократно подтверждается практикой.
Образование графита из жидкости или аустенита — медленно протекающий процесс, так как работа образования зародыша графита велика и требуется значительная диффузия атомов углерода для образования кристаллов графита, также необходим и отвод атомов железа от фронта кристаллизации графита.
В чистых железоуглеродистых сплавах непосредственное образование графита из жидкости было бы редко наблюдаемым явлением, если бы не одно обстоятельство, способствующее образованию графита,
Жидкость в высоко углеродистых сплавах (чугунах) не является практически совершенно чистой. Обычно чугун после его расплавления «замутнен», т. е. содержит во взвешенном состоянии мельчайшие частицы различных включений и примесей, в том числе и мельчайшие частицы графита. На этих частицах начинается процесс кристаллизации графита, они являются стенкой, на которой оседают атомы углерода, давая кристалл графита. В этом случае работа образования зародыша графита может быть и не больше работы образования зародыша цементита, и поэтому даже ниже температуры равновесия (1147°С) кинетически оказывается возможным образование кристаллов графита.
Перегрев чугуна значительно выше температуры плавления приводит к растворению взвешенных частиц, хотя, возможно, и неполному, что затрудняет непосредственное образование графита. Введение различных добавок к чугуну может привести к возникновению дополнительных центров кристаллизации графита, что способствует в ряде случаев образованию графита,
В зависимости от условий кристаллизации образуется графит различной формы, что имеет большое значение.
То, что сказано в отношении кристаллизации графита из жидкости, применимо и для кристаллизации графита из аустенита.
Кроме рассмотренного ранее процесса образования графита непосредственно при кристаллизации, возможен и другой способ образования графита. Как уже неоднократно указывалось, цементит — неустойчивое соединение и при определенных условиях (определенной температуре) распадается с образованием аустенита и графита или феррита и графита. Для осуществления этого процесса требуется диффузия углерода к центрам кристаллизации графита и самодиффузия железа от мест в которых графит выделяется. При нормальной комнатной температуре этот процесс практически не протекает, но с повышением температуры резко ускоряется. При температуре ниже линии P'S'K' устойчивыми фазами являются феррит и графит, поэтому цементит распадается на эти две фазы и реакцию распада цементита можно написать так:
Fe3C-Fea+C или Ц-ф+Г
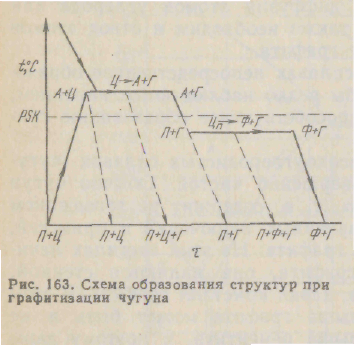
Выше линии P’S’K’ устойчивыми фазами являются аустенит и графит и реакция распада цементита сопровождается образованием таких фаз:
. Fe3C - Fev (С) + С или Ц - А + Г
Следовательно, в результате графитизации цементита образуется графит и феррит (ниже линии P'S'K') или аустенит (выше линии P'S'K')- Выше линии P'S'K' часть углерода находится в у-твердом растворе, поэтому, хотя процесс при более высокой температуре протекает быстрее, но к выделению всего углерода в свободном состоянии (т. е. в виде графита) он привести не может; при температуре ниже линии P'S'K' процесс протекает медленно, но он может закончиться полной графитизацией, т. е. выделением всего углерода в свободном состоянии.
2. Структура чугуна. Формы графита
Белый чугун. Такое название он получил по виду излома, который имеет матово-белый цвет. Фазовый состав белого чугуна (при нормальной температуре) цементит и феррит. Следовательно, в белом чугуне весь углерод находится в форме цементита, степень графитизации равна нулю. Белый чугун обладает высокой твердостью и хрупкостью, практически не поддается обработке режущим инструментом.
Серый чугун. Такое название чугун получил по виду излома, который имеет серый цвет. В структуре серого чугуна имеется графит, количество, формы и размеры которого изменяются в широких пределах. Таким образом, в сером чугуне имеется графит, а в белом его нет 1.
В микроструктуре чугуна следует различать металлическую основу и графитные включения.
По строению металлической основы чугун разделяют на:
перлитный чугун (рис. 164, а). Структура его состоит из перлита с включениями графита (на рис. 164, а графит в виде прожилок; типично для серого чугуна). Как известно, перлит содержит 0,8 % С, следовательно, это количество углерода в сером перлитном чугуне Находится в связанном состоянии (т. е. в виде Fe3C), остальное количество находится в свободном виде, т. е. в форме графита;
феррито-перлитный чугун (рис. 164, б). Структура этого чугуна состоит из феррита + перлит и включения веретенообразного графита. В этом чугуне количество связанного углерода меньше 0,8 %С.
ферритный чугун (рис. 164, в). В этом чугуне металлической основой является феррит, и весь углерод, имеющийся в сплаве, присутствует в форме графита (на фотографии в виде хлопьев углерода отжига).
Из рассмотрения структур указанных трех видов чугуна можно заключить, что их металлическая основа похожа на структуру эв-тектоидной стали, доэвтектоидной стали и железа.

Следовательно, по структуре серые чугуны отличаются от стали только тем, что в чугунах имеются графитные включения, предопределяющие специфические свойства чугунов.
Графит в чугунах может быть в четырех основных формах:
пластинчатый графит. В обычном сером чугуне графит образуется в виде лепестков; такой графит, называется пластинчатым. На рис. 165, а показана структура обычного ферритного чугуна с прожилками графита; пространственный вид таких графитных включений показан на рис. 166, а (видно пересечение пластинчатых включений плоскостью шлифа);
вермикулярный графит — в виде червеобразных прожилок (рис. 165, г);
шаровидный графит. В современных так называемых высокопрочных чугунах, выплавленных с присадкой небольшого количества магния (или церия), графит приобретает форму шара.
Нэ рис. 165, б показана микроструктура серого чугуна с шаровидным графитом, а на рис. ,166, б — фотография графитного включения;
хлопьевидный графит. Если при отливке получить белый чугун, затем, используя неустойчивость цементита, с помощью отжига
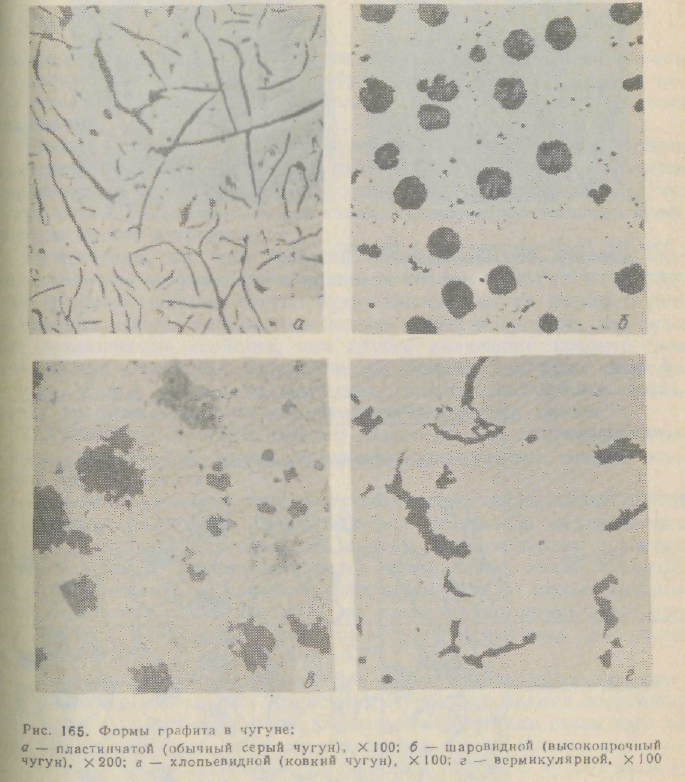
разложить его, то образующийся графит приобретает компактную, почти равноосную, но не округлую форму. Такой графит называется хлопьевидным или углеродом отжига. Микроструктура чугуна с хлопьевидным графитом показана на рис. 165, в. В практике чугун с хлопьевидным графитом называют ковким чугуном.
Таким образом, чугун с пластинчатым графитом называют обычным серым чугуном, с червеобразным графитом — серым вермикулярным чугуном;
чугун
с шаровидным графитом — высокопрочным
чугуном и
чугун с хлопьевидным графитом — ковким
чугуном.
На схемах структур (рис. 167) обобщается описанная выше классификация чугуна по строению металлической основы и форме графита.
3. Структура и свойства чугуна
Поскольку структура чугуна состоит из металлической основы и графита, то и свойства чугуна будут зависеть как от свойств металлической основы, так и от количества и характера графитных включений.
Графит по сравнению со сталью обладает низкими механическими свойствами, и поэтому графитные включения можно считать в первом приближении просто пустотами, трещинами. Отсюда следует, что чугун можно рассматривать как сталь, испещренную большим количеством пустот и трещин.
Естественно, что чем больший объем занимают пустоты, тем ниже свойства чугуна. При одинаковом объеме пустот (т. е. количестве графита) свойства чугуна будут зависеть от их формы и расположения. Следовательно, чем больше в чугуне графита, тем ниже его механические свойства, чем грубее включения графита, тем больше они разобщают металлическую основу, тем хуже свойства чугуна. Самые низкие механические свойства получаются тогда, когда графитные включения образуют замкнутый скелет.
На какие же свойства особенно сильно влияют графитные включения пластинчатой формы, играющие роль трещин, острых надрезов внутри металла?
При растягивающих нагрузках облегчается образование очагов разрушения по концам графитных включений. По механическим свойствам чугун характеризуется низким сопротивлением развитию трещины (тем не менее разрушается чугун вязко, излом ямочный), и, следовательно, обнаруживает низкие механические свойства при испытании, где превалируют нормальные растягивающие напряжения (например, при испытании на растяжение).
Если растягивающие напряжения имеют минимальные значения, как например при сжатии, свойства чугуна оказываются достаточно высокими и практически очень близкими к свойствам стали того же состава и структуры, что и металлическая основа чугуна.
Поэтому предел прочности при сжатии и твердость чугуна зависят главным образом от строения металлической основы и мало отличаются от этих свойств стали.
Такие же свойства чугуна, как сопротивление разрыву, а также изгибу, кручению, в основном обусловливаются количеством, формой и размерами графитных включений; в данном случае свойства чугуна сильно отличаются от свойств стали.
Сказанное относится главным образом к серому чугуну с пластинчатыми включениями графита. По мере скругления графитных включений указанное отрицательное влияние графитных включений уменьшается.
Округлые включения шаровидного графита не создают резкой концентрации напряжений, такие включения не являются «трещинами» и чугун с шаровидным графитом имеет значительно более высокую прочность при растяжении и изгибе, чем чугун с пластинчатым графитом (отсюда и название чугуна с шаровидным графитом — высокопрочный чугун). Ковкий чугун с хлопьевидным графитом занимает промежуточное положение по прочности между обычным серым и высокопрочным чугуном с вермикулярным графитом между серым и ковким.
Таким образом, прочность чугуна (в отношении нормальных напряжений) определяется строением металлической основы и формой графитных включений.
В чугуне с шаровидным графитом нет острых надрезов, так как нет пластинчатых графитных включений, и изменение структуры металлической основы в результате термической обработки заметно отражается на его свойствах. Для чугуна с шаровидным графитом принципиально возможны все виды термической обработки, применяемые для стали, и их следует использовать для улучшения свойств такого чугуна.
Как было отмечено, графитные включения вредны. Однако такое рассмотрение односторонне и не всегда правильно. В некоторых условиях образование графитных включений может быть полезным.
В ряде случаев именно благодаря наличию графита чугун имеет преимущества перед сталью: во-первых, наличие графита облегчает обрабатываемость резанием, делает стружку ломкой, стружка ломается, когда резец дойдет до графитного включения; во-вторых чугун обладает хорошими антифрикционными свойствами благодаря смазывающему действию графита; в-третьих, наличие графитных выделений быстро гасит вибрации и резонансные колебания; в четвертых, чугун почти нечувствителен к дефектам поверхности, надрезам и т. д. Действительно, поскольку в чугуне имеется огромное количество графитных включений, играющих роль надрезов и пустот, то совершенно очевидно, что дополнительные дефекты на поверхности уже не могут иметь влияние, хотя бы в незначительной степени напоминающего то большое воздействие, которое оказывают эти дефекты поверхности на свойства чистой от неметаллических включений высокопрочной стали.
Лучшие литейные свойства по сравнению со сталью. Более низкая температура плавления и окончание кристаллизации при постоянной температуре (образование эвтектики) обеспечивают не только удобство в работе, но и лучшие жидкотекучесть и заполняемость формы. Описанные преимущества чугуна делают его ценным конструкционным материалом, широко применяемым в деталях машин, главным образом тогда, когда они не испытывают значительных растягивающих и ударных нагрузок.
4. Примеси а чугуне
Обычный промышленный чугун — не двойной железоуглеродистый сплав — он содержит те примеси, что и углеродистая сталь, т. е. марганец, кремний, серу и фосфор, но в большем количестве, чем сталь. Эти примеси существенно влияют на условия графитизации и, следовательно, на структуру и свойства чугуна.
Кремний особенно сильно влияет на структуру чугуна, усиливая графитизацию. Содержание кремния в чугунах колеблется в широких пределах: от 0,3—0,5 до 3—5 %. Изменяя содержание кремния, можно получить чугуны, совершенно различные по свойствам и структуре — от малокремнистого белого до высококремнистого ферритного (серого с пластинчатым или высокопрочного с шаровидным графитом).
Марганец в отличие от кремния препятствует графитизации или, как говорят, способствует отбеливанию чугуна.
Сера также способствует отбеливанию чугуна, но одновременно ухудшает литейные свойства (в частности, снижает жидкотекучесть), поэтому содержание серы в чугуне лимитируется: верхний предел Для мелкого литья 0,08 %, для более крупного, когда можно допустить несколько худшую жидкотекучесть, до 0,1—0,12 % S.
Фосфор практически не влияет на процесс графитизации. Однако фосфор — полезная примесь в чугуне, так как он улучшает жидкотекучесть. Это объясняется образованием относительно легкоплавкой тройной эвтектики, плавящейся при 950°С.
Кроме этих постоянных примесей, в чугун часто вводят и другие элементы. Такие чугуны называются легированными. Если примеси содержались в рудах, из которых в доменной печи выплавляется чугун, то такие чугуны называются природно-легированными. Наиболее часто чугун легируют хромом, никелем, медью, алюминием титаном. Хром препятствует, а медь и никель способствуют графитизации чугуна.
Практическое применение диаграммы Fe—Fe3C.
Диаграмму Fe—Fe3C используют для определения видов и температурных интервалов термический обработки стали; для назначения температурного интервала при обработке давлением; для определения температуры плавления и заливки сплава и его литейных свойств (жидкотекучести, усадки).
Основой процессов термической обработки является полиморфизм железа и его твердых растворов на базе - и -железа. Полиморфные превращения стали данного состава происходят в определенном интервале температур, ограниченном нижней А1 и верхними А3 и Ат критическими точками.
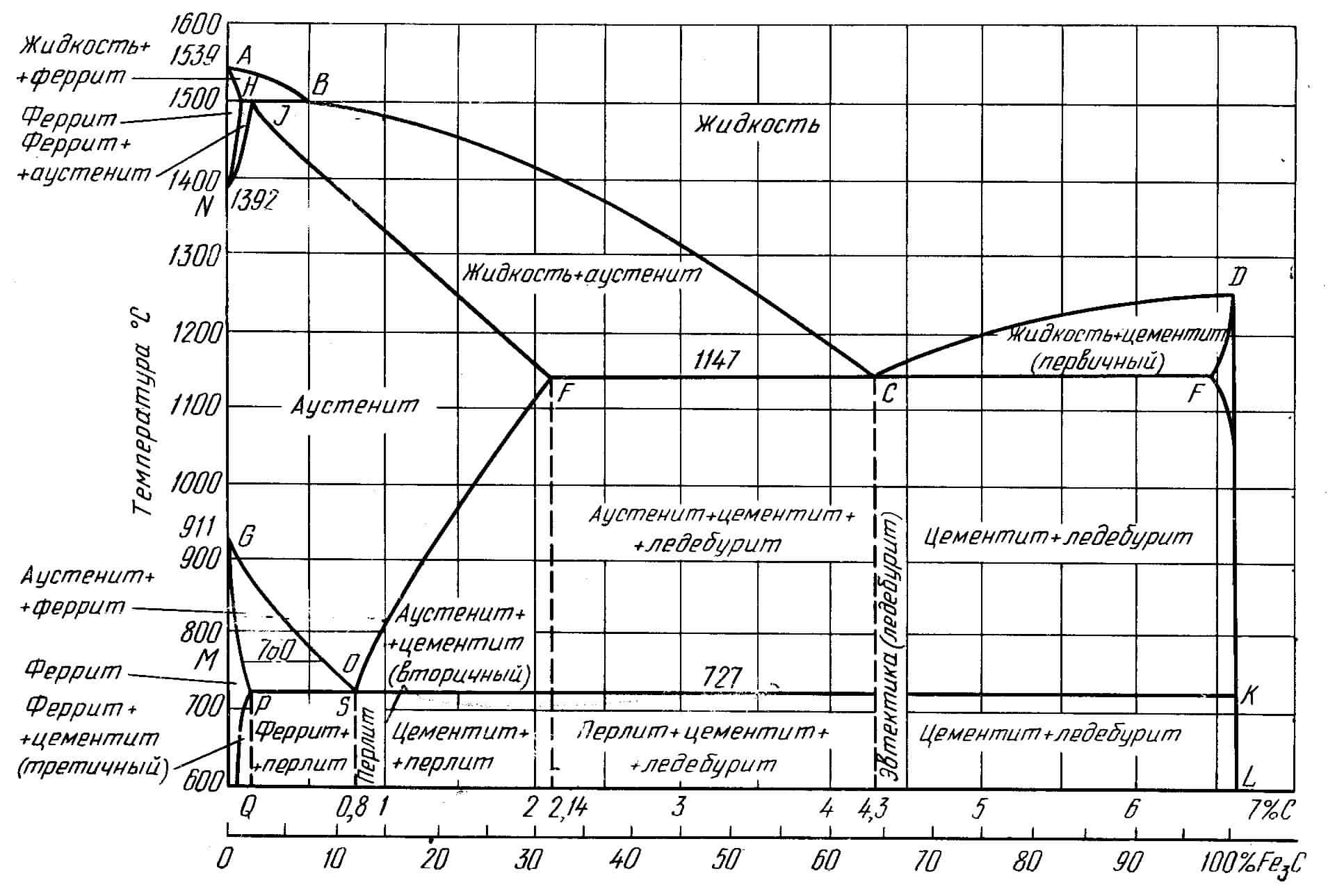
Рисунок 2. Диаграмма состояния железо – карбид железа
В результате полиморфизма происходит перекристаллизация в твердом состоянии. Перекристаллизация — это изменение кристаллического строения стали при ее нагреве или при охлаждении до определенных температур.
Таким образом, термическая обработка заключается в нагреве сплавов до определенных температур, выдержке их при этих температурах и последующем охлаждении с различной скоростью. При этом изменяются структура сплава, а следовательно, и его свойства. Изменяя режим термической обработки, можно получить различные физико-механические свойства и структуры железоуглеродистых
Сплавов.
ЛЕКЦИЯ 7
ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ
Стали, применяемые при изготовлении ответственных деталей машин и конструкций, должны иметь мелкозернистую структуру, так как в этом случае они имеют более высокий комплекс механических свойств по сравнение со сталями, имеющими крупнозернистую структуру.
Целью термической обработки является получение заданных механических свойств сплава путем изменения его внутренней структуры. В этом случае любая термическая обработка заключается прежде всего в том, что изделие нагревают до заданной температуры, делают выдержку при этой температуре и охлаждают с определенной скоростью. Очень часто изделия, нагретые до одной и той же температуры, но охлажденные с различными скоростями, приобретают совершенно разные механические свойства. Для получения мелкозернистой структуры стали подвергают перекристаллизации, для чего применяют отжиг или нормализацию.
Отжиг - термическая обработка стали, заключающаяся в нагреве выше критических температур Ac1 или Ас3, выдержке при данной температуре и затем медленном охлаждении вместе с печью. Нагрев выше Ac3 обеспечивает полную аустенизацию структуры стали. Нагрев выше температуры Ас1, но ниже Ac3, приводит только к аустенизации перлитной составляющей в. стали.
Нормализация заключается в нагреве стали выше критических температур Ас3 или Асm, выдержке и охлаждении на спокойном воздухе, что обеспечивает более быстрое охлаждение по сравнению с охлаждением в печи.
При изучении влияния режима термической обработки на размер зерна нужно обратить внимание на то, что по склонности к росту зерна аустенита при нагреве различают два типа сталей: наследственно мелкозернистые и наследственно - крупнозернистые. Первая характеризуется малой склонностью к росту зерна, вторая - повышенной.
Склонность к росту зерна аустенита при нагреве определяется условиями раскисления стали и ее составом. Стали, раскисленные алюминием, наследственно мелкозернистые, так как в них присутствуют дисперсные (очень мелкие) частицы тормозящие рост зерна. Рост зерна аустенита при нагреве задерживают также карбиды титана, ванадия, ниобия, вольфрама и молибдена, играющие роль барьеров для движения границ зерен. Марганец и фосфор способствуют росту зерна.
Изменение роста зерна при нагреве двух сталей, принципиально различающихся по кинетике роста зерна, показано на рис. I.
При изучении схемы роста зерна следует обратить внимание на то, что переход через критическую точку Ac1 сопровождается резким измельчением зерна. Это объясняется тем, что зерно еустенита образуется на границе ферритной и цементитной пластинок, в результате чего в каждой перлитной колонии зарождается множество зерен аустенита (рис.2).
При дальнейшем нагреве зерно аустенита в мелкозернистой стали не растет вплоть до 950 - 1000°С, после чего устраняются тормозящие рост факторы (карбиды, нитриды) и зерно начинает быстро расти. У крупнозернистой стали рост зерна начинается сразу после завершения перлито - аустенитного превращения.
При термообработке различают:
Начальное зерно - размер зерна аустенита в момент окончания перлито - аустенитного превращения;
наследственное (природное) зерно, характеризующее склонность аустенитных зерен к росту;
действительное зерно - размер зерна в стали, полученной в результате той или иной термообработки.
Размеры перлитных зерен, получающихся при медленном охлаждении стали из аустенитного состояния (отжиг стали) или при охлаждении на воздухе (нормализация), зависят от размеров зерен аустенита, из которых они образовались. Таким образом, чем крупнее зерно аустенита, тем большего размера перлитные зерна, которые из них образуются (рис.3).
Поэтому необходимым условием получения мелкого зерна в стали после отжига или нормализации является незначительное превышение критических температур Ac1 и Ас3 при нагреве (примерно на 30-50°), так как при дельнейшем повышении температуры зерно аустенита растет.
На технологические свойства стали влияет только действительный размер зерна. Если у двух сталей одной марки (одна наследственно крупнозернистая, другая наследственно мелкозернистая) при различных температурах термических обработок (отжиг или нормализация), будет получен одинаковый размер зерна, то свойства этих сталей будут одинаковыми. Если же размер зерна будет различный, то существенно будут различаться многие свойства стали.
Укрупнение действительного зерна сильно снижает ударную вязкость стали, особенно при низких температурах, а также предел текучести.
Существенного влияния на другие механические свойства, определяемые при испытании на растяжение и на твердость, размер - зерна не оказывает.
От склонности стали к росту зерна зависят режимы технологических процессов горячей деформации и термической обработки.
Истинный размер зерна и его величина, оцениваются баллами, путем сравнения зерен, видимых на шлифе под микроскопом при увеличении в 100 раз, с эталонными изображениями, приведенными в ГОСТ 5639-82. Между номером зерна (баллом) и количеством зерен, помещающихся на 1мм2 шлифа, существует зависимость.
Стали, имеющие балл зерна от 1 до 5, относят к группе крупнозернистых, а с баллом от 6 до 15 к мелкозернистым.
ЛЕКЦИЯ 8
ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ УГЛЕРОДИСТОЙ СТАЛИ
Термическая обработка (ТО) является одним из основных способов изменения и управления свойствами углеродистой стали. Являясь самым распространенным конструкционным материалом, углеродистая сталь очень редко применяется без ТО, так как даже в горячекатаном состоянии она часто имеет неудовлетворительную структуру, большие внутренние напряжения, обладает анизотропностью свойств и требует ТО (нормализации) для исправления структуры, снижения внутренних напряжений и повышения механических свойств - характеристик прочности, пластичности и особенно ударной вязкости.
Закалка и последующий отпуск наиболее часто применяются для упрочнения углеродистой стали. При этом важно помнить, что закаленные детали почти всегда подвергаются отпуску, а закалка с последующим высоким отпуском даже носит специальное название - улучшение. Очень часто для углеродистых сталей применяют нормализацию. Эта термическая операция нужна, как правило, тогда, когда требуется исправить структуру и понизить уровень напряжений, которые получают изделия в процессе прокатки, ковки, штамповки и других видов пластической деформации. Стали, которые должны подвергаться глубокой вытяжке (штамповке кузовов автомобилей и т.п.), должны иметь очень высокие пластические свойства, а внутренние напряжения должны быть минимальными. В этом случае применяется термическая операция, которая называется отжигом.
Любая ТО заключается в том, что изделие из углеродистой стали нагревают до заданной температуры, делают выдержку и охлаждают с определенной скоростью. Очень часто изделия, нагретые до одной и той же температуры, но охлажденные с различными скоростями, приобретают совершенно разные механические свойства. На вопрос, до каких температур нужно нагревать изделие и с какой скоростью охлаждать, чтобы получить желаемые механические свойства, в общих чертах дают ответ диаграммы состояния железо – углерод и изотермического превращения аустенита (рис. I и 2).
ВЛИЯНИЕ СКОРОСТИ ОХЛАЖДЕНИЯ ПРИ ТЕРМИЧЕСКОЙ ОБРАБОТКЕ НА СТРУКТУРУ И СВОЙСТВА УГЛЕРОДИСТОЙ СТАЛИ
(Закалка, нормализация и отжиг стали)
Закалкой называется термическая операция, заключающаяся в нагреве металла выше температуры превращения с последующим достаточно быстрым охлаждением для получения структурно-неустойчивого состояния сплава.
В результате закалки детали, изготовленные из углеродистой стали, приобретают повышенную твердость и прочность.
Технологическая операция закалки углеродистой стали заключается в том, что деталь нагревают до температуры выше Ас3 на 30-50°С (для доэвтектоидной стали), то есть в аустенитную область на диаграмме железо - углерод (рис.1) или выше Ac1 на 30 - 50°С (для заэвтектоидной стали), делают выдержку до полного выравнивания температуры по сечению изделия и после этого охлаждают с большой скоростью.
При скорости охлаждения стали больше критической (рис.2) происходит превращение аустенита А в мартенсит М:
В этом случае все атомы углерода остаются в твердом растворе. Такое превращение является бездиффузионным. При этом состав фаз не изменяется, а происходит только перестройка гранецентрированной решетки аустенита в тетрагональную решетку мартенсита, которая заметно отличается от кубической решетки α- железа. При превращении аустенита в мартенсит атомы не обмениваются местами, а лишь смещаются относительно друг друга на расстояния, не превышающие межатомные.
Температура мартенситного превращения Мн не зависит от скорости охлаждения и в сталях одного состава мартенситное превращение начинается при одной и той же температуре независимо от скорости охлаждения. Однако следует отметить, что чем меньше углерода в стали, тем при более высокой температуре начинается и заканчивается мартенситное превращение. Вот почему стали с содержанием углерода менъше 0,3% не удается, как правило, закалить на мартенсит. Мартенсит образуется при закалке, но при таких высоких температурах (500°С), что сразу же отпускается, распадаясь с образованием бейнитной структуры.
При охлаждении со скоростью, большей критической, получается пересыщенный твердый раствор углерода в α- железе, который мы называем мартенситом. Образование мартенсита сопровождается увеличением объема, что приводит к большим внутренним напряжениям, превышающим предел текучести аустенита. В результате этого в кристаллах аустенита происходит пластическая деформация, сопровождающаяся возникновением наклепа, получившего название фазового.
Искаженная за счет пересыщения и фазового наклепа тетрагональная решетка мартенсита имеет множество дефектов, которые препятствуют развитию сдвигов, движению дислокаций и таким образом упрочняют сталь.
Нагрев под закалку доэвтектоидной стали следует производить до температуры выше Ac3 на 30 - 50°С, а заэвтвктоидной стали - выше Ac1 (727°С) на 30 - 50°С (рис.1). Нагрев до более высоких температур доэвтектоидной стали приводит к росту зерна ауствнита, а это способствует образованию крупноигольчатого мартенсита, который обладает пониженными механическими свойствами.
Нагрев
заэвтектоидной стали до температур,
превышающих Ac1
+ 30 + 50°С, приводит к увеличению содержания
углерода в аустените за счет более
полного растворения вторичного
цементита, а следовательно, к увеличению
количества остаточного аустенита за
счет снижения температуры мартенситного
превращения. Так как аустенит -
относительно мягкая фаза, то увеличение
перегрева заэвтектоидной стали в
конечном итоге приводит к снижению
твердости закаленной стали.
Охлаждение малоуглеродистых и среднеуглеродистых сталей при закалке на мартенсит осуществляется в воде, а стали с содержанием углерода свыше 0,65% охлаждают, как правило, в масле. Это обусловлено тем, что закалочные напряжения в высокоуглеродистых сталях могут привести к образованию микро- и макротрещин, поэтому такие стали и охлаждают в менее резких закалочных средах.
При охлаждении стали со скоростью, меньшей критической, например, tj<$,**'w<r (см.рис.2), имеет место превращение аустенита феррито-цементитную смесь, которая, в зависимости от степени дисперсности, называется перлитом, сорбитом или трооститом.
Троостит - более мелкая структура, чем сорбит, а сорбит - более мелкая, чем перлит.
Термическая операция, заключающаяся в нагреве стали до температур немного выше Ac3 или Ac1, выдержке при этих температурах и последующем охлаждении, обеспечивающем распад аустенита в перлитной области с целью получения структуры, близкой к равновесному состоянию, называется отжигом.
Чем больше скорость охлаждения, тем дисперснее становится структура и тем выше твердость стали. Твердость и прочность феррито-цементитной смеси прямо пропорциональна площади поверхности раздела между ферритом и цементитом. Поэтому с увеличением степени дисперсности феррито - цементитной структуры, то есть понижением температуры распада аустенита, твердость, пределы прочности и текучести возрастают (рис.З).
Относительное удлинение и относительное сужение наивысшее у сорбита. При переходе к трооститу (более низкой температуре превращения) пластичность уменьшается.
Образование верхнего бейнита (распад при 550 - 450°С) снижает пластичность стали по сравнению с получаемой для продуктов распада аустенита в перлитной области. Твердость и прочность при этом не изменяются или несколько снижаются. Пониженная пластичность верхнего бейнита связана с выделением сравнительно грубых карбидов по границам ферритных зерен.
В результате распада аустенита в нижней области промежуточного превращения (рис.3) наблюдается некоторое повышение свойств: прочности, твердости и пластичности. Нижний бейнит по сравнению с продуктами распада аустенита в перлитной области (сорбит, троостит) имеет более высокую твердость и прочность при сохранении высокой пластичности.
Высокие прочностные свойства нижнего бейнита объясняются наличием внедренных атомов углерода и большой плотностью дислокаций в мартенситной фазе, а также образованием включений дисперсных карбидов, расположенных в кристаллах этой фазы.
При отжиге сталь, нагретую до температуры выше Ac3 (или выше Ас1 - неполный отжиг), охлаждают медленно (рис. 2) вместе с печью. При этом получается структура перлита (в эвтектоидных сталях) или перлита и феррите (в доэвтектоидных сталях). Твердость стали после отжига должна быть минимальной; она зависит от состава стали. Отжиг проводят:
-
для фазовой перекристаллизации и устранения перегрева, который проявляется в виде видманштеттовой структуры, ферритной или цементитной сетки;
-
для сфероидизации цементита в стали, улучшения ее штампуемости в холодном состоянии и обрабатываемости резанием стали с пониженной твердостью;
-
для гомогенизации, то есть уменьшения химической неоднородности стали.
Нормализацией называют такую термическую обработку, при которой сталь, нагретую до температуры выше Ас3 на 30 - 50°С (рис. I), охлаждают на спокойном воздухе (скорость охлаждения соответствует V2, рис. 2).
Ускоренное охлаждение на воздухе по сравнению с охлаждением с печью, как при отжиге, приводит к распаду аустенита при более низких температурах, что увеличивает количество перлита или, точнее, квази-эвтектоида типа сорбита или троостита. Для некоторых высоколегированных сталей охлаждение на воздухе, по существу, является закалкой.
Нормализация, естественно, более дешевая термическая операция, чем отжиг, так как печи используют только для нагрева и выдержки при температуре нормализации, охлаждение осуществляет на воздухе, вне печи.
Для низкоуглеродистых нелегированных сталей разница в свойствах между отожженным и нормализованным состоянием практически отсутствует, рекомендуется эти стали подвергать не отжигу, а нормализации. Для среднеуглеродистых сталей (0,3 - 0,5 %С) различие в свойствах нормализованной и отожженной стали более значительно; в этом случае нормализация не может заменить отжига.
Для этих сталей нормализацией часто заменяют более дорогую операцию улучшение (закалка + высокий отпуск). Например, ударная вязкость стали 45 после нормализации повышается в полтора раза по сравнению с ненормализованной, испытанной после прокатки или ковки. Значительное повышение механических свойств позволило ввести нормализацию как окончательную термическую обработку для таких ответственных деталей, как коленчатые валы автомобилей из углеродистой стали 45; после нормализации шейки коленчатых валов подвергают высокочастотной закалке.
Таким образом, видно, что изменяя скорость охлаждения стали после нагрева ее выше критических точек, можно изменить ее строение, а следовательно, и свойства в очень широких пределах. Получать различную скорость охлаждения стали можно путем использования различных сред.
ОТПУСК ЗАКАЛЕННОЙ СТАЛИ
Отпуском называют нагрев закаленной стали до температуры ниже критической точки Ac1, выдержку при заданной температуре с последующим охлаждением до комнатной температуры.
После закалки стальные изделия находятся в напряженном состоянии. Кроме того, структура и свойства закаленной стали нестабильны, склонны к постепенному изменению. Часто при вылеживании закаленных изделий уже через несколько часов в них появляются трещины, большие поводки и коробления.
Поэтому отпуск закаленных изделий во всех случаях является обязательной операцией. Его следует проводить немедленно после закалки.
Нагрев закаленной стали, со структурой, состоящей из мартенсита и остаточного аустенита, приводит к разнообразным превращениям. В стали с содержанием углерода 1,09 %, взятой в качестве примера, наблюдаются следующие изменения структуры при нагреве.
I. В интервале температур 80 - 180°С тетрагональный мартенсит переходит в отпущенный с образованием высокодисперсных частиц карбида, когерентно (непрерывно) связанных со старой решеткой матрицы.
На этой стадии отпуска мартенсит все еще содержит в растворе около 0,4 % С, а твердость стали за счет выделения карбида может даже слегка повыситься
2. При нагреве закаленной стали до температур 200-300°С остаточный аустенит, который всегда в том или ином количестве содержится в стали, закаленной на мартенсит, превращается в отпущенный мартенсит, содержащий около 0,2% С. При этом продолжается выделение карбидных частиц.
Отпуск закаленной на мартенсит стали до температур, не превышающих 250 - 300°С, носит название низкого отпуска и применяется, как правило, для инструмента, требующего высокую твердость.
3. На третьей стадии отпуска при нагреве до температур 300 -400°С (средний отпуск) происходит дельнейшее уменьшение углерода в мартенсите до равновесного состояния (0,006%), таким образом мартенсит превращается в феррит. При этом происходит срыв когерентности решеток цементита и мартенсита (феррита), благодаря чему в стали происходит резкое уменьшение внутренних напряжений.
Средний отпуск применяется для деталей, требующих повышенной прочности и твердости в сочетании с вязкостью (шестерни, валы и др.)
или же требуется высокий предел текучести (рессоры, пружины).
При нагреве выше 450°С (высокий отпуск) происходит укрупнение (коагуляция) мелких частиц цементита. При этом образуется сорбит, который имеет зернистое, а не пластинчатое строение. Такой вид отпуска обычно применяют для деталей, которые работают с ударными нагрузками, то есть там, где нужна повышенная вязкость.
Таким образом, троостит, сорбит и перлит можно получить не только из аустенита путем его распада при определенной скорости охлаждения, но и путем отпуска мартенсита, при распаде переохлажденного аустенита, при этом структура троостита и сорбита отпуска зернистая, а не пластинчатая, которая получается при распаде переохлажденного аустенита (рис. 4). Очевидно, что зернистые структуры будут иметь более высокую вязкость и больший предел циклической прочности.
Все виды отпуска - низкий, средний и высокий - предназначены для изменения механических свойств закаленной стали. Изменение твердости закаленных сталей с различным содержанием углерода в зависимости от температуры отпуска показано на рис. 5.
ВЛИЯНИЕ УГЛЕРОДА
НА ТВЕРДОСТЬ ТЕРМИЧЕСКИ ОБРАБОТАННЫХ
СТАЛЕЙ
Механические свойства сталей, в том числе и твердость, зависят от их внутреннего строения. Строение углеродистой стали прежде всего зависит от ее химического состава, который в основном характеризуется содержаниям углерода. При постоянном составе стали ее структурное состояние может быть изменено термической обработкой.
Из существующих видов термической обработки отжиг, с одной стороны, и закалка -с другой, дают наиболее резкое отличие в структуре и свойствах стали. В результате отжига сталь приобретает структуру, близкую к равновесной, прочностные свойства углеродистой стали при этом отличается сравнительно низким уровнем, а пластические - повышенным. Закалка, наоборот, дает крайне неравновесную структуру, высокие значения прочностных свойств и низкие - пластических.
ВЛИЯНИЕ УГЛЕРОДА НА СТРУКТУРУ И СВОЙСТВА
ОТОЖЖЕННЫХ СТАЛЕЙ
Ранее были изучены структуры чистых железоуглеродистых сплавов. Технические стали отличатся от чистых железоуглеродистых сплавов тем что содержат, кроме железа и углерода, еще ряд элементов примесей неизбежно попадающих в стали в связи с условием производства (плавки).
Если содержание примесей не превышает количества, указанного в ГОСТ 380-88, то их влияние на свойства сталей незначительно. Следовательно, структура и свойства технических сталей могут характеризоваться почти так же, как и чистых двойных сплавов, то есть в полном соответствии с диаграммой состояния железо - углерод. В соответствии с диаграммой состояния после отжига в равновесном состоянии структура стали представляет собой смесь феррита и цементита, в которой количество последнего увеличивается пропорционально содержанию углерода. Ясно, что свойства медленно охлажденных (отожженных) сталей будут определяться прежде всего свойствами и количеством составляющих фаз. Основной (преобладающей) фазой в сталях является феррит. Механические свойства феррита характеризуются следующими величинами:
Предел прочности при растяжении, МПа 250
Предел текучести при растяжении, МПа 120
Относительное удлинение, % 50
Относительное сужение, % 85
Твердость, НВ 80
Эти показатели могут, изменяться в некоторых пределах, так как на свойства феррита влияет ряд факторов (например, увеличение размеров зерен понижает твердость, а увеличение содержания примесей повышает твердость).
Цементит твердый (НВ - 800) и хрупкий. С изменением содержания углерода изменяется структура стали.
Структура технически чистого железа, содержащего до 0,006 %С, состоит только из феррита, что и определяет его низкие прочностные свойства. Технически чистое железо, содержащее 0,007 - 0, 02 %С, наряду с ферритом имеет в структуре небольшое (не более 0,29 %) количество цементита третичного, располагающегося в виде сравнительно крупных включений по границам ферритных зерен. Цементит третичный при таком его расположении оказывает незначительное влияние на прочностные свойства, несколько повышая их.
В структуре железоуглеродистых сплавов, содержащих свыше 0,02%С, появляется двухфазная структурная составляющая - перлит. Механические свойства перлита, в частности твердость, определяются количественным соотношением присутствующих в нем феррита (88%) и цементита (12%), так и формой и дисперсностью частичек цементита. Поэтому прочность перлита может изменяться от 550 МПа для крупнопластинчатого до 820 МПа для тонкопластинчатого, а твердость от НВ = 160 ед. до НВ = 250 ед.
Для, заэвтэктоидных сталей (углерода свыше 0,8э %), структура которых, кроме пластинчатого перлита, содержит цементит вторичный, наблюдается дальнейшее повышение твердости. Однако другая прочностная характеристика - предел прочности, достигнув наибольшего значения при 0,8 - 0,9%, при более высоких содержаниях углерода понижается. Это обусловлено наличием большого количества хрупкой цементитной фазы, а также тем, что часть ее (цементит вторичный) расположена в виде сплошной оболочки по границам зерен. В результате этого снижается сопротивление отрыву и предел прочности.
Пластические свойства сталей (относительное удлинение и относительное сужение, ударная вязкость) по мере увеличения содержания углерода в стали непрерывно понижаются.
ВЛИЯНИЕ УГЛЕРОДА НА СТРУКТУРУ И СВОЙСТВА ЗАКАЛЕННЫХ СТАЛЕЙ
Основная цель, преследуемая при закалке углеродистых сталей, - получение высоких прочностных свойств. Достигается эта цель за счет получения высокопрочной твердой мартенситной фазы, образующейся из аустенита при быстром охлаждении, то есть при мартенситном. превращении.
Мартенситное превращение в чистом железе и в безуглеродистых сплавах способно привести к повышению прочностных свойств по сравнению с отожженным состоянием. Так по сравнению с обычной ферритной структурой твердость железа а результате мартенситного превращения возрастает с 60 до 200 НV а предел прочности -с 200 до 900 МПа. Высокая твердость мартенсита объясняется повышенной плотностью дефектов в его решетке: двойниковых прослоек и дислокаций.
При закалке сталей достигается значительно большее упрочнение, чем в безуглеродистых железных сплавах, причем эффект закалки повышается с увеличением содержания углерода. Это можно объяснить следующим образом.
При мартенситном превращении в сталях весь углерод, растворенный в аустените остается в твердом растворе. Мартенсит - пересыщенный твердый раствор углерода в α - железе. Сохранение углерода в твердом растворе при мартенситном превращении вызывает искажение решетки, поэтому мартенсит имеет тетрагональную пространственную решетку, в которой один период С больше другого – А. Тетрагональность прямопропорциональна содержанию углерода. Большей пластичностью обладают более симметричные решетки, так как в них больше плоскостей легкого скольжения. Твердость же определяется сопротивлением внедрению в тело индентора, что связано с пластичностью.
Очень большое влияние на твердость мартенсита оказывает фазовый наклеп, возникающий при закалке стали. Природа фазового наклепа заключается в следующем. Мартенсит по сравнению с другими фазовыми составляющими стали и особенно аустенитом имеет наибольший удельный объем. Поскольку рост мартенситных кристаллов протекает с увеличением объема, то окружающий аустенит и мартенситные пластины подвергаются сильному наклепу. Этот наклеп называется фазовым, так как он связан с фазовым превращением.
С увеличением содержания углерода в стали удельный объем мартенсита возрастает значительно интенсивнее, чем удельный объем аустенита.
Необходимо помнить, что в зависимости от температуры нагрева закалку называют полной и неполной. При полной закалке сталь переводят в однофазное состояние, то есть нагревают выше критической температуры Ac3, при неполной закалке сталь нагревают до межкритических температур - между Ас1 и Ac3.
При быстром охлаждении в процессе закалки не весь аустенит успевает превратиться в мартенсит. Остается какая то его часть – остаточный аустенит, приводящий к снижению твердости и прочности. Количество остаточного аустенита прямопропорциоанально количеству углерода в стали.
Таким образом, углерод оказывает существенное влияние на структуру и свойства как отожженных, так и закаленных сталей.
ОПРЕДЕЛЕНИЕ
ПРОКАЛИВАЕМОСТИ СТАЛИ
Прокаливаемостью называется способность стали получать при закалке структуру мартенсита или троостит-мартенсита, а следовательно, и высокую твердость на ту или иную глубину по сечению детали. Толщина закаленного поверхностного слоя зависит как от характера закалочной среды, так и от природы стали.
Необходимо помнить, что при охлаждении стали ниже эвтектоидной температуры (Ac1). ayстенит становится неустойчивым и претерпевает превращения, характер которых зависит от скорости охлаждения. Если действительная скорость охлаждения стали будет превышать верхнюю критическую скорость закалки (рис.1), то сталь получит мартенситную структуру. Более медленное охлаждение, но со скоростью больше нижней критической приводит к образованию троостито - мартенситной структуры, а еще более медленное охлаждение приводит к переходу всего аустенита в феррито - цементитную смесь.
При закалке стального изделия скорость охлаждения по его сечению резко неоднородна и распределяется по сечению так, как показано на рисунке 1. Если действительная скорость охлаждения на некоторой глубине окажется меньше нижней критической, то изделие прокалится только на некоторую глубину. В этом случае в сердцевине произойдет распад аустенита с образованием пластинчатой феррито - карбидной структуры (троостита, сорбита или перлита). За глубину закаленного слоя условно принимают расстояние от поверхности до полумартенситной зоны (50 % мартенсита + 50 % троостита).
Диаметр заготовки, в центре которой после закалки в данной охлаждающей среде образуется полумартенситная структура, называют критическим диаметром. Величина критического диаметра определяет размер сечения изделия, прокаливающегося насквозь, то есть получающего высокую твердость, а после отпуска - и высокие механические свойства по всему сечению. Заготовки, диаметр которых меньше Дк, будут прокаливаться насквозь, а заготовки, диаметр которых больше Дк, насквозь прокаливаться не будут.
Прокаливаемость тем выше, чем меньше критическая скорость закалки, то есть чем выше устойчивость переохлажденного аустенита и чем правее на диаграмме изотермического распада аустенита расположены С - кривые. Поэтому все факторы, уменьшающие величину критической скорости закалки (повышающие устойчивость переохлажденного аустенита) увеличивают прокаливаемость. Основные факторы, влияющие на величину критической скорости закалки:
- Состав аустенита. Все элементы, растворимые в аустените (за исключением кобальта), замедляют превращение, то есть сдвигают С - кривые вправо;
- Нерастворенные частицы (карбиды, оксиды, интерметаллические соединения). Эти частицы ускоряет распад аустенита, так как являются дополнительными центрами перекристаллизации;
- Неоднородный аустенит быстрее превращается в перлит, так как скорость превращения определяется в этом случае менее насыщенной честью твердого раствора, а чем меньше в аустените углерода, тем левее расположены С - кривые;
- Размер зерна аустенита. Увеличение размера зерна замедляет превращение, так как центры перекристаллизации образуются преимущественно по границам зерен, а чем крупнее зерно, тем меньше суммарная протяженность границ.
Действительная скорость охлаждения зависит от того, в каком охладителе производится закалка. Например, масло охлаждает медленнее, чем вода. Следовательно, Дк.м.<Дк.в. Чтобы не ставить прокаливаемость в зависимость от способа охлаждения вводят понятие идеальный критический диаметр. Это диаметр максимального сечения, прокаливающегося насквозь в идеальной жидкости, отнимающей тепло с бесконечно большой скоростью.
Критический диаметр - важная и удобная величина при назначении марки стали на изделие. Если нужно, чтобы изделие при термической обработке прокаливалось насквозь, следует выбрать такую сталь, чтобы Дк<Дизд.
Для определения прокаливаемости применяют следующие методы: по излому, измерение твердости по сечению закаленного бруска, метод торцевой закалки.
По излому прокаливаемость определяется на образце сечением 20 - 20 мм из инструментальной стали с низкой прокаливаемостью. Закаленному слою соответствует фарфоровидная часть излома.
Измерением твердости определяют прокаливаемость на дисках, вырезанных из закаленного бруска длиной не менее четырех диаметров.
Метод торцевой закалки согласно ГОСТ 5657-69 является основным. Прокаливаемость определяют на стандартных образцах. Образец нагревают до температуры закалки стали данной марки. Время прогрева образца до температуры закалки составляет 30 - 50 минут. Выдержка образца при температуре закалки после нагрева - 30 минут. При нагреве торец образца, подлежащий охлаждению водой, должен быть предохранен от окисления и обезуглероживания. Если нагрев производят в печи без контролируемой атмосферы, то образец помещают в стальной цилиндрический стакан с крышкой. Торцом, предназначенным для охлаждения, образец ставят на графитовую пластину или на слой отработанного графита. Время с момента извлечения образца из печи до начала охлаждения не должно превышать 5 секунд. Образец должен находиться под струей воды до полного охлаждения (не менее 10 минут). Температура воды должна быть в пределах от 5 до 25°С. Закалка образца производится в специальной установке, состоящей из держателя образца и сопла. Установка должна соответствовать следующим основным требованиям:
а) образец должен устанавливаться вертикально: торцовой поверхностью над соплом. Оси образца и сопла должны совпадать;
б)
диаметр сопла, высота свободной струи
воды над соплом и расстояние от струи
до торца должны соответствовать
значениям, указанным в ГОСТе;
в) высота струи в процессе охлаждения образца должна быть постоянной;
г) вода должна касаться только торца образца, не омывая его цилиндрической поверхности.
Для замера твердости по всей длине закаленного образца сошлифовывают две диаметрально противоположные площадки.
Для построения кривой прокаливаемости стали на сошлифованных площадках производят замер твердости по Роквеллу - HRC ). Замер твердости начинают на расстоянии 1,5 мм от закаленного торца в осевом направлении. Первые 16 замеров от торца образца производят с интервалом 1,5 мм, а затем - через 3 мм. По этим данным строят график зависимости твердости от расстояния до торца (рис. 2). Взяв из таблицы значение твердости полумартенситной зоны, соответствующее содержанию углерода в исследуемой стали, определяют расстояние (рис. 2) до полумартенснтной зоны. Определив это расстояние, можно по номограмме (рис.3,) найти критический диаметр цилиндирической детали (с различным, отношением высоты к диаметру), шара или параллелепипеда для различных условий охлаждения.
В верхней части номограммы(рис. 3) даны две шкалы I и 2, характеризующие расстояние от охлажденного торца образца. Для определения наибольшего диаметра (называемого критическим) детали, прокаливающейся полностью с образованием мартенситной структуры, используют шкалу I, а для определения наибольшего диаметра для полумартенситной зоны (50 % мартенсита и 50 % троостита) - шкалу П. Схема пользования номограммой приведена на рисунке 3. На шкале I или соответственно шкале П находят расстояние от торца до конца мартенситной или полумартенситной зоны, найденное экспериментально для данной стали, Из этой точки опускают перпендикуляр до пересечения с линией по номограммы (точка I на рис.3), указывающей идеальное охлаждение. Из этой точки проводят горизонтальную линию влево до пересечения с линией номограммы (точка 2), соответствующей нужной в искомом случав среде охлаждения (вода, масло, воздух). Затем из точки 2 опускают перпендикуляр на шкалу "размер, мм" (в нижней части номограммы). В точке пересечения читается ответ - наибольший диаметр образца, прокаливающегося полностью в выбранной закалочной жидкости.
ЛЕКЦИЯ 9
ХИМИКО – ТЕРМИЧЕСКАЯ ОБРАБОТКА:
ЦЕМЕНТАЦИЯ СТАЛИ
СУЩНОСТЬ ПРОЦЕССА ЦЕМЕНТАЦИИ
Цементация - это химико-термическая обработка, при которой поверхность стальных деталей насыщается углеродом.
Цель цементации - получение на поверхности детали высокой твердости и износостойкости в сочетании с вязкой сердцевиной.
Цементации подвергают стали с низким содержанием углерода 0,1 - 0,2%. Насыщение поверхностного слоя происходит при нагреве детали до определенной температуры в среде, легко выделяющей углерод в активном состоянии. В результате изменения химического состава поверхностного слоя меняется также его фазовый состав и микроструктура. Основные параметры химико-термической обработки - температура и продолжительность выдержки. Она обеспечивает получение упрочненного слоя одинаковой толщины от поверхности. На поверхности концентрация углерода достигает 1,1 - 1,2 %. Более высокое содержание углерода приводит к образованию значительных количеств вторичного цементита, сообщающего слою повышенную хрупкость. Глубина цементованного слоя зависит не только от температуры, при которой осуществляется процесс, но и от времени выдержки при этой температуре (рис. I).
Обычно скорость цементации составляет примерно 0,1 мм за 1ч выдержки. Поскольку глубина цементованного слоя редко требуется более 0,5 мм, процесс осуществляют,- за 8 - 12 часов. Цементацию проводят в твердом, жидком и газообразном карбюризаторах. Среда, поставляющая углерод к поверхности детали, подвергаемой цементации, называется карбюризатором.
Твердая цементация производится в специальных ящиках, в которых детали 1 (см.рис.2) укладываются попеременно с карбюризатором 2. Ящики закрываются крышками и замазываются огнеупорной глиной для предотвращения утечки газов.
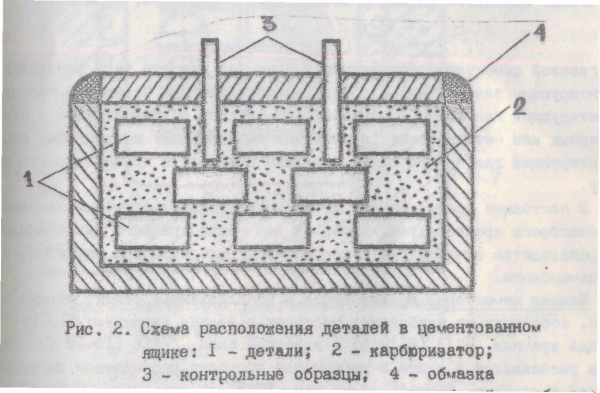
В качестве твердого карбюризатора используют дубовый или Березовый древесный уголь и активизаторы ВаСО3 или Nа2СО3 (сода). При нагреве до температуры 930 - 950°С идут диффузионные процессы при которых образующиеся активные атомы углерода диффундируют в кристаллическую решетку железа. Процесс цементации в твердом карбюризаторе проводят выше Ас3, когда сталь находится в аустенитном состоянии, в котором растворяется до 2 % углерода. Процесс твердой цементации - продолжительная операция и занимает в зависимости от требуемой глубины цементации несколько часов. Такая продолжительность процесса объясняется
малой
скоростью прогрева ящика, наполненного
нетеплопроводным карбюризатором. Для
контроля хода процесса цементации в
ящик через отверстия вставляет два
контрольных образца (свидетеля) 3,
изготовленных из той же стали. По излому
контрольных образцов судят, достигла
ли глубина цементованного слоя заданной
величины. Увеличение скорости цементации
достигается применением цементации в
газовых средах.
При газовой цементации (впервые была осуществлена Аносовым П.Д. на Златоустовском заводе) детали нагревают в герметичных печах в атмосфере углеродосодержащих газов. Для газовой цементации используют природный газ (содержит до 92 - 96 % метана) или искусственные газы, полученные пиролизом жидких углеводородов - керосина, бензола.
При газовой цементации герметически закрытая реторта печи наполнена цементирующим газом. Чаще с определенной скоростью через нее проходит цементирующий газ (рис. 3). Газовая цементация осуществляется в стационарных или методических (непрерывно действующих) конвейерных печах. Цементирующий газ приготовляют отдельно и подают в цементационную реторту.
В настоящее время газовая цементация является основным процессом для массового производства, и только для мелкосерийного, или единичного производства экномически целесообразен более простой способ твердой цементации.
Жидкая цементация производится в расплавленных солях, обычно в солях, состоящих из карбонатов щелочных металлов. Эту смесь расплавляют в ванне и цементации проводят посредством погружения деталей в расплав. Процесс ведут при 850°С на протяжении 0,5 - 3,0 часов, при этом глубина сдоя получается в пределах 0,2 - 0,5 мм. Основное достоинство процесса - возможность непосредственной закалки из цементационной ванны и малые деформации обработанных изделий.
В условиях индивидуального и мелкосерийного производства некоторое применение нашла цементация из паст. В этом случае на обрабатывавшуюся поверхность наносится обмазка, содержащая сажу (33 - 70 %), древесную пыль (20 - 60 % ), желтую кровяную соль (5 - 20 %) и другие компоненты. В качестве связующих материалов используют органические, органоминеральные и неорганические клеи. Толщина обмазки должна быть в 6 - 8 раз больше требуемой толщины цементованного слоя.
В качестве карбюризатора используют также керосин, бензол и некоторые масла. Интенсивность подачи определяют по
количеству
капель жидкости в I
мин и составляет от 120 - 180 капель.
Кроме перечисленных видов цементации в последние годы появились: цементация из паст, вакуумная цементация, цементация в псевдосжиженном слое, ионная цементация, которые предназначены для цементации деталей сложного профиля, ответственного назначения для сокращения длительности процесса.
ТЕРМИЧЕСКАЯ ОБРАБОТКА ЦЕМЕНТОВАННЫХ ДЕТАЛЕЙ
Полученный в результате цементации и последующего медленного охлаждения наружный слой содержит более 0,8 % углерода и имеет структуру заэвтектоидных сталей - перлит и вторичный цементит. Глубже лежит слой эвтектоидного состава с перлитной структурой, а далее - слой с феррито - перлитной структурой. Кроме того, после цементации из-за длительной выдержки при высоких температурах стали приобретают крупнозернистость.
Эти обстоятельства необходимо учитывать при назначении обязательной после цементации термической обработки, Целью термообработки цементованной стали является упрочнение поверхности с одновременным измельчением зерна и получением вязкой сердцевины. В зависимости от назначения детали применяет различные варианты термической обработки. Менее ответственные детали подвергают закалке непосредственно с цементационного нагрева с последующим низким отпуском (рис. 4,а).
Крупное зерно аустенита, выросшее в результате длительной цементации, дает .грубокристаллический мартенсит отпуска в поверхностном слое и крупнозернистую феррито -перлитную структуру в сердцевине детали. Эти недостатки в определенной мере устраняются при использовании наследственно мелкозернистых сталей, применении газовой цементации, сокращающей время пребывания стали при высокой температуре. Использование подстуживания при закалке до 750 - 800°С снижает внутренние напряжения, а обработка холодом уменьшает количество остаточного аустенита в цементованном слое.
При более высоких требованиях к структуре детали после цементации: ее подвергают охлаждению на воздухе, однократной закалке с нагревом выше Ас3 и низкому отпуску (ряс. 4,6). При этом в сердцевине и на поверхности детали происходит перекристаллизация и измельчение зерна. Однако в поверхностном высокоуглеродистом слое происходит некоторый перегрев, так как оптимальный закалочный нагрев заэвтектоидных сталей - это нагрев выше Ac1, но ниже Асm.
Особо ответственные детали после цементации подвергают двойной закалке с низким отпуском (рис. 4,в). При первой закалке с температуры на 30 - 50°С выше Асз происходит перекристаллизация сердцевины детали с образованием мелкого аустенитного зерна, обеспечивающего мелкозернистость продуктов распада. Одновременно при этом цементитная сетка в цементованном слое растворяется.
При нагреве под вторую закалку мартенсит, полученный после первой закалки, претерпевает отпуск и при этом образуются глобулярные карбиды, увеличивающие твердость поверхностного заэвтектоидного слоя. Кроме того при второй закалке с температуры выше Ac1 на 30 - 50°С обеспечивается мелкое зерно в поверхностном слое.
После такой термообработки поверхностный зазвтектоидный слой будет иметь структуру отпущенного мартенсита с включениями глобулярных карбидов. Структура сердцевины определяется химическим составом стали. При цементации углеродистой стали из-за низкой прокаливаемости сердцевина имеет феррито-перлитную структуру. Легированная сталь при цементации позволяет получать в сердцевине структуру сорбита, троостита или даже мартенсита, но благодаря низкой концентрации углерода сердцевина будет иметь высокую ударную вязкость.
На рис. 5 показана структура стали, содержащей в исходной состоянии 0,15 %С, после цементации без дополнительной термической обработки (охлаждение после цементации было медленным). Микроструктура поверхностного цементованного слоя состоит из перлита и сетки цементита. По мере удаления от поверхности к сердцевине количество перлита непрерывно уменьшается и ближе к центру образца - исходная структура стали, состоящая из феррита и незначительного количества перлита.
На рас. 6 и 7 показана структура цементованной стали после окончательной термической обработки, то есть нормализации при 900°С, закалки от 770°С и отпуска при 150°С. Структура поверхностного сдоя -мартенсит отпуска (см.рис. б). Структура сердцевины - мартенсит и феррит (рис. 7). Образец закалился насквозь, но так как закалка была произведена от 770°С, то для сердцевины это будет неполной закалкой и в структуре наряду с мартенситом встречается феррит (светлые зерна).
После цементации и термической обработки твердость поверхностных слоев составляет (НRC58 – 63).
Цементации
подвергают разнообразные детали:
зубчатые колеса, поршневые пальцы,
червяки, оси и другие детали, иногда
значительных размеров (например,
крупногабаритные кольца и ролики
шарикоподшипников).
ЛЕКЦИЯ 10
Маркировка и применение легированных сталей
Введение
В соответствии с классификацией, предложенной Н. Т. Гудцовым, все химические элементы содержащиеся в стали подразделяются на примеси и легирующие элементы, которые можно подразделить на четыре группы:
1. Постоянные или обыкновенные примеси. К этой группе относятся марганец, кремний, алюминий, титан, которые попадают в сталь в процессе раскисления и находятся в стали в незначительном количестве. К постоянным примесям следует отнести серу и фосфор.
2. Скрытые примеси. Это кислород, водород и азот, присутствующие в любой стали в очень малых количествах.
3. Случайные примеси. К этой группе относятся примеси, попадающие в сталь из шихтовых материалов или вследствие каких-либо случайных причин (например, при переплавке металлического лома – луженого, оцинкованного).
4. Легирующие элементы. Элементы, специально вводимые в сталь в определенных количествах с целью изменения ее строения и свойств, называются легирующими элементами. Для легирования стали наиболее часто применяют хром, никель, марганец, кремний, вольфрам, ванадий, молибден, титан, медь и др.
Легированными сталями называют стали, содержащие в своем составе, кроме железа и углерода, специально введенные элементы, которые способны изменить ее строение, а следовательно, и свойства.
Классификация легированных сталей
Углеродистые стали можно классифицировать по следующим признакам:
I. Классификация по назначению. В зависимости от назначения стали можно объединить в следующие группы:
а) конструкционная сталь, идущая на изготовление деталей машин. К ним относят: цементуемые, улучшаемые, строительные.
б) инструментальная сталь, идущая на изготовление режущего, измерительного, штампового и прочего инструмента.
в) стали и сплавы с особыми физико-химическими свойствами. К ним относятся стали, обладающие каким-нибудь резко выраженным свойством: нержавеющие, жаропрочные, теплоустойчивые, износоустойчивые, с особенностями теплового расширения, с особыми магнитными и электрическими свойствами и т. д.
II. Классификация по содержанию углерода:
а) малоуглеродистые (0,025 0,25 % С);
б) среднеуглеродистые (0,25 0,6 % С);
в) углеродистые ( 0,6 % С).
III. Классификация по содержанию легирующих элементов:
а) низколегированные стали с общим содержанием легирующих элементов не более 3 %;
б) среднелегированные стали – от 3 до 10 %;
в) высоколегированные стали – свыше 10 %;
г) сплавы – более 45 %.
IV. По качеству. Качество сталей определяется содержанием в них вредных примесей: серы и фосфора. По качеству легированные стали подразделяются на группы:
а) качественные (до 0,035 % S, до 0,035 % Р);
б) высококачественные (до 0,025%S, до 0,025%Р);
в) особовысококачественные (до 0,015 % S, до 0,025 % Р).
V. Классификация по химическому составу. В зависимости от состава легированные стали классифицируются как никелевые, хромистые, хромоникелевые, хромоникельмолибденовые и тому подобное, т. е. по виду легирующих элементов входящих в сплав.
VI. Классификация по структуре (подробно будет рассмотрена в лабораторной работе).
Маркировка легированных сталей
Химический состав легированной стали является основой для установления ее марки по ГОСТу. Маркировка легированных сталей позволяет в краткой форме указать примерный состав стали. В ее основу положена буквенно-цифровая система. Легирующие элементы обозначают буквами: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К – кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий.
Каждая марка составляется из сочетания букв и цифр. В конструкционных сталях первые две цифры указывают среднее содержание углерода в сотых долях процента. В инструментальных сталях первая цифра указывает на среднее содержание углерода в десятых долях процента, если его содержание 1 %. Если содержание углерода в инструментальных сталях 1 %, то цифра чаще отсутствует. Буквы обозначают легирующие элементы, а следующие за ними цифры – среднее содержание (в целых процентах) соответствующего легирующего элемента; отсутствие цифры указывает, что оно составляет примерно 1 1,5 % и менее. Исключение составляют дорогие и остродефицитные карбидообразующие элементы: Mo, W, V, Ti, их добавляют в небольшом количестве (например, до 0,3 % V и 0,1 % Ti), поэтому в расшифровке марки нужно указывать, что содержание этих элементов до 1 %.
Основная масса легированных сталей выплавляется качественными.
Высококачественные стали содержат меньше вредных примесей и обозначаются буквой «А», помещенной в конце марки.
Наиболее чистые по вредным примесям стали – особовысококачественные, обозначаются буквой «Ш» в конце марки (записывается через дефис).
Примеры маркировки:
30ХГС – конструкционная сталь, содержит 0,28 0,35 % С, в среднем 0,30 % С; 0,8 1,1 % Cr, в среднем 1,0 % Cr; 0,8 1,10 % Mn, в среднем 1,0 % Mn; 0,9 1,2 % Si, в среднем 1,0 % Si и соответствующее для качественной стали количество серы и фосфора ( 0,035 % S, 0,035 % Р).
30ХГС-Ш – конструкционная сталь, содержит 0,28 0,34 % С, в среднем 0,30 % С; 0,8 1,1 % Cr, в среднем 1,0 % Cr; 0,8 1,10 % Mn, в среднем 1,0 % Mn; 0,9 1,2 % Si, в среднем 1,0 % Si; сталь особовысококачественная, с минимальным содержанием вредных примесей ( 0,015 % S, 0,025 % Р).
12Х2Н4А – конструкционная сталь, содержит 0,09 0,15 % С, в среднем 0,12 % С; 1,25 1,65 % Cr, в среднем 2 % Cr; 3,25 3,65 % Ni, в среднем 4 % Ni; сталь высококачественная с содержанием 0,025 % S и 0,025 % Р.
7ХГ2ВМ – инструментальная сталь, содержит 0,68 0,76 % С, в среднем 0,7 % С; 1,5 1,8 % Сr, в среднем 1,0 % Cr; 1,8 2,30 % Mn, в среднем 2 % Mn; 0,55 0,90 % W, в среднем 1,0 % W; 0,5 0,8 % Mo, в среднем 1,0 % Мo; сталь качественная ( 0,025 % S и 0,025 % Р).
Х12М – инструментальная сталь, содержит 1,45 1,65 % С, в среднем более 1-го процента; 11,0 12,5 % Cr, в среднем 12 % Cr; 0,4 0,6 % Мо, в среднем 1,0 % Мо; сталь качественная ( 0,025 % S и 0,025 % Р).
Некоторые марки легированной стали в соответствующих ГОСТах выделены в особые группы и обозначаются буквами, которые ставятся впереди:
Ш – шарикоподшипниковая сталь. Должна обладать высокой твердостью, чистотой по неметаллическим включениям и минимальной пористостью. Содержание углерода от 0,95 до 1,05 %. Содержание хрома в десятых долях процента. Пример: ШХ15СГ – содержит 0,95 1,05 % С, в среднем 1,0 % С; 1,3 1,65 % Cr, в среднем 1,5 % Cr, 0,4 0,65 % Si, в среднем 1,0 % Si; 0,9 1,2 % Mn, в среднем 1,0 % Mn; 0,02 % S; 0,027 % Р.
Р – обозначает свойство стали – быстрорежущая (рапид – скорость). Быстрорежущие стали обладают высокой твердостью, прочностью, износостойкостью при высокой температуре. Содержание углерода в этих сталях 0,7 1,55 %. После буквы «Р» указывается содержание основного легирующего элемента данной стали – вольфрама (буквой не обозначается), в целых процентах. Во всех сталях данного типа содержится примерно 4 % хрома (также не обозначается в маркировке) и до 2-х % ванадия. Пример: Р18К5Ф2 – содержит 0,85 0,95 % С, в среднем 1,0 % С; 17,5 19 % W, в среднем 18 % W; 5,0 6,0 % Со, в среднем 5 % Со; 1,8 2,4 % V, в среднем 2 % V; 3,8 4,4 % Cr, в среднем 4 ,0 % Cr; 0,03 % S; 0,03 % Р.
Применение легированных сталей
Легирующие элементы придают стали специальные свойства, например, жаропрочные, коррозионно-стойкие, быстрорежущие, электротехнические, немагнитные, окалиностойкие и другие стали. Некоторые легированные стали, особенно коррозионно-стойкие, незаменимы в металлургической и химической промышленности, так как служат конструкционным материалом для изготовления аппаратуры и ее деталей, работающих в условиях одновременного воздействия высоких температур, давлений и агрессивных химических сред.
К недостаткам легированных сталей следует отнести высокую стоимость, сложность термической обработки, дефицитность некоторых легирующих элементов.
Конструкционные легированные стали. Их используют для изготовления деталей машин и механизмов, приборов, ответственных металлических конструкций. К этой группе относят среднелегированные и в основном низколегированные стали. Низколегированная сталь является переходной между углеродистыми и легированными сталями, она по своей основе соответствует малоуглеродистой стали (0,1 – 0,2%С), легированной кремнием, марганцем, хромом, никелем, медью, ванадием, ниобием и некоторыми другими элементами в небольших количествах.
Марганцовистые стали выпускают следующих марок: 10Г2, 14Г2, 35Г2, 50Г2 и др. Сталь 10Г2 отличается высокой пластичностью, хорошей свариваемостью, применяется для изготовления змеевиков, фланцев, штуцеров, пучков труб и крепежных деталей. Изделия из нее могут работать при низких температурах (до –70°С). Стали 35Г2, 50Г2 имеют повышенную износостойкость и служат для изготовления осей, небольших коленчатых валов, штоков, шестерен, пружин, амортизаторов. Марганцовистые стали хорошо поддаются обработке резанием и штамповке в холодном состоянии. Однако после закалки эти стали склонны к короблению и появлению трещин. При добавлении хрома и титана склонность марганцовистых сталей к таким дефектам существенно снижается.
Хромистые, хромоникелевые стали делят на цементуемые и улучшаемые. Из цементуемых сталей (например, 15Х, 20Х, 15ХРА, 12Х2Н4А, 18ХГТ) изготовляют детали (зубчатые колеса, шестерни, плунжеры, шлицевые валики, поршневые пальцы, толкатели и др.) относительно небольших размеров, работающие на износ при тяжелых нагрузках и имеющие высокие твердость поверхностного слоя и прочность сердцевины. Улучшаемые стали (например, 35Х, 38ХА, 35ХРА, 37ХН3А, 38ХНЗМФ) обладают высокой прочностью, пластичностью, высоким пределом выносливости, малой чувствительностью к отпускной хрупкости, хорошей прокаливаемостью (глубина закалки до 20 мм). Из них изготовляют детали крупных сечений, такие, как роторы турбокомпрессоров, фрикционные диски прессов, кривошипы, валы больших диаметров, шестерни крупных размеров и др.
Инструментальные легированные стали. Общие требования для всех инструментальных сталей – высокая твердость и прочность при удовлетворительной вязкости, хорошая износостойкость. Кроме того, инструментальные стали должны хорошо закаливаться, а сталь для режущего инструмента должна иметь высокую теплостойкость (красностойкость). Инструментальные стали применяют для изготовления режущего, ударно-штампового и измерительного инструмента.
Для режущего инструмента применяют низколегированные инструментальные стали с суммарным содержанием легирующих элементов от 1 до 6 % и углерода от 0,9 до 1,2 %. Основные легирующие элементы для сталей этой группы – хром, вольфрам или ванадий, которые, являясь сильными карбидообразующими элементами, несколько увеличивают твердость закаленной стали и значительно повышают ее износостойкость. Из сталей X, 9ХС, ХВГ, ХВСГ изготовляют сверла, фрезы, метчики, плашки, развертки, протяжки. На инструменте ставят клеймо с обозначением марки стали.
Для изготовления режущего инструмента, работающего при высоких скоростях резания и применяемого для обработки труднообрабатываемых материалов, применяют быстрорежущие стали, которые относят к высоколегированным сталям. Основные легирующие элементы для быстрорежущих сталей вольфрам, кобальт, молибден (более 1%) , ванадий, хром. Стали Р9Ф5, Р9К10, Р18К5Ф2, Р18, Р6М5 сохраняют красностойкость до 650 °С и твердость не ниже HRC 60. Высокие режущие свойства быстрорежущей стали достигаются термической обработкой, состоящей из нагрева до 1270—1290°С и последующего трехкратного отпуска при 560°С.
Легированные стали и сплавы с особыми свойствами. К этой группе относятся стали и сплавы на основе железа, в которых суммарное содержание легирующих элементов составляет более 10%: коррозионно-стойкие, износостойкие, жаропрочные, жаростойкие, магнитные, немагнитные, электротехнические, с особыми упругими свойствами и др.
Коррозионно-стойкие стали и сплавы получают при легировании железа с элементами, повышающими электрохимический потенциал сплава. Таким элементом, в частности, является хром. Сплавы, содержащие более 12% хрома, имеют электроположительный потенциал и обладают хорошей коррозионной стойкостью на воздухе, в воде, растворах солей, во многих щелочах, органических, а также в неорганических кислотах (в зависимости от их концентрации) и в других агрессивных средах. В состав этих сталей вводят также никель, марганец, титан, молибден.
Коррозионно-стойкие стали применяют для изготовления гальванических ванн, ванн промывки деталей в горячей воде, для изготовления деталей насосов для перекачки электролитов, теплообменной аппаратуры.
Коррозионно-стойкие хромистые стали 08X13, 12X13, 20X13, 30X13, 40X13, 12X17, 15Х25Т, 08Х17Т, 14Х17Н2 обладают достаточной стойкостью в условиях загрязненного воздуха, воды, пара, в растворах щелочей слабой концентрации, в некоторых кислотах. Наибольшая коррозионная стойкость указанных марок сталей достигается после термической обработки.
Хромоникелевые и хромоникелемолибденовые коррозионно-стойкие стали 12Х18Н9, 12Х18Н9Т, 04Х18Н10, Х17Н13М2Т, 14Х17Н2, 06ХН28МДТ получают увеличением содержания хрома или добавлением небольших количеств никеля к хромистой стали для увеличения ее коррозионной стойкости. Эти стали менее прочны, чем хромистые, но более пластичны. Широко применяют для сварных конструкций, работающих в высокоагрессивных средах, для изготовления деталей машин, используемых в пищевой промышленности.
Кроме того, из этих сталей изготовляют детали теплообменных аппаратов, мембран, сильфонов, вентиляторов (эксплуатирующихся в химических цехах). Для получения наибольшей коррозионной стойкости эти стали закаливают в воде после нагрева при 1100—1150°С.
Для экономии дорогостоящего никеля его частично заменяют марганцем. Например, сталь 10Х14Г14Н3 рекомендуется как заменитель стали 12Х18Н9; 08Х18Г8Н2Т как заменитель стали 08Х18Н10Т.
Эти стали и сплавы применяют для изготовления деталей и узлов автоматических линий нанесения гальванопокрытий (универсальных роботов, транспортируемых подвесок, устройств для загрузки деталей в гальванический барабан и др.).
Магнитные стали и сплавы в зависимости от магнитных свойств – значений коэрцитивной силы и магнитной проницаемости – делят на магнитно-твердые и магнитно-мягкие.
Магнитно-твердые стали и сплавы применяют для изготовления постоянных магнитов, они имеют большую коэрцитивную силу (напряженность магнитного поля, которое должно быть приложено к образцу для того, чтобы его размагнитить). Магниты небольшой мощности делают из хромистой стали и хромокобальтовой стали. Для изготовления магнитов небольшого размера, но большой мощности применяют магнитный сплав ЮНДК24 (9 % А1; 13,5 % Ni; 3 % Сu; 24 % Сo; остальное – железо), у него очень высокая коэрцитивная сила.
Магнитно-мягкие стали и сплавы обладают малой коэрцитивной силой и большой магнитной проницаемостью. К ним относят электротехническую нелегированную сталь или технически чистое железо и железоникелевые сплавы (пермаллои).
Жаропрочными называют стали и сплавы, способные работать в нагруженном состоянии и сохранять достаточную механическую прочность при высоких температурах (500—1000°С) в течение определенного времени от 100 до 100 000 ч.
Основными легирующими элементами в этих сталях и сплавах являются хром и никель. Для упрочнения сплава и уменьшения скорости ползучести добавляют тугоплавкие металлы: молибден, ниобий, вольфрам. Разработаны различные марки этих сталей, например 15Х11МФ, 15Х25Т, 09Х14Н16Б, ХН45Ю, 20Х23Н18; 40Х9С2, ХН70Ю, ХН77ТЮР. Жаропрочные стали используют преимущественно в котло- и турбиностроении.
Кроме рассмотренных выше сталей и сплавов в различных отраслях промышленности применяют также другие стали и сплавы: высокопрочные мартенситно-стареющие, графитизированные, стали и сплавы для работы при низких (ниже -80°С) температурах, сплавы с особыми тепловыми и упругими свойствами и др.
ЛЕКЦИЯ 11
Маркировка Цветных металлов и сплавов
Введение
Цветные металлы чаще всего имеют характерную окраску: красную, желтую, белую. Обладают большой пластичностью, малой твердостью, относительно низкой температурой плавления, (для них характерно отсутствие полиморфизма (кристаллическая решетка остается неизменной при разных температурах)). Наиболее типичным металлом этой группы является медь.
Цветные металлы подразделяются на:
1. Легкие металлы — бериллий, магний, алюминий, обладающие малой плотностью.
2. Тяжелые металлы – медь, никель, олово, свинец и сплавы на их основе.
Титан и сплавы на его основе занимают промежуточное положение между легкими и тяжелыми металлами.
3. Благородные металлы – серебро, золото, металлы платиновой группы (платина, палладий, иридий, родий, осмий, рутений).
К ним может быть отнесена и «полублагородная» медь. Обладают высокой устойчивостью против коррозии.
4. Легкоплавкие металлы — цинк, кадмий, ртуть, олово, свинец, висмут, таллий, сурьма и элементы с ослабленными металлическими свойствами – галлий, германий.
Медь и ее свойства
Медь – химический элемент I группы Периодической системы Д. И. Менделеева, порядковый номер 29, атомная масса 63,54. Медь – металл красного, в изломе розового цвета. Температура плавления 1083°С. Плотность меди 8,94 г/см3. Медь обладает наибольшими (кроме серебра) электропроводностью и теплопроводностью. В зависимости от чистоты медь изготовляют следующих марок: МОО (99,99 % Сu), МО (99,95 % Сu), М1 (99,9 % Сu), М2 (99,7 % Сu), М3 (99,50 % Сu). Присутствующие в меди примеси оказывают большое влияние на ее свойства.
Примеси Ni, Zn, Sb, Sn, А1, Аs, Fе, Р резко снижают электро- и теплопроводность меди, поэтому для проводников тока применяют медь марок МО и М1. Сурьма, кроме того, затрудняет горячую обработку давлением.
Примеси Рb, Вi образуют в меди легкоплавкие соединения; которые, выделяясь по границам зерен, затрудняют обработку давлением при содержании 0,005% Bi медь разрушается при горячей обработке давлением; при более высоком содержании висмута медь становится, кроме того, хладноломкой; на электропроводность эти примеси оказывают небольшое влияние.
Примеси кислорода и серы, образуют с медью хрупкие химические соединения Сu2О и Сu2S; на электропроводность эти примеси влияют слабо; сера улучшает обрабатываемость меди резанием; кислород, если он присутствует в меди, образует закись меди и вызывает «водородную болезнь». При нагреве меди в атмосфере, содержащей водород, происходит его диффузия в глубь меди. Если в меди присутствуют включения Сu2О, то они реагируют с водородом, в результате чего образуются пары воды по реакции Сu2О + Н2 2Сu + Н2О, протекающей с увеличением объема. Это создает в отдельных участках металла высокое давление и вызывает появление микротрещин, которые могут привести к разрушению детали.
Медь хорошо сопротивляется коррозии в обычных атмосферных условиях, в пресной и морской воде и других агрессивных средах, но обладает плохой устойчивостью в сернистых газах и аммиаке.
Механические свойства чистой меди:
– в литом состоянии: в = 150 200 МПа; = 15 25 %;
– прокатанная и отожженная: в = 250 270 МПа; = 40 50 %;
– после холодной деформации (нагартованная): в = 400 450 МПа;
= 12 %.
Сплавы на основе меди
Различают две основные группы медных сплавов: 1) латуни – сплавы меди с цинком; 2) бронзы – сплавы меди с другими элементами, в числе которых, но только наряду с другими, может быть и цинк.
Латунями называют двойные или многокомпонентные сплавы на основе меди, в которых основным легирующим элементом является цинк.
Зависимость механических свойств меди от содержания цинка показана на рис. 1. В начальный момент прочность и пластичность растут (максимальная пластичность (, %) у латуней достигает максимума при 30 % Zn) . После 32 % пластичность падает, а прочность продолжает возрастать примерно до 45 % Zn. При большем содержании цинка прочность сильно уменьшается из-за высокой хрупкости.
Однофазные латуни (структура сплава – однородные зерна) хорошо деформируются в горячем и холодном состояниях. Двухфазные латуни (структура сплава – разнородные зерна) малопластичны в холодном состоянии. Эти латуни обычно подвергают горячей обработке давлением при температурах выше 500 0С; двухфазные латуни по сравнению с однофазными латунями имеют большую прочность и износостойкость, но меньшую пластичность.
Латуни маркируются буквой Л, а за этой буквой указывается содержание меди в процентах. Таким образом, марка латуни Л96 означает, что в ней содержится 96 % меди и 4 % цинка. По ГОСТ 15527 – 70 в технике используют латуни Л96 (томпак), Л90, Л80, Л70, Л68 и Л63.
Для повышения коррозионной стойкости латуней и их прочности, используют принцип легирования. В этом случае легированные латуни называются специальными.
Маркируются специальные латуни буквой Л после которой ставятся буквы русского алфавита, обозначающие химические элементы. В цветных сплавах легирующие элементы обозначаются:
|
Цинк – Ц Алюминий – А Марганец – Мц Магний – Мг Олово – О Свинец – С Сурьма – Су |
Фосфор – Ф Никель – Н Хром – Х Железо – Ж Кремний – К Бериллий – Б |
После обозначения легирующих элементов указывается содержание меди в процентах, а затем – содержание легирующих элементов в порядке указания самих элементов. Например, латунь ЛАН 59-3-2 содержит 59 % меди, 3 % алюминия и 2 % никеля.
Все латуни по технологическому признаку подразделяют на две группы: деформированные, из которых изготовляют листы, ленты, трубы, проволоку и другие полуфабрикаты, и литейные – для фасонного литья.
Литейные латуни обладают хорошей жидкотекучестью, мало склонны к ликвации и обладают антифрикционными свойствами.
Литейные латуни маркируются иначе, чем деформируемые (согласно ГОСТ 17711 – 80). Например, латунь ЛЦ40С – содержит 40 % цинка, 1 % свинца, остальное медь.
Для улучшения обрабатываемости резанием латуни легируют свинцом, получая так называемые автоматные латуни (например, ЛС59-1, содержит 1 % свинца).
Для повышения сопротивления коррозии в морской воде в латуни добавляют олово и получают морскую латунь ЛО70-1 (содержит 1 % Sn).
Бронзами называют сплавы меди со всеми другими элементами, кроме цинка. Правда, цинк может вводится в бронзы только в небольших количествах (3 – 5 %). В зависимости от наиболее важного элемента в сплаве, их подразделяют на оловянные, свинцовые, алюминиевые, бериллиевые, кремнистые и т. д.
Оловянные бронзы являются сплавами на основе меди с оловом. Практическое применение в промышленности имеют сплавы с содержанием олова до 14 %.
Бронзы могут быть однофазными и двухфазными.
Неоднородная структура данного материала обладает хорошими антифрикционными свойствами, т. е. она хорошо работает в условиях внешнего трения скольжения.
Различают деформируемые и литейные оловянные бронзы. Деформируемые бронзы изготовляют в виде прутков, лент и проволоки в нагартованном (твердом) и отожженном (мягком) состояниях. Эти бронзы чаще предназначаются для пружин и пружинных деталей, применяемых в различных отраслях промышленности. Структура деформированных оловянных бронз – однофазная. Литейные бронзы, содержащие большое количество цинка, фосфора и нередко свинца, имеют двухфазную структуру.
Из бронз изготавливают вкладыши подшипников скольжения, венцы червячных колес, пружины, барометрические коробки, мембраны, антифрикционные детали и т. п.
Бронзы маркируются буквами Бр с последующим указанием элементов и их содержания. Для удешевления бронз в них вводится некоторое количество цинка, а для улучшения обрабатываемости резанием – свинец. Например, бронза марки БрОЦС6-6-3 имеет следующий химический состав: 6 % Sn, 6 % Zn, 3 % Pb (остальное медь). Механические свойства данного сплава: В = 180 220 МПа, = 8 12 %, твердость НВ 60.
Сплавы меди с алюминием носят название алюминиевых бронз. Алюминиевые бронзы являются хорошим заменителем дефицитной оловянной бронзы, уступая ей только в литейных свойствах. Практическое применение имеют сплавы меди с алюминием, содержащие до 10 – 11 % Al. Сплавы могут быть однофазными и двухфазными.
Сплавы, содержащие до 9,0 % А1, – однофазные.
Сплавы, содержащие до 4 – 5% А1, обладают высокой пластичностью и прочностью. Двухфазные сплавы имеют повышенную прочность, но пластичность их заметно ниже. При содержании свыше 10 – 12% А1 уменьшается уже и прочность сплавов. Двухфазные сплавы подвергаются термической обработке (закалке и отпуску).
Легирование железом измельчает зерно и повышает механические, и антифрикционные свойства алюминиевых бронз. Никель улучшает механические свойства и износостойкость как при низких, так и высоких температурах (500 – 600°С).
Алюминиевые бронзы хорошо сопротивляются коррозии и имеют высокие механические и технологические свойства; бронзы легко обрабатываются давлением в горячем состоянии, а при содержании до 7 – 8 % А1 – и в холодном. Вследствие хороших литейных свойств из них можно изготовлять разнообразные отливки. Однако в них наблюдается значительная усадка и газопоглощение.
Примеры маркировки алюминиевых бронз:
БрА5 – содержит 5 % Al, остальное медь;
БрАЖН10-4-4 – содержит 10 % Al, 4 % Fe, 4 % Ni, остальное медь.
Из алюминиевых бронз изготавливают ленты и полосы для пружин, шестерни, втулки, арматуру.
Алюминий и его сплавы
Алюминий – элемент III группы Периодической системы элементов Д. И. Менделеева, порядковый номер 13, атомная масса 26,98, температура плавления 660°С. Наиболее важной особенностью алюминия является низкая плотность – 2,7 г/см3, против 7,8 г/см3 для железа и 8,94 г/см3 для меди. Алюминий обладает высокой электропроводностью, составляющей 65% от электропроводности меди; высокой теплопроводностью. В зависимости от чистоты различают алюминий особой чистоты: А999 (99,999 % А1); высокой чистоты: А995 (99,995 % А1), А99 (99,99 % А1), А97 (99,99 % А1), А95 (99,95 % А1), и технической чистоты: А85, А8, А7, А6, А5, АО (99,0 % А1).
Технический алюминий изготовляется в виде листов, профилей, прутков, проволоки и других полуфабрикатов и маркируется АД0 и АД1.
Характерные свойства алюминия – высокая пластичность и малая прочность. Прокатанный и отожженный алюминий высокой чистоты имеет В = 58 Мпа; 0,2 = 20 Мпа; твердость 25 НВ, = 85 %; = 40 %.
Алюминий легко обрабатывается давлением, но обработка резанием затруднена, сваривается всеми видами сварки. Технический алюминий применяют для изготовления элементов, конструкций и деталей, не несущих нагрузки, когда требуется высокая пластичность, хорошая свариваемость, сопротивление коррозии и высокие тепло- и электропроводность. Так, например, из технического алюминия изготовляют различные трубопроводы, палубные надстройки морских и речных судов, кабели, электропровода, шины, конденсаторы, корпуса часов, фольгу, витражи, перегородки в комнатах, двери, рамы, посуду, цистерны для молока и т. д. Алюминий высокой чистоты предназначается для получения фольги, токопроводящих и кабельных изделий. Более широко используют сплавы алюминия.
Все сплавы алюминия можно разделить на три группы:
а) деформируемые, предназначенные для получения полуфабрикатов (листов, плит, прутков, профилей, труб и т. д.) путем прокатки, а также поковок и штамповок, получаемых, путем прессования, ковки и штамповки;
б) литейные, предназначенные для фасонного литья;
в) получаемые методом порошковой металлургии (САП – спеченные алюминиевые порошки, САС – спеченные алюминиевые сплавы).
На данной лекции познакомимся с литейными сплавами. (желательно добавить – дюралюмины).
Сплавы для фасонного литья должны обладать высокой жидкотекучестью, сравнительно небольшой усадкой, малой склонностью к образованию горячих трещин и пористости в сочетании с хорошими механическими свойствами, сопротивлением коррозии и др. Содержание легирующих элементов в литейных сплавах выше, чем в деформируемых.
Типичными литейными сплавами являются так называемые силумины. Это сплавы алюминия с кремнием. В технике используются силумины с содержанием кремния от 8 до 14 %.
Силумины маркируются буквами АЛ (алюминий литейный) с указанием номера по ГОСТ. Примеры сплавов: АЛ2, АЛ3, АЛ4, АЛ5, АЛ6, АЛ9.
Измельчение структуры и отсутствие первичных выделений хрупкого кремния улучшают механические свойства. Так, немодифицированный сплав с 13 % Si имеет в = 140 МПа, при = 3 %. После модифицирования свойства этого сплава следующие: в = 180 МПа, = 8 %.
Из силуминов изготавливают детали колес, детали моторов (блоки цилиндров двигателей, головки цилиндров, поршни, картеры), корпуса и детали приборов.
Подшипниковые сплавы
Подшипниковыми сплавами называются сплавы, из которых изготавливают вкладыши подшипников.
Антифрикционные подшипниковые сплавы на оловянной и свинцовой основах называются баббитами. К подшипниковым сплавам предъявляются следующие требования:
а) коэффициент трения между поверхностью вала и поверхностью подшипника должен быть небольшим;
б) обе трущиеся поверхности должны мало изнашиваться;
в) этот материал должен выдерживать достаточные удельные давления.
Первое и второе требования удовлетворяются тогда, когда поверхность вала и вкладыша разделена пленкой смазки. Если структура вкладыша неоднородна и состоит из твердых включений и мягкой основы, то после непродолжительной работы («приработки») на поверхности вкладыша образуется микрорельеф – выступают твердые включения и между валом и вкладышем образуется пространство, в котором удерживается смазка (так называемый «принцип Шарпи»). Подобной структурой обладают сплавы олова и сплавы свинца.
Наилучшим баббитом на оловянной основе является сплав Б83, состоящий из 83 % Sn, 11 % Sb и 6 % Cu.
При содержании сурьмы более 10,5 % образуюется неоднородная структура: мягкая основа сплава с отдельными твердыми включениями. Таким образом, при содержании в сплаве 11 % Sb образуется двухфазная структура, состоящая из мягкой пластичной основы твердого раствора и небольшого количества кристаллов, вкрапленных в эту массу. Такая структура является антифрикционной.
Сурьма и олово отличаются по плотности, поэтому сплавы этих металлов способны к значительной ликвации. Для предупреждения этого дефекта в баббиты вводят медь. Она образует с сурьмой химическое соединение Сu3Sn. Это соединение имеет более высокую температуру плавления и кристаллизуется первым, образуя разветвленные кристаллы (как бы скелет), которые препятствуют ликвации (всплыванию) основных кристаллов сплава. Кроме того, кристаллы Сu3Sn образуют в баббите твердые включения, дополнительно повышающие износостойкость вкладышей.
Температура начала и конца плавления баббита лежит в пределах 240 – 380 0С. Твердость НВ 28-34.
Недостатком такого баббита является большое содержание дефицитного олова.
Баббиты на свинцовой основе обладают значительно худшими качествами, чем на оловянной. Они являются сплавами с содержанием 16 –18 % Sb. Примером свинцовых баббитов является сплав БС (82 % Pb, 17 % Sb, 1 % Cu).
Двойные свинцовые сплавы еще сильнее ликвируют, чем оловянные, поэтому в сплав добавляют медь, которая образует с сурьмой соединение Cu2Sn. Это соединение препятствует всплыванию на поверхность основных кристаллов сплава.
Свинцовые баббиты являются менее качественными, чем оловянные, но дешевле последних. Они обладают большим коэффициентом трения. Температура начала и конца плавления баббита БС лежит в интервале 245 – 410 0С. Твердость НВ 22 – 26.
ЛЕКЦИЯ 12
КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ
ВВЕДЕНИЕ
Первым создателем композиционных материалов была сама природа. Множество природных конструкций (стволы деревьев, кости животных, скелеты насекомых, зубы людей) имеют характерную волокнистую структуру. Она состоит из сравнительно пластичного матричного вещества и более твердых и прочных веществ, имеющих форму волокон. Например, древесина - это композиционный материал, состоящий из пучков высокопрочных целлюлозных волокон трубчатого сечения, связанных между собой матрицей из органического вещества (лигнина), придающего древесине поперечную жесткость. Зубы людей и животных состоят из твердого поверхностного слоя (эмали) и более мягкой сердцевины (дентина). И эмаль, и дентин содержат неорганические кристаллы игольчатой формы, распространенные в мягкой органической матрице. Различие в свойствах эмали и дентина связано, в основном, с различным соотношением органической и неорганической составляющих: в эмали кристаллы занимают 99% объема, а в дентине 70%. Подобную структуру имеет и слоновая кость.
Примерами КМ могут быть и такие природные образования как минералы. Нефрит, например, состоит из плотно упакованных игольчатых кристаллов, связанных друг с другом на поверхностях раздела. Такая структура обеспечивает высокую вязкость нефрита и, поэтому различные племена использовали его как материал для изготовления топоров. Сооружая жилища, люди в глину для кирпичей добавляли солому и получали типичный армированный материал повышенной прочности. Они знали, что лук из нескольких слоев дерева прочнее лука, не имеющего в своей конструкции границ раздела. Таких примеров можно привести много, однако все это были случайные находки.
Наука о КМ зародилась совсем недавно. Первым примером научного подхода к созданию искусственных композиционных материалов можно считать появление железобетона и стеклопластиков. Как известно, бетон отлично сопротивляется сжатию и очень плохо выдерживает растягивающие нагрузки. Композиция из бетона и стальной арматуры, обладающая высокой прочностью на растяжение, объединяет в одном материале положительные свойства обоих компонентов, железобетон можно отнести к числу первых образцов армированной керамики.
Первый патент на композиционный полимерный материал был выдан в 1909 году. Он предусматривал упрочнение синтетических смол природными волокнами. Армировали первые полимерные КМ рубленым природным волокном, целлюлозной бумагой, хлопчатобумажными или льняными тканями. Стеклопластики запатентованы в 1935 году. Это были первые полимерные материалы, в которых как упрочнитель использовали неорганические волокна.
Промышленный выпуск стеклопластиков налажен после второй мировой войны, с тех пор их интенсивно используют в технике. В 50-х годах 20 века обнаружили, что многие материалы в виде тонких кристаллов игольчатой формы обладают фантастически высокой прочностью (10000 МПа и более). Были получены новые виды неорганических поликристаллических волокон - углеродные, борные с прочностью 3000 – 3500 МПа и модулем упругости 300 - 500 МПа. Возникла идея использовать все эти сверхпрочные волокнистые материалы для армирования различных матриц, и в первую очередь металлов.
История металлических армированных материалов насчитывает не более 40 лет, но успехи в этом направлении достигнуты значительные. Разработаны теоретические основы упрочнения металлов волокнами; созданы композиции на алюминиевой, титановой, никелевой и других основах, обладающие значительно большей прочностью, чем стандартные промышленные материалы на той же основе. Проводятся работы по созданию керамических композиционных материалов. Железобетон - пример “макроармированной” керамики: в нем используют толстую арматуру, диаметр которой измеряется миллиметрами и десятками миллиметров.
Сейчас разработаны “микроармированные” керамические материалы на основе различных оксидов, карбидов, боридов, нитридов и др., диаметр тугоплавких армирующих волокон в которых составляет доли миллиметра или даже микрометры. За счет такого армирования удалось получить высокотемпературные керамические материалы с высоким сопротивлением термическим и динамическим нагрузкам, т.е. ликвидировать наиболее уязвимые места керамики.
В настоящий момент наиболее широко используются стеклопластики. Их применяют не только в сложных и ответственных конструкциях, но и в изделиях широкого потребления. Такие материалы как боро- и углепластики, металлические композиции типа алюминий - бор и алюминий - графит, используются главным образом в условиях действия высоких нагрузок, когда первостепенную роль играет надежность конструкции, ее масса, а вопросы стоимости отступают на второй план - в сверхзвуковых самолетах, ракетах, космической аппаратуре, батискафах. Пока эти материалы дороже обычных промышленных, поскольку объем их производства невелик, а некоторые из них исследовались только в лабораториях. Наряду с несомненными преимуществами по сравнению с традиционными материалами у армированных КМ есть недостатки, в частности, многим из них присуща низкая прочность при сдвиговых нагрузках, некоторые КМ плохо сопротивляются сжатию.
КЛАССИФИКАЦИЯ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ И ПЕРСПЕКТИВЫ РАЗВИТИЯ
К композиционным материалам относят не встречающиеся в природе материалы, которые обладают следующей совокупностью признаков: состоят из двух или более компонентов, различающихся по своему химическому составу или структуре и разделенных выраженной границей; имеют новые свойства, отличающиеся от свойств составляющих их компонентов, при этом свойства определяются каждым из компонентов; неоднородны в микромасштабе и однородны в макромасштабе; состав, форма и распределение компонентов “запроектированы” заранее.
Исходя из вышесказанного ясно, что КМ являются синтетическими материалами, конструируемыми с целью реализации заданных свойств, применительно к функциональному назначению детали либо конструкции. Как правило, материал формируется в процессе изготовления детали.
По топологическому признаку “связности” один из компонентов, образующих сложный массив, называют “матрицей”. Другие же компоненты, упрочняющие или армирующие матрицу, могут быть либо в виде “несвязных”, изолированных друг от друга частиц, нитей, волокон, пластин, либо в виде связной конструкции, подобной “сетке“ арматуры в железобетонной конструкции.
Композиционные армированные материалы можно классифицировать по следующим признакам:
-
материалу компонентов;
-
типу арматуры и ее ориентации;
-
способу получения композиции и изделий из них;
-
по назначению.
1.В зависимости от материала матрицы (материаловедческий принцип) все КМ можно разбить на три группы:
-
композиции с металлической матрицей (металлические композиционные материалы МКМ);
-
композиции с полимерной матрицей (полимерные композиционные материалы ПКМ);
-
композиции с керамической матрицей (керамические композиционные материалы ККМ);
-
дисперсионно упрочненные сплавы.
Полимерные КМ обычно называют по материалу армирующих волокон. ПКМ, армированные стеклянными волокнами называют стеклопластиками (стекловолокнитами), металлическими - металлопластиками (металловолокнитами), органическими - органопластиками (органоволокнитами), борными - боропластиками (бороволокнитами), углеродными - углепластиками (углеволокнитами), асбестовыми - асбопластики (асбоволокнитами) и т.д.
В отношении металлических и керамических КМ пока нет четко установленных правил присвоения названий. Чаще других вначале пишут материал матрицы, затем материал волокна. Например, обозначение “медь - вольфрам” (Cu-W) относится к конструкционным материалам с медной матрицей и вольфрамовыми волокнами; “оксид алюминия -молибден” (Al2О3 - Мо ) - к КМ на основе Аl2O3 с арматурой из молибденовых проволок. В зависимости от исходного, структурного и фазового состояния матричного материала различают МКМ с порошковой, литой и листовой матрицей. КМ, набирающиеся из чередующихся слоев волокон и тонких листов матричного материала называют иногда КМ типа “сэндвич”. Для получения ККМ чаще всего используют матрицу в виде порошка.
2.По ориентации и типу арматуры (конструкционный принцип) все КМ можно разбить на две группы - изотропные и анизотропные.
Изотропными называют материалы, имеющие одинаковые свойства во всех направлениях.
Среди КМ, к числу изотропных относятся дисперсионноупрочненные и хаотичноармированные материалы. В первом случае упрочняющие элементы имеют примерно равноосную форму, во втором упрочнения осуществляется короткими (дискретными) частицами игольчатой формы, хаотично ориентированными в пространстве. В качестве таких частиц обычно используют отрезки волокон или нитевидные кристаллы (усы); при этом КМ получаются квазиизотропными, т.е. анизотропными в микрообъемах, но изотропными в объеме всего изделия. Анизотропными называют материалы, свойства которых зависят от направления. К таким КМ относят материалы, волокна которых ориентированы в определенных направлениях - однонаправленные, слоистые и трехмерно армированные. По форме армирующие волокна разделяют на три основные группы:
-
нульмерные, наполнители, имеющие в трех направлениях одинаково малые размеры одного порядка;
-
одномерные наполнители, имеющие малые размеры в двух направлениях и значительно превосходящий их размер в третьем измерении (волокна);
-
двумерные, наполнители, имеющие два размера, соизмеримые с размером композиционного материала, значительно превосходящий третий (пластины, ткань).
Анизотропия конструкционных материалов конструкционна: ее специально закладывают в конструкционные материалы для изготовления конструкций, где она наиболее желательна. В отличие от такой анизотропии существует технологическая анизотропия, возникающая при пластической деформации изотропных материалов (металлов), и физическая анизотропия, присущая кристаллам в связи с особенностями строения их кристаллической решетки.
В технике обычно используют анизотропные конструкционные материалы с определенной симметрией свойств. При изучении их физико-механических характеристик реальный, как правило, весьма неоднородный, материал представляют как некоторую идеализированную сплошную однородную среду с симметрией строения и свойств.
К анизотропным относятся материалы со следующими типами укладки волокон:
-
Продольно - поперечная укладка (рис. 4.1). При этом используют нуль- одномерные и двухмерные наполнители. Нульмерные и одномерные наполнители располагают в плоскостях, параллельных друг другу. Одномерные наполнители расположены также в параллельных плоскостях. При этом в пределах каждой плоскости они расположены параллельно, а по отношению к другим плоскостям под разными углами. Двухмерные наполнители расположены параллельно друг другу.
2) Однонаправленные композиционные материалы (рис. 4.2). При этом типе армирования используют нуль-, и одномерно армированные наполнители. Нульмерные располагаются так, что расстояние между ними по одной оси значительно меньше чем по двум другим. Одномерные наполнители располагаются параллельно друг другу.
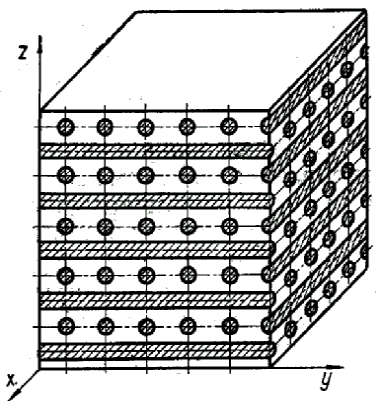
Рисунок 4.1 – Схематическое изображение структуры КМ с
продольно-поперечной укладкой волокон
Рисунок 4.2 – Схематическое изображение структуры одно-
направленного КМ (черные области волокна,
белые – матрица)
3) Слоистые композиционные материалы, армированные в двух неортогональных направлениях под углом 2 (рис. 4.3).
Рисунок 4.3 – Направления осей армирования в КМ с неортогональной укладкой волокон
4) Слоистые материалы со звездной укладкой волокон в смежных слоях (рис. 4.4).
Рисунок 4.4 – Схема ориентации арматуры в слоистых КМ со
звездной укладкой волокон в смежных слоях
Для расширения комплекса свойств или усиления какого-либо свойства возможно одновременное использование наполнителей различной формы. Например, для усиления прочности связи между одномерными наполнителями (стеклянными или углеродными волокнами) и полимерной матрицей в нее вводят нульмерный наполнитель (частицы асбеста, карбида кремния и др.). С этой же целью применяют армирование наполнителями одной формы, но разного состава. Так, для повышения модуля упругости композиционных материалов с полимерной матрицей, армированной стеклянным волокном, дополнительно вводят волокна бора.
Для армирования КМ материалов 3 и 4 способом используют нуль- и одномерные наполнители.
Армирующие наполнители могут располагаться в матрице отдельно, не находясь друг с другом в связанном состоянии, а могут образовывать различные сплетения (рис. 4.5).
Композиционные материалы, которые содержат два и более различных наполнителя, называют полиармированными.
3. По способу получения (технологический принцип) полимерные конструкционные материалы можно разделить на:
-
литейные;
-
прессованные;
-
намоточные.
ПКМ с хаотичной структурой обычно получают литьем и прессованием, а с ориентированной - намоткой и прессованием.
Металлические КМ по этому способу делят на:
-
литейные;
-
деформируемые.
Литейные получают, пропитывая арматуру расплавленным матричным сплавом, либо применяя направленную кристаллизацию
сплавов эвтектического состава с выделением упрочняющей армирующей фазы непосредственно из расплава (так называемый метод «in situ» - в себе, на месте пребывания). Для получения деформируемых МКМ применяют спекание, горячее прессование, диффузионную сварку, горячую штамповку и ковку на молотах, взрывное прессование, электролитическое, химическое напыление и др.
Большинство из этих твердофазных методов, исключая динамические, применяют и для получения керамических композиционных материалов.
4. По назначению (эксплуатационный принцип) КМ можно разбить на материалы:
-
общеконструкционного назначения (для различного рода несущих конструкций самолетов, ракет, судов, автомобилей, двигателей, сосудов высокого давления, предметов широкого потребления и др.);
-
жаропрочные (для лопаток турбин, камер сгорания и других изделий, работающих при повышенных температурах);
-
термостойкие (для изделий, работающих в условиях резких теплосмен, например для облицовки каналов МГД-генераторов);
-
фрикционные и антифрикционные (подшипники скольжения, шестерни и др.);
-
ударопрочные (броня самолетов, танков и т.п.);
-
теплозащитные и КМ со специальными свойствами (электрическими, магнитными, ядерными и др.).
В настоящее время наиболее широкое применение находят композиты на основе полимерных матриц. Они достаточно полно изучены и позволяют по достаточно простой технологии изготавливать крупногабаритные детали и конструкции сложной формы. Среди этой группы первое место по объему использования (95%) занимают стеклопластики. Они обладают высокими прочностными характеристиками, в несколько раз большей по сравнению с металлами стойкостью к усталостным напряжениям и трещинообразованию, а также к коррозионному воздействию при значительном снижении массы деталей, что позволяет резко сократить затраты на производство, обслуживание и ремонт изделий.
В сочетании с достаточно низкой стоимостью эти преимущества предопределили широкое использование стеклопластиков в судостроении, строительстве, транспортном машиностроении, электротехнике, приборостроении и других областях техники для изготовления различных емкостей и трубопроводов.
Углепластики и органопластики наряду со всеми положительными свойствами стеклопластиков имеют в полтора раза меньшую удельную массу, в 3 - 4 раза большую жесткость и более высокую прочность. Но, в связи со значительно более высокой стоимостью, они в настоящее время используются главным образом в аэрокосмической, оборонной промышленности, в автомобилестроении. С удешевлением углеродных волокон и, особенно с развитием производства дешевых пековых волокон применение этих композитов значительно расширяется. То же относится к материалам типа углерод-углерод, которые в настоящее время применяются только в аэрокосмической технике, где используется их механическая прочность при высоких температурах в сочетании с низкой массой, а также в медицине для протезирования костно-опорного аппарата в связи с их прочностью, жесткостью и хорошей биологической совместимостью. При дальнейшем снижении стоимости их можно будет применять в машиностроении, автомобилестроении, приборостроении и т.д.
Из КМ на основе металлических матриц в настоящее время находят применение алюминий, армированный борными или углеродными волокнами, эвтектические композиты на основе никелевых сплавов. Исследования в области металлических композиционных материалов по темпам и объему финансирования значительно опережают аналогичные работы по полимерным композитам. То же относится к КМ на основе керамики, несмотря на то, что в настоящее время их использование крайне ограничено, кроме стеклобетонов. В использовании КМ на основе металлов и особенно керамики перспективным является их применение при высоких температурах, что дает возможность значительно повысить рабочие температуры двигательных установок и тем самым резко повысить их экономичность.
МЕТАЛЛИЧЕСКИЕ КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ
МКМ представляют собой такие материалы, в которых матрицей выступают металлы и их сплавы, а арматурой - металлические и неметаллические волокна.
В МКМ конструкционного назначения армирующие элементы (нитевидные кристаллы, поликристаллические и аморфные неметаллические волокна, металлические проволоки) воспринимают нагрузку, а металлическая матрица передает нагрузку волокнам и распределяет ее между ними. Поэтому механические свойства МКМ зависят, прежде всего, от свойств волокон.
Выбор матричного материала определяется требованиями совместимости его с материалом арматуры, а также технологическими и эксплуатационными характеристиками. СОВМЕСТИМОСТЬЮ называют способность арматуры сохранять форму и структуру, а, следовательно, и высокую прочность, как в процессе изготовления МКМ, так и в условиях его эксплуатации. Наиболее остро проблема совместимости возникает в МКМ, где арматурой служат металлические волокна, т.к. они подвержены химическому взаимодействию с матрицей и взаимной диффузии. Эти явления могут привести к растворению и рекристаллизации волокон, возникновению хрупких фаз на границе раздела волокно - матрица и, как следствие, к разупрочнению арматуры и материала в целом.
К технологическим требованиям относят способность компонентов материала, и в первую очередь матрицы, подвергаться тому или иному виду пластической деформации, литья, порошковой металлургии и пр.
Эксплуатационные свойства МКМ характеризуются способностью противостоять воздействию внешней среды (температуры, давления, вибрации, коррозии и т.д.).
Поскольку матрица оформляет конфигурацию изделия из МКМ и в большей степени, чем волокна, граничит с внешней средой, при выборе матричного материала необходимо учитывать и его сопротивление рабочим температурам, коррозии, эррозионному износу и т.п.
В качестве матричных материалов при изготовлении МКМ используют промышленные металлы и сплавы, которые уже применяются в различных областях техники, а также новые сплавы, разработанные специально для армирования их тем или иным видом волокон. В зависимости от условий эксплуатации, и в первую очередь от рабочих температур, в МКМ используют следующие матричные материалы:
-
легкие металлы и их сплавы (на основе алюминия и магния);
-
титан и сплавы на его основе;
-
медь и ее сплавы;
-
жаростойкие и жаропрочные сплавы на основе железа, никеля и кобальта;
-
тугоплавкие металлы и сплавы.
Все перечисленные металлические матрицы по технологическому принципу можно разделить на три больших класса: деформируемые, литейные и порошковые.
К деформируемым алюминиевым сплавам относят не упрочняемые термической обработкой сплавы марок АМц, АМг, АМг3 и др., Основными легирующими элементами являются марганец и магний. Эти сплавы обладают, хорошей пластичностью, коррозионной стойкостью, свариваемостью, но сравнительно небольшой прочностью. Большую группу деформируемых алюминиевых сплавов составляют упрочняемые термической обработкой дюралюмины (Д1, Д16 и др.) и сплавы групп АВ, АК, В95. После термической обработки (закалки и искусственного старения) эти сплавы имеют повышенную механическую прочность.
Из литейных алюминиевых сплавов наиболее распространены силумины, которые обладают хорошими литейными свойствами и в качестве основного легирующего элемента содержат 4 - 13% Si. Однако они малопластичны, имеют низкую ударную вязкость и коррозионную стойкость. Теплостойкость силуминов также невелика.
Весьма перспективны для жаропрочных МКМ на алюминиевой основе матричные материалы типа САП (спеченный алюминиевый порошок), которые представляют собой алюминий, упрочненный дисперсными частицами AL2O3. Главное преимущество САП в их высокой жаропрочности. Кроме того, эти материалы хорошо обрабатываются давлением и резанием, обладают высокой коррозионной стойкостью.
Магний и его сплавы выгодно отличаются от других конструкционных материалов низкой плотностью, относительно высокими механическими свойствами, хорошей способностью сопротивляться ударным нагрузкам и вибрациям. Такие деформируемые магниевые сплавы как МА5, МА8-1, технологически пластичны и хорошо обрабатываются давлением. Сплав МА2-1 легко поддается прокатке и всем операциям листовой штамповки: гибке, отбортовке, вытяжке (при нагреве до 250 - 300С). Кроме того, он хорошо сваривается аргоно-дуговой сваркой.
При 20С этот сплав обладает прочностью 280 - 290 МПа, а его относительное удлинение составляет 16 -18 %.
Литейные магниевые сплавы, такие как МЛ5, МЛ12, МЛ15, обладают хорошей жидкотекучестью и малой линейной усадкой 1,3 - 1,6%. После термической обработки (старения) они значительно упрочняются. Их обрабатывают методами литья в песчаные формы, в кокиль и под давлением.
Из листовых МКМ наиболее распространены тонкие листы или фольга, получаемые прокаткой.
Титан и его сплавы обладают ценными физико-механическими свойствами. При малой плотности (4,5 г/см3) титановые сплавы могут иметь предел прочности от 500 (для нелегированного титана) до 1500МПа (для сплавов). Технический титан ВТ1 и большинство сплавов титана, например ВТ5, ВТ3, ВТЛ-1, имеют хорошие литейные свойства и применяются для производства фасонных и тонкостенных отливок. Мелкие фасонные отливки (до 15 кг) изготовляют литьем в оболочковые формы из графита.
Титан и его сплавы можно обрабатывать давлением, особенно в горячем состоянии в интервале температур 600 - 1200С, всеми известными способами.
Медь, имеющая высокую электро- и теплопроводность в сочетании с высокой коррозионной стойкостью, широко применяется в электротехническом аппаратостроении. В технологическом отношении медь очень удобный металл, так как она хорошо куется, прокатывается в пруток, ленту, фольгу, протягивается в проволоку. Многие медные сплавы обладают хорошими литейными свойствами и их часто используют для получения фасонных отливок методом точного литья.
Из металлических матриц на основе железа, никеля и кобальта при создании МКМ чаще всего применяют окалиностойкие и жаропрочные стали и сплавы. Окалиностойкими (жаростойкими ) обычно называют стали и сплавы, обладающие стойкостью против разрушения поверхности в газовых средах при нагревании выше 500С и работающие в ненагруженном или слабонагруженном состоянии (нихромы, сильхромы и т.д.). Армирование таких сплавов тугоплавкими волокнами позволяет резко повысить их жаропрочность и использовать их при температурах на 150 - 200С выше, чем рабочие температуры неармированных матриц.
Жаропрочные сплавы также обладают значительной окалиностойкостью, но главное их качество - это способность работать в нагруженном состоянии при высоких температурах. Повышенная длительная прочность, высокое сопротивление ползучести и усталости в никелевых сплавах достигается за счет введения Ti и AL, образующих дисперсные упрочняющие фазы, а также при легировании тугоплавкими элементами (W, Mo, Nb), упрочняющими твердый никелевый раствор, и малыми добавками бора, церия и других элементов. Примеры таких сплавов - деформируемые сплавы ЭИ437А, ЭИ437Б, ЭИ617 и др.
Методами порошковой металлургии стало возможно получить МКМ с матрицей из особо тугоплавких металлов - ниобия, вольфрама, молибдена и сплавов на их основе. Чаще всего такие матрицы подвергают дисперсионному упрочнению частицами тугоплавких соединений примерно равноосной формы с размерами в пределах 0,01 - 0,1 мкм. Волокнистыми наполнителями (усами, волокнами тугоплавких соединений) эти матрицы армируют для того, чтобы придать им особые эксплуатационные характеристики - ударопрочность, термостойкость, специальные физические свойства. Создавая такие МКМ, используют матричный материал в виде тонких порошков с размерами 0,1 - 5 мкм, тонкой металлической фольги толщиной 10 – 100 мкм, а также применяют различные методы осаждения матрицы на волокна с последующим уплотнением покрытых волокон горячим прессованием, прокаткой и т.д.
ПРИМЕНЕНИЕ МЕТАЛЛИЧЕСКИХ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ
Перспективность использования металлических композиционных материалов в различных отраслях техники определяется их широким спектром самых различных свойств. Высокие прочность и удельная жесткость, малая чувствительность к концентраторам напряжений и высокое сопротивление усталостному разрушению и т.д. определяют области применения МКМ.
Весьма перспективным является применение металлических композиционных материалов в ракето- и авиастроении, в частности при создании тяжелых транспортных и сверхзвуковых пассажирских самолетов.
Применение таких материалов в количестве до 30% позволяет снизить массу самолета на 15 - 20%. Наиболее рационально в этом случае применение титановых и алюминиевых сплавов, армированных волокнами бора и борсика или титановых сплавов армированных волокнами из боралюминия, соединяемых пайкой.
Боралюминиевые композиционные материалы могут применяться на космических летательных аппаратах, в узлах конструкций, подвергающихся нагреву от реактивной струи двигателя, в герметических кабинах экипажа.
Композиционные материалы на основе алюминия и титана, армированные бериллиевой проволокой применяются при создании газотурбинных двигателей для изготовления лопаток вентилятора и компрессора.
Применяются металлические композиционные материалы также в машиностроении, судостроении, автомобилестроении. Целесообразность их применения связана со значительным уменьшением массы конструкций при сохранении или даже повышении прочностных характеристик (например, для облегчения кузовов, коробок передач, поршней цилиндров, передаточных механизмов, рессор и т.д.).
Композиционные материалы со свинцовой матрицей, армированные углеродными волокнами, применяют в химической промышленности при производстве батарей и аккумуляторов, в строительстве, в изделиях, работающих на трение, и др.
В сельскохозяйственном машиностроении из МКМ изготовливают режущие части плугов, дисковых косилок, детали тракторов и т.д., что позволяет увеличить срок службы сельскохозяйственной техники.
Применение МКМ в мостостроении позволяет увеличить длину пролетов в связи с более высокой жесткостью указанной композиции, что приводит к уменьшению металлоемкости мостовых конструкций и улучшению их транспортабельности.
Применяют МКМ и в ядерной технике. Так, алюминиевый сплав, армированный стекловолокном, содержащим окись урана, обладает повышенной прочностью при температурах 550С и может быть использован в качестве топливных пластин реакторов.
Для изготовления подшипников, работающих без смазки, успешно опробовали антифрикционный композиционный материал на основе свинца, армированный 20% проволоки из нержавеющей стали или оловянистой бронзы. В космических условиях, где применение обычной смазки в узлах трения невозможно, можно также применять МКМ с нитевидными кристаллами Al2O3.
Как износостойкий материал в коробках передач, дисковых муфтах, направляющих пусковых устройствах и других тяжелонагруженных механизмах можно использовать МКМ, армированные усами и волокнами.
В сварочной технике смогут применяться армированные присадочные материалы. Например, алюминий или его сплав с 4% Cu, армированный небольшими долями волокон Al2O3 или SiC, успешно использовали для сварки плавлением алюминия и его сплавов. Армирующая фаза при сварке переходит в сварочный шов, способствуя его упрочнению.
Достаточно эффективно МКМ используются и в других областях техники и народного хозяйства. Однако эффективным применение МКМ оказывается только при выполнении следующих условий:
-
специальное конструирование деталей и узлов конструкций с учетом особенностей свойств этих материалов;
-
создание специальной технологии изготовления деталей, поскольку способы изготовления деталей из традиционных сплавов неприемлемы для композиционных материалов;
-
осуществление контроля технологического процесса и качества исходных материалов и изделий на основных этапах их изготовления для обеспечения надежности материалов при длительной эксплуатации.
Необходимо иметь в виду, что МКМ, так же как и традиционные сплавы не являются универсальными. Использование их по назначению в той или иной конструкции рационально только в том случае, когда это является технически обоснованным и экономически целесообразным.
ПОЛИМЕРНЫЕ КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ
Полимерными композиционными материалами (ПКМ), или пластиками, называют системы, состоящие из полимерной матрицы (связующего) и упрочняющего наполнителя в виде волокон или порошкообразных веществ.
В настоящее время создана целая индустрия ПКМ. Из них изготавливают баллоны для сжатых газов, корпусы ракетных двигателей, цистерны для нефтепродуктов, лопасти винтов вертолетов, трубы для химических веществ, авиационные шасси, волноводы, понтоны, корпусы лодок, ракетки для тенниса, ружейные стволы, удочки, печатные электросхемы, рессоры автомобилей и многие другие изделия.
Одним из факторов, сдерживающих широкое применение ПКМ, в частности стеклопластиков, была их сравнительно низкая жесткость. За последние годы в связи с разработкой новых сортов стеклянных волокон с повышенным модулем упругости, а также таких высокомодульных волокон, как углеродные, борные, карбидокремниевые, удалось резко повысить жесткость пластиков. Угле - и боропластики имеют модуль Юнга, близкий к стали, а по удельной жесткости в несколько раз превосходят промышленные металлы. Это дало возможность применять ПКМ в ответственных, сильно нагруженных конструкциях, которые раньше изготавливались исключительно из металлов.
Во многих случаях, когда от изделий требуется высокая несущая способность при минимальном весе, высокопрочные и высокомодульные пластики оказываются эффективнее металлов. Кроме высоких механических характеристик и низкого удельного веса к числу ценных качеств ПКМ следует отнести их стойкость к воздействию кислот, щелочей, органических растворителей, масел и морской воды. Армированные пластики технологичны, обладают высокой демпфирующей способностью и вибростойкостью, радиопрозрачностью, тепло- и электроизоляционными свойствами, нечувствительностью к магнитному полю. Технологические процессы их производства можно полностью автоматизировать и механизировать, изделия из них имеют красивый внешний вид и не требуют специальной защитной окраски.
Основные преимуществами новых ПКМ по сравнению с МКМ: простота изготовления, технологичность, дешевизна, низкая плотность. Основной их недостаток - ограниченный температурный интервал эксплуатации, сравнительно низкие значения межслойной сдвиговой прочности и отрыва. Современные полимерные связующие могут обеспечить работоспособность изделий из них до температур, не превышающих 300 - 400С.
В качестве связующих в ПКМ применяют синтетические высокомолекулярные вещества различного химического состава - полимеры, которые были рассмотрены подробно ранее в разделе органические полимерные материалы.
Следует напомнить, что молекулы полимеров представляют собой соединения, состоящие из большого числа элементарных звеньев - мономеров. Строение молекул полимеров и химическая природа мономеров определяют свойства полимерных материалов.
Как было отмечено ранее, по поведению при нагреве и охлаждении полимерные материалы принято разделять на термопластичные и термореактивные.
В качестве связующих для конструкционных ПКМ, работающих под нагрузками, в подавляющем большинстве случаев используют термореактивные смолы.
Выбор связующего определяет особенности технологии изготовления ПКМ и его эксплуатационные свойства. Наиболее широко в производстве конструкционных ПКМ применяют эпоксидные, полиэфирные, фенольные, кремнийорганические и полиамидные смолы.
КЕРАМИЧЕСКИЕ КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ (ККМ)
Керамические композиционные материалы (ККМ) представляют собой материалы, в которых матрица состоит из керамики, а арматура - из металлических или неметаллических, волокнистых наполнителей. Армированные волокнами материалы на основе порошковых комбинированных матриц, в которые входят тугоплавкие неметаллические частицы и металл - связка, условно будем относить также к ККМ.
Керамические материалы характеризуются высокими точками плавления, высокой прочностью на сжатие, сохраняющейся при достаточно высоких температурах, и высокой стойкостью к окислению. Эти свойства керамики в течении многих веков использовались при изготовлении футеровки печей, огнеупорных изделий и т.д. В настоящее время требования к керамике, как к конструкционному изделию значительно возросли. Наряду с перечисленными свойствами от нее требуется высокая прочность на растяжение и ударная вязкость, стойкость к вибрациям и термоудару. Такими свойствами обладают, например, некоторые металлы. Сопоставление свойств керамики и металлов привело к попыткам создать КМ, в которых керамическая матрица сочетается с металлическими включениями в виде порошка. Так появились керметы.
Дальнейшими исследованиями было установлено, что еще больший эффект дает введение в керамическую матрицу волокон металла. Так, чтобы достичь одинаковой с керметом термостойкости, в керамику нужно ввести примерно в 3 раза меньше металла в форме волокон, чем виде порошка. Аналогичные исследования были, затем проведены в области введения в керамическую матрицу керамических волокон.
В ККМ нагрузка переносится с малопрочной матрицы на более прочную арматуру. Однако эффект увеличения предела прочности при растяжении наблюдается у ККМ не всегда. В некоторых случаях композиция получается менее прочной, чем неармированная матрица. Объяснить это можно сочетанием в ККМ малой пластичности с высоким модулем упругости при растяжении. Из-за этого удлинение матрицы при напряжении ее разрушения оказывается недостаточным для того, чтобы передать значительную часть нагрузки армирующим элементам.
Увеличение ударной вязкости армированной керамики объясняется лучшим распределением механических усилий, а также ограничением распространения трещин в матрице за счет армирующих волокон. Аналогично объясняется и повышение стойкости армированной керамики к термоудару.
Для изготовления ККМ применяют три основных метода: горячее прессование, прессование с последующим спеканием и шликерное литье.
Выбирая металлические волокна для армирования, нужно учитывать их способность к рекристаллизации в области высоких температур. Большое значение имеет и геометрия волокон, т.к. на прочность сцепления волокон с матрицей кроме диффузионных и химических процессов влияет и чисто механическое сцепление. Улучшить последнее можно, создавая шероховатость на поверхности волокон ворсовкой их или травлением.
Химическое взаимодействие между волокном и матрицей протекает преимущественно по поверхностям контакта компонентов.
Важен и вопрос ориентации волокон. Они могут располагаться в матрице, как направлено, так и хаотично. Знать ориентацию волокон в материале необходимо для выбора схемы его работы.
Примером ККМ, в котором модуль упругости матрицы ниже модуля упругости армирующих волокон, может быть армированная вольфрамовой проволокой керамика, состоящая из 50% каолина, 30% кремнезема и 20% полевого шпата. Этот матричный состав применяют обычно для электрических изоляторов. У таких композиций волокно в состоянии воспринять на себя значительную часть общей нагрузки даже при малых относительных удлинениях, которые допускает керамика до своего разрушения. При содержании арматуры свыше 40% сопротивление растяжению композиции ухудшается. Это связано с тем, что при больших объемных содержаниях проволок не удается получить беспористый материал.
Керамические композиции с керамическими волокнами имеют некоторые преимущества перед ККМ с металлической арматурой. Это малое различие в значениях модуля Юнга и коэффициентах термического расширения; химическое сродство, жаростойкость оксидов в процессе изготовления и работы КМ и т.д.
Характерными керамическими композициями, для которых армирование волокнами открывает новые области использования, являются, например ККМ на основе оксида хрома. Для изготовления огнеупорных изделий чистый оксид хрома практически не применяют, т.к. он плохо спекается. Его пористость при обычных методах производства керамики составляет 40% и выше, а механические свойства низкие. Существенно повысить прочность и термостойкость оксида хрома удалось использованием в качестве армирующей добавки усов муллита.
Наиболее обширной группой керамических композиционных материалов являются ККМ на основе бескислородной керамики (нитридов и карбидов кремния). Например, армирование нитрида кремния кристаллами муллита 3Al2O3/2SiO2. Основное преимущество этого материала заключается в высокой стойкости к температурам, превышающей стойкость обычного нитрида в 6 - 7 раз, тогда как механическая прочность материала после 200 теплосмен снижается лишь на 10 - 20%.
Высокие прочностные характеристики КМ на основе нитрида кремния позволяют их использовать в качестве быстрорежущего материала. Например используют КМ, состоящий из смеси порошков Si3N4 и Y2O3 как матричную фазу и карбидов титана, частиц вольфрама, тантала, гафния и кремния в качестве упрочняющей фазы, средний размер которых составляет 2 мкм, а количество варьируется от 10 до 50%. Указанные материалы обладают высокой устойчивостью к окислению, термостойки, устойчивы к химическому и абразивному износу и могут быть использованы не только взамен быстрорежущего вольфрамсодержащего инструмента, но и как конструкционный материал, обладающий высокой износоустойчивостью.
В последние годы предпринимаются попытки получить армированные волокнами КМ на основе порошковых композиций из тугоплавких частиц, например, карбидов, и металла-связки (керметы). Это такие материалы, как твердые сплавы типа ВК и ТК, армированные тонкими проволоками из вольфрама. Введение вольфрамовой проволоки в твердые сплавы ВК3, ВК6, ВК20, Т5К10, Т15К6 увеличивает сопротивление ударным нагрузкам и вибрациям, повышает их износостойкость и способность работать в условиях резких теплосмен. Однако еще предстоит решить проблему взаимодействия вольфрамовых проволок с металлом-связкой в процессе получения композиций горячим прессованием. Структурно стабильные композиции на основе керметов можно создать легированием металла-связки или нанесением барьерного покрытия на арматуру. Более перспективными армирующими наполнителями для керметов могут стать волокна тугоплавких соединений.
Керметы близки по своему типу к так называемым ДУКМ (дисперсионноупрочненным композиционным материалам). Объемная доля керамической фазы может составлять 45 - 60 %. Примером керметов являются карбидостали или ферротитаны, в которых стальная матрица упрочнена частицами карбида титана TiC со средним размером 2 - 5 мкм. Это очень износостойкие материалы, используемые в деталях, подверженных износу трением. По режущим свойствам они превышают быстрорежущие стали и только немного уступают твердым сплавам, будучи значительно дешевле последних. Так карбидосталь с мартенситной матрицей (0,65%С; 3% Cr; 3% Mo; 1,5% Cu) и 33% TiC при плотности 6,5 г/см3 имеет предел прочности при испытаниях на сжатие 3800 МПа, предел прочности при испытаниях на изгиб 1500 МПа, твердость 69 HRC. В обычных инструментальных сталях доля карбидной фазы не может превышать 25%, т.к. иначе сталь становится недеформируемой. Это ограничивает твердость и износостойкость этих сталей. Карбидостали лишены этого недостатка. Кроме того, при использовании окалиностойких матриц (12Х18Н10Т) карбидостали имеют очень высокую жаростойкость и стойкость в агрессивных средах.
В отдельную группу ККМ можно выделить сверхпроводящую оксидную керамику (СП) на основе систем Y - Ba - Cu - O (YBa2Cu3O7-х или 123, где цифры - число атомов металлов в соединении), Bi - Sr - Ca - Cu - O (2212) и Bi - Pb - Sr - Ca - Cu - O (2223). Эти СП работают при температурах выше 90 - 105К, т.е. могут охлаждаться жидким азотом. Такие СП выпускают в виде проводов (проволоки, ленты) в серебряной оболочке длиной до 600 м, а также в виде штабиков. цилиндров и т.д.
Интересными и перспективными направлениями использования СП - керамики являются: магнитные подшипники, допускающие скорость вращения до 100 тыс.об/мин; гистерезисные электродвигатели с удельной мощностью в 5 - 7 раз выше, чем у обычных двигателей; транспорт на магнитной подушке.
ДИСПЕРСИОННОУПРОЧНЕННЫЕ СПЛАВЫ (ДС)
В отличии от волокнистых композиционных материалов в дисперсионно-упрочненных композиционных материалах матрица является основным элементом, несущим нагрузку, а дисперсные частицы тормозят движение в них дислокаций. Высокая прочность достигается при размере частиц 10 - 500 нм при среднем расстоянии между ними 100 - 500 нм и равномерном распределении их в матрице. Прочность и жаропрочность в зависимости от объемного содержания упрочняющих фаз не подчиняется закону аддитивности. Оптимальное содержание второй фазы для различных металлов неодинаково, но обычно не превышает 5 -10%.
Использование в качестве упрочняющих фаз стабильных тугоплавких соединений (оксиды тория, гафния, иттрия, сложные соединения оксидов и редкоземельных металлов), нерастворяющиеся в матричном металле, позволяет сохранить высокую прочность материала до 0,9 - 0,95Тпл. В связи с этим такие материалы применяют чаще как жаропрочные материалы. Дисперсионно-упрочняемые композиционные материалы могут быть получены на основе большинства применяемых в технике металлов и сплавов.
Т.о., дисперсионноупрочненными сплавами называют КМ, в которые на одной из технологических операций искусственно вводят высокодисперсные равномерно распределенные на заданном расстоянии частицы, не взаимодействующие активно с матрицей и не растворяющиеся в ней заметно, вплоть до температур плавления фаз.
Технология получения ДС заключается в выборе упрочняющей фазы и метода ее введения, определении объемного содержания, а также разработке рациональных режимов деформации и термической обработки. Выбирая упрочняющую фазу, следует исходить из ее термодинамических свойств, диффузионной подвижности в матрице и других параметров, учитывающий условия эксплуатации данной композиции. Объемное содержание упрочняющей фазы определяется технологическими возможностями равномерно распределить входящие в состав сплава компоненты.
В ДС обычно существует два типа структур - агрегатная и дисперсная. В агрегатной структуре частицы упрочняющей фазы окружены несколькими зернами матрицы, имеющими различную кристаллографическую ориентацию, в дисперсной же структуре частицы упрочняющей фазы полностью окружены одинаково ориентированной матрицей. Преобладание той или иной структуры определяется способом получения порошковых смесей.
При формовании, спекании и термической обработке в полученной композиции по возможности должны сохраняться дисперсность и характер распределения упрочняющей фазы. В некоторых случаях за счет измельчения частиц при прессовании удается существенно улучшить структурные параметры по сравнению с параметрами исходных порошкообразных смесей.
Процесс получения ДС должен быть таким, чтобы обеспечить создание стабильной дислокационной структуры, способствующей многократному повышению прочности и сохранению пластичности.
Дисперсионно-упрочненные сплавы называют также дисперсионно-упрочненными композиционными материалами (ДУКМ). ДУКМ имеют металлическую матрицу, а вторая фаза представлена в виде мелких (< 1 мкм) частиц нитридов, оксидов или карбидов. Очень важны - физическая, химическая совместимость материалов в матрице и армирующей фазе. Есть различные примеры таких материалов со специальными свойствами (например, система “медь-графит” для скользящих электроконтактов), но важнейшим видом этих композитов являются - САП, ДС на основе никеля и вольфрама, интерметаллидов.
САП (спеченный алюминиевый порошок) представляет собой композицию, упрочненную ее оксидами (Al2O3). Этот дисперсно-упрочненный материал уже более 20 лет производят в промышленном масштабе.
Несмотря на многообразие вариантов технологии производства изделий и полуфабрикатов из САП, все они имеют общие особенности и включают следующие операции: получение порошковых смесей, холодное прессование, предварительное спекание, горячее прессование и выдавливание спеченной алюминиевой заготовки в форме изделия, которые можно подвергать дополнительной термической обработке.
Свойства изделий зависят от степени деформации материала. Все марки отечественных и зарубежных сплавов типа САП удовлетворительно деформируются в горячем состоянии, а сплавы с 6 - 9% AL2O3 хорошо деформируются и на холоде. Так, из сплава САП-1 экструзией и холодным волочением можно получить трубы с толщиной стенки 0,4 мм, а прокаткой на специальных станках трубы переменного сечения (с уменьшением сечения 75%) или с поперечными винтовыми ребрами. Прокаткой листов удается получить фольгу толщиной до 0,03 мм.
С увеличением содержания упрочняющей фазы характеристики прочности постоянно растут. Отечественные и зарубежные марки сплавов типа САП содержат 4 - 14% AL2O3. При увеличении количества упрочняющей фазы повышаются твердость прочность и жаропрочность сплава САП, а пластичность уменьшается. Наиболее распространены сплавы со средним содержанием оксидной фазы 7% (САП-1, SAP - 930), 10 -11%(САП-2, SAP-895) и 13-14% (САП-3, SAP-865).
ДС на основе никеля. В качестве матрицы используют никель и его сплавы с хромом ( 20%) со структурой твердых растворов. Сплавы с такой матрицей обладают высокой жаростойкостью. Упрочнение осуществляется тугоплавкими оксидами AL, Mg, Be, Zr, Co, Ti, Cr и Th, а также дисперсными частицами бескислородных тугоплавких соединений.
Временное сопротивление в зависимости от содержания упрочняющей фазы изменяется по кривой с максимумом. Наибольшее упрочнение достигается при содержании 3,5 - 4% упрочняющей фазы на основе гафния. Легирование никелевой матрицы W, Ti, Al, обладающими переменной растворимостью в никеле, дополнительно упрочняет материалы в результате дисперсионного твердения матрицы, происходящего в процессе охлаждения от температур спекания.
Методы получения этих материалов достаточно сложны. Они заключаются в смешивании порошков металлического хрома и легирующих элементов с заранее приготовленным (методом химического осаждения) порошком никеля, содержащим дисперсный оксид гафния или другого элемента. После холодного прессования смеси порошков проводят горячую экструзию брикетов.
В промышленных масштабах освоены два типа ДС: ТД-никель и ТД-нихром, которые изготавливают в виде труб, прутков, проволоки, листов, фольги и применяют в авиационном двигателестроении.
ДС на основе вольфрама. Для упрочнения вольфрама можно использовать тугоплавкие оксиды, карбиды и нитриды. Чтобы затормозить рост зерен при сварке и повысить эмиссионные свойства, в вольфрам вводят присадки ThO2. В странах СНГ выпускаются сплавы типа ВТ-7, ВТ-10, ВТ-15, ВТ-30, ВТ-50, которые содержат до 5% ThO2. Позднее в качестве упрочнителей вольфрамовой проволоки стали вводить добавки оксидов лантана и иттрия (ВЛ и ВИ).
Данные сплавы широко применяют в электротехнической, электровакуумной и металлургической промышленности.
К группе дисперсионноупрочненных композиционных материалов следует отнести также спеченные твердые сплавы, применяемые как материал для изготовления инструменты высокой твердости. К ним относятся материалы, состоящие из высокотвердых и тугоплавких карбидов вольфрама, титана, тантала, соединенных металлической связкой.
Твердые сплавы изготавливают методами порошковой металлургии. Порошки карбидов смешивают с порошком кобальта, выполняющего роль связки, прессуют и спекают при 1400 - 1550ºС. При спекании кобальт растворяет часть карбидов и плавится. В результате получается плотный материал (пористость не более 2%), структура которого на 80 – 95% состоит из карбидных частиц, соединенных связкой.
Твердые сплавы производят в виде пластин, которыми оснащают резцы. сверла фрезы и другие режущие инструменты. Такие инструменты сочетают высокую твердость (74 – 76 HRC) и износостойкость с высокой теплостойкостью (800 - 1000ºС). По своим эксплуатационным свойствам они превосходят инструмент из быстрорежущих сталей и применяются для резания с высокими скоростями.
В зависимости от состава карбидной основы, спеченные твердые сплавы выпускают трех групп.
Первую (вольфрамовую) группу составляют сплавы системы WC – Co. Они маркируются буквами ВК и цифрой, показывающей содержание кобальта в процентах. Карбидная фаза состоит из зерен WC. Сплавы этой группы применяют для режущих инструментов при обработке материалов, дающих прерывистую стружку (чугуна, цветных металлов, фарфора, керамики и т.п.). Сплавы с высоким содержанием кобальта (ВК20 и ВК25) применяют для изготовления штамповых инструментов. Их применяют также как конструкционный материал для деталей машин и приборов, от которых требуется высокой сопротивление пластической деформации или изнашиванию.
Вторую группу (титановольфрамовую) образуют сплавы системы TiC – WC – Co. Они маркируются буквами Т, К и цифрами, показывающими содержание в процентах карбидов титана и кобальта. Сплавы этой группы характеризуются более высокой, чем у сплавов первой группы теплостойкостью (900 - 1000ºС), которая повышается по мере увеличения количества карбида титана. Их наиболее часто применяют для высокоскоростного резания сталей.
Третью группу (титанотанталвольфрамовую) образуют сплавы системы TiС – TaC – WC – Co. Цифра в марке после букв ТТ обозначает суммарное содержание (в процентах) карбидов TiС + TaC, а после буквы К количество кобальта в процентах. От сплавов предыдущей группы они отличаются большей прочностью и лучшей сопротивляемостью вибрациям и выкрашиванию. Они применяются при более тяжелых условий резания (черновая обработка стальных слитков, отливок, поковок).
Химический, состав, свойства некоторых спеченных сплавов приведены в таблице 4.5.
Таблица 4.5 – Химический состав и свойства некоторых
спеченных сплавов
|
Группа |
Сплав |
Состав шихты, % |
HRA, не менее |
|||
|
WC |
TiC |
TaC |
Co |
|||
|
Вольфрамовая |
ВК3 |
97 |
_ |
_ |
3 |
89,5 |
|
ВК4 |
96 |
_ |
_ |
4 |
89,5 |
|
|
ВК6 |
94 |
_ |
_ |
6 |
88,5 |
|
|
ВК8 |
92 |
_ |
_ |
8 |
87,5 |
|
|
ВК10 |
90 |
_ |
_ |
10 |
87 |
|
|
ВК15 |
85 |
_ |
_ |
15 |
86 |
|
|
ВК20 |
80 |
_ |
_ |
20 |
84 |
|
|
ВК25 |
75 |
_ |
_ |
25 |
82 |
|
|
Титано- вольфрамовая |
Т30К4 |
66 |
30 |
_ |
4 |
92 |
|
Т15К6 |
79 |
15 |
_ |
6 |
90 |
|
|
Т5К10 |
85 |
5 |
_ |
10 |
88,5 |
|
|
Титанотантало-вольфрамовая |
ТТ7К12 |
81 |
4 |
3 |
12 |
87 |
|
ТТ8К6 |
84 |
6 |
2 |
6 |
90,5 |
|
Разработаны твердые сплавы, не содержащие дефицитного вольфрама. Безвольфрамовые твердые сплавы выпускают на основе TiC + Ni + Mo (сплав ТН-20) и на основе карбонитрида титана Ti(NC) + Ni + Mo (КНТ-16). Никель и молибден образуют связывающую матрицу. Сплавы применяются при чистовом и получистовом точении и фрезеровании сталей и цветных металлов.