Файл: Задача 2 Рутин ( Rutinum) 3 рутозид кверцетина 3рамногликозил3,5,7, 3 1,4 1 пентаоксифлавон.doc
Добавлен: 08.11.2023
Просмотров: 102
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
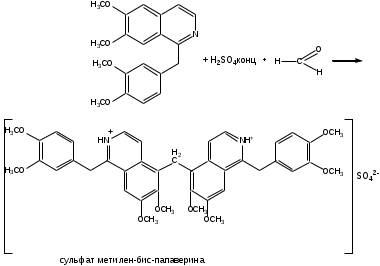
-
Окисление серной кислотой концентрированной. К препарату добавляют серную кислоту концентрированную, нагревают. Образуются продукты окисления, окрашенные в фиолетовый цвет.
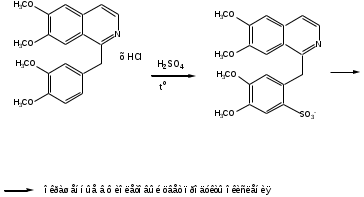
-
Выделение основания папаверина. Препарат растворяют в горячей воде, прибавляют раствор ацетата натрия, оставляют до получения кристаллов папаверина, которые отфильтровывают, промывают водой, сушат. Температура плавления выпавшего основания должна быть 145-147оС.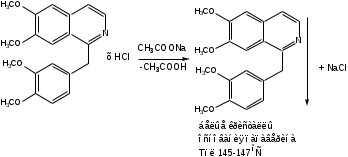
Фильтрат дает характерную реакцию на хлориды:
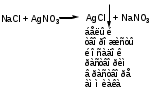
Чистота:
-
Кислотность (рН 2% раствора 3,0 – 4,5. Потенциметрически) -
Органические примеси. -
Сульфатная зола.
Количественное определение:
Метод неводного титрования.
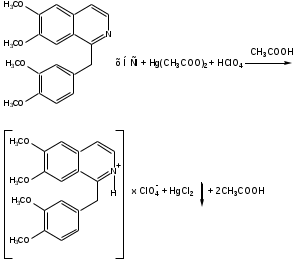
Метод основан на свойстве папаверина гидрохлорида усиливать основные свойства в среде протогенного растворителя. Ацетат окисной ртути необходим для связывания хлорид-ионов.
Около 0,3 препарата (точная навеска) растворяют в 10 мл безводной уксусной кислоты при слабом нагревании на водяной бане. После охлаждения добавляют 5 мл раствора ацетата окисной ртути и титруют 0,1Н раствором хлорной кислоты до зеленого окрашивания.
Т – 0,1 М кислота хлорная
Индикатор - кристаллический фиолетовый.
f = 1
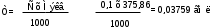
Хранение: список Б, в хорошо укупоренной таре, предохраняющей от действия света.
Применение: спазмолитик.
Дротаверина гидрохлорид (Drotaverine hydrochloride)
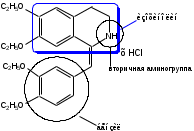
1-(3,4-диэтоксибензилиден)-6,7-диэтокси-1,2,3,4-тетрагидроизохинолина гидрохлорид
Дротаверина гидрохлорид является производным бензилизохинолина.
Описание: светло-желтый или зеленовато-желтый кристаллический порошок без запаха или почти без запаха.
Растворимость: растворим в этаноле, легко растворим в хлороформе, мало растворим в ацетоне.
Подлинность:
-
ИК-спектр в области 4000-400 см-1, который должен соответствовать спектру сравнения. -
УФ-спектр в 0,1М растворе соляной кислоты, снятый в области 220-420 нм, имеет максимумы поглощения при 241, 302, 353 нм и минимумы при 223, 262, 322 нм. -
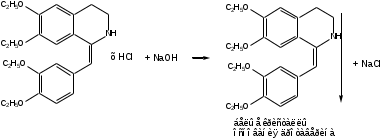
Выделение основания дротаверина. ЛП проявляет более сильные основные свойства, чем папаверина гидрохлорид, поэтому для выделения основания из раствора препарата следует добавить раствор щелочи.
-
Реакция окисления концентрированной серной кислотой. Реакция основана на восстановительных свойствах дротаверина.
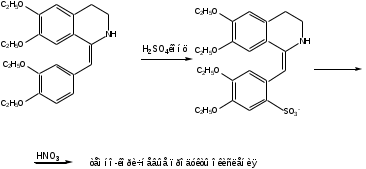
Чистота:
Отсутствие примесей определяют методом ВЭЖХ и ТСХ.
Количественное определение:
Метод неводного тирования. Метод основан на слабых основных свойствах дротаверина гидрохлорида, которые усиливаются в среде протогенного растворителя.
Препарат растворяют в кислоте уксусной ледяной, добавляют ацетат ртути (для связывания хлорид-ионов) и титруют 0,1 М раствором кислоты хлорной.
Т – 0,1 М кислота хлорная
Индикатор – кристаллический фиолетовый
До зеленого окрашивания.
f = 1
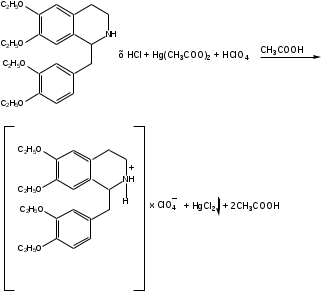
Хранение: список Б, в хорошо укупоренной таре, предохраняющей от действия света.
Применение: спазмолитик.
Вопрос: рН раствора папаверина гидрохлорида 3,0
Ответ: при действии света и кислорода воздуха образуются продукты окисления – солянокислые растворы папаверинола и папаверальдина. рН среды изменилась за счет наличия продуктов окисления.
Викасол (Vicasolum)
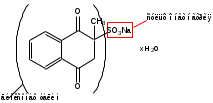
2,3-Дигидро-2-метил-1,4-нафтохинон-2-сульфонат натрия
Викасол является производным 2-метил-1,4-диоксонафталина.
Описание: белый или белый с желтоватым оттенком кристаллический порошок без запаха.
Растворимость: легко растворим в воде, трудно растворим в спирте, очень мало растворим в эфире.
Подлинность:
-
ИК-спектр должен совпадать со спектром стандарта -
УФ-спектр 0,0005% водного раствора в области 220-280 нм имеет максимумы поглощения при 230 и 265 нм, минимум – при 248 нм. -
Реакция удаления из молекулы сульфоната натрия в щелочной среде. Сущность реакции заключается в образовании сульфита натрия и 2-метил-1,4-диоксонафталина:
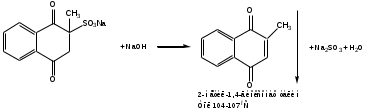
Осадок извлекают хлороформом, очищают от примесей и устанавливают температуру плавления.
-
Окисление серной кислотой концентрированной.
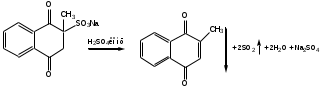
Ощущается запах сернистого газа.
-
На натрий: окрашивает бесцветное пламя горелки в желтый цвет.
Чистота:
-
Прозрачность и цветность раствора. -
Бисульфит натрия.
1,0 препарата растворяют в 30 мл воды. Полученный раствор добавляют к смеси, состоящей из 20 мл 0,1 Н раствора серной кислоты и 30 мл 0,1 Н раствора йода. Избыток йода оттитровывают 0,1 Н раствором тиосульфата натрия. Индикатор-крахмал.
1 мл 0,1 Н раствора йода соответствует 0,005203 г натрия тиосульфата, которого в препарате должно быть не более 2%.
-
2-метил-1,4-нафтогидрохинон-3-сульфонат.
0,1 препарата растворяют в 5 мл воды. От прибавления 2 капель раствора о-фенантролина не должна появляться муть.
-
Тяжелые металлы.
Количественное определение:
Цериметрический метод.
Около 0,3 препарата (точная навеска) растворяют в 20 мл воды, переносят в делительную воронку, прибавляют 5 мл 1 Н раствора едкого натра и извлекают хлороформом (3 раза по 20 мл). Объединенные хлороформные извлечения промывают 10 мл воды, фильтруют через бумажный фильтр, смоченный хлороформом, и промывают фильтр 5 мл хлороформа. Хлороформ удаляют досуха в вакууме при комнатной температуре. Остаток растворяют в 15 мл ледяной уксусной кислоты, добавляют 15 мл разведенной соляной кислоты, 3 г цинковой пыли и оставляют на 30 минут в темном месте, изредка перемешивая. Затем содержимое колбы быстро фильтруют через вату в другую колбу. Осадок в колбе и фильтр немедленно промывают водой (3 раза по 10 мл). к полученному фильтрату прибавляют 2-3 капли о-фенантролина и титруют 0,1 Н раствором сульфата церия до появления зеленого окрашивания.
Метод основан на восстановлении цинковой пылью извлеченного хлороформом из навески 2-метил-1,4-диоксонафталина (в присутствии хлороводородной кислоты):
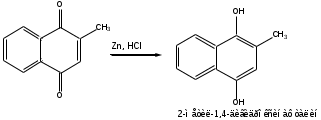
Полученный 2-метил-1,4-дигидроскинафталин затем титуют 0,1 М р-ром сульфата церия (IV) в присутствии индикатора о-фенантролина до зеленого окрашивания. Сульфат церия окисляет 2-метил-1,4-дигидроскинафталин в кислой среде до 2-метил-1,4-диоксонафталина:
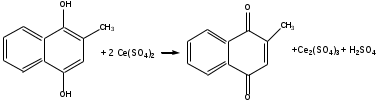
В эквивалентной точке о-фенантролин, растворенный в 1,48% растворе сульфата железа (II) меняет окраску:
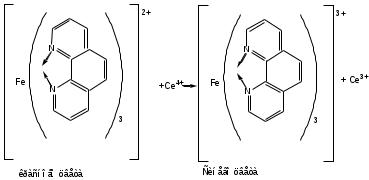
Титруют до зеленого окрашивания, которое появляется вследствие сочетания синего цвета комплекса с желтым раствором титранта.
f =1/2
Т = 0,1 М сульфат церия (IV)
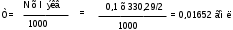
Хранение: список Б, в хорошо укупоренной таре, предохраняющей от действия света.
Применение: препарат группы витамина К.
Задача № 22
Кислота аскорбиновая (Acidum ascorbinicum)
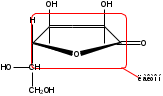
Гамма-лактон-2,3-дегидро-L-гулоновой кислоты
Аскорбиновая кислота относится к производных ненасыщенных полиокси-гамма-лактонов.
Описание: белый кристаллический порошок без запаха, кислого вкуса.
Растворимость: легко растворим в воде, растворим в спирте, практически нерастворим в эфире, бензоле, хлороформе.
Подлинность:
-
ИК-спектр должен совпадать со спектром стандарата. -
УФ-спектр. Аскорбиновая кислота имеет максимум поглощения при 265 нм (буферный раствор рН 7). -
Тпл 190-193оС. -
Удельное вращение от +22о до +24о (2% водный раствор). Данный метод обусловлен за счет оптически активного центра. -
Реакция окисления нитратом серебра. Основана на восстановительных свойствах аскорбиновой кислоты. К водному раствору препарата прибавляют раствор нитрата серебра, наблюдается выпадение темного осадка.
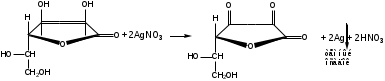
-
Реакция окисления. Восстановительными свойствами кислоты аскорбиновой обусловлено превращение окрашенного в синий цвет раствора 2,6-дихлорфенолиндофенола в бесцветное лейкооснование. К водному раствору препарата по каплям добавляют 2,6-дихлорфенолиндофенол. Синяя окраска последнего постепенно исчезает.
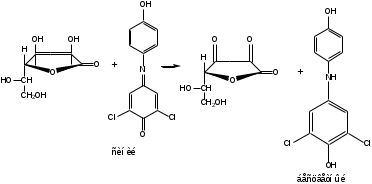
Чистота:
-
Сульфатная зола и тяжелые металлы. -
Органические примеси.
Количественное определение:
-
Йодатометрия. Метод основан на восстановительных свойствах кислоты аскорбиновой.
Около 0,5 препарата ( точная навеска) растворяют в воде в мерной колбе емкостью 50 мл, доводят объем раствора водой до метки и перемешивают. К 10 мл приготовленного раствора водой до метки и перемешивают. К 10 мл приготовленного раствора прибавляют 0,5 мл 1% раствора йодата калия, 2 мл раствора крахмала и 1 мл 2% раствора соляной кислоты и титруют 0,1 н раствором йодата калия до появления стойкого слабо синего окрашивания.
1 мл 0,1 н раствора йодата калия соответствует 0,008806 г аскорбиновой кислоты, которой в препарате должно быть не менее 99,0%.
Т – 0,1М раствор калия йодата
f =1/2 2С
+1
 2С+2
2С+2Индикатор – крахмал
В среде кислоты соляной.
Препарат растворяют в воде, добавляют калия йодид, кислоту соляную и крахмал. Титруют раствором калия йодата до появления слабо синей окраски.
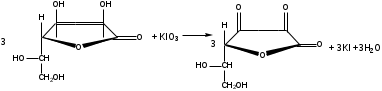
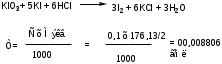
При данном виде титрования рационально добавление формальдегида, который будет реагировать с калия иодатом, т.к. в инъекционом растворе кислоты аскорбиновой следует учитывать наличие антиоксидантов – стабилизаторов, которые могут вступить в реакцию с калия йодатом. Формальдегид предотвращает взаимодействие антиоксидантов-стабилизаторов с калия йодатом.
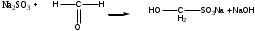
-
Йодометрия. Кислота аскорбиновая окисляется титрованным раствором йода в нейтральной, слабокислой и слабощелочной средах до кислоты дегидроаскорбиновой.
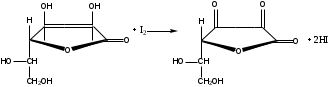
Кислота аскорбиновая используется в виде порошков, таблеток и растворов для инъекций. Поскольку в растворах она легко окисляется, иъекционные растворы готовят на воде, насыщенной CO2 , с добавлением стабилизаторов-антиоксидантов (Na2SO3, Na2S2O5). В раствор для инъекций добавляют натрия гидрокарбонат, так как препарат имеет кислую реакцию среды, раздражающую ткани.
-
Алкалиметрия. Вариант вытеснения. Реакция основана на наличии в молекуле аскорбиновой кислоты двух енольных гидроксилов. В разбавленных растворах щелочей она ведет себя как одноосновная кислота. Разрыва лактонного цикла в этих условиях не происходит, а образуется нейтральная растворимая монозамещенная соль:
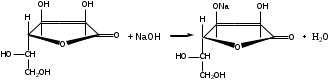
Т – 0,1 раствор натрия гидроксида
Индикатор – ф/ф
f = 1
Хранение: в хорошо укупоренной таре, предохраняющей от действия света.
Применение: при цинге, кровотечениях различной этиологии, инфекционных заболеваниях и интоксикациях, заболеваниях печени, почек.
Кислота никотиновая (Acidum nicotinicum)
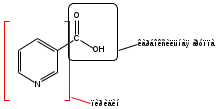
Пиридинкарбоновая – 3 кислота