ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 23.10.2023
Просмотров: 252
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Gazni quritish - gazlar tarkibidagi suv bugʻlarini ajratib olish. Fizik-kimyoviy hamda fizik usullar yordamida bajariladi. Fizik-kimyoviy usul absorbsiya va adsorbsiya usullarini oʻz ichiga oladi.Absorbsiya usullari gazlardagi suv bugʻlarini suyuq moddalarga yuttirishga asoslangan. Bu usulda kuritiladigan gaz avval sovitiladi, keyin absorbsion apparatning pastki qismiga kiritiladi. Apparatning yuqori qismidan gaz yunalishiga qarama-qarshi absorbent eritmasi (maye, dietilenglikol) beriladi. Absorbent sifatida kalsiy xlorid (35—40%), glitserin (85%), dietilenglikol (85—97%), uchetilenglikol, sulfat kislota (94—96%) va b. moddalarning eritmalari ishlatiladi. Gaz tarkibidagi namlik absorbentga oʻtadi. Bunday usulda quritilgan gaz tarkibida kupi bilan 0,2 g/m3 nam qoladi. Adsorbsiya usullari qoʻllanilganda gazlardan nam qattiq moddalar — adsorbentlarga yutiladi. Adsorbent sifatida qattiq holdagi CaCI2, NaOH, KON, MgO, P2O5, boksitlar, silikagel, alyumogel va b. ishlatiladi. Bu moddalar oʻz ogʻirligiga nisbatan 2% dan 10% gacha namni yuta oladi. Adsorbentlar gazlarni absorbentlarga nisbatan yaxshiroq quritadi. Fizik usullar nam gazni issiqdik almashish apparatlarida suv yoki boshqa issiqlik yutuvchi suyuqpiklar bilan sovitish, gazni siqishdan soʻng sovitish va siqilgan gazni birdaniga kengaytirishga asoslanadi. Gazlarni oʻta quritish uchun odatda, ikki pogʻonali sxema tatbiq etiladi. Bunda nam gaz dastlab absorbsion va soʻngra adsorbsion qurilmalarda quritiladi. G.qdan maqsad koʻp komponentli gazlarni fraksiyalarga ajratish, yonuvchi gazlarni quvurlar orqali joʻnatish va b. Sanoat uchun G.q.ning ahamiyati katta.
Adsorbsiya
Adsorbsiya – qattiq yoki suyuq moddalar (adsorbentlar) sirtiga suyuq yoki gaz holidagi modda (adsorbat)larning konsentrlanishi (yutilishi). A. adsorbent sirtidagi molekulalararo kuch ta’sirida sodir bo‘ladi. Adsor-bat molekulalari adsorbent sirtiga yaqinlashib, unga tortiladi va adsorbatning bir (mono-), ikki (bi-) va hokazo ko‘p (poli-) molekulali adsorbsion qavati hosil bo‘ladi. Adsorbatning adsorbsion qavatdagi konsentratsiyasi ma’lum dara-jaga yetganidan keyin desorbsiya boshla-nadi. Yutilgan modda adsorbsion qavatda o‘z xususiyatini saqlab qolsa, fizik A., o‘zgarsa, ya’ni adsorbent bilan kimyoviy bi-riksa, kimyoviy A. deyiladi. Fizik A. temperatura, bosim, konsentratsiyaga, adsorbent va adsorbatning tabiatiga, shuningdek, adsorbent tuzilishiga ham bog‘liq. A. hodisasi tabiatda keng tarqalgan. Yerga solingan o‘g‘it, avvalo tuproqqa A. lanadi. O‘simlik tuproqdagi ozuqani ildizi orqali A. jarayoni asosida o‘zlashtiradi. A. gaz va suyuq aralash-malarni ajratish-da (qarang Xromatografiya), biologik jarayon-da, havoni iflos gazlardan tozalashda, eritmalarni har xil qo‘shilmalardan holi qilishda, ulardan erigan moddalarni ajratib olishda A. dan keng foydalaniladi.
Adsorbentlar (lot. ad – yonida va sorbens – yutuvchi) – tabiatda uchraydigan va sun’iy yo‘l bilan tayyorlanadigan, disperelik darajasi yuqori bo‘lgan (qarang Dispers sistemalar) juda katta tashqi (g‘ovaksiz) yoki ichki (g‘ovakdor) sirtli jismlar. Suyuq yoki gaz holidagi moddalar adsorbsiyasi xuddi shu A. sirtida sodir bo‘ladi. Tabiiy A.ga opoka (govaqtosh), gilmoya va boshqa kiradi. Sun’iy A. uglevodo-rodlarni termik parchalash yoki tutatish (kurum olish), o‘ta qizdirilgan suv bug‘i bilan kremniy-organik moddalarni gi-drolizlash (aerosillar), dag‘al dispers sistemalarni kimyoviy jihatdan faol-lash yoki modifikatsiyalash (faol kumir, faollantirilgan gil) va boshqa yo‘llar bilan olinadi. A.ning adsorbsion xususiyati qattiq jismning tabiatiga, sirt tuzi-200lishiga, kattaligiga, g‘ovaklarining tu-zilishiga bog‘liq. Ular, asosan, g‘ovaksiz, yirik g‘ovakli, mayda govakli va aralash g‘ovakli turlarga bo‘linadi. A. protivo-gazlarda ishlatiladi, gaz va suyukli-klarni tozalash va quritishda, polimerlarning to‘ldirgichlari sifatida va boshqa maqsadlarda keng qo‘llaniladi.
Adsorberlarning tuzilishi.
Adsorberlar ish rejimiga ko׳ra davriy va uzluksiz ishlovchi bo׳ladi.
Adsorbent qatlamining tuzilishiga ko׳ra davriy adsorberlar qo׳zgalmas va mavhum qaynash qatlamli
bo׳ladi.
Desorbsiya
Yuqori faollikka ega bo׳lgan adsorbentlar qimmatbaho materiallar qatoriga kiradi, shu sababli ulardan bir necha marotaba foydalanish lozim. Buning uchun adsorbsiya jarayonidan so׳ng adsorbent
regenerasiya qilinadi, ya’ni unda yutilgan modda ajralib chiqariladi. Adsorbsiyaga teskari boradigan jarayon desorbsiya deb ataladi.
Adsorbent quyidagi usullar yordamida regenerasiya qilinishi mumkin:
1) adsorbentning haroratini oshirish yoki uning ustidagi bosimni kamaytirish;
2) adsorbent qatlami orqali isitilgan gaz yoki qizdirilgan bug`ni haydash;
3) adsorbentda yutilgan komponentlarni yutish xossasi yuqori bo׳lgan boshqa modda yordamida siqib chiqarish.
Absorbsiya (lot. absorbtio – yutilish, absorbeo – yutayapman so‘zidan) – eritma yoki gaz aralashmasidagi modda (absorbat)larning qattiq jism yoki suyuqlik (absorbent)larga hajmiy yutilishi. Gazlarning suyuqliklarga Absorbsiyalanishidan neftni qayta ishlash, koks-benzol va boshqa sanoat sohalarida foydalaniladi. Gazlarning bug‘ va suyuqliklarda erish darajasining turliligiga asoslangan holda absorbsiyadan texnikada gazlarni tozalash va ajratishda hamda ularni bug‘ gaz aralashmalaridan ajratishda foydalaniladi. Absorbsiyaga qarama-qarshi jarayon desorbsiya deyiladi, u eritma yutgan gazni ajratib olish va absorbentni regeneratsiya qilishda qo‘llaniladi.[1]
Absorber
Absorber – absorbsiya jarayoni amalga oshiriladigan uskunaning asosiy apparati. Unda gazlardagi moddalar (shu jumladan zararli moddalar) suyuqlikka yutiladi. Kimyo sanoatida, kosmik kemalarning hayotni ta’minlash tizimlari va boshqalarda qo‘llaniladi.[1]
Sorbentlar (lot. sorbens — yutuvchi) — gaz, bugʻ va erigan moddalarni yutish uchun qoʻllanadigan qattiq yoki suyuq moddalar. Yutuvchi modda sorbent, yutiladigan modda esa sorbtiv yoki sorbat deyiladi. Adsorbsiya, absorbsiya va kapillyar kondensatsiya kabi oddiy jarayonlar yigʻindisidan iborat murakkab fizikkimyoviy jarayon sorbsiyadir. Agar sorbtivning yutilishi uning sorbent bilan taʼsirlanishi natijasida boʻlsa, bunday jarayon xemosorbsiya deb ataladi. Xemosorbsiya koʻpincha sorbent satxida sodir boʻladi. Faollangan kumir, silikagel, alyuminiy oksid, seolitlar koʻplab ishlatiladigan S.dir. Sintetik ionlovchi smolalar (qarang Ionitlar) ham muxim S. hisoblanadi. Suyuq S. kimyo sanoatida qoʻllanadi.
Sorbsiya (lot. sorbeo — yutaman) — gaz, bugʻ va erigan moddalarning kattik, jism yoki suyuqlikda yutilishi. Yutuvchi jismlar sorbentlar, yutiluvchi modda sorbat (yoki sorbtiv) deyiladi. S.ning quyidagi turlari bor: adsorbsiya, absorbsiya, xemosorbsiya va kapillyar kondensatsiya — yutuvchi moddaning gʻovak va kapillyarlarida suyuq faza hosil boʻlishi. S. — koʻpgina tabiiy jarayonlarning asosiy tarkibiy qismi; u kimyoda keng qoʻllanadi. Muhim sorbentlarga faollangan kumir, silikogel, seolitlar, smektit, navbaxtit va boshqa kiradi.
termodinamikaning birinchi qonunining ba’zi jarayonlarga tadbiqini ko`raylik.
2.
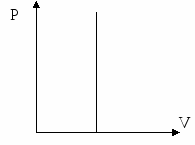 Izoxorik jarayon. Ideal gazning hajmi o`zgarmay (V=const) uning bosimi va temperatura o`zgaradi.Agar gazning hajmi o`zgarmasa tashqi kuchlarga qarshi ish bajarilmaydi, ya’ni A=0.Unda termodinamikaning birinchi qonuni
Izoxorik jarayon. Ideal gazning hajmi o`zgarmay (V=const) uning bosimi va temperatura o`zgaradi.Agar gazning hajmi o`zgarmasa tashqi kuchlarga qarshi ish bajarilmaydi, ya’ni A=0.Unda termodinamikaning birinchi qonuniQ=
ko`rinishni oladi. Demak ideal gazga berilayotgan issiqlik miqdori uning ichki energiyasini o`zgartirishga boshqacha aytganda temperaturaning ko`tarilishiga sarflanadi.
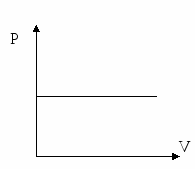
Izobarik jarayon. Ideal gazning bosimi o`zgarmas(P=const), uning hajmi va temperatura o`zgaradi.Bunda gazga berilgan issiqlik miqdorining bir qismi uning ichki energiyasini orttirishga, bir qismi esa tashqi kuchlarga qarshi ish bajarishga sarflanadi.
Q =
Izobarik jarayonda gaz bajargan ish
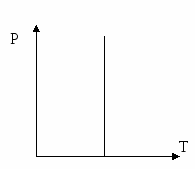
Izotermik jarayon.Ideal gazning temperatura o`zgarmas (T=const), uning hajmi va bosimi o`zgaradi. Agar gazning temperaturasi o`zgarmasa, demak uning ichki energiyasi ham o`zgarmaydi
Adiabatik jarayon. Atrof muhit bilan issiqlik miqdori almashmasdan ro`y beradigan jarayonga adiabatik jarayon deyiladi.
Adiabatik jarayonga tez ro`y beradigan jarayonlar misol bo`ladi. Misol uchun gaz tez siqilganda bajaralgan ish uning temperaturasining, ya’ni ichki energiyasining ortishiga olib keladi. Temperatura ortishi natijasida atrofga issiqlik miqdori tarqalishi uchun esa ma’lum vaqt kerak. SHuning uchun ham Q=0. Ichki yonish dvigatelida yoqilg`i aralashmasining yonishi adiabatik jarayonga yaxshi misol bo`ladi.
Entropiyaham holat parametrlaridan b o ‘lib, С harfi bilan belgilanadi va o ‘zgarish m a’nosini bildiradi. Tizimga issiqlik berilganda uning holati o ‘zgaradi. Elementar qismda berilgan issiqlik dq va harorati T ga teng. 24 www.ziyouz.com kutubxonasi ^ = ds т (39) Entropiya — tizim holatning shunday funksiyasiki, bu funksiyaning qaytuvchan jarayondagi cheksiz kichik o‘zgarishi mazkur tizimga kiritilgan cheksiz kichik issiqlik miqdorining shu issiqlik kiritilgan holatdagi harorat nisbatiga teng.
Entalpiya (yun. — isitaman) — termodinamikada — termodinamik tizimning holat funksiyalaridan biri (N). Qaytar izobarik jarayonda E.ning oʻzgarishi tizimga berilgan (yoki tizimdan olingan) issiqlik miqdoriga teng . Shuning uchun E. bosim oʻzgarmaydigan sharoitda sodir boʻluvchi fazalar almashuvlarida, kimyoviy reaksiyalar va boshqalarda isiqlik effektini ifodalaydi. Bosim oʻzgarmaydigan adiabatik jarayonlarda E.ning qiymati ham oʻzgarmaydi. Baʼzan E. issiqlik funksiyasi deb ataladi.
Valentlik (lot. valentia — kuch) — maʼlum element atomining boshqa element atomi bilan kimyoviy bogʻ hosil qilib birlashish yoki almashish xususiyati.
Nemis fizigi V. Kossel nazariyasiga (1916) muvofiq, elementlar yoki elementlar guruhi oʻzaro birikkanda bittasi elektron beradi, ikkinchisi esa bu elektronni qabul qilib oladi. Berilgan elektron soniga qarab musbat V., qabul qilib olingan elektron soniga qarab manfiy V. deb aytiladi. Shunga koʻra, natriy musbat bir, xlor esa manfiy bir valentlikka ega.
uglerod valentligi 4ga teng
Azotning valentligi 3
Yoqilg'i brendiga qarab, A-76 + 20 0S hajmidagi 1 litr benzin zichligi 0,730 kilogramm.
Eng og'ir benzin A-98 og'irligi 0,780 kilogramm.
AI-92 rusumli benzinning bir litri 0,735 kilogramm
A-76 litrdan bir litr benzin 730 gramm.
A-92 litrdan bir litr benzin 760 gramm.
A-95 litrdan bir litr benzin 750 gramm.
Bu og'irlik (ortiqcha yoki bir necha gramm kam) + 20S haroratida benzinga ega bo'ladi.
1 litr benzin og'irligi 720 dan 775 grammgacha.
Neft : Neft yerning cho’kindi qatlamida joylashgan moyli, o’ziga xos hidli, och qo’ng’irdan qora rangacha, yonuvchi suyuqlik, muhim foydali qazilma. Qaynash temperaturasi 250 – 300 oC dagi neft fraksiyasi tarkibidagi u yoki bu sinf uglevodorodining ko’proq miqdorda bo’lishiga bog’liq holda neftning qudagi asosiy turlari farqlanadi:
-
Metanli neft –ko’proq tarmoqlanmagan alkanlardan tarkib topgan. -
Naftenli neft – asosan siklik aromatik bo’lmagan uglevodorodlar – sikloalkanlar yoki naftanlardan tarkib topgan. -
Aralash neft – alkanlar, naftenlar va aromatik uglevodorodlar aralashmasini o’z ichiga oladi.
Neft alkanlar ba’zi siklanlar va arenlar, shuningdek kislorodli sulfitli va azotli birikmalarning murakkab aralashmasidir.
Klassifikasiyasi – ba’zan neftni fizik xossalari bo’yicha klassifikasiyalanadi, masalan yengil neft zichligi 0,92 g/ml gacha va ancha og’ir neft. Bu jihatdan yengil neft zichligi 0,65 - 0,87 g/cm3, o’rtacha neft zichligi 0,910 – 1,05 g/sm3 ga bo’linadi.
Neft tarkibidagi oltingugurt miqdoriga qarab kam sulfatli (tarkibida 0,5% gacha S), sulfatli (0,5 – 2%) va yuqori sulfatli (2% dan yuqori) deb farqlanadi. Neft juda qadimdan (miloddan avvalgi 6000 yillikdan boshlab) ishlatilib kelinadi.
Neftdan olinadigan mahsulotlar :
Neftdan xalq xo’jaligi uchun juda katta ahamiyatga ega bo’lgan turli mahsulotlar ajratib olinadi : neftning asosiy fraksiyalari :
-
Gazolin, benzinlar fraksiyasi :
Bu fraksiya tarkibida uglevodorod atomlarining soni C5 – C11 gacha bo’ladigan uglevodorodlardan iborat bo’lib, ulardan quydagi mahsulotlar olinadi :
-
Yengil benzin – gazolin yoki petroley efiri. Qaynash temperaturasi 40 – 70 o C, zichligi 0,64 -0,66 g/sm3. Petroley efiri asosan erituvchi sifatida ishlatiladi. -
O’rtacha benzin – (aqiqiy benzin) qaynash temperaturasi 70 – 120o C, zichligi 0,7 g/cm3,. Benzin fraksiyasi texnikaning qaysi sohasida ishlatilishiga ko’ra aviasion, avtomobil benzini va boshqalarda ishlatiladigan benzinlarga bo’linadi. Texnikada o’rta benzin fraksiyasi asosan ichki yonuv divigatellarida yonilg’i sifatida ishlatiladi. -
Og’ir benzin – yoki ligroin fraksiyasi. Qaynash temperaturasi 120 – 140 oC, zichligi 0,73 – 0,77 g/ sm3. Bu fraksiyada C8H18 dan C17H30 gacha bo’lgan uglevodorodlar bo’ladi. Ligroin fraksiyasi dizel dvigatallari uchun yoqilg’i sifatida ishlatiladi.
-
Kerosin fraksiyasi – bu fraksiyada C10H22 dan C18H38 (ayrim manbalarda C9 – C14) gacha bo’lgan uglevodorodlar bo’ladi. Qaynash temperaturasi 180 – 300 oC gacha bo’ladi. Kerosin tozalangandan keyin traktorlar, reaktiv samalyotlar va raketalar uchun yoqilg’i sifatida ishlatiladi. Kerosin fraksiyasidan uy – ro’zg’orda ham yoqilg’i sifatida ham foydalaniladi.
Gazoyl fraksiyasi – qaynash temperaturasi 240 – 360oC, tarkibida C11H24 dan C20H42 gacha bo’lgan uglevodorodlar bo’ladi. Undan dizel yoqilg’isi, bug’ qozonlarida yoqilg’i va kreking uchun xomashyo sifatida ishlatiladi.
-
Qoramoy (mazut) fraksiyasi – bu fraksiyadagi uglevodorodlar ko’p sonli uglerod (C16 dan yuqori) atomlaridan iborat uglevodorodlar bo’ladi.
Mazut – qayta ishlanganda solyar moylari, dizel yoqilg’isi, surkov moylari, avtotraktorlar, aviasion, industrial va boshqalar uchun, vazelin (kosmetik vosita va dorilarga) va x. lar olinadi.
Mazut qayta ishlanganda uning tarkibidagi uglevodorodlar parchalanib ketmasligi uchun u suv bug’i vositasida yoki vakumda haydaladi.
Katalitik kreking – katalitik kreking ancha past temperaturada katalizatordan foydalangan holda amalga oshiriladi. Katalitik kreking asosan yuqori oktan sonli benzinlar olishda ishlatiladi. Maxsus tanlangan katalizatorlar uglevodorodlarni izomerlanishini va sikllanishini taminlaydi, buning natijasida benzinning oktan soni ortadi. Bunday katalizatorlar sifatida mAl2O3∙nSiO2 tarkibli alyumosilikatlar amalda seolitlardan foydalaniladi.
Oktan soni — karbyuratorli yoki injektor ichki yonuv dvigateli yonilğilarining detonatsiyaga turğunligini ifodalaydigan koʻrsatkich. Yonilğining Oktan soni etalon yonilği aralashmasiga taqqoslab aniqlanadi. Etalon yonilgi sifatida izooktan (2, 2, 4-uch metilpentan) va geptan aralashmasi qabul qilingan. Izooktanning detonatsiyaga turgʻunligi 100, normal geptanniki nol deb olingan. Etalon yonilgʻi aralashmasidagi izooktanning foizlardagi miqdori sinaladigan yonilgʻining Oktan sonini belgilaydi. Yonilgining Oktan soni qancha katta boʻlsa, detonatsiyaga moyilligi shuncha kichik boʻladi. Avtomobillarda Oktan soni 66—98 ga teng benzin, siqish darajasi yuqori boʻlgan dvigatellarda Oktan soni yuqori ben-zinlar ishlatiladi.