ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.11.2023
Просмотров: 105
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Сравнение результатов 2-х методов по F-критерию
По кривым титрования находим объём титранта.
| Номер опыта | Объем пробы, мл | Объем NaOH в первой ТЭ, мл | Объем NaOH во второй ТЭ, мл |
| 2 | 20 | 15,60 | 16,30 |
| 3 | 20 | 15,20 | 16,10 |
Рассчитываем массу:
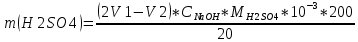
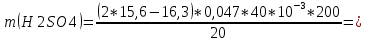
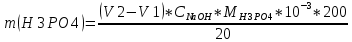
| Номер опыта | m 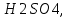 г. г. | m 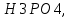 г. г. |
| 2 | | |
| 3 | | |
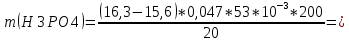
-
Кислотно-основное титрование
Вычислим среднее значение процентного содержания
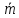 :
:Для H2SO4
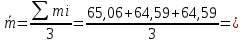
Для H3PO4
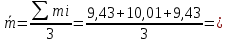
Стандартное отклонение S:
Для H2SO4
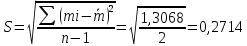
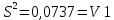
Для H3PO4
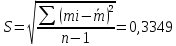
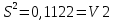
-
Потенциометрия
Вычислим среднее значение процентного содержания
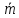
:
Для H2SO4
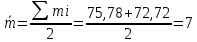
Для H3PO4
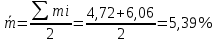
Стандартное отклонение S:
Для H2SO4
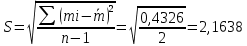
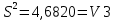
Для H3PO4
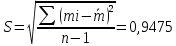
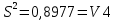
Для H2SO4
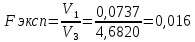 Fтабл =19,00
Fтабл =19,00Если Fрасч> Fтабл, то различие дисперсий статистически значимо, дисперсии неоднородны, два средних значения нельзя сравнивать.
Для H3PO4
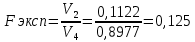 Fтабл =19,00
Fтабл =19,00????эксп <????табл., следовательно, расхождение между дисперсиями двух выборок незначительное, обе выборки равнозначны, дисперсии однородны. Продолжим статистическую обработку, объединив результаты 2-х методов в одну выборку большего объема.
-
Сравнение результатов двух методов по правильности
(по критерию Стьюдента – t)
С помощью t-критерия можно оценить расхождение между средними значениями результатов (
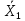 и
и 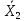 ), полученных двумя методами.
), полученных двумя методами. Для этого:
-
Рассчитывают средневзвешенную дисперсию по формуле:
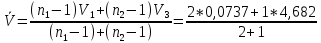 = 1,6098
= 1,6098-
Рассчитывают критерий Стьюдента (tрасч):
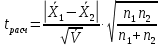 =
= 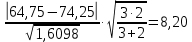
-
Полученное значение tрасч сравнивают с табличным при числе степеней свободы f = n1 + n2 – 2 и определенной доверительной вероятности Р, %.
Для H2SO4
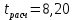
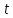 табл =9,92
табл =9,92Если tрасч > tтабл, то расхождение между
 и
и  значимо, выборки не принадлежат одной генеральной совокупности
значимо, выборки не принадлежат одной генеральной совокупностиДля H3PO4
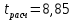
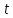 табл =9,92
табл =9,92-
Если tрасчтабл, то расхождение между средними двух серий результатов незначительное, обе выборки результатов следует объединить и рассматривать их как одну выборочную совокупность из (n1 + n2) результатов. Систематическая ошибка отсутствует. Проводят одну общую статистическую обработку для (n1 + n2) результатов, рассчитывают среднее значение (Хср), стандартное (S) и относительное стандартное (Sr, %) отклонение и доверительный интервал (ΔХ).
Статистическая обработка результатов
Для H2SO4
Все полученные значения m:
64,59; 64,59; 65,06; 72,72; 75,78;
Среднее значение массовой доли H2SO4:
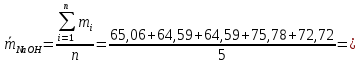
Стандартное отклонение S:
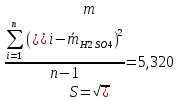
Относительное стандартное отклонение
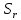 :
: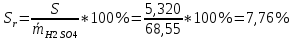
Доверительный интервал для среднего
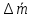 :
: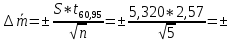
Результат анализа:
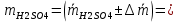
Для H3PO4
Все полученные значения m, гр:
4,72; 6,06; 9,43; 9,43; 10,01;
Среднее значение массовой доли
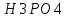
3:
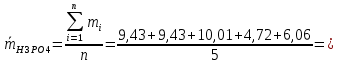
Стандартное отклонение
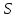 :
: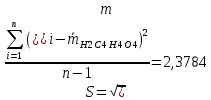
Относительное стандартное отклонение
 :
: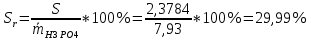
Доверительный интервал для среднего
 :
: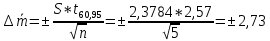
Результат анализа:
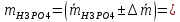
Вывод
После выполнения курсовой работы было определено содержание и H3PO4 и H2SO4 в растворе методами кислотно-основного титрования с визуальной индикацией точки эквивалентности и потенциометрического титрования, получены следующие результаты:
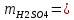
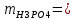
Наличие погрешностей, связанно с неточным отбором объема титранта и смеси кислот с помощью пипетки, а также погрешностью самого прибора для потенциометрического титрования.
Библиографический список
-
С. Ю. Сараева. Химические и физико-химические методы анализа. Сборник задач. Екатеринбург Издательство Уральского университета 2016. Текст: электронный. URL: https://elar.urfu.ru/bitstream/10995/43904/1/978-5-7996-1860-5_2016.pdf (Дата обращения: 18.12.2022) -
Титрование. Лабораторный и химический анализ. Текст: электронный. URL: https://nationalteam.worldskills.ru/skills/titrovanie/ (Дата 18.12.2022) -
Индикаторы кислотно-основного титрования. Текст: электронный. URL: https://studme.org/334728/matematika_himiya_fizik/indikatory_kislotno_osnovnogo_titrovaniya (Дата обращения 18.12.2022) -
Потенциометрия. Текст: электронный. URL: http://www.chemport.ru/data/chemipedia/article_3088.html (Дата обращения 20.12.2022) -
Что такое потенциометрия и потенциометрический метод? Текст: электронный. URL: https://www.izmteh.ru/articles/potentsiometriya.php/ (Дата обращения 20.12.2021) -
Электрохимические методы анализа. Индикаторный электрод и электрод сравнения. Текст: электронный. URL: http://bookwu.net/book_elektrohimicheskie-metody-analiza_1091/6_-2-indikatornyj-elektrod-i-elektrod-sravneniya (Дата обращения 20.12.2021) -
https://teach-in.ru/file/synopsis/pdf/analitchem-M.pdf -
http://afh.samgtu.ru/sites/afh.samgtu.ru/files/posobie_ahifhma.pdf