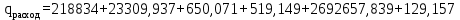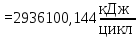Файл: Тема выпускной квалификационной работы Анализ ассортимента, свойства и применение термопластичных фторсодержащих полимеров.docx
Добавлен: 03.12.2023
Просмотров: 142
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
1.5 Виды маркировок для известных фторопластов
1.6 Современные отечественные производители
2.1. Молекулярная масса и структура фторопласта-3.
2.2. Свойства политрифторхлорэтилена
2.3 Получение политрифторхлорэтилена.
3 Термодинамический анализ реакции полимеризации ТФХЭ
4. Материальный баланс реакции полимеризации трифторхлорэтилена
5. Тепловой баланс реакции полимеризации трифторхлорэтилена
7. Разработка и описание операторной и технологической схемы
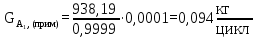
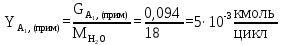
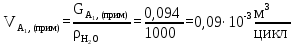
Расчет загрузки среды (воды). Рассчитывается из соотношения загрузки среды к мономеру 2:1
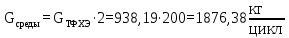
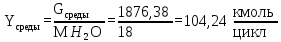
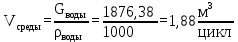
Расчет пероксида водорода (инициатор) (В):
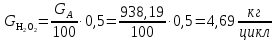
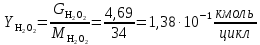
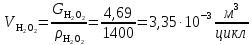
Расчет реагента С:
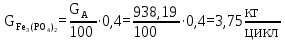
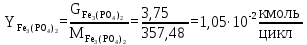
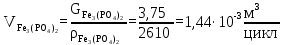
Расчет реагента D:
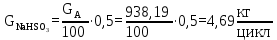
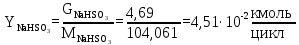
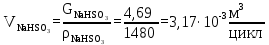
Расчет непрореагировавшего ТФХЭ:
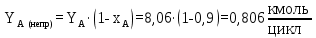
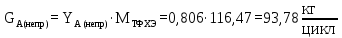
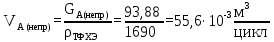
Составим уравнение материального баланса на входе в реактор:
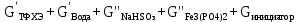
На выходе из реактора состав веществ будет состоять из:
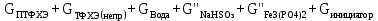
Таблица 13 – Данные материального баланса
| Приход | ||||||
| Наименование компонента | Gi, кг/цикл | %, (масс.) | Yi, Кмоль/цикл | %, (кмоль) | Объем V, м3/цикл | %, (об.) |
| ТФХЭ (А) | 938,19 | 33,18 | 8,06 | 7,17 | 0,56 | 22,86 |
| Вода (прим А1) | 0,09 | 0,003 | 5·10-3 | 0,004 | 0,09·10-3 | 0,004 |
| Пероксид водорода (В) | 4,69 | 0,17 | 1,38·10-1 | 0,12 | 3,35·10-3 | 0,14 |
| Фосфат железа (С) | 3,75 | 0,13 | 1,05·10-2 | 0,006 | 1,44·10-3 | 0,06 |
| Гидросульфит натрия (D) | 4,69 | 0,17 | 4,51·10-2 | 0,04 | 3,17·10-3 | 0,16 |
| Вода (среда) | 1876,38 | 66,35 | 104,24 | 92,66 | 1,88 | 76,77 |
| Итого | 2827,79 | 100,00 | 112,49 | 100,00 | 2,45 | 100,00 |
| Расход | ||||||
| ПТФХЭ(F) | 844,37 | 29,86 | 7,25 | 6,45 | 0,49 | 20,46 |
| ТФХЭ (непр.) | 93,78 | 3,32 | 0,81 | 0,72 | 55,6*10-3 | 2,27 |
| Вода (Прим.) | 0,09 | 0,003 | 5·10-3 | 0,004 | 0,09*10-3 | 0,004 |
| Вода (среда) | 1876,38 | 66,35 | 104,24 | 92,67 | 1,88 | 76,73 |
| Пероксид водорода | 4,69 | 0,17 | 1,38·10-1 | 0,12 | 3,35·10-3 | 0,14 |
| Фосфат железа | 3,75 | 0,13 | 1,05·10-2 | 0,01 | 1,44·10-3 | 0,06 |
| Гидросульфит натрия | 4,69 | 0,17 | 4,51·10-2 | 0,03 | 3,17·10-3 | 0,13 |
| Итого | 2827,79 | 100,00 | 112,49 | 100,00 | 2,45 | 100,00 |
При производстве политрифторхлорэтилена, для получения 844,37 кг. за цикл нам необходимо загрузить в реактор производительностью 765 т/год 938,19 кг. ТФХЭ, 1876,38 кг. среды, 4,69 кг. H2O2, 4,69 кг.NaHSO3, и 3,75 кг. Fe3(PO4)2
5. Тепловой баланс реакции полимеризации трифторхлорэтилена
Перед началом расчетов занесем необходимые данные в таблицу
Таблица 14 - Исходные данные для расчета теплового баланса
| Приход | |||
| Наименование | Мольный поток Y, моль/цикл | Теплоемкость Cоp, Дж/Моль*К | ТемператураТ,К |
| ТФХЭ (А) | 8060 | 83,9 | 293 |
| Вода (прим А1) | 5 | 75,31 | 293 |
| H2O2 (катализатор) (В) | 138 | 88,41 | 293 |
| Фосфат железа(С) | 10,5 | 180,5 | 293 |
| Гидросульфит натрия (D) | 45.1 | 33,56 | 293 |
| Вода (среда) | 104240 | 75,31 | 293 |
| Расход | |||
| ПТФХЭ (F) | 7250 | 88 | 343 |
| ТФХЭ (непр.) | 810 | 83,9 | 343 |
| Вода (Прим. А1) | 5 | 75,31 | 343 |
| H2O2 (катализатор) (В) | 138 | 88,41 | 343 |
| Фосфат железа(С) | 10,5 | 180,5 | 343 |
| Гидросульфит натрия (D) | 45,1 | 33,56 | 343 |
| Вода (среда) | 104240 | 75,31 | 343 |
Тепловой баланс рассчитывается по данным материального баланса с учетом тепловых эффектов (экзо- или эндотермических) химических реакций и фазовых превращений (испарение, конденсация, плавление, кристаллизация, возгонка), происходящих в реакторе, подвода тепла с исходным сырьем и отвода тепла с продуктами реакции, тепловых потерь. Тепловой баланс составляется на основе закона сохранения энергии в соответствии с которым [27].
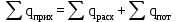 (11)
(11)Для стадии синтеза, в котором, наряду с процессами теплообмена, происходят химические и фазовые превращения, сопровождающиеся выделением или поглощением тепла, уравнение теплового баланса принимает вид (12) :
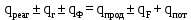 , (12)
, (12)Расчет тепла, входящее в реактор с реагентами реакции ведется по формуле (13) :
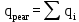 , (13)
, (13)где
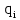 – тепло, поступающее с i – реагентом, кДж/цикл.
– тепло, поступающее с i – реагентом, кДж/цикл. qi находится по формуле (14) :
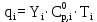 , (14)
, (14)где
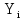 – мольный поток i – реагента, моль/цикл;
– мольный поток i – реагента, моль/цикл; 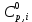 – теплоемкость i
– теплоемкость iРасчет тепла, входящее в реактор с реагентами реакции ведется по формуле (15) :
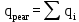 , (15)
, (15)где
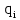 – тепло, поступающее с i – реагентом, кДж/цикл.
– тепло, поступающее с i – реагентом, кДж/цикл. qi находится по формуле (16):
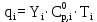 , (16)
, (16)где
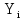 – мольный поток i – реагента, моль/цикл;
– мольный поток i – реагента, моль/цикл; 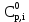 – теплоемкость i – реагента, Дж/моль·К;
– теплоемкость i – реагента, Дж/моль·К; 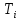 – температура i – реагента.
– температура i – реагента.Рассчитаем тепло входящее в реактор с реагентами
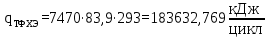
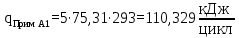
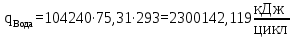
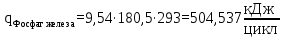
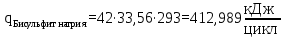
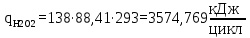
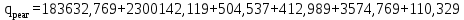
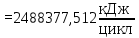
Тепло, выделяющееся (или поглощающееся) в результате химических превращений рассчитывается по формуле (17):
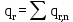 , (17)
, (17)где
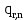 – теплота n – й химической реакции (основной и побочных), кДж/цикл.
– теплота n – й химической реакции (основной и побочных), кДж/цикл.Теплота химической реакции находится по формуле (18):
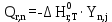 , (18)
, (18)где
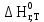 – тепловой эффект n – химической реакции, реакции 102,236 кДж/моль;
– тепловой эффект n – химической реакции, реакции 102,236 кДж/моль; 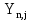 – мольный поток полученного n – продукта реакции, моль/цикл.
– мольный поток полученного n – продукта реакции, моль/цикл.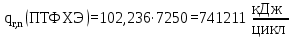
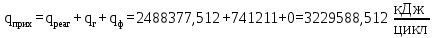
Расчет тепла, выходящее из реактора с продуктами реакции, ведется по формуле (19):
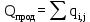 , (19)
, (19)где
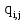 – тепло, выходящее из реактора с i – продуктами реакции, кДж/цикл.
– тепло, выходящее из реактора с i – продуктами реакции, кДж/цикл. Тепло, выходящее из реактора рассчитывается по формуле (20):
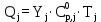 , (20)
, (20)где
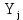 – мольный поток j – продукта реакции, моль/цикл;
– мольный поток j – продукта реакции, моль/цикл; 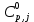 – теплоемкость j – продукта реакции, Дж/моль·К;
– теплоемкость j – продукта реакции, Дж/моль·К; 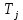 – температура j – продукта реакции, К.
– температура j – продукта реакции, К.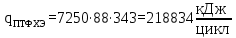
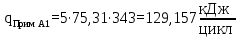
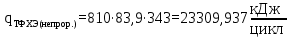
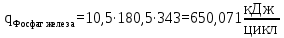
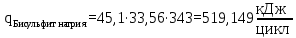
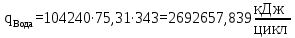
Тогда, тепло выходящее из реактора с продуктами реакции будет составлять: