Файл: Физические основы применения лазерной техники в медицине.rtf
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.12.2023
Просмотров: 84
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
На практике оптимальная выходная мощность для хирургии находится в диапазоне от 15 до 60 Вт в зависимости от длины волны лазерного излучения и области применения.
3. Перспективные лазерные методы в медицине и биологии
Развитие лазерной медицины идет по трем основным ветвям: лазерная хирургия, лазерная терапия и лазерная диагностика. Уникальные свойства лазерного луча позволяют выполнять ранее невозможные операции новыми эффективными и минимально инвазивными методами.
Растет интерес к немедикаментозным методам лечения, включая физиотерапию. Нередко возникают ситуации, когда необходимо проводить не одну физиопроцедуру, а несколько, и тогда пациенту приходиться переходить из одной кабины в другую, несколько раз одеваться и раздеваться, что создает дополнительные проблемы и потерю времени.
Многообразие методик терапевтического воздействия требует применения лазеров с различными параметрами излучения. Для этих целей служат различные излучающие головки, которые содержат один или несколько лазеров и электронное устройство сопряжения сигналов управления от базового блока с лазером.
Излучающие головки подразделяются на универсальные, позволяющие использовать их как наружно, (с использованием зеркальных и магнитных насадок), так и внутриполостно с использованием специальных оптических насадок; матричные, имеющие большую площадь излучения и применяющиеся поверхностно, а также специализированные. Различные оптические насадки позволяют доставлять излучение к требуемой зоне воздействия.
Блочный принцип позволяет применять широкий спектр лазерных и светодиодных головок, обладающих различными спектральными, пространственно-временными и энергетическими характеристиками, что, в свою очередь, поднимает на качественно новый уровень эффективность лечения за счет сочетанной реализации различных методик лазерной терапии. Эффективность лечения определяется прежде всего эффективными методиками и аппаратурой, которая обеспечивает их реализацию. Современные методики требуют возможность выбора различных параметров воздействия (режим излучения, длина волны, мощность) в широком диапазоне. Аппарат лазерной терапии (АЛТ) должен обеспечивать эти параметры, их достоверный контроль и отображение и вместе с тем быть простым и удобным в управлении.
4. Лазеры, применяемые в медицинской технике
4.1 CO2-лазеры
CO2-лазер, т.е. лазер, излучающей составляющей активной среды которого является углекислый газ CO2, занимает особое место среди всего многообразия существующих лазеров. Этот уникальный лазер отличается прежде всего тем, что для него характерны и большой энергосъем, и высокий КПД. В непрерывном режиме получены огромные мощности – в несколько десятков киловатт, импульсная мощность достигла уровня в несколько гигаватт, энергия импульса измеряется в килоджоулях. КПД CO2-лазера (порядка 30%) превосходит КПД всех лазеров. Частота следования в импульсно-периодическом режиме может составить несколько килогерц. Длины волн излучения CO2-лазера находятся в диапазоне 9-10 мкм (ИК-диапазон) и попадают в окно прозрачности атмосферы. Поэтому излучение CO2-лазера удобно для интенсивного воздействия на вещество. Кроме того, в диапазон длин излучения CO2-лазера попадают резонансные частоты поглощения многих молекул.
На рисунке 1 показаны нижние колебательные уровни основного электронного состояния вместе с условным представлением формы колебаний молекулы CO2.
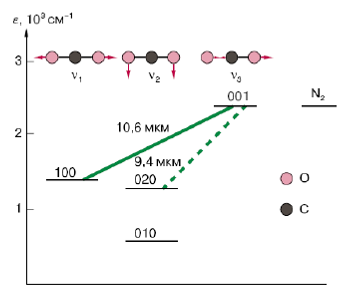
Рис. 1. Нижние уровни молекулы CO2
Цикл лазерной накачки CO2-лазера в стационарных условиях выглядит следующим образом. Электроны плазмы тлеющего разряда возбуждают молекулы азота, которые передают энергию возбуждения несимметричному валентному колебанию молекул CO2, обладающему большим временем жизни и являющемуся верхним лазерным уровнем. Нижним лазерным уровнем обычно является первый возбужденный уровень симметричного валентного колебания, сильно связанный резонансом Ферми с деформационным колебанием и поэтому быстро релаксирующий вместе с этим колебанием в столкновениях с гелием. Очевидно, что тот же канал релаксации эффективен в том случае, когда нижним лазерным уровнем является второй возбужденный уровень деформационной моды. Таким образом, CO2-лазер – это лазер на смеси углекислого газа, азота и гелия, где CO2 обеспечивает излучение, N2 – накачку верхнего уровня, а He – опустошение нижнего уровня.
CO2-лазеры средней мощности (десятки – сотни ватт) конструируются отдельно в виде относительно длинных труб с продольным разрядом и продольной прокачкой газа. Типичная конструкция такого лазера показана на рисунке 2. Здесь 1 – разрядная трубка, 2 – кольцевые электроды, 3 – медленное обновление среды, 4 – разрядная плазма, 5 – внешняя трубка, 6 – охлаждающая проточная вода, 7,8 – резонатор.
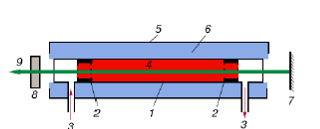
Рис.2. Схема CO2-лазера с диффузионным охлаждением
Продольная прокачка служит для удаления продуктов диссоциации газовой смеси в разряде. Охлаждение рабочего газа в таких системах происходит за счет диффузии на охлаждаемую снаружи стенку разрядной трубки. Существенной является теплопроводность материала стенки. С этой точки зрения целесообразно применение труб из корундовой (Al2O3) или бериллиевой (BeO) керамик.
Электроды делают кольцевыми, не загораживающими путь к излучению. Джоулево тепло выносится теплопроводностью к стенкам трубки, т.е. используется диффузионное охлаждение. Глухое зеркало делают металлическим, полупрозрачное – из NaCl, KCl, ZnSe, AsGa.
Альтернативой диффузионному служит конвекционное охлаждение. Рабочий газ с большой скоростью продувают через область разряда, и джоулево тепло выносится разрядом. Применение быстрой прокачки позволяет поднять плотности энерговыделения и энергосъема.
CO2-лазер в медицине применяется почти исключительно как «оптический скальпель» для резания и испарения во всех хирургических операциях. Режущее действие сфокусированного лазерного пучка основано на взрывном испарении внутри- и внеклеточной воды в области фокусировки, благодаря чему разрушается структура материала. Разрушение ткани приводит к характерной форме краев раны. В узко ограниченной области взаимодействия температура 100 °С превышается лишь тогда, когда достигнуто обезвоживание (испарительное охлаждение). Дальнейшее повышение температуры приводит к удалению материала путем обугливания или испарения ткани. Непосредственно в краевых зонах образуется из-за плохой в общем случае теплопроводности тонкое некротическое утолщение толщиной 3040 мкм. На расстоянии 300600 мкм уже не образуется повреждение ткани. В зоне коагуляции кровеносные сосуды диаметром до 0,51 мм спонтанно закрываются.
Хирургические устройства на основе CO2-лазера в настоящее время предлагаются в достаточно широком ассортименте. Наведение лазерного луча в большинстве случаев осуществляется с помощью системы шарнирно установленных зеркал (манипулятора), оканчивающейся инструментом со встроенной фокусирующей оптикой, которым хирург манипулирует в оперируемой области.
4.2 Гелий-неоновые лазеры
В гелий-неоновом лазере рабочим веществом являются нейтральные атомы неона. Возбуждение осуществляется электрическим разрядом. В чистом неоне создать инверсию в непрерывном режиме трудно. Эта трудность, носящая достаточно общий для многих случаев характер, обходится введением в разряд дополнительного газа – гелия, выполняющего функцию донора энергии возбуждения. Энергии двух первых возбужденных метастабильных уровней гелия (рисунок 3) довольно точно совпадают с энергиями уровней 3s и 2s неона. Поэтому хорошо реализуются условия
резонансной передачи возбуждения по схеме
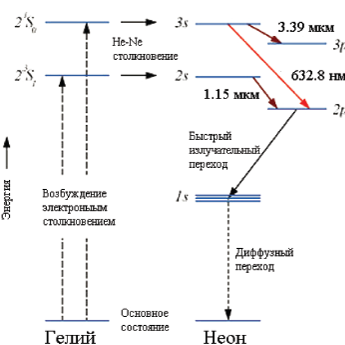
Рис.3.Схема уровней He-Ne лазера
При правильно выбранных давлениях неона и гелия, удовлетворяющих условию можно добиться заселения одного или обоих уровней 3s и 2s неона, значительно превышающего таковое в случае чистого неона, и получить инверсию населенностей.
Опустошение нижних лазерных уровней происходит в столкновительных процессах, в том числе и в соударениях со стенками газоразрядной трубки.
Возбуждение атомов гелия (и неона) происходит в слаботочном тлеющем разряде В лазерах непрерывного действия на нейтральных атомах или молекулах для создания активной среды чаще всего используется слабоионизированная плазма положительного столба тлеющего разряда. Плотность тока тлеющего разряда составляет 100-200 мА/см2. Напряженность продольного электрического поля такова, что число возникающих на единичном отрезке разрядного промежутка электронов и ионов компенсирует потери заряженных частиц при их диффузии к стенкам газоразрядной трубки. Тогда положительных столб разряда стационарен и однороден. Электронная температура определяется произведением давления газа
Для гелий-неонового лазера оптимальные значения