Файл: Сборник заданий Москва 2018 удк 541. 18183 ббк 24. 5.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 703
Скачиваний: 2
СОДЕРЖАНИЕ
ОСНОВНЫЕ ПОНЯТИЯ ДИСЦИПЛИНЫ. ТЕРМОДИНАМИКА ПОВЕРХНОСТНОГО СЛОЯ
АДСОРБЦИЯ НА ГРАНИЦЕ РАСТВОР – ГАЗ
АДСОРБЦИЯ НА ГРАНИЦЕ ГАЗ – ТВЕРДОЕ ТЕЛО
АДСОРБЦИЯ НА ГРАНИЦЕ РАСТВОР – ТВЕРДОЕ ТЕЛО
ОПТИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ СВОЙСТВА
ЭЛЕКТРОПОВЕРХНОСТНЫЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ ДИСПЕРСНЫХ СИСТЕМ
СТРУКТУРНО-МЕХАНИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
РАСТВОРЫ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ
ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ ДИСПЕРСНЫХ СИСТЕМ
«Введение. Термодинамика поверхностного слоя»
«Адсорбция на границе раздела раствор - газ»
«Адсорбция на границе газ – твердое тело»
«Адсорбция на границе раствор – твердое тело»
«Оптические свойства дисперсных систем»
«Молекулярно-кинетические свойства дисперсных систем»
«Электроповерхностные свойства дисперсных систем»
«Устойчивость и коагуляция дисперсных систем»
АДСОРБЦИЯ НА ГРАНИЦЕ ГАЗ – ТВЕРДОЕ ТЕЛО
Один правильный ответ
-
Какие силы обеспечивают взаимодействие полярных молекул (например, воды и аммиака)?
-
водородные связи; -
индукционные; -
ориентационные; -
дисперсионные.
-
Каким уравнением описывается изотерма мономолекулярной адсорбции Ленгмюра?
-
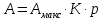 ;
;
-
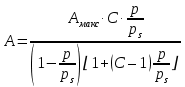 ;
; -
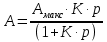 ;
; -
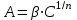 .
.
-
Какая теория адсорбции является универсальной?
-
Ленгмюра; -
БЭТ; -
Поляни; -
Генри.
-
Как изменяется величина физической адсорбции при понижении температуры?
-
увеличивается; -
не изменяется; -
уменьшается; -
сначала увеличивается, затем уменьшается.
-
Какие адсорбционные силы являются наиболее универсальными?
-
дисперсионные; -
ориентационные; -
индукционные; -
водородные связи.
-
Каким уравнением описывается изотерма полимолекулярной адсорбции?
-
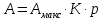 ;
; -
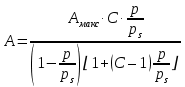 ;
; -
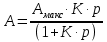 ;
; -
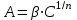 .
.
-
В каких единицах измеряется интегральная теплота адсорбции?
-
Дж/м2 адсорбента; -
Дж/кг адсорбата; -
Дж/кг адсорбента; -
Дж/моль адсорбата.
-
Какое уравнение описывает зависимость времени пребывания адсорбтива на поверхности адсорбента от теплоты адсорбции?
-
τ =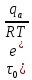 ;
; -
τ =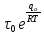 ;
; -
τ =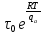 .
.
-
Как изменяется энергия активации хемосорбции по мере заполнения активных центров адсорбента?
-
уменьшается; -
не изменяется; -
возрастает.
-
Какой вид имеет динамическое уравнение адсорбции?
-
α = nρ; -
α = cτ; -
α = kτ; -
α =nτ.
-
В каких единицах измеряется емкость монослоя?
-
моль/м2; -
моль/м; -
кмоль/л; -
кмоль/кг.
-
Чему равна энергия активации хемосорбции при степени заполнения адсорбента θ =0?
-
Е акт > 0; -
Е акт < 0; -
Е акт = 0.
-
Какой вид имеет уравнение мономолекулярной адсорбции Фрейндлиха?
-
 ;
; -
 ;
; -
 ;
; -
 .
.
-
Какие участки изотермы описывает уравнение Ленгмюра?
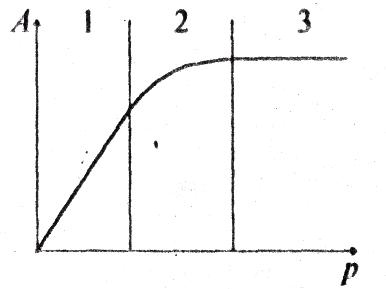
-
1; -
1 и 2; -
3; -
1,2,3.
-
Что описывает первое слагаемое в уравнении Леннард-Джонса: ?
?
-
энергию борновского отталкивания; -
энергию индукционного взаимодействия; -
энергию межмолекулярного притяжения; -
энергию ориентационного взаимодействия.
-
Что описывает второе слагаемое в уравнении Леннард-Джонса: ?
?
-
энергию борновского отталкивания; -
энергию индукционного взаимодействия; -
энергию межмолекулярного притяжения; -
энергию ориентационного взаимодействия.
-
Сколько равновесных участков имеется на изобаре адсорбции?
-
один; -
два; -
три.
-
Изотерма адсорбции имеет вид …….
-
экспоненты; -
гиперболы; -
прямой линии; -
параболы.
-
Изотермы физической адсорбции азота на TiO2 и BaSO4:
-
отличаются; -
азот не адсорбируется на TiO2; -
совпадают; -
азот не адсорбируется на BaSO4.
-
Зависимость интегральной теплоты адсорбции от величины адсорбции:
-
имеет минимум; -
имеет максимум; -
линейна, так как активные центры равны по энергии; -
нелинейна, так как активные центры энергетически неравноценны.
-
Дифференциальная теплота адсорбции с увеличением количества адсорбированного вещества …….
-
увеличивается; -
не изменяется; -
уменьшается; -
сначала увеличивается, затем уменьшается.
Множественные ответы
-
Каковы предпосылки теории мономолекулярной адсорбции Ленгмюра?
-
адсорбция вызывается силами, близкими к химическим; -
адсорбция происходит на всей поверхности адсорбента; -
адсорбция происходит только на активных центрах; -
один активный центр адсорбирует только одну молекулу; -
взаимодействие между соседними адсорбированными молекулами не учитывается; -
устанавливается равновесие адсорбция ↔ десорбция.
-
В каких единицах измеряется удельная поверхность адсорбента?
-
м2/кг; -
м2/г; -
моль/г; -
м-1.
-
Химическая адсорбция ………
-
необратима; -
специфична; -
полимолекулярна; -
локализована; -
обратима; -
мономолекулярна.
-
На рисунке представлена изотерма адсорбции в координатах линейной формы уравнения Ленгмюра. Как можно определить константы уравнения Ленгмюра?
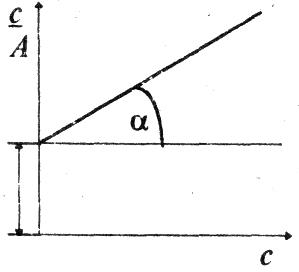
-
Амакс = сtgα; -
Aмакс равна отрезку, отсекаемому на оси ординат; -
1/Амакс·К равна отрезку, отсекаемому на оси ординат; -
К = сtgα.
-
Каковы условия самопроизвольного протекания процесса адсорбции при T = const?
-
ΔS<0; -
ΔS>0; -
ΔH<0; -
ΔH>0; -
ΔG<0.
-
Каковы предпосылки теории БЭТ?
-
на поверхности адсорбента имеется определенное число равноценных в энергетическом отношении активных центров; -
для упрощения взаимодействием соседних адсорбированных молекул в первом и последующих случаях пренебрегают; -
адсорбционные силы зависят от температуры; -
теплоты адсорбции второго и всех последующих слоев равны теплоте объемной конденсации; -
каждая молекула первого слоя представляет собой возможный центр для адсорбции и образования второго адсорбционного слоя, каждая молекула второго слоя является возможным центром адсорбции в третьем и т. д.; -
теплота адсорбции первого слоя равна теплоте объемной конденсации; -
теплота адсорбции первого слоя равна теплоте адсорбции; -
адсорбционные силы не зависят от температуры.
-
Каковы особенности физической адсорбции?
-
обратимость; -
не специфичность; -
не локализованность; -
способность к полимолекулярной адсорбции.
-
Каковы предпосылки теории Поляни?
-
адсорбция происходит за счет химических сил; -
адсорбция происходит за счет физических сил; -
адсорбция происходит только на активных центрах адсорбента; -
поверхность адсорбента не имеет активных центров; -
адсорбционные силы действуют на больших расстояниях и прекращают свое действие на некотором удалении от поверхности; -
адсорбция локализована; -
адсорбционные силы не зависят от температуры, что способствует созданию определенного адсорбционного объема вблизи поверхности.
-
Каковы отличия физической адсорбции от химической?
-
физическая адсорбция протекает с выделением малого количества тепла; -
физическая адсорбция протекает с выделением большого количества тепла; -
физическая адсорбция мономолекулярна; -
физическая адсорбция может быть как моно-, так и полимолекулярной; -
энергия активации физической адсорбции равна энергии диссоциации молекул адсорбируемого газа.
-
По первым буквам фамилий каких авторов получила название теория адсорбции, обобщающая представления Ленгмюра и Поляни?
-
Теллер; -
Эйнштейн; -
Эммет; -
Траубе; -
Бедекер; -
Брунауэр.
-
Зависимость интегральной теплоты адсорбции от величины адсорбции не линейна, т. к. …..
-
поверхность адсорбента энергетически неоднородна; -
поверхность адсорбента энергетически однородна; -
вначале адсорбция идет на более активных центрах и выделяется большое тепла; -
количество выделяющегося тепла не зависит от степени заполнения активных центров адсорбента; -
при увеличении степени заполнения активных центров адсорбента -
количество выделяющегося тепла снижается.