Файл: Курсовая работа на тему Модель многосубстратного процесса микробного роста Простейшие кинетические схемы обобщенная модель многосубстратного микробного процесса.doc
Добавлен: 23.11.2023
Просмотров: 91
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, доступный в исследованиях с применением антител, значительно варьирует. Кроме того, этот метод, как и метод определения липидов, ограничен распознаванием культивируемых бактерий, так как их используют при этом для получения антител. Следует учитывать также, что поверхностные свойства бактерий (образование слизи, присутствие адгезинов и другие характеристики) в природных условиях и лабораторных культурах могут существенно различаться. Таким образом, этот подход пригоден для определенных, хорошо изученных систем, но в целом его применимость весьма ограничена. С успехом он используется для идентификации метаногенов в анаэробном активном иле.
Новые возможности для изучения микробных сообществ открывает применение молекулярно-биологических методов. Принцип учета микробов на основе анализа рРНК состоит в том, что синтезированные олигонуклеотидные рРНК-зонды для участков рРНК гибридизуются специфически с определенными участками рРНК клеток в исследуемом образце. Эти участки должны быть предварительно, путем сравнения всех имеющихся данных о последовательностях рРНК, определены как высоко- или низковариабельные и как специфические для какого-либо домена, типа, подтипа или таксона более низкого ранга в пределах данной системы, в некоторых случаях вплоть до видового уровня. К такому зонду, состоящему примерно из 18 или большего числа нуклеотидов, присоединяют флуоресцентный краситель, и благодаря этому при специфической гибридизации зонда с рРНК клетка-мишень приобретает флуоресцентную окраску. Живые клетки бактерий содержат несколько тысяч копий молекул рРНК, поэтому связывание флуоресцентного зонда с клетками-мишенями обеспечивает хорошо заметное свечение во флуоресцентном микроскопе.
Этот метод применим, во-первых, для выявления определенной бактерии в микробном сообществе с помощью высокоспецифичного зонда. Во-вторых, использование менее специфичных зондов позволяет в первом приближении идентифицировать неизвестные бактерии в сообществе, относя их к определенным филогенетическим группам. Таким способом до 90% общей микробной популяции в пробах озерной воды может быть распределено по двум основным доменам прокариот. Другой пример подобного использования рРНК-зондов - идентификацию бактерий в активном иле - иллюстрирует рис. 3.
С помощью более специфических зондов можно определять некультивируемые формы прокариот, обитающие, например, в организме простейшего, до уровня рода. Если молекулярные зонды, специфичные для групп различных уровней в пределах данной таксономической системы прокариот, связывать с различными флуоресцентными красителями, в одном препарате из природного образца можно наблюдать распределение микробов по группам различных филогенетических уровней.
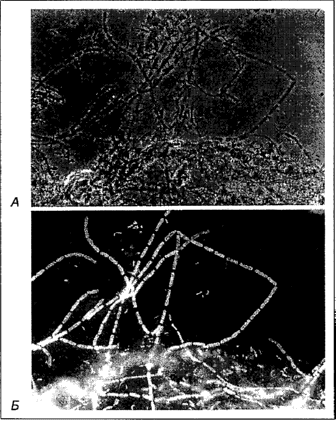
Рис. 3 - Определение протеобактерий с группоспецифическим нуклеотидным зондом к рРНК. А. Фазово-контрастная микроскопия. Б. Тот же препарат при флуоресцентной микроскопии с УФ-эпиосвещением
Этот метод дает чрезвычайно эффектные результаты при его сочетании с конфокальной лазерной микроскопией, позволяя одновременно визуализировать группы бактерий различного систематического уровня в виде трехмерной картины и выявлять, например, их пространственные взаимосвязи.
Применение полимеразной цепной реакции позволяет копировать даже единственную молекулу 16S-рРНК (в виде ДНК) в экстрактах из природных образцов для сравнения нуклеотидных последовательностей этой ДНК с ДНК известных прокариот. Таким способом предлагается изучать филогенетические связи некультивируемых бактерий с другими прокариотами. Амплифицированную ДНК можно использовать для создания зондов, специфичных к нуклеиновым кислотам неизвестных микроорганизмов, и таким образом оценивать разнообразие микробного сообщества, независимо от способности данных микроорганизмов расти в культуре. Этот же метод может быть использован для того, чтобы проследить судьбу некультивируемого организма при тех или иных способах изучения общей популяции, например в процессе получения накопительной культуры нового организма с неизвестными потребностями или при изменениях в популяциях некультивируемых бактерий, например активного ила, в результате стрессовых природных ситуаций.
Наряду с перспективностью методов молекулярных зондов для микробной экологии следует отметить и их ограничения. Эти методы позволяют установить присутствие определенного типа микроорганизмов и его принадлежность к той или иной ветви филогенетической системы, созданной на основе анализа последовательностей. Однако в большинстве случаев они не дают возможности определить экологическую нишу (тип метаболизма) некультивируемого организма, поскольку филогенетические группы не гомологичны метаболическим группам, даже на уровне мельчайших разветвлений системы. Кроме того, не все прокариоты одинаково доступны для применения молекулярных зондов. Некоторые бактерии, особенно обладающие толстыми клеточными стенками или окруженные капсулой либо слизью, остаются трудными объектами для экстракции ДНК или гибридизации РНК с зондами. Поскольку метод зондов к тому же селективен, определенные бактерии, возможно важные, при анализе популяций этим способом могут остаться незамеченными.
Заключение
Основным лимитирующим фактором в условиях природных экосистем для микроорганизмов является количество субстрата.
Механизмы устойчивости к голоданию включают увеличение числа высокоаффинных транспортных систем, увеличение клеточной поверхности, образование спор, уменьшение размеров клеток, адаптацию клеточного метаболизма путем синтеза индуцируемых голоданием белков и образование слизи.
Апробированные и разработанные простые модели искусственных экосистем (хемостаты) являются эффективным инструментом для изучения законов функционирования микробных популяций и их сообществ в природных экосистемах. При разработке подходов устойчивого развития биосферы экспериментальные и теоретические исследования позволяют выявить закономерности взаимодействия микробных популяций с остальными обитателями экосистем и найти подходы к управлению ими в моделях искусственных экосистем.
Однако все питательные среды и условия инкубации селективны для небольшой фракции общей бактериальной популяции, имеющейся в исследуемом образце; попытки составить менее специфические, более соответствующие природным условиям культуральные среды, позволяющие более точно оценивать разнообразие и численность микроорганизмов, пока не дали успеха.
Определение численности микроорганизмов в природных образцах можно осуществлять путем прямого подсчета под микроскопом флуоресцентно окрашенных клеток, радиоавтографии клеток, меченных 14С или 3Н, подсчета колоний, выросших на плотной питательной среде, определения роста в жидкой среде с учетом разведения, измерения общего содержания АТР, ДНК или более специфических клеточных компонентов, таких как жирные кислоты или хлорофилл, либо методами с применением флуоресцентно меченных антител. Все эти методы имеют свои ограничения.
Одиночные клетки или популяции микроорганизмов можно идентифицировать путем гибридизации с синтетическими рРНК-зондами или с рРНК-зондами, полученными на основе амплифицированной (методом ПЦР) ДНК. Эти методы можно применять в сочетании с оптическими для выявления в том числе некультивируемых микроорганизмов в природных образцах.
Список источников
культура субстрат хемостат микроорганизм
1. Современная микробиология: прокриоты: В 2-х томах: Т. 1,2. Пер. с англ. / Под ред. Й. Лендлегера, Г. Древса, Г. Шлегеля. - М.: Мир, 2005. - 496 с.: ил., 24 с.
2. http://zhurnal.ape.relarn.ru/articles/2006/062.pdf - Электронный научный журнал «Исследовано в России». Статья «Использование малых моделей искусственных экосистем для изучения взаимодействия ризобактерий с растением-хозяином и микроскопическими почвенными грибами».
Новые возможности для изучения микробных сообществ открывает применение молекулярно-биологических методов. Принцип учета микробов на основе анализа рРНК состоит в том, что синтезированные олигонуклеотидные рРНК-зонды для участков рРНК гибридизуются специфически с определенными участками рРНК клеток в исследуемом образце. Эти участки должны быть предварительно, путем сравнения всех имеющихся данных о последовательностях рРНК, определены как высоко- или низковариабельные и как специфические для какого-либо домена, типа, подтипа или таксона более низкого ранга в пределах данной системы, в некоторых случаях вплоть до видового уровня. К такому зонду, состоящему примерно из 18 или большего числа нуклеотидов, присоединяют флуоресцентный краситель, и благодаря этому при специфической гибридизации зонда с рРНК клетка-мишень приобретает флуоресцентную окраску. Живые клетки бактерий содержат несколько тысяч копий молекул рРНК, поэтому связывание флуоресцентного зонда с клетками-мишенями обеспечивает хорошо заметное свечение во флуоресцентном микроскопе.
Этот метод применим, во-первых, для выявления определенной бактерии в микробном сообществе с помощью высокоспецифичного зонда. Во-вторых, использование менее специфичных зондов позволяет в первом приближении идентифицировать неизвестные бактерии в сообществе, относя их к определенным филогенетическим группам. Таким способом до 90% общей микробной популяции в пробах озерной воды может быть распределено по двум основным доменам прокариот. Другой пример подобного использования рРНК-зондов - идентификацию бактерий в активном иле - иллюстрирует рис. 3.
С помощью более специфических зондов можно определять некультивируемые формы прокариот, обитающие, например, в организме простейшего, до уровня рода. Если молекулярные зонды, специфичные для групп различных уровней в пределах данной таксономической системы прокариот, связывать с различными флуоресцентными красителями, в одном препарате из природного образца можно наблюдать распределение микробов по группам различных филогенетических уровней.

Рис. 3 - Определение протеобактерий с группоспецифическим нуклеотидным зондом к рРНК. А. Фазово-контрастная микроскопия. Б. Тот же препарат при флуоресцентной микроскопии с УФ-эпиосвещением
Этот метод дает чрезвычайно эффектные результаты при его сочетании с конфокальной лазерной микроскопией, позволяя одновременно визуализировать группы бактерий различного систематического уровня в виде трехмерной картины и выявлять, например, их пространственные взаимосвязи.
Применение полимеразной цепной реакции позволяет копировать даже единственную молекулу 16S-рРНК (в виде ДНК) в экстрактах из природных образцов для сравнения нуклеотидных последовательностей этой ДНК с ДНК известных прокариот. Таким способом предлагается изучать филогенетические связи некультивируемых бактерий с другими прокариотами. Амплифицированную ДНК можно использовать для создания зондов, специфичных к нуклеиновым кислотам неизвестных микроорганизмов, и таким образом оценивать разнообразие микробного сообщества, независимо от способности данных микроорганизмов расти в культуре. Этот же метод может быть использован для того, чтобы проследить судьбу некультивируемого организма при тех или иных способах изучения общей популяции, например в процессе получения накопительной культуры нового организма с неизвестными потребностями или при изменениях в популяциях некультивируемых бактерий, например активного ила, в результате стрессовых природных ситуаций.
Наряду с перспективностью методов молекулярных зондов для микробной экологии следует отметить и их ограничения. Эти методы позволяют установить присутствие определенного типа микроорганизмов и его принадлежность к той или иной ветви филогенетической системы, созданной на основе анализа последовательностей. Однако в большинстве случаев они не дают возможности определить экологическую нишу (тип метаболизма) некультивируемого организма, поскольку филогенетические группы не гомологичны метаболическим группам, даже на уровне мельчайших разветвлений системы. Кроме того, не все прокариоты одинаково доступны для применения молекулярных зондов. Некоторые бактерии, особенно обладающие толстыми клеточными стенками или окруженные капсулой либо слизью, остаются трудными объектами для экстракции ДНК или гибридизации РНК с зондами. Поскольку метод зондов к тому же селективен, определенные бактерии, возможно важные, при анализе популяций этим способом могут остаться незамеченными.
Заключение
Основным лимитирующим фактором в условиях природных экосистем для микроорганизмов является количество субстрата.
Механизмы устойчивости к голоданию включают увеличение числа высокоаффинных транспортных систем, увеличение клеточной поверхности, образование спор, уменьшение размеров клеток, адаптацию клеточного метаболизма путем синтеза индуцируемых голоданием белков и образование слизи.
Апробированные и разработанные простые модели искусственных экосистем (хемостаты) являются эффективным инструментом для изучения законов функционирования микробных популяций и их сообществ в природных экосистемах. При разработке подходов устойчивого развития биосферы экспериментальные и теоретические исследования позволяют выявить закономерности взаимодействия микробных популяций с остальными обитателями экосистем и найти подходы к управлению ими в моделях искусственных экосистем.
Однако все питательные среды и условия инкубации селективны для небольшой фракции общей бактериальной популяции, имеющейся в исследуемом образце; попытки составить менее специфические, более соответствующие природным условиям культуральные среды, позволяющие более точно оценивать разнообразие и численность микроорганизмов, пока не дали успеха.
Определение численности микроорганизмов в природных образцах можно осуществлять путем прямого подсчета под микроскопом флуоресцентно окрашенных клеток, радиоавтографии клеток, меченных 14С или 3Н, подсчета колоний, выросших на плотной питательной среде, определения роста в жидкой среде с учетом разведения, измерения общего содержания АТР, ДНК или более специфических клеточных компонентов, таких как жирные кислоты или хлорофилл, либо методами с применением флуоресцентно меченных антител. Все эти методы имеют свои ограничения.
Одиночные клетки или популяции микроорганизмов можно идентифицировать путем гибридизации с синтетическими рРНК-зондами или с рРНК-зондами, полученными на основе амплифицированной (методом ПЦР) ДНК. Эти методы можно применять в сочетании с оптическими для выявления в том числе некультивируемых микроорганизмов в природных образцах.
Список источников
культура субстрат хемостат микроорганизм
1. Современная микробиология: прокриоты: В 2-х томах: Т. 1,2. Пер. с англ. / Под ред. Й. Лендлегера, Г. Древса, Г. Шлегеля. - М.: Мир, 2005. - 496 с.: ил., 24 с.
2. http://zhurnal.ape.relarn.ru/articles/2006/062.pdf - Электронный научный журнал «Исследовано в России». Статья «Использование малых моделей искусственных экосистем для изучения взаимодействия ризобактерий с растением-хозяином и микроскопическими почвенными грибами».