Файл: Методические указания к лабораторным работам для студентов всех направлений.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 02.12.2023
Просмотров: 117
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Лабораторная работа № 1. Приготовление раствора и определение его концентрации
Лабораторная работа № 2. Исследование РЕакций в растворах электролитов
Лабораторная работа № 3. Исследование гидролиза солей
Лабораторная работа № 4. Исследование окислительно-восстановительных реакций
Лабораторная работа № 5. Исследование скорости химических реакций и химического равновесия
Лабораторная работа № 6. Исследование комплексных соединений
ионно-молекулярным уравнением (или, что то же самое, ионной формой уравнения). Ионно-молекулярные уравнения, в отличие от молекулярных, отображают сущность протекающей химической реакции, т. е. процессы, которые реально происходят в растворе.
Правила записи ионно-молекулярных уравнений. Общий принцип записи ионно-молекулярных уравнений состоит в том, что те вещества, которые находятся в растворе и при этом полностью (или почти полностью) диссоциированы на ионы, записывают в виде отдельных ионов; прочие же вещества – в виде молекул. Отсюда следует, что в диссоциированной форме (т. е. в виде отдельных ионов) следует записывать только такие хорошо растворимые вещества, которые в то же время являются сильными электролитами. Остальные вещества записывают в недиссоциированной (т. е. молекулярной) форме, а именно:
1) Соединения, обладающие низкой растворимостью;
2) Соединения, являющиеся слабыми электролитами. Эти соединения могут хорошо растворяться в воде, но большая часть их молекул будет находиться в недиссоциированном состоянии, а значит, и само вещество следует указывать в молекулярной форме;
3) Газообразные соединения типа CO2, NH3 и т. д., оксиды, кислотные остатки (например, SO42-).
4) Комплексные частицы (например, [HgI4]2-).
В лаборатории: песчаная баня − 1 шт. В штативе: хлорид железа (III), сульфат меди (II), сульфат никеля (II), нитрат свинца (II), иодид калия, хлорид бария, сульфат натрия, сульфат хрома (III), сульфат цинка, сульфат алюминия, хлорид аммония, карбонат натрия, сульфат магния, ацетат натрия, гидроксид аммония, гидроксид натрия, гидроксид калия, гидроксид аммония − растворы концентрацией 5 %; пробирки − 5 шг., стеклянные палочки для перемешивания.
В вытяжном шкафу: соляная кислота – раствор концентрацией 15 %; гидроксид натрия, гидроксид калия – 6 н. растворы; гидроксид аммония – концентрированный раствор; сульфид натрия – раствор концентрацией 5 %; силикат натрия – раствор концентрацией 5 %.
Опыт 1. Образование малорастворимых оснований. В одну пробирку налить 3−5 капель раствора соли железа (III), в другую – столько же раствора соли меди (II), в третью – раствора соли никеля (II). В каждую пробирку добавить по несколько капель раствора щелочи до выпадения осадков. Осадки сохранить до следующего опыта.
Являются ли эти гидроксиды сильными основаниями?
Опыт 2. Растворение малорастворимых оснований. К полученным в предыдущем опыте осадкам добавить по несколько капель раствора соляной кислоты концентрацией 15 % до их полного растворения.
Какое новое малодиссоциированное соединение образуется при растворении оснований в кислоте?
Опыт 3. Образование малорастворимых солей.
A. В две пробирки налить по 3−5 капель раствора нитрата свинца (II) и прибавить в одну пробирку несколько капель йодида калия, в другую – хлорида бария.
Что наблюдается в каждой пробирке?
Б. В одну пробирку налить 3−5 капель раствора сульфата натрия, в другую – столько же раствора сульфата хрома (III). В каждую пробирку добавить несколько капель раствора хлорида бария до выпадения осадков.
Какое вещество образуется в качестве осадка? Будет ли протекать аналогичная реакция хлорида бария, например, с сульфатом железа (III)?
Опыт 4. Изучение свойств амфотерных гидроксидов.
А. В две пробирки внести по 3 капли раствора соли цинка и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида цинка. Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного раствора едкого натра (из вытяжного шкафа).
Б. В две пробирки внести по 3 капли раствора соли алюминия и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида алюминия. Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного
раствора едкого натра (из вытяжного шкафа).
В. В две пробирки внести по 3 капли раствора соли хрома (III) и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида хрома (III). Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного раствора едкого натра (из вытяжного шкафа).
Опыт 5. Образование малодиссоциированных соединений. В пробирку внести 3−5 капель раствора хлорида аммония и добавить несколько капель раствора едкого натра. Обратите внимание на запах, объясните его появление на основе уравнения реакции.
Опыт 6. Образование комплексов. В пробирку налить 3−5 капель раствора сульфата меди (II), затем по каплям добавить разбавленный (из штатива с реактивами!) раствор аммиака до образования осадка сульфата гидроксомеди (II).
Добавить к осадку избыток концентрированного раствора аммиака (из вытяжного шкафа!). Обратить внимание на растворение осадка.
Какую окраску имеет образующийся растворимый амминокомплекс меди?
Опыт 7. Образование газов.
A. Налить в пробирку 3−5 капель раствора карбоната натрия и несколько капель серной кислоты. Что наблюдается?
Б. Налить в пробирку 3−5 капель раствора сульфида натрия и 1 каплю серной кислоты. Обратить внимание на запах выделяющегося газа.
Опыт 8. Характер диссоциации гидроксидов. Пронумеровать 5 пробирок и внести по 4−5 капель растворов: в первую пробирку соли магния, во вторую соли алюминия, в третью силиката натрия, в четвертую соли никеля, в пятую соли цинка. Прибавить в пробирки 1, 2, 4, 5 по несколько капель (до начала выпадения осадков гидроксидов) раствор щелочи, в пробирку 3 - раствор соляной кислоты. Определить химический характер гидроксидов. Для этого половину суспензии гидроксида магния отлить в чистую пробирку и прибавить к ней 4−5 капель раствора НС1, к оставшейся части в первой пробирке добавить дополнительно 6−8 капель раствора щелочи.
В обоих ли случаях растворился осадок? Кислотными, основными или амфотерными свойствами обладает Mg(OH)2? Аналогичным образом исследовать свойства гидроксидов алюминия, кремния, никеля (II) и цинка. В чем они растворяются? Каковы их химические свойства?
По каждому опыту записать используемые при проведении эксперимента реактивы и результаты проведения реакций: образование или растворение осадка, цвет образующегося осадка (раствора), выделение газа (и его запах), изменение цвета раствора и т.д.
1. Название работы.
2. Цель работы.
3. Уравнения реакций в молекулярной и ионной форме, результаты проведения реакций, ответы на вопросы.
1. Что называется процессом электролитической диссоциации?
2. Что такое степень диссоциации?
3. Как диссоциируют сильные электролиты?
4. Какие формы вещества содержатся в растворе слабого электролита?
5. Какие кислоты и основания относят к сильным электролитам?
6. Каковы основные правила написания молекулярно-ионных уравнений реакций в растворах электролитов?
7. Каковы условия протекания реакций в растворах электролитов?
8. Почему при составлении ионного уравнения осадки записывают в молекулярной форме?
9. Как диссоциируют комплексные соединения?
10. Что такое константа диссоциации?
Цель работы: ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза.
Гидролизом называют процесс химического взаимодействия солей с водой. Продуктами гидролиза являются малодиссоциированные соединения в растворе, иногда – осадки или газы. Соответственно соли, образованные сильной кислотой и сильным основанием, не гидролизуются. К ним относятся, например, хлориды, нитраты и сульфаты щелочных металлов, стронция и бария. Различают три типа гидролизующихся солей:
Гидролиз соли, образованной сильным основанием и слабой кислотой. Гидролизуется анион слабой кислоты: А + Н2О = НА + ОН, в растворе появляются ионы ОН, поэтому среда – щелочная, рН > 7. Например, Na2CO3 образован сильным основанием NaOH и слабой угольной кислотой H2CO3. Диссоциация карбоната натрия описывается уравнением:
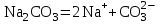 .
.
С водой взаимодействует карбонат-ион по реакции:
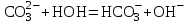 .
.
Распределяя катионы натрия по образующимся в ходе гидролиза анионам, получим молекулярное уравнение гидролиза:
Na2CO3 + H2O = NaHCO3 + NaOH.
Гидролиз соли, образованной слабым основанием и сильной кислотой. Гидролизуется катион слабого основания: М+ + Н2О МОН + Н+, в растворе появляются ионы Н+, поэтому среда кислая, рН < 7. Например, FeSO4 образован слабым основанием Fe(OH)2 и сильной кислотой H2SO4. Сульфат железа (II) диссоциирует по реакции:
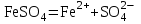 .
.
С водой реагирует остаток слабого основания – катион Fe2+:
Fe2+ + HOH FeOH+ + H+.
Так как в ходе гидролиза образуются ионы H+, то среда в растворе FeSO4 будет кислой.
Молекулярное уравнение гидролиза:
2FeSO4 + 2H2O = (FeOH)2SO4 + H2SO4.
Степень гидролиза солей этих двух групп невелика
Правила записи ионно-молекулярных уравнений. Общий принцип записи ионно-молекулярных уравнений состоит в том, что те вещества, которые находятся в растворе и при этом полностью (или почти полностью) диссоциированы на ионы, записывают в виде отдельных ионов; прочие же вещества – в виде молекул. Отсюда следует, что в диссоциированной форме (т. е. в виде отдельных ионов) следует записывать только такие хорошо растворимые вещества, которые в то же время являются сильными электролитами. Остальные вещества записывают в недиссоциированной (т. е. молекулярной) форме, а именно:
1) Соединения, обладающие низкой растворимостью;
2) Соединения, являющиеся слабыми электролитами. Эти соединения могут хорошо растворяться в воде, но большая часть их молекул будет находиться в недиссоциированном состоянии, а значит, и само вещество следует указывать в молекулярной форме;
3) Газообразные соединения типа CO2, NH3 и т. д., оксиды, кислотные остатки (например, SO42-).
4) Комплексные частицы (например, [HgI4]2-).
Оборудование и реактивы
В лаборатории: песчаная баня − 1 шт. В штативе: хлорид железа (III), сульфат меди (II), сульфат никеля (II), нитрат свинца (II), иодид калия, хлорид бария, сульфат натрия, сульфат хрома (III), сульфат цинка, сульфат алюминия, хлорид аммония, карбонат натрия, сульфат магния, ацетат натрия, гидроксид аммония, гидроксид натрия, гидроксид калия, гидроксид аммония − растворы концентрацией 5 %; пробирки − 5 шг., стеклянные палочки для перемешивания.
В вытяжном шкафу: соляная кислота – раствор концентрацией 15 %; гидроксид натрия, гидроксид калия – 6 н. растворы; гидроксид аммония – концентрированный раствор; сульфид натрия – раствор концентрацией 5 %; силикат натрия – раствор концентрацией 5 %.
Выполнение работы
Опыт 1. Образование малорастворимых оснований. В одну пробирку налить 3−5 капель раствора соли железа (III), в другую – столько же раствора соли меди (II), в третью – раствора соли никеля (II). В каждую пробирку добавить по несколько капель раствора щелочи до выпадения осадков. Осадки сохранить до следующего опыта.
Являются ли эти гидроксиды сильными основаниями?
Опыт 2. Растворение малорастворимых оснований. К полученным в предыдущем опыте осадкам добавить по несколько капель раствора соляной кислоты концентрацией 15 % до их полного растворения.
Какое новое малодиссоциированное соединение образуется при растворении оснований в кислоте?
Опыт 3. Образование малорастворимых солей.
A. В две пробирки налить по 3−5 капель раствора нитрата свинца (II) и прибавить в одну пробирку несколько капель йодида калия, в другую – хлорида бария.
Что наблюдается в каждой пробирке?
Б. В одну пробирку налить 3−5 капель раствора сульфата натрия, в другую – столько же раствора сульфата хрома (III). В каждую пробирку добавить несколько капель раствора хлорида бария до выпадения осадков.
Какое вещество образуется в качестве осадка? Будет ли протекать аналогичная реакция хлорида бария, например, с сульфатом железа (III)?
Опыт 4. Изучение свойств амфотерных гидроксидов.
А. В две пробирки внести по 3 капли раствора соли цинка и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида цинка. Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного раствора едкого натра (из вытяжного шкафа).
Б. В две пробирки внести по 3 капли раствора соли алюминия и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида алюминия. Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного
раствора едкого натра (из вытяжного шкафа).
В. В две пробирки внести по 3 капли раствора соли хрома (III) и несколько капель разбавленного раствора едкого натра (из штатива с реактивами) до образования осадка гидроксида хрома (III). Растворить полученные осадки: в одной пробирке – в растворе соляной кислоты, в другой – в избытке концентрированного раствора едкого натра (из вытяжного шкафа).
Опыт 5. Образование малодиссоциированных соединений. В пробирку внести 3−5 капель раствора хлорида аммония и добавить несколько капель раствора едкого натра. Обратите внимание на запах, объясните его появление на основе уравнения реакции.
Опыт 6. Образование комплексов. В пробирку налить 3−5 капель раствора сульфата меди (II), затем по каплям добавить разбавленный (из штатива с реактивами!) раствор аммиака до образования осадка сульфата гидроксомеди (II).
Добавить к осадку избыток концентрированного раствора аммиака (из вытяжного шкафа!). Обратить внимание на растворение осадка.
Какую окраску имеет образующийся растворимый амминокомплекс меди?
Опыт 7. Образование газов.
A. Налить в пробирку 3−5 капель раствора карбоната натрия и несколько капель серной кислоты. Что наблюдается?
Б. Налить в пробирку 3−5 капель раствора сульфида натрия и 1 каплю серной кислоты. Обратить внимание на запах выделяющегося газа.
Опыт 8. Характер диссоциации гидроксидов. Пронумеровать 5 пробирок и внести по 4−5 капель растворов: в первую пробирку соли магния, во вторую соли алюминия, в третью силиката натрия, в четвертую соли никеля, в пятую соли цинка. Прибавить в пробирки 1, 2, 4, 5 по несколько капель (до начала выпадения осадков гидроксидов) раствор щелочи, в пробирку 3 - раствор соляной кислоты. Определить химический характер гидроксидов. Для этого половину суспензии гидроксида магния отлить в чистую пробирку и прибавить к ней 4−5 капель раствора НС1, к оставшейся части в первой пробирке добавить дополнительно 6−8 капель раствора щелочи.
В обоих ли случаях растворился осадок? Кислотными, основными или амфотерными свойствами обладает Mg(OH)2? Аналогичным образом исследовать свойства гидроксидов алюминия, кремния, никеля (II) и цинка. В чем они растворяются? Каковы их химические свойства?
Содержание протокола лабораторной работы
По каждому опыту записать используемые при проведении эксперимента реактивы и результаты проведения реакций: образование или растворение осадка, цвет образующегося осадка (раствора), выделение газа (и его запах), изменение цвета раствора и т.д.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Уравнения реакций в молекулярной и ионной форме, результаты проведения реакций, ответы на вопросы.
Контрольные вопросы
1. Что называется процессом электролитической диссоциации?
2. Что такое степень диссоциации?
3. Как диссоциируют сильные электролиты?
4. Какие формы вещества содержатся в растворе слабого электролита?
5. Какие кислоты и основания относят к сильным электролитам?
6. Каковы основные правила написания молекулярно-ионных уравнений реакций в растворах электролитов?
7. Каковы условия протекания реакций в растворах электролитов?
8. Почему при составлении ионного уравнения осадки записывают в молекулярной форме?
9. Как диссоциируют комплексные соединения?
10. Что такое константа диссоциации?
Лабораторная работа № 3. Исследование гидролиза солей
Цель работы: ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза.
Общие сведения
Гидролизом называют процесс химического взаимодействия солей с водой. Продуктами гидролиза являются малодиссоциированные соединения в растворе, иногда – осадки или газы. Соответственно соли, образованные сильной кислотой и сильным основанием, не гидролизуются. К ним относятся, например, хлориды, нитраты и сульфаты щелочных металлов, стронция и бария. Различают три типа гидролизующихся солей:
Гидролиз соли, образованной сильным основанием и слабой кислотой. Гидролизуется анион слабой кислоты: А + Н2О = НА + ОН, в растворе появляются ионы ОН, поэтому среда – щелочная, рН > 7. Например, Na2CO3 образован сильным основанием NaOH и слабой угольной кислотой H2CO3. Диссоциация карбоната натрия описывается уравнением:
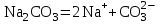 .
.С водой взаимодействует карбонат-ион по реакции:
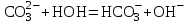 .
.Распределяя катионы натрия по образующимся в ходе гидролиза анионам, получим молекулярное уравнение гидролиза:
Na2CO3 + H2O = NaHCO3 + NaOH.
Гидролиз соли, образованной слабым основанием и сильной кислотой. Гидролизуется катион слабого основания: М+ + Н2О МОН + Н+, в растворе появляются ионы Н+, поэтому среда кислая, рН < 7. Например, FeSO4 образован слабым основанием Fe(OH)2 и сильной кислотой H2SO4. Сульфат железа (II) диссоциирует по реакции:
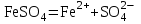 .
. С водой реагирует остаток слабого основания – катион Fe2+:
Fe2+ + HOH FeOH+ + H+.
Так как в ходе гидролиза образуются ионы H+, то среда в растворе FeSO4 будет кислой.
Молекулярное уравнение гидролиза:
2FeSO4 + 2H2O = (FeOH)2SO4 + H2SO4.
Степень гидролиза солей этих двух групп невелика