Файл: Химия нефти и газа л. 78 Методы разделения и концентрирования компонентов нефти.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 57
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Л. 8 Методы разделения и концентрирования компонентов нефти. Абсорбция, адсорбция и экстракция. Термодиффузия и диффузия через мембраны. Методы разделения нефти по группам веществ. Химические методы выделения веществ.
Явление диффузии и его использование в нефтяном анализе.
Диффузия – перенос вещества, как результат выравнивания его концентрации в первоначально неоднородных системах. Диффузия происходит вследствие теплового движения атомов и молекул. В результате диффузии происходит самопроизвольное взаимное проникновение друг в друга соприкасающихся веществ.
Мерой оценки величины (интенсивности) диффузии является диффузионный поток.
Количество вещества, переходящее в единицу времени через единицу площади поверхности, перпендикулярной направлению переноса, называется диффузионным потоком.
Если в системе имеется градиент концентрации некоторого вещества в направлении х
dc/dx ,
то диффузионный поток I определяется соотношением, называемым первым законом Фика:
I = -Ddc/dx ,
где D – коэффициент диффузии. Минус указывает на направление потока от больших концентраций к меньшим. Величина коэффициета D зависит от массы и размера диффундирующих молекул, от состава системы, от температуры и давления и практически не зависит от концентрации.
Если в системе происходит выравнивание концентраций n-компонентов, диффузионный поток каждого зависит от градиента концентраций всех остальных компонентов.
Наиболее интенсивна диффузия в газах (D
10-4 м2\с). В жидкостях D
10-9 м2\с, в твердых телах D
10-12 м2\с диффузия гораздо слабее.
Л. 8 Методы разделения и концентрирования компонентов нефти. Абсорбция, адсорбция и экстракция. Термодиффузия и диффузия через мембраны. Методы разделения нефти по группам веществ. Химические методы выделения веществ.
Явление диффузии и его использование в нефтяном анализе.
Диффузия – перенос вещества, как результат выравнивания его концентрации в первоначально неоднородных системах. Диффузия происходит вследствие теплового движения атомов и молекул. В результате диффузии происходит самопроизвольное взаимное проникновение друг в друга соприкасающихся веществ.
Мерой оценки величины (интенсивности) диффузии является диффузионный поток.
Количество вещества, переходящее в единицу времени через единицу площади поверхности, перпендикулярной направлению переноса, называется диффузионным потоком.
Если в системе имеется градиент концентрации некоторого вещества в направлении х
dc/dx ,
то диффузионный поток I определяется соотношением, называемым первым законом Фика:
I = -Ddc/dx ,
где D – коэффициент диффузии. Минус указывает на направление потока от больших концентраций к меньшим. Величина коэффициета D зависит от массы и размера диффундирующих молекул, от состава системы, от температуры и давления и практически не зависит от концентрации.
Если в системе происходит выравнивание концентраций n-компонентов, диффузионный поток каждого зависит от градиента концентраций всех остальных компонентов.
Наиболее интенсивна диффузия в газах (D
10-4 м2\с). В жидкостях D Явление диффузии эффективно используется при разделении компонентов нефти или газа.
Наиболее развита техника разделения диффузией через мембраны и термодиффузия.
Диффузия через мембраны.
Мембраны – непористые полимерные перегородки, через которые УВ способны диффундировать.
Разделение на мембранах основано на различии форм и размеров разделяющихся молекул, а также на их растворимости в материале мембраны.
Перенос вещества через непористые мембраны включает стадии сорбции, диффузии и десорбции с противоположной стороны мембраны.
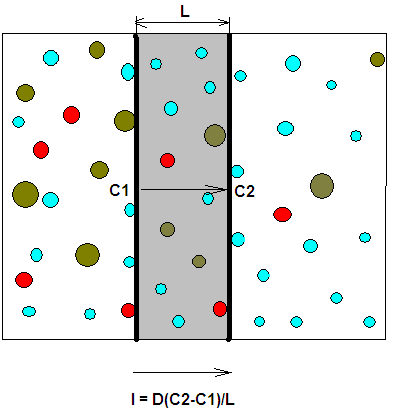
Скорость переноса определяется самой медленной стадией процесса – диффузией и выражается первым законом Фика (см рис.), где С1 и С2 – концентрации компонента на граничных поверхностях мембраны.
Обычно диффузией через мембраны разделяют газовые смеси. Для газовых смесей закон Фика принимает немного другую форму, так как для газов выполняется закон Генри С = σP :
I = Dσ(P2 – P1)/L, ,
где, σ – коэффициент растворимости газа в материале мембраны
Высокой проницаемостью через мембраны обладают молекулы с малым поперечным сечением и хорошо растворимые в материале мембраны.
Мембранные процессы применяют для:
- выделения водорода из водородсодержащих газов
- для удаления H2S, СО2 из горючих газов
Основное препятствие для широкого использования мембран – малый срок службы в агрессивных средах и низкая селективность процесса разделения. Имеющиеся на сегодня полимеры способны концентрировать вещества, но полного отделения пока не удается достичь. Перспективы в этой области зависят от синтеза полимеров для более высокоселективных и стабильных мембран.
Термодиффузия.
Явление термодиффузии было открыто Людвигом К. в 1856 г. и состоит в том, что если к смеси, состоящей из нескольких компонентов, приложить температурный градиент, возникает градиент концентраций.
Полноценной теории термодиффузионного процесса не существует. Эмпирически (из эксперимента) установлено, вблизи холодной стенки сосуда концентрируются: 1)углеводороды более высокомолекулярные и более высококипящие; 2) с наименьшим молярным объемом, то есть более компактные молекулы.
Термодиффузионный аппарат представляет собой два цилиндра, вставленных друг в друга с зазором между ними 0,25-3,0 мм. Разделяемая смесь помещается в пространство между цилиндрами, один из которых нагревают, другой – охлаждают.
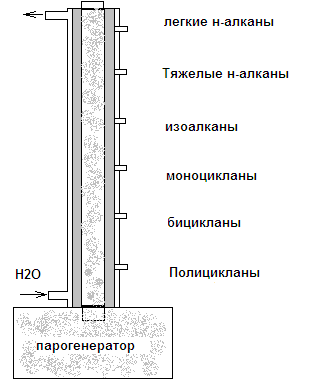
Молекулы одних веществ перемещаются к холодной стенке и в результате конвекции опускаются вниз, а молекулы других направляются к горячей стенке и концентрируются в верхней части колонки.
Термодиффузия не отделяет насыщенные УВ от ароматических, нет деления также по молекулярной массе. Основной фактор деления – это плотность молекул и молекулярный объем.
Существенное влияние на термодиффузионное разделение оказывает вязкость компонентов. Чем
менее вязкий образец, тем легче дифференцируются вещества, быстрее устанавливается равновесие.
На эффективность разделения влияют также 1. параметры процесса и 2. конструкция аппарата:
-
температурный градиент, длительность процесса, концентрация компонентов -
зазор, длина рабочего пространства
Раньше термодиффузионные планировалось использовать в промышленности для разделения алканов и циклоалканов, но из-за малой производительности колонн в настоящее время практически не используются.
В ИХН в Томске имеется и используется для исследовательских целей при изучении смолистых компонентов нефти и тяжелых углеводородов.
Сорбционные процессы разделения компонентов нефти.
Для разделения сложных смесей веществ по групповому признаку применяют ряд методов селективных к группам веществ, такие как экстракция и адсорбция.
Общим для этих методов является то, что используются селективные растворители или твердые вещества, у которых энергия взаимодействия с разделяемыми веществами различна.
Как происходит процесс сорбции в статических условиях?
Предположим, что в замкнутом сосуде находится некоторое количество сорбента и растворитель. Если внести в систему растворимый в растворителе сорбат, так чтобы концентрация была С0, то начнется уменьшение этой концентрации за счет поглощения сорбата из раствора сорбентом. Через некоторое время изменение концентрации прекратится и установится сорбционное равновесие концентрации сорбата в растворе С и концентрации его на сорбенте Сс. В области малых концентраций (абсолютные растворы) это соотношение имеет линейный вид и описывается законом Генри:
Сс = КС
Концентрации С и Сс при этом выражают в мг/см3 или мкмоль/см3. Тогда коэффициент Генри (коэффициент распределения) безразмерная величина и зависит от природы сорбента, сорбата, растворителя и температуры.
Закон Генри выполняется только для истинных растворов. При высоких концентрациях молекулы сорбата начинают взаимодействовать не только с растворителем и адсорбентом, но и друг с другом. И уравнение Сс = КС принимает нелинейную форму Сс = f(С), вид которой устанавливают из специальных экспериментов.
Процесс адсорбции – это всегда динамический процесс. Когда мы говорим, что установилось сорбционное равновесие
, это не значит, что часть молекул всегда находится в газовой или жидкой фазе, а часть в сорбированном состоянии. На деле между сорбированными и «свободными» молекулами все время происходит обмен. То есть молекулы часть времени ta находятся в сорбированном, а часть td – в свободном состоянии. Чем больше ta, тем сильнее сорбция. Отношение этих величин пропорционально концентрации сорбата в объеме системы:
ta/td = Масса сорбата на сорбенте в 1 см3 слоя\Масса сорбата в растворе в 1 см3 слоя
Здеси именно количество вещества в 1 см3 слоя, а не равновесные концентрации Сс и С.
Это отношение есть частный коэффициент Генри, который индивидуален для каждого вещества и позволяет оценить его сорбционную активность.
Сорбция – поглощение газов, паров или растворенных веществ твердыми или жидкими поглотителями. Поглощаемые вещества - сорбаты, а поглотители – сорбенты.
Если сорбат поглощается всем объемом сорбента, то процесс называется абсорбцией, а поглотитель – абсорбент. Если сорбат концентрируется на поверхности поглотителя, то процесс называется адсорбцией, а поглотитель – адсорбент.
Адсорбенты чаще всего твердые тела – силикагели, алюмогели, молекулярные сита (цеолиты), активные угли, пористые полимеры.
Абсорбенты – жидкости или газы.
Рассмотрим природу сорбционных сил.
Силы взаимодействия между сорбатом и сорбентом можно назвать физическими или ван-дер-ваальсовыми. Это те же силы, которые проявляются в жидкостях, удерживая их молекулы друг возле друга или в некоторых твердых, так называемых молекулярных кристаллах, например твердой углекислоте.
Силы взаимодействия в сорбции сводятся к:
- ориентационным
- индукционным
- дисперсионным и
- специфическим.
Ориентационное взаимодействие.
Атомы – электронейтральные частицы и не обладают дипольным моментом, так как центры их положительных и отрицательных зарядов совпадают. В некоторых молекулах, составленых из разных атомов всегда имеется постоянный дипольный момент, то есть центры их положительных и отрицательных зарядов смещены друг относительно друга, хотя в целом молекула электронейтральна. Такие молекулы называют полярными.
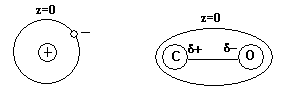
При растворении полярных сорбатов в полярных абсорбентах противоположно заряженные концы диполей ориентируются за счет электростатических сил друг относительно друга, что и является ориентационным взаимодействием.

Рассматривая ориетационное взаимодействие становится понятным классическое правило химии подобное растворяется в подобном.
Некоторые адсорбенты несут на поверхности локально сконцентрированный заряд. Взаимодействие такого локально сконцентрированного заряда с одним из концов диполя также приводит к ориентационному эффекту (см. рис.).
Индукционное взаимодействие.
Некоторые неполярные молекулы под влиянием дипольных моментов абсорбента или локальных зарядов адсорбента способны деформироваться с образованием наведенного дипольного момента. Взаимодействие наведенного диполя с полярной молекулой называют индукционным. Оно составляет 5-7 % от общей энергии взаимодействия и вносит определенный вклад в адсорбционное (хроматографическое) разделение.
Дисперсионное взаимодействие наиболее универсальное. Оно проявляется как между полярными так и неполярными молекулами.
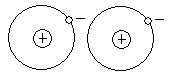
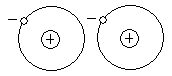
При вращении электрона вокруг атома, в в какойто момент времени положение электрона оказывается смещенным по отношению к протону и весь атом приобретает мгновенный дипольный момент. При сближении атомов возникает синхронизация в движении электронов и мгновенные диполи начинают взаимодействовать.
Дисперсионное взаимодействие является главным при растворении или адсорбции неполярных веществ на неполярных сорбентах (углеродные сорбенты).
Специфические взаимодействия.
К специфическим относят донорно-акцепторные (координационные) взаимодействия и как частный случай таких взаимодействий - водородную связь.
Такое взаимодействие возникает когда электронная пара с полностью заполненной орбитали атома-донора передается на вакантную орбиталь атома акцептора. При этом образуется общая связывающая молекулярная орбиталь.
Образующаяся координационная связь очень похожа на ковалентную, отличие только в том, что в ковалентная связь образуется из неспаренных электронов обоих атомов, а в координационной – электронная пара поставляется одним атомом – лигандом.
Например, если водород образует химическую связь с электроотрицательными атомами фтора, кислорода, азота, то электроны оттягиваются от водорода так сильно, что его орбитали практически пустеют