Файл: В настоящее время понятие "фуллерены" применяется к широкому классу многоатомных молекул углерода С, где.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 56
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, к которому подмешан металлический порошок или порошок окиси металла, внедряемого (интеркалируемого) в фуллерен. При этом в оптимальных условиях выход эндоэдралов не превышает нескольких процентов от выхода фуллеренов.
Другие оригинальные способы получения некоторых эндо- эдральных комплексов фуллеренов заключаются в том, что фул- лерит облучается или а-частицами с образованием в последующем комплексов типа Неп@Сбо, или бомбардируется из ионной пушки ионами Li+ с энергией около 30 эВ на ион с образованием соединений типа 1л@Сбо, 1л2@Сбо и 1л3@Сбо- Дело в том, что в центрах образующих фуллерен шестиугольников имеются отверстия, при прямом попадании в которые ионы лития с энергией не менее 5 эВ или а-частицы проникают внутрь сферы, захватывают (в случае а-частиц) два электрона и остаются внутри сферы.
Очень часто при традиционных синтезах эндоэдральных комплексов фуллеренов наблюдается выход комплексов не с одним, а с несколькими интеркалированными атомами, при этом одновременно растет в саже и доля высших фуллеренов. Так, при синтезе эндоэдральных комплексов со скандием получаются соединения Sc@C82, Sc2@C82, Sc3@C82, Sc2@Cs4, Sc2@C86. Встречаются также и эндоэдралы, включающие в свой состав и несколько атомов иттрия, формирующих оболочки в виде низших фуллеренов, которые включают в себя некоторые молекулы - СО, Н2 и др. Предполагается, что стабильность эндоэдральных комплексов растет с ростом размеров углеродной оболочки.
Для разделения и очистки эндоэдралов используют те же подходы, что и для разделения и очистки самих фуллеренов. Эти подходы, основанные на различной сорбционной активности различных фуллеренов и эндоэдралов в растворах по отношению к различным сорбентам, представляют собой разновидности жидкостной хроматографии.
Для реализации такого подхода необходимо, чтобы эндоэдрал, подлежащий выделению, обладал существенной растворимостью в тех растворителях, которые могут быть использованы в жидкостных хроматографах. Это позволяет выделить указанные вещества в чистом виде и исследовать их физико-химические свойства.
Другим вопросом, возникающим при исследовании эндоэдральных комплексов фуллеренов, является способ координации атомов внутри углеродной сферы.
В настоящее время уже известно достаточно большое количество эндоэдральных комплексов фуллеренов как с индивидуальными атомами
, так и с некоторыми молекулами. Несмотря на то, что на эти экзотические соединения в свое время было обращено пристальное внимание как экспериментаторов, так и теоретиков, пожалуй, самый интересный вопрос - способы координации атомов и молекул-гостей - в общем виде так и не был решен. Действительно, до настоящего времени были получены лишь единичные экспериментальные сведения о структуре твердых тел на основе эндоэдралов, как например структура Y@C6o, для которого известно, что атом иттрия жестко прилеплен изнутри к углеродной стенке, а сами эндоэдральные молекулы в молекулярном твердом теле координированы способом “голова к хвосту”.
Впрочем, в теоретическом плане способы координации атомов - гостей изучены немногим лучше. Так, известно, что некоторые атомы - к примеру Не, К+ и ряда тяжелых ионов и благородных газов должны координироваться в центре углеродной сферы, а некоторые другие атомы и ионы, к примеру Li+, Na+, смещены к оболочке. О конкретных способах координации большинства атомов вблизи стенки в настоящее время ничего не известно, хотя из самых общих положений ясно, что для одного атома-гостя их должно быть 5 (координация по центрам шестиугольника, пятиугольника, ребра шестиугольник-шестиугольник, ребра пятиугольник-шестиугольник и к вершине усеченного икосаэдра). Очевидно, что в случае наличия более одного атома- гостя способов координации их внутри углеродной сферы может быть еще больше.
Ионы лития в эндоэдральном комплексе 1л2@Сбо координируются к противоположным вершинам шестиугольников, лежащих друг против друга таким образом, что ось фрагмента 1л2 находится как раз посередине сферы (см. рис. 1.19, б), причем расстояние Li—Li - 0,99 нм, что хорошо совпадает с расстоянием С-С между противоположными углеродами из шестиугольников оснований, а расстояние Li-C (до углеродов, принадлежащих шестиугольникам) - 0,328 нм.
Во внутреннюю полость фуллерена можно поместить различные атомы и молекулы малых размеров, а снаружи возможны химические реакции присоединения других атомов. В настоящее время в полость фуллерена смогли ввести Са, Ва, Sr.
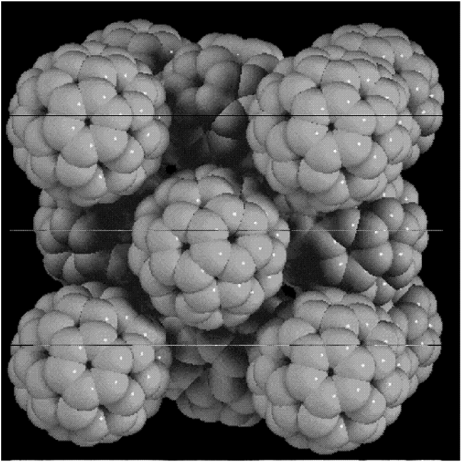
Молекулы Сбо при комнатной температуре конденсируются в структуру с плотной упаковкой, где каждая молекула имеет 12 ближайших соседей. Такие молекулярные кристаллы называют фуллеритами. Установлено, что фуллерит имеет высокую степень кристаллического порядка. При комнатной температуре фулле- рит, состоящий из кластеров Сбо, имеет структуру кубической гранецентрированной (ГЦК) плотной упаковки (рис. 1.20), а при температуре менее 261 К - простую кубическую. При фазовом переходе меняются тип решетки и характер вращательного движения молекул в ее узлах.
Расстояние между центрами ближайших молекул в гранецентрированной решетке, удерживаемых слабыми вандерваальсо- выми силами, составляет около 1 нм. Плотность данной формы углерода равна 1,69 г/см3. Благодаря высокой симметричности и замкнутости всех связей молекулы Сбо обладают высокой термической стабильностью (-1500 °С в инертной среде).
В плотно упакованной решетке ГЦК фуллерита Сбо на каждую молекулу приходится одна октаэдрическая пора радиусом 0,206 нм и две тетраэдрические радиусом 0,112 нм. В эти поры могут быть внедрены различные атомы и небольшие молекулы (рис. 1.21). Такие материалы называют интеркалированными фул- леренами. Если они передают свои валентные электроны молекулам Сбо, соединение называют фуллеридом, если нет - клатратом.
900 °С.
Под давлением были синтезированы образцы фуллеритов, объемно-прошитые ковалентными связями. Такие материалы могут царапать алмаз.
На рис. 1.22 приведена зависимость твердости фуллеритов, образованных при давлениях 9,5 ГПа и 13 ГПа и разных температурах синтеза.
С увеличением давления при синтезе фуллеритов до 13 ГПа получен быстрый рост плотности фуллеритов вплоть до 3,5 г/см3, что сопровождается ростом твердости до рекордного значения 300 ГПа, что в два раза превосходит твердость алмаза. Удельное сопротивление таких образцов при комнатной температуре также быстро возрастает до 106 Ом/см. Такие материалы с уникальными механическими свойствами уже нашли применение для изготовления инденторов в устройствах для измерения твердости и трибологических характеристик твердых материалов, включая наноструктурные пленки.
Как выяснилось несколько позже, существуют и природные фуллерены. В 1992 г они были обнаружены в природном углеродном минерале - шунгите. Свое название этот минерал получил от названия поселка Шуньга в Карелии. Правда, содержание фуллерена в шунгите очень незначительно, не превышает 0,001 %. Более того, в 1993 году в шунгитах было обнаружены и другие многоатомные молекулы и микрочастицы углерода - С70, "нанотрубы", "матрешки", "луковицы".
Важное значение, помимо фуллеренов, имеют близкие по механизму образования наноразмерные углеродные трубки (УНТ - рис. 1.23). В 1991 г. японский исследователь С. Иджима, рассматривая в электронном микроскопе сажу, полученную в результате распыления графита в плазме электрической дуги, обнаружил тонкие протяженные нити - цилиндрические структуры диаметром от одного до нескольких нанометров и длиной до нескольких микрометров. Они состояли из одного или нескольких свернутых в трубку гексагональных графитовых слоев, торцы которых закрывались полусферической головкой. Они были названы нанотрубками.
Нанотрубки можно рассматривать как частный случай наноматериалов, под которыми понимают объекты с размерами порядка КГ9 м хотя бы вдоль одной координаты. Диаметр нанотрубок отвечает этому требованию.
УНТ образуются в результате химических превращений углерода при высоких температурах. Можно выделить три основных способа их получения: электродуговое распыление графита, абляция графита с помощью лазерного или солнечного облучения и каталитическое разложение углеводородов. Обычно УНТ получают при конденсации углеродно-металлического пара путем каталитического пиролиза углеводородных композиций из СО, СН
Другие оригинальные способы получения некоторых эндо- эдральных комплексов фуллеренов заключаются в том, что фул- лерит облучается или а-частицами с образованием в последующем комплексов типа Неп@Сбо, или бомбардируется из ионной пушки ионами Li+ с энергией около 30 эВ на ион с образованием соединений типа 1л@Сбо, 1л2@Сбо и 1л3@Сбо- Дело в том, что в центрах образующих фуллерен шестиугольников имеются отверстия, при прямом попадании в которые ионы лития с энергией не менее 5 эВ или а-частицы проникают внутрь сферы, захватывают (в случае а-частиц) два электрона и остаются внутри сферы.
Очень часто при традиционных синтезах эндоэдральных комплексов фуллеренов наблюдается выход комплексов не с одним, а с несколькими интеркалированными атомами, при этом одновременно растет в саже и доля высших фуллеренов. Так, при синтезе эндоэдральных комплексов со скандием получаются соединения Sc@C82, Sc2@C82, Sc3@C82, Sc2@Cs4, Sc2@C86. Встречаются также и эндоэдралы, включающие в свой состав и несколько атомов иттрия, формирующих оболочки в виде низших фуллеренов, которые включают в себя некоторые молекулы - СО, Н2 и др. Предполагается, что стабильность эндоэдральных комплексов растет с ростом размеров углеродной оболочки.
Для разделения и очистки эндоэдралов используют те же подходы, что и для разделения и очистки самих фуллеренов. Эти подходы, основанные на различной сорбционной активности различных фуллеренов и эндоэдралов в растворах по отношению к различным сорбентам, представляют собой разновидности жидкостной хроматографии.
Для реализации такого подхода необходимо, чтобы эндоэдрал, подлежащий выделению, обладал существенной растворимостью в тех растворителях, которые могут быть использованы в жидкостных хроматографах. Это позволяет выделить указанные вещества в чистом виде и исследовать их физико-химические свойства.
Другим вопросом, возникающим при исследовании эндоэдральных комплексов фуллеренов, является способ координации атомов внутри углеродной сферы.
В настоящее время уже известно достаточно большое количество эндоэдральных комплексов фуллеренов как с индивидуальными атомами
, так и с некоторыми молекулами. Несмотря на то, что на эти экзотические соединения в свое время было обращено пристальное внимание как экспериментаторов, так и теоретиков, пожалуй, самый интересный вопрос - способы координации атомов и молекул-гостей - в общем виде так и не был решен. Действительно, до настоящего времени были получены лишь единичные экспериментальные сведения о структуре твердых тел на основе эндоэдралов, как например структура Y@C6o, для которого известно, что атом иттрия жестко прилеплен изнутри к углеродной стенке, а сами эндоэдральные молекулы в молекулярном твердом теле координированы способом “голова к хвосту”.
Впрочем, в теоретическом плане способы координации атомов - гостей изучены немногим лучше. Так, известно, что некоторые атомы - к примеру Не, К+ и ряда тяжелых ионов и благородных газов должны координироваться в центре углеродной сферы, а некоторые другие атомы и ионы, к примеру Li+, Na+, смещены к оболочке. О конкретных способах координации большинства атомов вблизи стенки в настоящее время ничего не известно, хотя из самых общих положений ясно, что для одного атома-гостя их должно быть 5 (координация по центрам шестиугольника, пятиугольника, ребра шестиугольник-шестиугольник, ребра пятиугольник-шестиугольник и к вершине усеченного икосаэдра). Очевидно, что в случае наличия более одного атома- гостя способов координации их внутри углеродной сферы может быть еще больше.
Ионы лития в эндоэдральном комплексе 1л2@Сбо координируются к противоположным вершинам шестиугольников, лежащих друг против друга таким образом, что ось фрагмента 1л2 находится как раз посередине сферы (см. рис. 1.19, б), причем расстояние Li—Li - 0,99 нм, что хорошо совпадает с расстоянием С-С между противоположными углеродами из шестиугольников оснований, а расстояние Li-C (до углеродов, принадлежащих шестиугольникам) - 0,328 нм.
Во внутреннюю полость фуллерена можно поместить различные атомы и молекулы малых размеров, а снаружи возможны химические реакции присоединения других атомов. В настоящее время в полость фуллерена смогли ввести Са, Ва, Sr.
Молекулы Сбо при комнатной температуре конденсируются в структуру с плотной упаковкой, где каждая молекула имеет 12 ближайших соседей. Такие молекулярные кристаллы называют фуллеритами. Установлено, что фуллерит имеет высокую степень кристаллического порядка. При комнатной температуре фулле- рит, состоящий из кластеров Сбо, имеет структуру кубической гранецентрированной (ГЦК) плотной упаковки (рис. 1.20), а при температуре менее 261 К - простую кубическую. При фазовом переходе меняются тип решетки и характер вращательного движения молекул в ее узлах.
Расстояние между центрами ближайших молекул в гранецентрированной решетке, удерживаемых слабыми вандерваальсо- выми силами, составляет около 1 нм. Плотность данной формы углерода равна 1,69 г/см3. Благодаря высокой симметричности и замкнутости всех связей молекулы Сбо обладают высокой термической стабильностью (-1500 °С в инертной среде).
В плотно упакованной решетке ГЦК фуллерита Сбо на каждую молекулу приходится одна октаэдрическая пора радиусом 0,206 нм и две тетраэдрические радиусом 0,112 нм. В эти поры могут быть внедрены различные атомы и небольшие молекулы (рис. 1.21). Такие материалы называют интеркалированными фул- леренами. Если они передают свои валентные электроны молекулам Сбо, соединение называют фуллеридом, если нет - клатратом.

Рис. 1.20. Структура кристалла фуллерита (ГЦК-решетка) 38
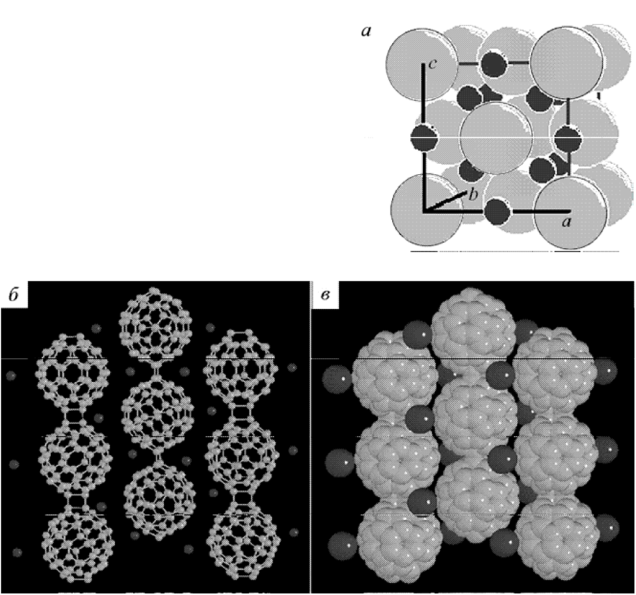
Рис. 1.21. Легированный фуллерит:
а - схема возможного заполнения октаэдрических и тетраэдрических меж-узлий в решетке фуллерена Сбо атомами металла; б - схема легирования фуллерита рубидием; в - структура интеркалированного рубидием фуллерита
Разработаны методы синтеза таких композиций, как металло- фуллереновые пленки (распыление в вакууме и электрохимическое осаждение), полимерфуллерены и эндофуллерены (фул- лереновые молекулы, содержащие в полости сферы один или несколько неуглеродных атомов). Эти композиции являются материалами с новыми свойствами, пригодными для использования в электронике, оптике, медицине, химической промышленности и др.
Чистый фуллерен при комнатной температуре является изолятором с величиной запрещенной зоны более 2 эВ или полупроводником с очень низкой проводимостью. Кристаллы Сбо, легированные атомами щелочных металлов, обладают металлической проводимостью и переходят в сверхпроводящее состояние в диапазоне температур 19-55 К. Соединения типа К3Сбо и Шэ3Сбо являются сверхпроводниками с достаточно высокими температурами сверхпроводящего перехода порядка 30 К и объемом сверхпроводящей фазы до 85 %. Такие температуры являлись рекордными для молекулярных сверхпроводников, пока в 1994 г не был обнаружен металлофуллерен Си„Сбо с температурой перехода около 120 К, т. е. выше температуры жидкого азота. В отличие от сложных оксидов меди - это изотропные сверхпроводники, т. е. параметры сверхпроводящего состояния оказываются одинаковыми по всем кристаллографическим направлениям, что является следствием высокой симметрии кубической кристаллической решетки фуллерена.
Существуют два основных подхода к объяснению организации сверхпроводящего состояния в металлофуллеренах.
Во-первых, традиционное для классических полупроводников электрон-фононное взаимодействие, приводящее к образованию куперовских электронных пар. При этом отмечается высокая температура Дебая (7Ъ = 1000 К) для внутримолекулярных колебательных мод, используя которую действительно нетрудно получить температуры фазового перехода порядка 30-40 К Однако, внутримолекулярные колебания могут связать электроны на молекуле Qo, поэтому остается неясным, как происходит транспорт куперовских пар, учитывая слабую межмолекулярную связь.
Во-вторых, электроны могут образовать куперовские пары за счет обменно-корреляционного взаимодействия, которое, скорее всего, ответственно за организацию сверхпроводящего состояния в сложных оксидах меди. Такой подход позволяет объяснить значительное увеличение температуры сверхпроводимости при замене щелочного металла медью. Следует признаться, что проблема теоретического описания сверхпроводимости металло- фуллеренов, как и "традиционных" высокотемпературных сверхпроводников на основе оксидов меди, в настоящее время далека от разрешения.
Фуллерен, внутри которого расположены атомы таких элементов, как тербий, гадолиний и диспрозий, обладает свойствами магнитного диполя, ориентацией которого можно управлять с помощью внешнего поля. В настоящее время в качестве накопителей информации используют магнитные диски, что дает возможность получить поверхностную плотность записи 107 бит/см2. Если же в качестве носителей информации использовать фулле- реновые магнитные диполи, расположенные на поверхности жесткого диска на расстоянии 5 нм друг от друга, то плотность записи достигнет фантастического значения - 4 • 1012 бит/см2.
Синтезированные из фуллеренов углеродные частицы имеют твердость около 40 ГПа и аномально высокую упругость, что обеспечивает очень перспективные свойства материалов: абразивный износ композита в 10 раз меньше, чем стали ШХ15, его коэффициент трения (-0,1) соответствует уровню алмазоподобных покрытий.
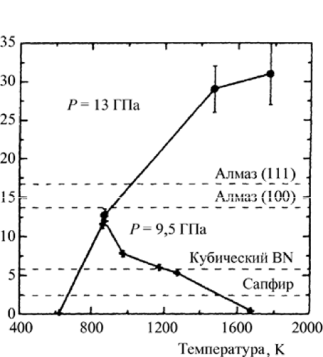
Рис. 1.22. Зависимость твердости фуллеритов от температуры синтеза при двух величинах давления. Пунктирные линии соответствуют твердости алмаза, нитрида бора и сапфира
Полученный композит имеет твердость HRC 62-65, предел прочности при сжатии 2500 МПа. Преимущества композита возрастают с повышением жесткости условий износа.
Превращение фуллере- на в алмаз происходит в более мягких условиях по сравнению с графитом. Это превращение при комнатной температуре реализуется уже при давлении 20 ПТа, в то время как для перевода графита в алмаз необходимо приложить давление 35-40 ГПа при температуре
900 °С.
Под давлением были синтезированы образцы фуллеритов, объемно-прошитые ковалентными связями. Такие материалы могут царапать алмаз.
На рис. 1.22 приведена зависимость твердости фуллеритов, образованных при давлениях 9,5 ГПа и 13 ГПа и разных температурах синтеза.
С увеличением давления при синтезе фуллеритов до 13 ГПа получен быстрый рост плотности фуллеритов вплоть до 3,5 г/см3, что сопровождается ростом твердости до рекордного значения 300 ГПа, что в два раза превосходит твердость алмаза. Удельное сопротивление таких образцов при комнатной температуре также быстро возрастает до 106 Ом/см. Такие материалы с уникальными механическими свойствами уже нашли применение для изготовления инденторов в устройствах для измерения твердости и трибологических характеристик твердых материалов, включая наноструктурные пленки.
Как выяснилось несколько позже, существуют и природные фуллерены. В 1992 г они были обнаружены в природном углеродном минерале - шунгите. Свое название этот минерал получил от названия поселка Шуньга в Карелии. Правда, содержание фуллерена в шунгите очень незначительно, не превышает 0,001 %. Более того, в 1993 году в шунгитах было обнаружены и другие многоатомные молекулы и микрочастицы углерода - С70, "нанотрубы", "матрешки", "луковицы".
Важное значение, помимо фуллеренов, имеют близкие по механизму образования наноразмерные углеродные трубки (УНТ - рис. 1.23). В 1991 г. японский исследователь С. Иджима, рассматривая в электронном микроскопе сажу, полученную в результате распыления графита в плазме электрической дуги, обнаружил тонкие протяженные нити - цилиндрические структуры диаметром от одного до нескольких нанометров и длиной до нескольких микрометров. Они состояли из одного или нескольких свернутых в трубку гексагональных графитовых слоев, торцы которых закрывались полусферической головкой. Они были названы нанотрубками.
Нанотрубки можно рассматривать как частный случай наноматериалов, под которыми понимают объекты с размерами порядка КГ9 м хотя бы вдоль одной координаты. Диаметр нанотрубок отвечает этому требованию.
УНТ образуются в результате химических превращений углерода при высоких температурах. Можно выделить три основных способа их получения: электродуговое распыление графита, абляция графита с помощью лазерного или солнечного облучения и каталитическое разложение углеводородов. Обычно УНТ получают при конденсации углеродно-металлического пара путем каталитического пиролиза углеводородных композиций из СО, СН