ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.12.2023
Просмотров: 79
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Эндоскопическое исследование с прицельной биопсией при раке толстой кишки позволяет не только существенно повысить процент выявления опухолей этой локализации (на 20–30 % по сравнению с данными ирригоскопии), но и установить гистологическое строение опухоли, что имеет значение для выбора объема оперативного вмешательства, а также определения прогноза заболевания.
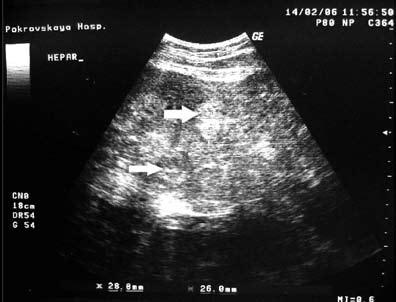
Рис. 3. УЗИ печени. Стрелками указаны участки метастатического поражения печени
Ультразвуковое исследование органов брюшной полости и забрюшинного пространства является обязательным при обследовании больного как с подозрением на рак ободочной кишки, так и с установленным диагнозом. Основной задачей УЗИ является выявление метастазов в паренхиматозные органы (печень, селезенку и др.), лимфатические узлы, а также диагностика сопутствующей патологии (желчнокаменная болезнь, патология гениталий и др.). Ранее считалось, что провести УЗИ органов, содержащих газ, нельзя, поскольку они полностью отражают ультразвуковые волны. В последнее время наблюдается значительный прогресс трансабдоминальной ультразвуковой диагностики заболеваний полых органов, в частности, толстой кишки.
В настоящее время существует две методики УЗИ ободочной кишки:
УЗИ через переднюю брюшную стенку:
• ободочной кишки без специальной подготовки;
• ободочной кишки с наполнением (ультразвуковая ирригоскопия).
Внутриполостное исследование толстой кишки с помощью ультразвукового колоноскопа.
При последнем исследовании при раке ободочной кишки выявляют локальный участок стенки кишки с неравномерным утолщением до 0,8–3,0 см.
Компьютерная томография (КТ) является важным современным методом первичного обследования больных раком ободочной кишки. При этом исследовании можно оценить местное распространение опухоли, в том числе прорастание ее в прилежащие к кишке органы, выявить наличие отдаленных метастазов (например, в печень) (рис. 185), вовлечение в опухолевый процесс лимфатических узлов. Для повышения чувствительности КТ используют дополнительное контрастирование, которое особенно эффективно при исследовании паренхиматозных органов. В спорных случаях (при неоднозначной трактовке очаговых изменений в печени) возможно выполнение пункционной биопсии органа под контролем УЗИ или КТ.
Виртуальная колоноскопия.
В последние годы для диагностики опухолей ободочной кишки применяют т. н. виртуальную колоноскопию. Метод представляет собой компьютерное томографическое исследование ободочной кишки после предварительного ее заполнения воздухом. Отличие получаемых результатов от классической КТ в том, что программное обеспечение на основании получаемых с датчиков данных строит трехмерную модель кишки, очень похожую на картину, видимую в обычный фиброколоноскоп (рис. 186). Данное исследование значительно легче переносится больными в сравнении с оптической фиброколоноскопией. Но диагностические возможности метода меньше, чем ФКС: полипы размером менее 1 см не видны.
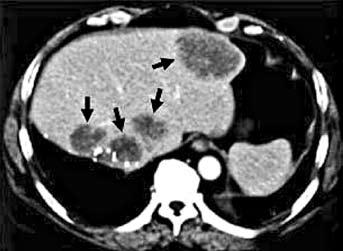
Рис. 4. КТ печени. Стрелками указаны участки метастатического поражения печени
В объем диагностических процедур, независимо от местного распространения опухоли, должна быть включена рентгенография органов грудной клетки, которая позволяет оценить состояние органов грудной полости, в том числе и с точки зрения их метастатического поражения.
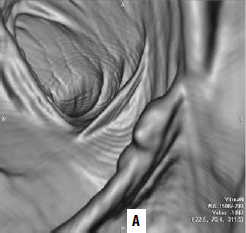
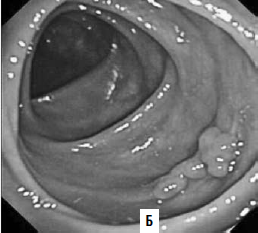
Рис. 5. А – виртуальная колоноскопия, Б – фиброколоноскопия
Дифференциальная диагностика
Выше были описаны несколько вариантов клинического течения рака ободочной кишки. При этом может возникнуть необходимость проведения дифференциальной диагностики с другими заболеваниями.
Энтероколитическая форма рака толстой кишки может протекать под видом хронической дизентерии (амебной и бациллярной), хронического колита и периколита, язвенного колита, полипоза толстой кишки и проявляться запорами, поносами, чередованием запоров и поносов, запоров и нормального стула, вздутием живота и урчанием кишечника, периодическими болями в животе, наличием патологических выделений из прямой кишки кровянистого, слизистого и гнойного характера.
Диспептическая форма – может протекать в начальных стадиях заболевания под видом хронического холецистита, заболеваний желудка, двенадцатиперстной кишки и поджелудочной железы. Среди начальных клинических проявлений диспептической формы рака появляются симптомы функциональных расстройств желудочнокишечного тракта: потеря аппетита, тошнота, отрыжка, неприятные ощущения во рту, периодические рвоты, наличие неопределенных болей в животе, чаще с локализацией в эпигастральной области или в правой половине живота.
Явления хронической непроходимости кишечника при обтурационной форме рака, особенно на ранних стадиях заболевания, дают клиническую картину, сходную с приступами хронической спаечной непроходимости. В дифференциальной диагностике имеют значение указания на ранее перенесенные оперативные вмешательства, ранения живота и воспалительные процессы в брюшной полости. Кроме того, при обтурационной форме рака продолжительность и частота приступов хронической непроходимости постепенно нарастают, вплоть до развития полной непроходимости, а для спаечной болезни более характерны не нарастающие приступы частичной кишечной непроходимо сти.
Псевдовоспалительная форма рака толстой кишки может протекать с клинической картиной острого аппендицита в стадии аппендикулярного инфильтрата или ограниченного абсцесса, острого воспалительного процесса в забрюшинном пространстве и брюшной стенке (псоит, паранефрит, абсцесс или флегмона брюшной стенки).
Рак слепой кишки, осложнившийся воспалительным процессом, клинически может протекать под видом аппендикулярного инфильтрата. Острый аппендицит в стадии инфильтрата имеет соответствующую клиническую картину и появляется вслед за острым приступом аппендицита. Под воздействием лечения такие инфильтраты довольно быстро рассасываются и полностью исчезают. Поэтому перед началом лечения аппендикулярного инфильтрата необходимо выполнить ирригоскопию.
Токсикоанемическую клиническую форму рака толстой кишки в начальных стадиях часто принимают за болезни крови, хронический сепсис, эндокардит, ревматизм, бруцеллез, хронический тонзиллит и другие заболевания.
Таким образом, соблюдение диагностического комплекса мероприятий, включающего рентгенологические и эндоскопические методы исследования с морфологической идентификацией опухоли, позволит врачу установить точный диагноз рака ободочной кишки.
Лечение
Основным методом лечения рака ободочной кишки является хирургический. Выбор метода оперативного вмешательства зависит от локализации опухоли и наличия осложнений.
Хирургическое лечение включает в себя:
Радикальные операции:
• Одномоментные: правосторонняя гемиколэктомия, резекция поперечной ободочной кишки, левосторонняя гемиколэктомия, резекция сигмовидной кишки, субтотальная и тотальная колэктомия.
• Двухэтапные: операция Гартмана – резекция ободочной кишки с опухолью и формирование одноствольной колостомы (первый этап), устранение колостомы с восстановлением непрерывности ободочной кишки путем формирования анастомоза (второй этап – выполняется через 5–6 месяцев с момента первого этапа).
• Трехэтапные операции: операция Цейдлера-Шлоффера (формирование колостомы (первый этап), резекция ободочной кишки с опухолью (второй этап), закрытие колостомы (третий этап).
• Комбинированные операции с резекцией смежных органов и окружающих тканей при местнораспространенных формах рака ободочной кишки.
Радикальное оперативное лечение рака ободочной кишки обязательно включает в себя вмешательство на лимфатических путях. Объем резекции зависит от расположения опухоли и путей ее регионарного метастазирования. При этом необходимо удалить определенную часть толстой кишки в одном блоке с околокишечной клетчаткой и зоной возможного регионарного метастазирования – лимфатическими узлами, расположенными вдоль кровеносных сосудов.
По топографии лимфометастазов рака слепой и восходящей ободочной кишки для радикального удаления зон регионарного метастазирования необходима правосторонняя гемиколэктомия с резекцией 25–30 см тонкой кишки, перевязкой и пересечением основных стволов a. Ileocolica и a. colica dextra. Одним блоком с кишкой удаляется забрюшинная клетчатка с лимфатическими узлами. При раке печеночного изгиба и проксимальной трети поперечной ободочной кишки удалению подлежит лимфоколлектор по ходу a. colica media. Операция заканчивается формированием илеотрансверзоанастомоза (анастомоза между подвздошной и поперечной ободочной кишкой).
Левосторонняя гемиколэктомия выполняется при локализации опухоли в селезеночном изгибе, в нисходящем отделе и проксимальной части сигмовидной кишки. Пересекается a. mesenterica inferior непосредственно у места ее отхождения от абдоминальной аорты. Одновременно удаляется забрюшинная клетчатка с лимфатическими узлами. Операция заканчивается формированием трансверзо сигмоидного анастомоза (анастомоза между поперечной ободочной и сигмовидной кишкой).
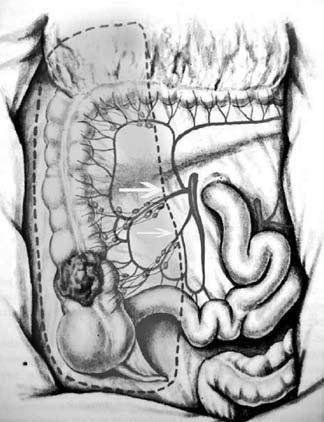
Рис. 6. Объем операции при раке слепой и восходящей ободочной кишки. Стрелками показаны лигируемые основные сосуды
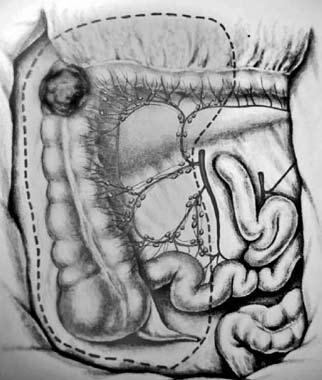
Рис. 7. Объем операции при раке печеночного изгиба ободочной кишки
Сегментарная резекция выполняется при опухолях средней трети поперечной ободочной кишки и сигмовидной кишки. Вместе с участком кишки производится клиновидное иссечение брыжейки (рис. 190). Колэктомия показана в случаях возникновения рака на фоне тотального полипоза или неспецифического язвенного колита, либо при первичномножественной локализации рака (в двух и более участках толстой кишки). При этом операция завершается формированием илеоректального анастомоза и прямой кишкой) либо формированием илеостомы.
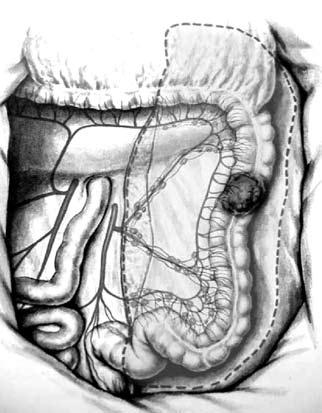
Рис. 8. Левосторонняя гемиколэктомия (анастомоза между подвздошной
Выбор хирургической тактики у больных с осложнениями рака ободочной кишки необходимо проводить в зависимости от вида осложнений, степени запущенности опухолевого процесса и тяжести общего состояния пациентов
.
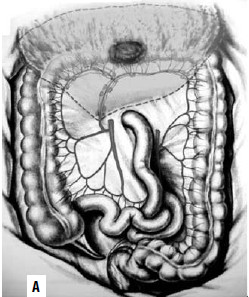
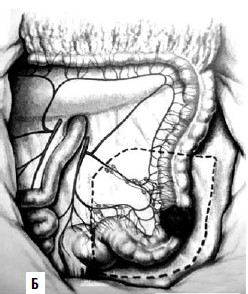
Рис. 9. А – резекция поперечной ободочной кишки; Б – резекция сигмовидной кишки
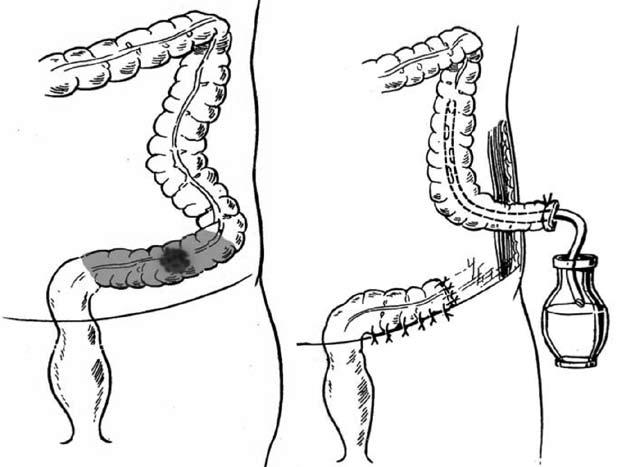
Рис. 10. Операция Гартмана
При выраженных явлениях кишечной непроходимости с левосторонней локализацией опухоли и тяжелом общем состоянии больного необходимо выполнять радикальные многоэтапные хирургические вмешательства. Чаще всего операцией выбора является операция Гартмана. В связи с тем, что кишка при выполнении оперативного вмешательства не подготовлена, заполнена каловыми массами и газом, а также имеются выраженные нарушения микроциркуляции стенки кишки, воспалительный процесс, существует большой риск развития несостоятельности толстотолстокишечного анастомоза. Учитывая данное обстоятельство анастомоз не формируется, а накладывается одноствольная колостома, которая может быть устранена с восстановлением непрерывности толстой кишки вторым этапом, через 5–6 месяцев после первого оперативного вмешательства. При нерезектабельности опухоли принято выполнять паллиативные операции:
• формирование обходного анастомоза;
• формирование кишечной стомы – илеостома, цекостома, трансверзостома, сигмостома.
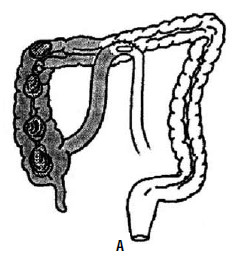
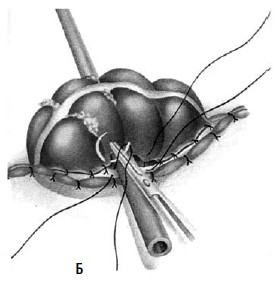
Рис. 11. А – нерезектабельный рак слепой кишки, сформирован обходной илеотрансверзоанастомоз; Б – двуствольная сигмостома
Противоопухолевая химиотерапия
Противоопухолевые препараты могут дополнять оперативное лечение после выполненных операций, независимо от стадии рака (адъювантная химиотерапия). Они могут применяться и самостоятельно при неоперабельных опухолях. Ведущим препаратом для химиотерапии уже более 40 лет является представитель фторпиримидинов – 5-фторурацил (5ФУ). Он используется либо в виде монотерапии или в сочетании с другими цитостатиками или биомодуляторами.