ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.03.2024
Просмотров: 159
Скачиваний: 0
СОДЕРЖАНИЕ
Міністерство аграрної політики україни
Лабораторна робота № 1 макроаналіз металів і сплавів
Контрольні питання для самопідготовки
Лабораторна робота № 2 мікроаналіз металів і сплавів
Установка для термічного аналізу
Контрольні питання для самопідготовки
Лабораторна робота № 4 аналіз діаграм стану подвійних систем
Контрольні питання для самопідготовки
Лабораторна робота № 5 діаграма стану сплавів системи залізо - вуглець
Контрольні питання для самопідготовки
Лабораторна робота № 6 вивчення мікроструктур вуглецевих сталей у рівноважному стані
Контрольні питання для самопідготовки
Лабораторна робота № 8 термічна обробка сталей
Контрольні питання для самопідготовки
Лабораторна робота № 9 термічна обробка алюмінієвих сплавів
Аналіз кривих охолодження
На рис. 3.2 зображені криві охолодження для чистих металів (Pb, Sb) I, V та їх сплавів II, III, IV.
Для аналізу кривих охолодження застосовують правило фаз (закон Гіббса), яке виражається формулою
С = К- Ф + 1,
де: С - число ступенів вільності, тобто число зовнішніх факторів (температура, концентрація), які можна змінювати без зміни числа фаз в сплаві; К - число компонентів ( в сплавах свинець - сурма К = 2 , це свинець і сурма); Ф - число фаз.
Температура плавлення чистого свинцю - 327°С, сурми - 630 °С.
Доевтектичному сплаву (6% Sb, 94% Pb) відповідає крива II.Вище точки 1 сплав знаходиться в рідкому стані і має одну фазу, тоді С = 2-1+1=2. При двох ступенях вільності в цій області можна змінювати концентрацію та температуру, а сплав залишиться однорідним - рідким. Крива охолодження круто падає вниз.
Точка 1 - початок кристалізації, точка 2 - кінець кристалізації. В інтервалі температур від точки 1 до точки 2 проходить .утворення кристалів свинцю, на цій ділянці сплав являє собою суміш рідини і кристалів свинцю. Тобто між точками 1 і 2 існує дві фази - рідка і тверда: С = 2-2+1=1. При одному ступені вільності незалежною змінною являється тільки температура. З пониженням температури сплаву кристалів утворюється більше, рідини залишається менше.
На ділянці 2-2´ залишки рідини .кристалізуються в механічну суміш свинцю та сурми - евтектику, де матимемо три фази (кристали свинцю, кристали сурми і рідкий сплав). Число ступенів вільності С = 2-3+1=0. При цьому виділяється велика кількість теплоти і температура залишається постійною.
Нижче точки 2 сплав знаходиться повністю в твердому стані і його структура складається з кристалів свинцю та евтектики (дрібнодисперсної суміші кристалів свинцю та сурми). Таким чином, сплав в даній області складається з двох фаз - кристалів свинцю і сурми: С=2-2+1=1.
Крива IIIохолодження евтектичного сплаву ( 13% Sb, 87%Pb). Евтектичний сплав має криву охолодження аналогічну кривій чистого металу, тільки із більш швидким охолодженням розчину. Кристалізація протікає при сталій температурі і концентрації (в точці С). Утворюється механічна суміш компонентів (свинцю та сурми).
Заевтектичному сплаву відповідає крива IV. Точка 1 відповідає початку кристалізації, 2 - кінцю кристалізації. В інтервалі температур від т.1 до т.2 проходить утворення кристалів сурми. На цій ділянці сплав являє собою суміш рідини та кристалів сурми. З пониженням температури сплаву кристалів утворюється більше, рідини залишається менше. На ділянці 2-2´ залишок рідини кристалізується в механічну суміш кристалів свинцю та сурми (евтектику).
Схеми мікроструктури сплавів після охолодження показані на рис.3.3.
Схеми мікроструктури: а – чистий свинець, б - доевтектичний сплав, в – евтектичний слав, г - заевтектичний сплав..
Аналіз мікроструктури показує, що в залежності від концентрації компонентів змінюється мікроструктура сплаву.
Діаграма стану дає можливість визначити стан сплаву при будь-якій температурі та заданій концентрації.
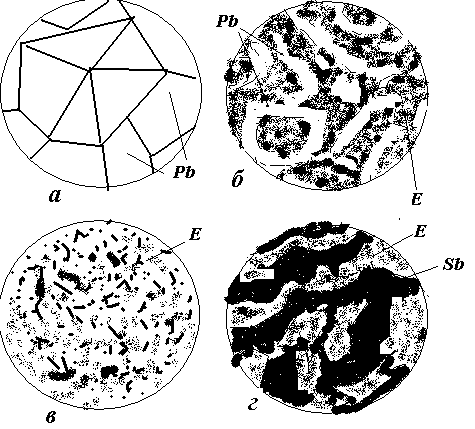
Рис. 3.3 Структура сплавів
свинець – сурма:
а – чистий свинець;
б – доевтектичний сплав;
в – евтектичний сплав;
г – заевтектичний сплав
Установка для термічного аналізу
Установка для термічного аналізу (рис. 3.4) складається з нагрівальної та контролюючої апаратури.
Навіски 3 в тиглях з заданою концентрацією компонентів (Pb, Sb) доводять до повного розплавлення з перегрівом на 20...30° С в муфелі електропечі 1. Контроль температури здійснюється хромель-алюмелевою (ХА) термопарою 4, підключеною до потенціометра 5. Після того, як температура буде достатньою для термічного аналізу, тигель з навіскою установлюють на вогнетривку підставку. Холодні кінці термопари з'єднані з клемами вимірювального приладу 5 - мілівольтметра ВЗ-36. Для знаходження відповідності показань
мілівольтметра (мВ) значенням температури сплаву (°С) проводять тарування термопари. Дані заносяться в таблицю .
Слід відзначити, що отриманими даними (табл.) можна користуватися тільки для даної термопари. Це і є таруванням термопари. Отримані дані мілівольтметра (mВ) під час досліду згідно з таблицею переводять в відповідні значення температур (°С).
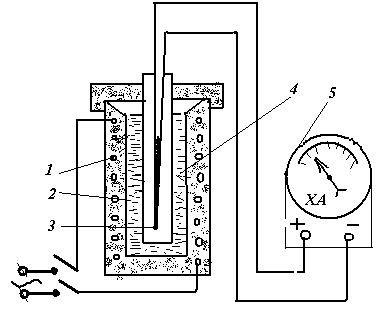
Рис.3.4 Схема установки для визначення критичних точок металів і сплавів:
1 – електропіч; 2 – тигель; 3 – термопара;
4 - розплавлений метал (сплав); 5 – гальванометр.
Порядок виконання роботи
Тиглі з чистими свинцем, сурмою та трьома сплавами: доевтектичним (6% сурми), евтектичним (13% сурми) та заевтектичним (55% сурми) нагрівати в електричній печі. Температуру заміряти гальванометром термопари.
Виймати і охолоджувати тиглі потрібно в такій послідовності: евтектичний сплав – при досягненні температури 260…270оС, доевтектичний сплав відповідно 290…300оС, чистй свинець – 340…350оС, заевтектичний сплав – 475…480оС, чиста сурма – 645…650оС фіксуючи показання гальванометра через 10…15 с до закінчення затвердівання металу (сплаву). Результати замірів внести в таблицю
|
τ, с |
|
|
|
|
|
|
|
mВ |
|
|
|
|
|
|
|
T oС |
|
|
|
|
|
|
3. За результатами дослідів побудувати на міліметровому папері криві охолодження кожного металу (сплаву). При цьому зручно брати масштаб 10 с = 1 мм і 10о = 1 мм.
4. За кривими охолодження побудувати діаграму стану сплавів свинець – сурма, переносячи критичні точки з кривих охолодження на діаграму стану.
Зміст звіту
В звіті необхідно вказати призначення термічного аналізу, схему установки для дослідження металів і сплавів термічним методом, таблицю з дослідними даними, криві охолодження і діаграму стану, висновки про роботу, в яких зробити аналіз перетворень при охолодженні одного із сплавів із застосуванням правила фаз.
Контрольні питання для самопідготовки
Що являє собою діаграма стану сплавів?
Які методи застосовують для побудови діаграм стану сплавів?
Які точки на кривих нагрівання чи охолодження називають критичними?
Поясніть значення термінів: евтектика, солідус, ліквідус.
Покажіть на діаграмі стану сплавів ці лінії та точки.
Чим пояснюється зміна швидкості охолодження сплаву?
Який з досліджених сплавів є евтектичним? доевтектичним? заевтектичним?.
Лабораторна робота № 4 аналіз діаграм стану подвійних систем
Мета роботи : навчитися робити аналіз діаграм стану різних типів, визначати наявність фаз та структур у сплавах різного хімічного складу при різних температурах; навчитись визначати кількість фаз або структурних складових в сплавах; навчитися визначати перетворення в сплавах.
Матеріали та обладнання. Для виконання даної лабораторної роботи студентам видаються рисунки діаграм стану систем різних типів з описанням механізму формування структур типових сплавів в цих системах.
Теоретичні відомості. Більшість металевих матеріалів, які використовуються в машинобудуванні – сплави, що складаються з двох, трьох або більшої кількості елементів. Основним елементом сплаву зазвичай є метал, який і визначає назву сплавів (сплави на основі заліза, міді, алюмінію тощо). Інші компоненти сплавів можуть бути як металами, так і неметалами. Їх додають до основного компоненту умисне для зміни структури та властивостей сплаву у бажаному напрямі.
Будь-який сплав складається з однієї або декількох фаз. Ними можуть бути: 1) чисті компоненти; 2) тверді розчини; 3) хімічні сполуки. Знання фазового складу є дуже важливим при дослідженні сплавів, але не достатнім для визначення їх властивостей. Більше інформації містить у собі структурний склад сплаву, тобто наявність у ньому певних структурних складових – окремих елементів мікроструктури, які відрізняються від інших. Кількість структурних складових металевої системи часто переважає кількість фаз, оскільки містить усі фази цієї системи, а також їхні суміші, що кристалізуються водночас і разом (евтектика, евтектоїд). Тому на діаграмах стану наводять не тільки фазовий, а і структурний склад для кожної їх області.
Діаграми стану, або діаграми фазової рівноваги у зручній графічній формі показують фазовий і структурний склад сплавів в залежності від температури та концентрації. Діаграми стану будують для умов рівноваги, які досягаються тільки при дуже малих швидкостях охолодження або тривалому нагріванні. Справжній рівноважний стан в практичних умовах досягається рідко. В більшості випадків сплави знаходяться в метастабільному стані, тобто такому, коли вони мають обмежену стійкість і під впливом зовнішніх факторів набувають інших більш стійких станів. В багатьох випадках метастабільні стани надають сплавам високих механічних або інших властивостей. Завданням металознавства є встановлення природи метастабільних станів, які забезпечували б оптимальний комплекс властивостей і розроблення режимів термічної або іншої обробки сплавів, що дозволяли б отримувати ці неврівноважені стани. Вихідним положенням при вирішуванні таких питань є знання діаграм стану. Саме діаграми стану дозволяють розробити раціональні режими різних видів обробки матеріалів і реалізувати їх на практиці. З іншого боку, вони дають можливість наукового прогнозу створення матеріалів з потрібними властивостями.