Файл: Лабораторная работа 10 изучение скорости инверсии тростникового сахара.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 01.12.2023
Просмотров: 121
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
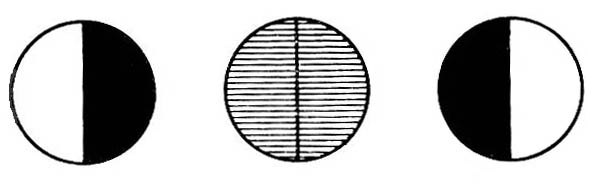
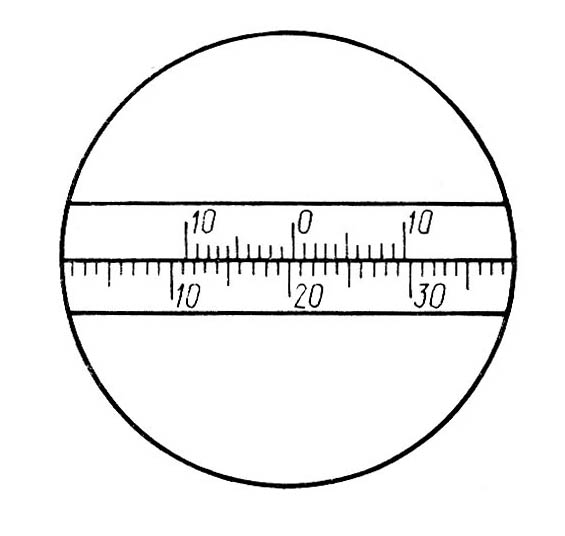
а б в г
Рис.3. Поле зрения в окуляре полутеневого поляриметра (а, б, в);
г - отсчет по шкале поляриметра
Для получения параллельных пучков светового потока в приборе имеется система линз. Источником светового потока служит электрическая лампа. В белом световом потоке определению равной освещенности полей мешает разноцветность (вращательная дисперсия). Поэтому пользуются примерно монохроматическим световым потоком, употребляя светофильтр. Угол поворота анализатора отсчитывается по шкале (лимбу), движущейся при его вращении и неподвижному нониусу с точностью до десятых долей градуса. Отсчеты производятся следующим образом. Число целых градусов определяют по последнему делению шкалы, которое оказывается слева от нуля (центральной метки) нониуса; десятые доли градуса определяют на правой части шкалы нониуса по делению, совпадающему в данном положении с каким-либо делением основной шкалы лимба. Так отсчитывают положительные углы вращения. Например, на рис. 3(г) угол вращения соответствует 20,3°. При вращении анализатора в противоположную сторону отсчитывают отрицательные углы вращения. Десятые доли градуса определяются по делениям в левой части шкалы нониуса. Для удобства наблюдений и измерений, связанных с освещенностью, поляриметр закрывают черным чехлом.
Последовательность выполнения работы1.
Приготовить 50 мл раствора тростникового сахара (концентрация указывается преподавателем), для этого отвесить на техниче-
Количественной характеристикой скорости реакции первого порядка кроме константы скорости могут служить период полупревращения (полураспада) 1/2, а также среднее время жизни частицы. . Среднее время жизни определяется как время, необходимое для того, чтобы концентрация исходного вещества уменьшилась в е раз. Выражение (5) можно представить в экспоненциальной форме
,
откуда следует, что (а—х) достигает а/е в момент времени =1/k, т. е. среднее время жизни одной исходной молекулы (частицы) равно обратной величине константы скорости реакции.
Как 1/2 реакций первого порядка, так и непосредственно связаны с константами скоростей и не зависят от начальной концентрации вещества.
режима. Наиболее часто встречающиеся виды гомогенного катализа.
Практическая часть
Изучение скорости инверсии тростникового сахара
Процесс инверсии сахара является гидролитическим расщеплением сахарозы С12Н22О11 на глюкозу (декстрин) и фруктозу (левулеза) по уравнению:
С12Н22О11 + Н2О С6Н12О6 + С6Н12О6
фруктоза глюкоза
Эта реакция бимолекулярна, однако, в большом избытке воды (слишком велика разница в молекулярных массах компонентов) она протекает по первому порядку:
Скорость инверсии сахара в нейтральной среде очень мала. Присутствие ионов водорода как катализатора ускоряет реакцию и делает ее доступной для наблюдения, причем скорость инверсии пропорциональна концентрации ионов водорода в растворе.
Тростниковый сахар и продукты его разложения принадлежат к числу оптически активных веществ, т. е. веществ, способных изменять положение плоскости поляризации проходящего через них поляризованного светового потока (светового потока, в котором колебания происходят в определенной плоскости). Оптическая активность таких веществ связана с наличием в их молекулах асимметричных атомов углерода. Угол поворота плоскости колебаний поляризованного луча называется углом вращения плоскости поляризации и обозначается . Его величина прямо пропорциональна толщине слоя d и концентрации активного вещества С:
где а – коэффициент пропорциональности (постоянная поляризации или удельное вращение), который зависит от природы вещества, длины волны, температуры и природы растворителя. Для гомогенных оптически активных жидкостей концентрация в уравнении (6) заменяется на плотность. Вращательная способность приблизительно обратно пропорциональна квадрату длины волны (вращательная дисперсия), а с температурой изменяется незначительно.
Удельное вращение равно углу вращения (в градусах) в слое раствора толщиной 1 дм, содержащего 1 г вещества в 1 мл при 20°С, при определенной длине волны (например, при длине волны желтой линии спектра паров натрия 589,6 нм). Зная угол вращения, удельное вращение (см. справочник) и толщину слоя раствора, легко вычислить его концентрацию.
Скорость инверсии тростникового сахара удобно изучать по измерению меняющегося со временем угла вращения плоскости поляризации исследуемого раствора. Тростниковый сахар вращает плоскость поляризации вправо ( = 66,55°), а смесь продуктов инверсии - влево, так как глюкоза вращает вправо (г = 52,5°), a фруктоза - влево (ф = 91,9°). Поэтому по мере протекания реакции угол вращения плоскости поляризации уменьшается, падает до нуля и затем становится отрицательным (инверсия вращения). Окончанию реакции соответствует предельное, не изменяющееся отрицательное значение угла вращения .
Для измерения угла вращения плоскости поляризации используются специальные оптические приборы поляриметры. Чаще всего применяются так называемые полутеневые поляриметры (рис. 2).
Поляризатор 3 состоит из двух призм Николя (при другой конструкции их может быть и три), причем меньшая по размерам призма прикрывает половину поля зрения. Плоскости поляризации этих призм находятся под некоторым углом друг к другу, поэтому поле зрения, рассматриваемое в окуляр 7, разделено на две части, отличающиеся по цвету и яркости освещения. Поляризатор неподвижен. Анализатор 8 (также призмы Николя) может вращаться вокруг оптической оси прибора. Вращением анализатора вокруг оси прибора можно достичь положения, при котором призмы Николя оказываются скрещенными и проходящий световой поток гасится.
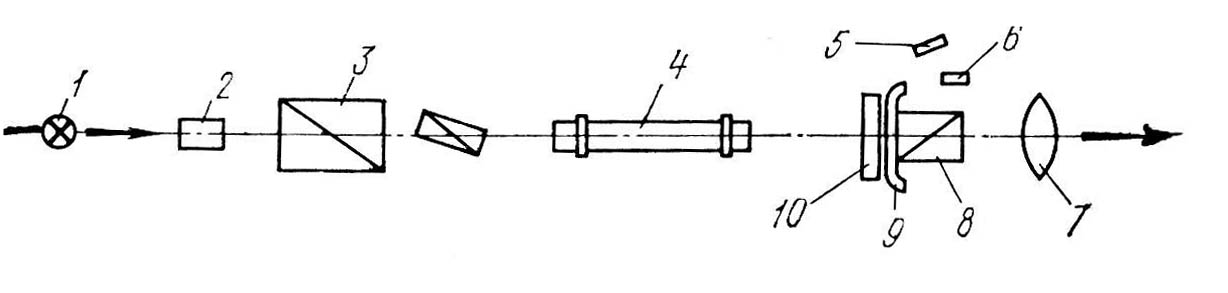
Рис. 2. Схема поляриметра:
1 - источник света; 2 - светофильтр; 3 - поляризатор; 4 – поляриметрическая
трубка; 5 - зеркало; 6 - лупа; 7 - окуляр; 8 - анализатор; 9 - указатель; 10 - лимб
Е
а
б
в
г
сли между поляризатором и анализатором расположен оптически активный раствор, то скрещенная призма уже не будет гасить проходящий световой поток, и для достижения темноты необходим дополнительный поворот анализатора на некоторый угол. В полутеневом поляриметре положение плоскости поляризации светового потока определяется не по затемнению в окуляре прибора всего поля зрения, а по наступлению равной слабой освещенности (установка на полутень). В других положениях анализатора поле зрения в окуляре резко разделено на две части по освещенности или все освещено ярко. Такое устройство обеспечивает более высокую точность измерений, так как чувствительность глаза к различию в освещенности значительно выше, чем к установлению полного затемнения. Если полутеневое положение найдено правильно (рис. 3, б), то малейший поворот анализатора вправо (рис. 3, а) или влево (рис. 3, в) нарушает равномерность освещения вплоть до резкого контраста в освещенности обеих половин поля зрения. При отсутствии поляриметрической трубки в желобке поляриметра полутеневое положение должно соответствовать нулю по шкале (нулевое положение поляриметра).
-
ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ
КОНЦЕНТРАЦИИ РЕАГИРУЮЩИХ ВЕЩЕСТВ
Простые односторонние реакции. Односторонними, или необратимыми, реакциями называются такие, в которых конечные продукты отсутствуют (в начальные моменты для любой реакции) или присутствуют лишь в очень небольших количествах (выпадают в осадок, выделяются в виде газа, образуют малодиссоцинрованное соединение), а также такие, в которых скорости прямой и обратной реакций несоизмеримы (k1k1), т. е. протекают в одном направлении.
В тексте используются следующие обозначения: а и b– начальные концентрации исходных веществ А и В соответственно (Cоа и Сов); (а – х) и (b – х) — концентрации этих веществ к моменту времени t от начала реакции (CA и CB); х – концентрация прореагировавшего вещества за истекший промежуток времени (от начала реакции до момента определения концентрации, т. е. концентрация продукта реакции, Сx).
Реакции первого порядка. К этим реакциям относятся реакции изомеризации, термического разложения веществ, радиоактивного распада и многие бимолекулярные реакции при условии, что концентрация одного из реагирующих веществ поддерживается постоянной. Для реакции типа АВ скорость выражается уравнением:
Интегрируя уравнение (XV.3), получим:
ln(a-x)=- k t + const. (4а)
Интегрирование (4а) в пределах от to= 0 до t приводит к уравнению:
из которого видно, что константа скорости реакции первого порядка имеет размерность, обратную времени: k =
Лабораторная работа № 10
изучение скорости инверсии тростникового сахара
1 Прежде чем начать работу, следует ознакомиться с устройством поляриметра и работой на нем.