ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 01.12.2023
Просмотров: 456
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1. Глинка Н.Л. Общая химия.–М.: Интегралл-пресс, 2004.
2. Ерохин Ю.М., Фролов В.И. Сборник задач и упражнений по химии.–М.: Высшая школа, 2005.
3. Сыркин А.М., Зорина Л.Н. Классификация и номенклатура неорганических веществ: учеб. пособие.- Уфа: УГНТУ, 2006.
4. Курс общей химии /под ред. Н.В.Коровина-М.:Высшая школа, 1999.
Задание №9 по теме "Комплексные соединения"
-
Примеры решения задач
Пример 1. Для соединений Na[Co(SCN)4(H2O)2] и [Fe(NH3)5(NO2)]Cl2 определить тип комплекса, степени окисления всех составляющих и указать комплексообразователь, лиганды, ионы внешней и внутренней сферы и координационное число. Записать уравнения диссоциации комплексных соединений и константу нестойкости для комплексных ионов.
Решение.
Сначала проанализируем состав комплексного соединения. В комплексном соединении содержится сложный комплексный ион, который показан в квадратных скобках. Комплексный ион состоит из комплексообразователя и лигандов. Комплексообразователь записывается первым в квадратной скобке, а далее следуют лиганды. Лигандами могут быть как заряженные частицы: I
Существует целый ряд лигандов, которые в комплексах являются практически всегда бидентатными. Это - этилендиамин, карбонат-ион, оксалат-ион и т.п. Каждая молекула или ион бидентатного лиганда образует с комплексообразователем две химические связи в соответствии с особенностями своего строения:
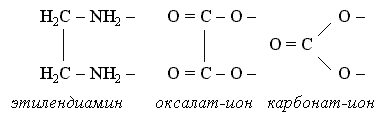
Комплексообразователь и лиганды связаны прочной ковалентной связью донорно-акцепторного типа. Комплексный ион является ионом внутренней сферы. Снаружи располагаются ионы внешней сферы. Ионы внешней и внутренней сферы связаны ионной связью.
Заряд комплексообразователя определяют исходя из зарядов ионов внешней сферы, лигандов, их количества и нейтральности молекулы в целом. Определим заряд комплексообразователя для рассматриваемых комплексных соединений.
Na+[Cox(SCN)
1+ х + 4(-1) + 2·0 = 0 х + 0·5 + (-1) + (-1)·2 = 0
х = +3 х = +3
Следовательно комплексообразователем в первом соединении является Со3+, а во втором – Fe3+.
В приведенном примере вокруг комплексообразователя Со3+ расположены лиганды: (SCN)
Далее определим тип приведенных комплексных соединений. Классификацию комплексных соединений можно провести
1) по заряду комплекса. По этому признаку комплексные соединения делятся на катионные (например, [Zn(NH3)4]Cl2), анионные (K3[Fe(CN)6]), катионно-анионные ([Cu(NH3)4][PtCl6]), нейтральные ([Pd(NH3)2Cl2]0).
2) по виду лигандов комплексные соединения подразделяются на аквакомплексы ([Cr(H2O)6](NO3)3]), гидроксокомплексы (Na[Al(OH)4]), аммиакаты ([Ag(NH3)2]Cl), ацидокомплексы (K2[PtCl6]), гидридные комплексы (Na[BH4]), карбонильные комплексы ([Fe(CO)5]), π-комплексы ([Fe(C5H5)2]), хелаты ([Cu(NH2CH2COO)2]) и смешанные комплексы ([Co(NH3)4Cl2]NO3).
Л





Комплексо-образователь


иганды



Ион внешней сферы
Ион внутренней
сферы (комплекс-
ный ион)
Лиганды




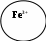


Рис. 1а. Схема комплексного соединения Na[Co(SCN)4(H2O)2]




Лиганды

Комплексо-образователь

Ион
внешней сферы
Ион
внешней сферы
Ион внутрен-ней сферы
(комплексный
ион)

Лиганды



Рис. 1б. Схема комплексного соединения [Fe(NH3)5 NO2]Cl2
3) по составу внешней сферы среди комплексных соединений выделяют кислоты (Н2[PtCl6]), основания ([Ag(NH3)2]ОН), соли (KFe[Fe(CN)6]), неэлектролиты ([Cr(NH3)3(NCS)3]).
Используя приведенную классификацию, комплексное соединение Na[Co(SCN)4(H2O)2] относится к анионным комплексам, так как комплексная частица [Co(SCN)4(H2O)2]¯ является анионом. По виду лигандов – это смешанный комплекс, так как во внутреннюю координационную сферу входят различные лиганды - (SCN)
[Fe(NH3)5(NO2)]Cl2 относится к катионным комплексам, так как комплексная частица [Fe(NH3)5NO2]2+ является катионом. По виду лигандов – это смешанный комплекс, так как во внутреннюю координационную сферу входят различные лиганды - (NH
3)0 и (NO2)–, их число равно 6. По составу внешней сферы данное соединение является комплексной солью.
Комплексные соединения, имеющие ионную внешнюю сферу, в растворе подвергаются диссоциации на комплексный ион и ионы внешней сферы. Они ведут себя в разбавленных растворах как сильные электролиты: диссоциация протекает моментально и практически нацело. Комплексные соединения при диссоциации образуют комплексные ионы:
Na[Co(SCN)4(H2O)2] → Na+ + [Co(SCN)4(H2O)2]
[Fe(NH3)5NO2]Cl2 → [Fe(NH3)5NO2]2+ + 2Cl
Если во внешней сфере комплексного соединения находятся гидроксид-ионы, то это соединение – сильное основание (диссоциация идет нацело, рН>>7). Пример соединения этого типа – гидроксид тетраамминцинка (II):
[Zn(NH3)4](OH)2 → [Zn(NH3)4]2+ + 2OH-
Комплексные соединения с внешнесферными катионами водорода (типа гексафторосиликата водорода или тетрафторобората водорода) в водном растворе нацело подвергаются протолизу. Они являются сильными кислотами:
H[BF4] + H2O → [BF4]- + H3O+
Однако на отщеплении внешнесферных ионов процесс электролитической диссоциации не заканчивается. Комплексные ионы, в свою очередь, подвергаются обратимой электролитической диссоциации, уже как слабые электролиты, по схеме:
[Co(SCN)4(H2O)2]
[Fe(NH3)5(NO2)]2+
Такая диссоциация протекает ступенчато: лиганды удаляются из внутренней сферы постепенно, один за другим (точнее, происходит реакция замещения лиганда на молекулы растворителя - воды). Применяя закон действующих масс к обратимым процессам, получим выражения констант нестойкости комплексных ионов: