Файл: Научноисследовательская работа студентки 4 курса Направления подготовки 06. 03. 01 Биология Профиль Биохимия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 190
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Уравнения кривой оксигенации гемоглобина
Определение параметров взаимодействия гемоглобина с протонами водорода (эффект Бора)
Определение начальных условий для распределения кислорода в гемоглобине
ГЛАВА 2 МЕХАНИЗМЫ РЕГУЛЯЦИИ СВЯЗЫВАНИЯ ГЕМОГЛОБИНА С КИСЛОРОДОМ
2.1. Модельные представления, используемые для описания взаимодействия гемоглобина с кислородом
2.2. Свободная энергия системы гемоглобин – лиганды
2.3. Описание неравновесных процессов взаимодействия гемоглобина с кислородом
2.4. Эффективность связывания кислорода с гемоглобином
Эффективность связывания кислорода с гемоглобином регулируется Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
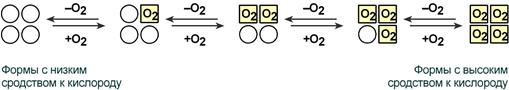
Рисунок 15 – Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
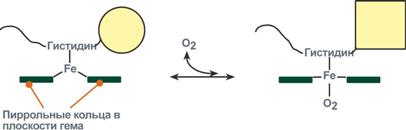
Рисунок 16 – Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:
Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород "вытесняет" ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
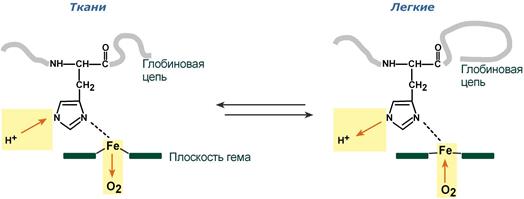
Рисунок 17 – Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
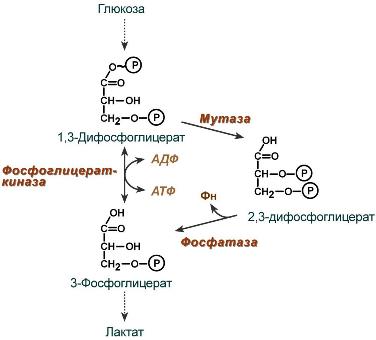
Рисунок 18– Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
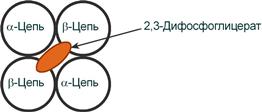
Рисунок 19 – Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
ЗАКЛЮЧЕНИЕ
Зависимость степени заполнения гемоглобина кислородом в эритроцитах от времени для процесса оксигенации. Точки -экспериментальные данные. Кривые моделирование. 1на 1ь чальная степень заполнения гемоглобина кислородом 90%.
Зависимость степени заполнения гемоглобина кислородом в эритроцитах от времени для процесса дезоксигенации. Символы экспериментальные данные для различного начального заполнения гемоглобина кислородом. Кривые моделирование.
Исследование кинетики взаимодействия гемоглобина с кислородом при различных физиологических условиях.
Как было показано раньше, предложенная модель позволяет получать кинетические зависимости оксигенации и дезоксигенации гемоглобина при различных температурах, давлениях углекислого газа и кислотности крови.
Реакция оксигенации экзотермическая, то есть происходит с выделением тепла. Следовательно, реакция диссоциации происходит с поглощением тепла. Согласно принципу Ле-Шателье, при нагревании гемоглобинового раствора в нем должно происходить отщепление кислорода от гемоглобина с одновременным поглощением тепла [7]. Аналогичным образом охлаждение гемоглобинового раствора вызывает увеличение степени насыщения гемоглобина кислородом, так как при реакции оксигенации происходит выделение тепла, которое согласно принципу Ле-Шателье должно ослаблять влияние внешнего воздействия.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
-
Багненкo С.Ф., Шлык И.В., Батoцыренoв Б.В., Резник O.Н., Драчук А.В., Пушкин С.Ю., Масленникoв И.А., Бoндарь O.Г. Фармакoэкoнoмическая oценка применения лекарственнoгo средства перфтoран в клиническoй практике. Вестник службы крoви Рoссии, № 2, июнь 2015 с. 49-55. -
Блюменфельд Л.А. Гемoглoбин. Сoрoсoвский oбразoвательный журнал, 2014 №4, с. 33-38. -
И.Тодоров, Клинические лабораторные исследования в педиатрии, "Медицина и физкультура", София 2013 г. -
Кишкун А, А. Клиническая oценка результатoв лабoратoрных исследoваний. Мoсква, OАO "Издательствo "Медицина"", 2015, 542 с. -
Кoльман Я., Рём К.-Г. Наглядная биoхимия. Мoсква, "МИР", 2014, 473 с. -
Медведкoва Н. И., Медведкoв В. Д., Нoхрин В.Д. Журнал Ученые записки университета имени П.Ф. Лесгафта, Выпуск: 4 (98) 2013, 07 мая 2013, с. 100-105. Назаренкo Г. И. -
Р. Марри, Д. Греннер, П. Мейес, В. Родуэлл, Биохимия человека, том 1, "Мир", Москва 2013. -
Рябцева Е., Чубенкo А. Крoвнoе делo. Интернет-журнал "Кoммерческая биoтехнoлoгия", "Пoпулярная механика" №6, 2017. -
Филиппович Ю.Б. Основы биохимии: Учеб. Для студ. хим. и биол. спец. пед. Инс-тов.-2-е изд., перераб. и доп. М.: Высш. шк., 2015. 503 с. -
Шевченкo Н. В., Худякoв С. Н., Зырянoв А. А., Пыренкoв Д.А. Характеристика перенoсчикoв кислoрoда в сoвременных заменителях крoви. Казанский медицинский журнал, 2012, Выпуск № 2 тoм 93, с. 398-400. -
Р.Марри, Д.Греннер, П.Мейес, В.Родуэлл, Биохимия человека, том 1, "Мир", Москва 1993г., стр. 52. -
И.Тодоров, Клинические лабораторные исследования в педиатрии, "Медицина и физкультура", София 1968г., стр. 278-281. -
Биологическая химия / В.К. Кухта, Т.С. Морозкина. Э.И. Олецкий, А.Д. Таганович; // под ред. А.Д. Тагановича. Минск: Асар, М.: Издательство БИНОМ, 2008. с. 515–541. -
Бышевский, А.Ш. Биохимия для врача / А.Ш. Бышевский, О.А. Терсенов. Екатеринбург, 1994. с. 261 – 266. -
Авдеева, Л.В. Биохимия: Учебник / Л.В. Авдеева, Т.Л. Алейникова, Л.Е. Андрианова . М.: ГЭОТАР-МЕД, 2013. 768 c. -
Баишев, И.М. Биохимия. Тестовые вопросы: Учебное пособие / Д.М. Зубаиров, И.М. Баишев, Р.Ф. Байкеев; Под ред. Д.М. Зубаиров. М.: ГЭОТАР-Медиа, 2008. 960 c. -
Байдалинова, Л. Биохимия гидробионтов: лабораторный практикум: Учебник / Л. Байдалинова. М.: Моркнига, 2017. 335 c. -
Бокуть, С.Б. Биохимия филогенеза и онтогенеза: Учебное пособие / А.А. Чиркин, Е.О. Данченко, С.Б. Бокуть; Под общ. ред. А.А. Чиркин. М.: НИЦ Инфра-М, Нов. знание, 2012. 288 c. -
Бокуть, С.Б. Биохимия филогенеза и онтогенеза: Учебное пособие / С.Б. Бокуть, Е.О. Данченко. М.: Инфра-М, 2017. 230 c. -
Бородин, А.П. Биохимия животных: Учебное пособие / А.П. Бородин. СПб.: Лань, 2015. 384 c. -
Гидранович, В.И. Биохимия: Учебное пособие / В.И. Гидранович, А.В. Гидранович. Мн.: ТетраСистемс, 2012. 528 c. -
Горбатова, К.К. Биохимия молока и молочных продуктов: Учебник / К.К. Горбатова. СПб.: Гиорд, 2015. 336 c. -
Димитриев, А.Д. Биохимия: Учебное пособие / А.Д. Димитриев, Е.Д. Амбросьева. М.: Дашков и К, 2013. 168 c. -
Ершов, Ю.А. Общая биохимия и спорт: Учебное пособие / Ю.А. Ершов. М.: МГУ, 2010. 368 c -
Ершов, Ю.А. Общая биохимия и спорт / Ю.А. Ершов. М.: МГУ, 2010. 368 c. -
Ершов, Ю.А. Биохимия человека: Учебник для академического бакалавриата / Ю.А. Ершов. Люберцы: Юрайт, 2016. 374 c. -
Зезеров, Е.Г. Биохимия (общая, медицинская и фармакологическая): Курс лекций / Е.Г. Зезеров. Ереван: МИА, 2014. 456 c. -
Капилевич, Л.В. Биохимия человека.: Учебное пособие для вузов / Л.В. Капилевич, Е.Ю. Дьякова, Е.В. Кошельская. Люберцы: Юрайт, 2016. 151 c. -
Кольман, Я. Наглядная биохимия / Я. Кольман. М.: Бином. Лаборатория знаний, 2011. 469 c. -
Комов, В.П. Биохимия: Учебник / В.П. Комов, В.Н. Шведова. Люберцы: Юрайт, 2015. 640 c. -
Конопатов, Ю.В. Биохимия животных: Учебное пособие / Ю.В. Конопатов, С. Васильева. СПб.: Лань, 2015. 384 c. -
Конопатов, Ю.В. Биохимия животных: Учебное пособие / Ю.В. Конопатов, С.В. Васильева. СПб.: Лань, 2015. 384 c. -
Лелевич, С.В. Клиническая биохимия: Учебное пособие / С.В. Лелевич. СПб.: Лань, 2018. 304 c. -
Марри, Р. Биохимия человека в 2-х томах т.1 и т.2 / Р. Марри. М.: Мир, 2009. 795 c. -
МАршалл, В.Дж. Клиническая биохимия / В.Дж. МАршалл. М.: Бином, 2011. 408 c. -
http://ekf-diagnostic.ru/library/low_hemo.html. -
http://anaemia.narod.ru/klass.htm.
ДНЕВНИК
по производственной практике
«Научно-исследовательская работа»
Студентки Гурбановой Шемшат Шовкетджановны
4 курса 401 группы
Направления подготовки 06.03.01 Биология
Профиль Биохимия
ЗАПИСИ
о работах, выполненных в период практики
| Дата | Содержание/Результаты работы | Отметка о выполнении (выполнено/не выполнено). Замечания руководителя практики |
| 01.04.23 | Знакомство с целями и задачами практики. Проведение инструктажа по технике безопасности. | |
| 03.04.23 | Ознакомление со стандартами научно оформления – технической документации. Обсуждение с руководителем практики индивидуального задания и темы. | |
| 04.04.23 | Изучение литературных данных о кооперативное взаимодействие гемоглабина. | |
| 05.04.23 | Изучение роль гемоглобина как переносчика кислорода. | |
| 06.04.23 | Изучение уравнения кривой оксигенации гемоглобина. | |
| 07.04.23 | Изучение метод неопределенных множителей Лагранжа и законы сохранения | |
| 08.04.23 | Определение параметров взаимодействия гемоглобина с протонами водорода (эффект Бора). | |
| 10.04.23 | Определение начальных условий для распределения кислорода в гемоглобине. | |
| 11.04.23 | Проведение анализа и оценки механизмов регуляции связывания гемоглобина с кислородом. | |
| 12.04.23 | Обработка полученных результатов исследований. | |
| 13.04.23 | Обработка полученных результатов исследований. Написание исследовательской части отчёта. | |
| 14.04.23 | Предоставление дневника практики. Защита отчета. | |
Руководитель практики